Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.75 n.2 Buenos Aires mar./abr. 2007
Tratamiento endovascular de la aorta torácica descendente. Resultados a mediano plazo
Hernán G. Bertoni, Mario P. Fava, Germán A. Girella, Cristian Zgrablich, Pablo Ruda Vega, Gustavo A. Salvo, Fabián A. Azzari†, Gustavo Andersen, Adrián CharaskMTSAC, Jorge H. LeguizamónMTSAC
Artery Group. Unidad de Terapéutica Endovascular, Cardiología Intervencionista y Cirugía Cardiovascular. Buenos Aires, Argentina
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
† Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
Dirección para separatas: Dr. Hernán Gabriel Bertoni Fax: 5237-1000 (int 11) Tel. 5217-0038/0039
e-mail: hernangbertoni@yahoo.com.ar
Recibido: 06/11/2006
Aceptado: 05/01/2007
RESUMEN
Objetivo
El propósito de esta publicación es comunicar nuestros resultados inmediatos y a mediano plazo del tratamiento endovascular de la aorta torácica descendente mediante implante de endoprótesis.
Material y métodos
Entre agosto de 1999 y agosto de 2006, 74 pacientes consecutivos, 53 hombres y 21 mujeres, fueron tratados por vía endovascular con implante de una prótesis autoexpandible. La edad media fue de 60 ± 14,8 años. Las indicaciones para tratamiento fueron disección aguda (n = 8); 11%, disección crónica (n = 31); 42%, hematoma intramural (n = 5); 7%, aneurisma verdadero (n = 17); 23%, úlcera penetrante (n = 4); 5% y seudoaneurisma traumático (n = 9); 12%.
Resultados
El implante del dispositivo fue exitoso en 73 (98,6%) pacientes; no se requirió conversión quirúrgica en ninguno de ellos. Ningún paciente presentó paraplejía o déficit neurológico. La mortalidad a los 30 días fue del 8,1% (n = 6). La mediana de seguimiento fue de 33,5 meses (rango 1-79) y la sobrevida global fue del 84% (IC 69-92%) y del 91% (IC 77-97%), según se incluyese o no la mortalidad temprana. El 93% (IC 84-97%) de los pacientes estaban libres de complicaciones relacionadas con el procedimiento. La mayoría de las complicaciones ocurrieron durante el primer año de seguimiento.
Conclusiones
El tratamiento endovascular de la aorta torácica descendente con implante de endoprótesis autoexpandible es factible y seguro. La baja incidencia de eventos en relación con las series quirúrgicas publicadas hace que este procedimiento sea de elección en pacientes seleccionados.
Palabras clave: Aorta torácica; Prótesis vascular; Stent
Abreviaturas:
AV Aneurisma verdadero;
DTB Disección aórtica tipo B;
HIM Hematoma intramural;
SAT Seudoaneurisma traumático;
UAP Úlcera aórtica penetrante.
SUMMARY
Endovascular Treatment of the Descending Thoracic Aorta. Mid-Term Results
Objective
The purpose of this paper is to assess and report our immediate and mid-term results with the endoluminal treatment of aneurysmal disease of the descending thoracic aorta, using an endoprosthesis or stent-graft.
Material and Methods
From August 1999 to August 2006, 74 consecutive patients (53 men and 21 women) were treated with an endovascular self-expanding stent-graft. Their mean age was 60 ± 14.8 years. Indications for treatment were: acute dissection in 8 patients (11%), chronic dissection in 31 patients (42%), intramural hematoma in 5 patients (7%), true aneurysm in 17 patients (23%), penetrating ulcer in 4 patients (5%) and posttraumatic pseudoaneurysm in 9 patients (12%).
Results
The implant of the device was successful in 73 patients (98.6%); no patient required surgical conversion. There were no cases of paraplegia or neurological deficit. Thirty-day mortality was 8.1% (n = 6). Median follow-up time was 33.5 months (range: 1-79 months) and overall survival was 84% (CI: 69-92%) and 91% (CI: 77-97%), according to whether early mortality was included or not. Ninetythree percent of patients (CI: 84-97%) were free from procedure- related complications. Most complications occurred during the first year of follow-up.
Conclusions
Endovascular treatment of the descending thoracic aorta with self-expanding stent-grafts is feasible and safe. Based on the low incidence of events reported in the surgical series published, we believe this is the procedure of choice in selected patients.
Key words: Aorta; Thoracic; Blood vessel prótesis; Stent
INTRODUCCIÓN
Las enfermedades de la aorta torácica descendente representan un grupo de patologías con una mortalidad elevada. Entre ellas se encuentran la disección aórtica tipo B (DTB), el hematoma intramural (HIM), el aneurisma verdadero (AV), la úlcera aórtica penetrante (UAP) y el seudoaneurisma traumático (SAT). A pesar de un mayor consenso médico acerca de un diagnóstico precoz y un tratamiento apropiado, no existen aún guías y recomendaciones de tratamiento precisas.
El tratamiento quirúrgico con interposición de una prótesis de Dacron ha sido por muchos años el tratamiento preferido en estos pacientes. (1) En los últimos años, las técnicas quirúrgicas han avanzado y las complicaciones perioperatorias disminuyeron; sin embargo, la mortalidad y la morbilidad asociadas siguen siendo elevadas, aun en centros con experiencia documentada. (2, 3)
El implante de una endoprótesis ofrece una alternativa menos invasiva al tratamiento quirúrgico. (4, 5) Desde la primera comunicación de Dake y colaboradores en pacientes con aneurismas torácicos, (6) importantes progresos técnicos y la creciente experiencia de algunos grupos médicos han mejorado la seguridad y la eficacia de este tipo de tratamiento y han ampliado sus indicaciones. (7)
El número de pacientes con patología aórtica ha mostrado un incremento progresivo debido al aumento de la expectativa de vida y a una mejor disponibilidad y desarrollo de las técnicas diagnósticas no invasivas.
El propósito de esta publicación es presentar los resultados inmediatos y a mediano plazo de una serie de pacientes con patología de la aorta torácica descendente, tratados por vía endoluminal.
MÉTODOS
Entre agosto de 1999 y agosto de 2006, 74 pacientes consecutivos con patología de la aorta torácica descendente fueron tratados con implante de una endoprótesis autoexpandible (Talent® en 71 pacientes y Relay® en 3 pacientes).
En los pacientes con DTB no complicadas, AV y SAT, la indicación se basó sobre la presencia de dolor torácico asociado con hipertensión arterial, signos de compresión de estructuras vecinas, diámetro aórtico ≥ 60 mm o aumento de éste > 5 mm/año.
Desde el punto de vista anatómico, el cuello proximal y distal debían tener una longitud de 15 mm desde el origen de la arteria subclavia izquierda y proximal al origen del tronco celíaco, respectivamente, cuyos diámetros debían ser de 22-42 mm y el acceso vascular iliofemoral debía tener un diámetro suficiente para permitir el avance del sistema de entrega de la endoprótesis (> 7 mm). (7) En los pacientes con cuello proximal insuficiente, la endoprótesis se implantó cubriendo el origen de la arteria subclavia izquierda, luego de confirmar la permeabilidad de la arteria vertebral derecha y la conformación de la circulación vertebrobasilar. Las endoprótesis implantadas tenían un diámetro > 3-4 mm que el de la aorta sana a fin de permitir una fijación adecuada y disminuir el riesgo de migración.
Todos los procedimientos se realizaron bajo anestesia general. Una vez logrado el acceso vascular por el cirujano cardiovascular, todos los implantes fueron realizados por el mismo operador (H.G.B.) en distintos centros.
La liberación de las endoprótesis se realizó bajo hipotensión sistémica controlada (presión arterial media ≤ 70 mm Hg en los casos del cayado aórtico y ≥ 70 mm Hg para la aorta descendente).
Descripción de las endoprótesis
Se utilizaron endoprótesis autoexpandibles de nitinol cubiertas por una membrana de Dacron (Medtronic Talent®, Santa Rosa, EE.UU., y Bolton Relay®, Sunrise, EE.UU.). El extremo proximal de ambas consiste en un stent no cubierto (graft free) de 15 mm de longitud que sirve de fijación a la aorta.
Los diámetros disponibles son de 28 a 46 mm, con un largo de 130 mm hasta el año 2005 y de 150 a 200 mm desde entonces.
Seguimiento
Se realizó seguimiento clínico y por imágenes al mes, a los 6 y 12 meses y luego anualmente. Se realizó tomografía helicoidal o multicorte en todos los pacientes, excepto en cuatro casos que fueron seguidos mediante RMN debido a insuficiencia renal.
Se registró en forma prospectiva la ocurrencia de complicaciones relacionadas con el procedimiento (rotura aórtica, integridad de las endoprótesis o presencia de endoleaks).
Análisis estadístico
El análisis estadístico se realizó con el programa Statistics 7.
Las variables continuas se expresan como mediana o media y desviación estándar y las categóricas como porcentaje. Para estimar la probabilidad acumulada de permanecer libre de eventos (mortalidad y complicaciones) se utilizó el método de Kaplan-Meier. Los intervalos de confianza (IC) se calcularon con un nivel del 95%.
RESULTADOS
Se incluyeron 53 hombres y 21 mujeres; la edad media fue de 60 ± 14,8 años. Las características clínicas de los pacientes tratados se enumeran en la Tabla 1.
Tabla 1. Características demográficas, factores de riesgo cardiovascular y comorbilidades

El riesgo quirúrgico, de acuerdo con la Sociedad Americana de Anestesiología (ASA), fue: ASA I (n = 9), ASA II (n = 42), ASA III (n = 17) y ASA IV (n = 6).
La patología aórtica de base fue DTB aguda (n = 8); 11%, DTB crónica (n = 31); 42%, HIM (n = 5); 7%, AV (n = 17); 23%, UAP (n = 4); 5% y SAT (n = 9); 12%.
En 7 pacientes con DTB aguda no complicada, la decisión de tratamiento se debió a dolor torácico persistente (n = 5), hipertensión arterial refractaria al tratamiento médico (n = 2), en todos los casos asociada con falso lumen permeable y diámetro aórtico ≥ 40 mm. El último paciente ingresó en shock debido a un hemotórax izquierdo masivo. En todos los casos se cubrió el tear proximal y se logró expandir el lumen verdadero, sin que se registraran endoleaks. Por debajo de la endoprótesis, el lumen falso persistió permeable, sin evidencias de aumento del diámetro aórtico durante el seguimiento.
En los pacientes con DTB crónica y en 14 pacientes con AV, la indicación de tratamiento fue un diámetro aórtico ≥ 60 mm. Tres pacientes con AV ingresaron en estado de shock, debido a rotura del saco aneurismático.
Todos los pacientes con HIM fueron tratados por dolor torácico persistente y aumento del diámetro del hematoma durante la internación.
De los pacientes con UAP, tres presentaban una úlcera gigante sintomática (dolor torácico) y uno de ellos una fístula aortoesofágica.
En los pacientes con PAT, el diámetro aórtico medio en el momento del tratamiento fue de 70 mm (rango 57-77).
El implante del dispositivo fue exitoso en 73 (98,6%) pacientes; en un paciente no se pudo ascender el dispositivo a pesar de haber realizado un abordaje retroperitoneal de la arteria ilíaca derecha. En ningún caso se requirió conversión a cirugía convencional.
El tiempo operatorio medio fue de 110 minutos (rango 45-240).
En 11 pacientes se debió cubrir el origen de la arteria subclavia izquierda, sin requerimiento de bypass subclavio carotídeo. Durante el seguimiento se constató diferencia de presión entre el brazo derecho (sistólica 137 ± 13 mm Hg) y el brazo izquierdo (sistólica 100 ± 20 mm Hg).
Cinco pacientes recibieron tres endoprótesis cada uno para cubrir la aorta en el sector toracoabdominal (Figura 1).
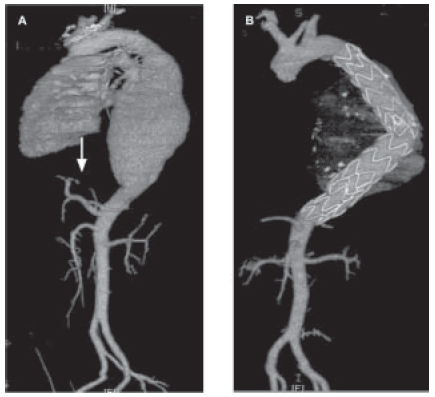
Fig. 1. A. Reconstrucción volumétrica de una TAC multicorte, que muestra un aneurisma toracoabdominal, que se extiende 2 cm por encima del tronco celíaco (flecha). B. Control a los seis meses luego del implante de tres endoprótesis.
Seguimiento
La mediana de seguimiento fue de 33,5 meses (rango 1-79).
1. Mortalidad temprana
Seis pacientes fallecieron durante el período perioperatorio (8,1%).
Un paciente con síndrome de Marfan que presentaba una DTB crónica sintomática murió a las 12 horas del procedimiento por isquemia mesentérica debido a oclusión del lumen verdadero distal a la endoprótesis. Un segundo paciente en shock con DTB aguda murió a las 72 horas del procedimiento. Otros 4 pacientes murieron por falla multiorgánica secundaria a rotura del aneurisma (3 pacientes) y a una fístula aortoesofágica (1 paciente).
2. Mortalidad tardía (a partir de los 30 días)
Durante el seguimiento se constataron 4 muertes (5,4%); la sobrevida a los 43 meses fue del 84% (IC 69-92%) y del 91% (IC 77%-97%), según se incluyese o no la mortalidad temprana (Figura 2).
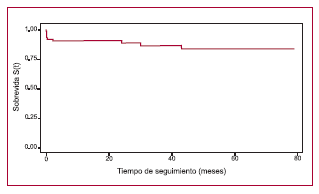
Fig. 2. Curva de Kaplan-Meier de sobrevida.
Dos pacientes murieron por un infarto agudo de miocardio a los 30 y a los 43 meses del procedimiento. Un tercer paciente falleció a causa de rotura aórtica por migración distal de un cuerpo protésico a los 24 meses del procedimiento. Un último paciente, con enfermedad de Marfan, falleció súbitamente a los 2 meses del procedimiento.
3. Complicaciones tempranas
Ningún paciente presentó trastornos isquémicos medulares o déficit neurológico.
En 3 pacientes (dos DTB crónicas y un SAT, 4%) se constataron endoleaks tipo I. Fueron tratados con implante de una extensión proximal a los 20 y a los 30 días, respectivamente.
En 2 (2,7%) pacientes se observó una disección segmentaria de la arteria ilíaca externa durante el ascenso de la endoprótesis con restricción significativa al flujo sanguíneo. Ambos casos se trataron con implante de un stent.
4. Complicaciones tardías (a partir de los 30 días)
El 97% (IC 89-99%), el 95% (IC 86-98%) y el 93% (IC 84-97%) de los pacientes estaban libres de complicaciones relacionadas con el procedimiento al mes, a los 6 meses y al final del seguimiento, respectivamente. La mayoría de las complicaciones ocurrieron durante el primer año (Figura 3).
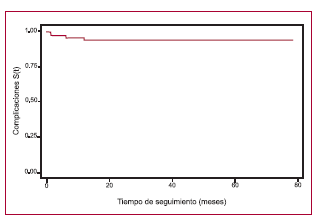
Fig. 3. Curva de Kaplan-Meier de sobrevida libre de complicaciones relacionadas con el procedimiento (rotura del aneurisma o endoleak).
Dos pacientes (tratados por DTB aguda) fueron reinternados por presentar dolor torácico a los 40 y a los 90 días del procedimiento con diagnóstico de disección aguda tipo A. En uno de ellos se desarrolló de novo y en otro a partir de la fijación proximal de la endoprótesis. Ambos pacientes fueron intervenidos quirúrgicamente en forma exitosa.
Durante el seguimiento se registraron dos endoleaks secundarios (uno tipo I y otro tipo III). El primero se debió a migración distal de la endoprótesis, que fue corregida con implante de una extensión proximal a los 6 meses. El segundo falleció por rotura aórtica antes de recibir tratamiento.
DISCUSIÓN
Historia natural de la patología aórtica
Los pacientes con disección tipo B no complicada tienen una mortalidad a los 30 días del 10%, (8) con una sobrevida a los 3 años del 75%. (9, 10) Marui y colaboradores muestran que el 67% de los pacientes con diámetro aórtico > 40 mm y falsa luz permeable evolucionaban a una dilatación severa o rotura aórtica a los 5 años de seguimiento, mientras que esto sucedía en el 6% de los pacientes que no presentaban ninguna de estas características en la fase aguda. (11)
El hematoma intramural afecta a pacientes de mayor edad y con más factores de riesgo ateroscleróticos que la disección aórtica; se origina a partir de la rotura espontánea de los vasa vasorum o de una UAP y en el 60% de los casos se localiza en la aorta torácica descendente. (12) Los HIM asociados con una UAP suelen presentar una dilatación progresiva, desarrollo de disección o rotura, mientras que aquellos no asociados con una UAP tienen una evolución más estable (48% versus 8%, respectivamente), sobre todo cuando se limitan a la aorta torácica descendente. (13)
La úlcera penetrante aórtica aguda y sintomática tiene un riesgo igual o superior al de la disección aórtica o al del HIM y se localiza frecuentemente en la aorta torácica descendente. (14) La incidencia de rotura es del 10-40%, mayormente cuando se asocian con un HIM.
Los aneurismas de la aorta torácica suelen afectar a una población añosa con múltiples comorbilidades; su incidencia es de 6-10 cada 100.000 pacientes/ año. (7) La tasa de crecimiento es mayor cuando se localizan en la aorta descendente o se asocian con disección aórtica o con síndrome de Marfan. (15) El riesgo de rotura se relaciona con la edad del paciente, el tamaño del aneurisma (> 60 mm), la enfermedad pulmonar obstructiva crónica, la hipertensión arterial no controlada y el dolor torácico crónico. (16)
Los seudoaneurismas traumáticos, aun siendo pequeños, tienen una evolución insidiosa. Tienden a expandirse o romperse y pueden fistulizarse a órganos adyacentes, comprimir estructuras vecinas o embolizarse. (17) Cuando un SAT involucra el ligamento arterioso, localizándose en la ventana aórticopulmonar, puede tener una evolución crónica y permanecer asintomático por largo tiempo; sin embargo, en el 42% y en el 89% de los casos producirá síntomas dentro de los 5 y los 20 años, respectivamente. (18)
En general, el tratamiento médico inicial de las patologías descriptas consiste en el control estricto de la tensión arterial; se indica cirugía en caso de hipotensión o shock, dolor intratable, hematoma periaórtico, compromiso vascular visceral o de miembros inferiores, diámetro aórtico ≥ 60 mm o expansión rápida de él. La mortalidad y el riesgo de paraplejía durante la cirugía se correlacionan con la indicación electiva o urgente (7-12% y 0-10% versus 25-65% y > 15%, respectivamente) y con la experiencia del equipo quirúrgico. (1, 19, 20)
Resultados y ventajas del tratamiento endovascular
Las ventajas teóricas del tratamiento endovascular son muchas: no requiere toracotomía, paro circulatorio ni clampeo aórtico, con lo que disminuye drásticamente el riesgo de paraplejía, incluso en pacientes cuya aorta torácica descendente es cubierta completamente.
Como ocurrió con el tratamiento endoluminal de la aorta abdominal, las primeras publicaciones incluían sólo pacientes de alto riesgo quirúrgico con aneurismas torácicos o disecciones aórticas; sin embargo, la baja mortalidad y morbilidad comunicada con esta modalidad terapéutica generó una enorme expectativa. (21-23)
Desde entonces, el uso de estos dispositivos se ha extendido al tratamiento de otras patologías (HIM, UAP y PAT), con el 4-9% de mortalidad, < 3% de paraplejía y < 5% de déficit neurológico; son predictores de muerte y complicaciones hospitalarias el riesgo quirúrgico, la edad y el tratamiento de emergencia. (24-27)
En la actualidad, numerosos registros multicéntricos prospectivos están evaluando el tratamiento endoluminal de los aneurismas de la aorta torácica descendente en pacientes de bajo a moderado riesgo quirúrgico. (28)
Nosotros consideramos a los pacientes con DTB no complicada buenos candidatos para ser tratados por vía endoluminal, con el objetivo de inducir trombosis completa del falso lumen y evitar así la dilatación y la rotura aórtica (Figura 4). (29) El estudio europeo INSTEAD, que se encuentra en fase de inclusión, tiene la finalidad de comparar la mortalidad a los 2 años de la DTB no complicada tratada con implante de una endoprótesis Talent® versus tratamiento médico solo. (30)

Fig. 4. A. Disección aórtica aguda tipo B con colapso de la luz verdadera (flecha) y falso lumen expandido (estrella). B. Control inmediato luego del implante de la endoprótesis; se observa restauración del flujo únicamente a través del lumen verdadero.
Si bien en nuestra experiencia la mortalidad perioperatoria fue del 8,1%, 5 de las 6 muertes ocurrieron en pacientes en shock tratados de emergencia. En un metaanálisis reciente, Eggebrecht y colaboradores comunicaron una mortalidad del 9,8% ± 2,2% versus 3,2% ± 1,4%, en pacientes con diagnóstico de DTB en período agudo o crónico, respectivamente. (21)
Respecto del desarrollo de paraplejía, se ha relacionado con el descenso de la presión arterial media durante el procedimiento a < 70 mm Hg, (31) lo cual sugiere que la perfusión espinal dependería más de la circulación colateral (sensible a cambios hemodinámicos bruscos) que de las arterias segmentarias (arteria de Adamkiewicz). Asimismo, el tratamiento previo de la aorta abdominal (quirúrgico o endoluminal) aumenta el riesgo de paraplejía por ausencia de circulación colateral a través de las arterias lumbares. (32) En nuestra experiencia, todos los pacientes mantuvieron durante el procedimiento una presión arterial media > 70 mm Hg y ninguno de ellos sufrió esta complicación.
Todos los pacientes en los que se cubrió la arteria subclavia izquierda, en concordancia con lo comunicado en la literatura, permanecieron asintomáticos durante el seguimiento, sin déficit funcional del miembro superior ni diferencia de temperatura. (33-35)
Limitaciones
En primer lugar cabe mencionar que todos los implantes fueron realizados por un solo operador experimentado, lo cual limita la generalización de estos resultados. (21, 36)
Segundo, hemos incluido una población heterogénea en lo que respecta al tipo de patología tratada y al riesgo operatorio; sin embargo, nuestros resultados se corresponden con los publicados por otros autores. (25-27)
Tercero, se utilizaron distintos tipos y generaciones de dispositivos, por lo cual es dable inferir que muchas de las dificultades y complicaciones registradas al inicio de la experiencia se hayan atenuado con el avance en el desarrollo de dichos dispositivos.
Por último, es imperativo un seguimiento clínico más prolongado a fin de establecer la eficacia y la seguridad alejadas de esta técnica.
CONCLUSIONES
El tratamiento endovascular de la aorta torácica descendente con implante de una prótesis autoexpandible es factible y seguro. La baja incidencia de eventos en comparación con la cirugía hace que este procedimiento sea de elección en pacientes seleccionados. No obstante, son indispensables un número mayor de pacientes y un seguimiento más prolongado para confirmar estos resultados.
Conflicto de intereses
El Dr. Hernán G. Bertoni es Proctor de Medtronic para América latina.
BIBLIOGRAFÍA
1. Kouchoukos NT, Dougenis D. Surgery of the thoracic aorta. N Engl J Med 1997;336:1876-88 [ Links ]
2. Cambria RP, Davison JK, Carter C, Brewster DC, Chang Y, Clark KA, et al. Epidural cooling for spinal cord protection during thoracoabdominal aneurysm repair: A five-year experience. J Vasc Surg 2000;31:1093-102 [ Links ]
3. Safi HJ, Miller CC 3rd, Iliopoulos DC, Letsou GV, Baldwin JC. Staged repair of extensive aortic aneurysm: improved neurologic outcome. Ann Surg 1997;226:599-605 [ Links ]
4. Bortone AS, Schena S, Mannatrizio G, Paradiso V, Ferlan G, Dialetto G, et al. Endovascular stent-graft treatment for diseases of the descending thoracic aorta. Eur J Cardiothorac Surg 2001;20:514-9. [ Links ]
5. Won JY, Lee DY, Shim WH, Chang BC, Park SI, Yoon CS, et al. Elective endovascular treatment of descending thoracic aortic aneurysms and chronic dissections with stent-grafts. J Vasc Interv Radiol 2001;12:575-82. [ Links ]
6. Dake MD, Miller DC, Semba CP, Mitchell RS, Walker PJ, Liddell RP. Transluminal placement of endovascular stent-grafts for the treatment of descending thoracic aortic aneurysms. N Engl J Med 1994;331:1729-34. [ Links ]
7. Katzen BT, Dake MD, MacLean AA, Wang DS. Endovascular repair of abdominal and thoracic aortic aneurysms. Circulation 2005; 112:1663-75. [ Links ]
8. Hagan PG, Nienaber CA, Isselbacher EM, Bruckman D, Karavite DJ, Russman PL, et al. The International Registry of Acute Aortic Dissection (IRAD): new insights into an old disease. JAMA 2000; 283:897-903. [ Links ]
9. Glower DD, Fann JI, Speier RH, Morrison L, White WD, Smith LR, et al. Comparison of medical and surgical therapy for uncomplicated descending aortic dissection. Circulation 1990; 82:IV39-46. [ Links ]
10. Tsai TT, Fattori R, Trimarchi S, Isselbacher E, Myrmel T, Evangelista A, Hutchison S, Sechtem U, Cooper JV, Smith DE, et al. Long- Term Survival in Patients Presenting With Type B Acute Aortic Dissection. Insights From the International Registry of Acute Aortic Dissection. Circulation 2006;114:2226-31. [ Links ]
11. Marui A, Mochizuki T, Mitsui N, Koyama T, Kimura F, Horibe M. Toward the best treatment for uncomplicated patients with type B acute aortic dissection: A consideration for sound surgical indication. Circulation 1999;100:II275-280. [ Links ]
12. Evangelista A, Mukherjee D, Mehta RH, O'Gara PT, Fattori R, Cooper JV, et al. Acute intramural hematoma of the aorta: a mystery in evolution. Circulation 2005;111:1063-70. [ Links ]
13. Ganaha F, Miller DC, Sugimoto K, Do YS, Minamiguchi H, Saito H, et al. Prognosis of aortic intramural hematoma with and without penetrating atherosclerotic ulcer: a clinical and radiological analysis. Circulation 2002;106:342-8. [ Links ]
14. Movsowitz HD, Lampert C, Jacobs LE, Kotler MN. Penetrating atherosclerotic aortic ulcers. Am Heart J 1994;128:1210-7. [ Links ]
15. Isselbacher EM. Thoracic and abdominal aortic aneurysms. Circulation 2005;111:816-28. [ Links ]
16. Griepp RB, Ergin MA, Galla JD, Lansman SL, McCullough JN, Nguyen KH, et al. Natural history of descending thoracic and thoracoabdominal aneurysms. Ann Thorac Surg 1999;67:1927-30. [ Links ]
17. Pretre R, Chilcott M. Blunt trauma to the heart and great vessels. N Engl J Med 1997;336:626-32. [ Links ]
18. Creasy JD, Chiles C, Routh WD, Dyer RB. Overview of traumatic injury of the thoracic aorta. Radiographics 1997;17:27-45. [ Links ]
19. Trimarchi S, Nienaber CA, Rampoldi V, Myrmel T, Suzuki T, Bossone E, et al. Role and results of surgery in acute type B aortic dissection: insights from the International Registry of Acute Aortic Dissection (IRAD). Circulation 2006;114:I357-64. [ Links ]
20. Black JH 3rd, Cambria RP. Current results of open surgical repair of descending thoracic aortic aneurysms. J Vasc Surg 2006;43: 6A-11A. [ Links ]
21. Eggebrecht H, Nienaber CA, Neuhauser M, Baumgart D, Kische S, Schmermund A, et al. Endovascular stent-graft placement in aortic dissection: a meta-analysis. Eur Heart J 2006;27:489-98. [ Links ]
22. Dake MD, Kato N, Mitchell RS, Semba CP, Razavi MK, Shimono T, et al. Endovascular stent-graft placement for the treatment of acute aortic dissection. N Engl J Med 1999;340:1546-52. [ Links ]
23. Nienaber CA, Fattori R, Lund G, Dieckmann C, Wolf W, von Kodolitsch Y, et al. Nonsurgical reconstruction of thoracic aortic dissection by stent-graft placement. N Engl J Med 1999;340:1539-45. [ Links ]
24. Bortone AS, De Cillis E, D'Agostino D, de Luca Tupputi Schinosa L. Endovascular treatment of thoracic aortic disease: four years of experience. Circulation 2004;110:II262-7. [ Links ]
25. Fattori R, Nienaber CA, Rousseau H, Beregi JP, Heijmen R, Grabenwoger M, et al. Results of endovascular repair of the thoracic aorta with the Talent Thoracic stent graft: the Talent Thoracic Retrospective Registry. J Thorac Cardiovasc Surg 2006;132:332-9. [ Links ]
26. Leurs LJ, Bell R, Degrieck Y, Thomas S, Hobo R, Lundbom J; EUROSTAR; UK Thoracic Endograft Registry collaborators. Endovascular treatment of thoracic aortic diseases: combined experience from the EUROSTAR and United Kingdom Thoracic Endograft registries. J Vasc Surg 2004;40:670-9. [ Links ]
27. Wheatley GH 3rd, Gurbuz AT, Rodriguez-Lopez JA, Ramaiah VG, Olsen D, et al. Midterm outcome in 158 consecutive Gore TAG thoracic endoprostheses: single center experience. Ann Thorac Surg 2006;81:1570-7. [ Links ]
28. Cho JS, Haider SE, Makaroun MS. US multicenter trials of endoprostheses for the endovascular treatment of descending thoracic aneurysms. J Vasc Surg 2006;43:12A-19A. [ Links ]
29. Erbel R, Oelert H, Meyer J, Puth M, Mohr-Katoly S, Hausmann D, et al. Effect of medical and surgical therapy on aortic dissection evaluated by transesophageal echocardiography. Implications for prognosis and therapy. The European Cooperative Study Group on Echocardiography. Circulation 1993;87:1604-15. [ Links ]
30. Nienaber CA, Zannetti S, Barbieri B, Kische S, Schareck W, Rehders TC. INvestigation of STEnt grafts in patients with type B Aortic Dissection: design of the INSTEAD trial- a prospective, multicenter, European randomized trial. Am Heart J 2005;149:592-9. [ Links ]
31. Chiesa R, Melissano G, Marrocco-Trischitta MM, Civilini E, Setacci F. Spinal cord ischemia after elective stent-graft repair of the thoracic aorta. J Vasc Surg 2005;42:11-7. [ Links ]
32. Grabenwoger M, Hutschala D, Ehrlich MP, Cartes-Zumelzu F, Thurnher S, Lammer J, et al. Thoracic aortic aneurysms: treatment with endovascular self-expandable stent grafts. Ann Thorac Surg 2000;69:441-5. [ Links ]
33. Rehders TC, Petzsch M, Ince H, Kische S, Korber T, Koschyk DH, et al. Intentional occlusion of the left subclavian artery during stentgraft implantation in the thoracic aorta: risk and relevance. J Endovasc Ther 2004;11:659-66. [ Links ]
34. Schoder M, Grabenwoger M, Holzenbein T, Cejna M, Ehrlich MP, Rand T, et al. Endovascular repair of the thoracic aorta necessitating anchoring of the stent graft across the arch vessels. J Thorac Cardiovasc Surg 2006;131:380-7. [ Links ]
35. Sueda T, Watari M, Okada K, Orihashi K, Matsuura Y. Endovascular stent-grafting through the aortic arch: an alternative approach for distal arch aortic aneurysm. Ann Thorac Surg 2000; 70:1251-4. [ Links ]
36. Kouchoukos NT, Bavaria JE, Coselli JS, De La Torre R, Ikonomidis JS, Karmy-Jones RC, et al. Guidelines for credentialing of practitioners to perform endovascular stent-grafting of the thoracic aorta. Ann Thorac Surg 2006;81:1174-6. [ Links ]














