Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.75 n.2 Buenos Aires mar./abr. 2007
La embolización septal con alcohol está indicada en todos los pacientes sintomáticos con miocardiopatía hipertrófica y gradiente significativo
José M. GabayMTSAC (Agonista), Alejandro HitaMTSAC (Antagonista)
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
Agonista
José M. Gabay
Para fundamentar la afirmación que motiva esta controversia es necesario conocer inicialmente algunas características fisiopatológicas de la enfermedad. Se sabe que la miocardiopatía hipertrófica obstructiva (MCHO) es una alteración primaria del músculo cardíaco que se caracteriza por hipertrofia ventricular asimétrica del ventrículo izquierdo acompañada por obstrucción dinámica del tracto de salida, una entidad de transmisión hereditaria en la que, de acuerdo con su expresión genética, los portadores pueden presentar muerte súbita o evolucionar a la insuficiencia cardíaca. (1) En estos pacientes, el área a nivel del tracto de salida del ventrículo izquierdo se encuentra considerablemente disminuida; aproximadamente el 25% presentan un gradiente dinámico en el tracto de salida del ventrículo izquierdo (TSVI) causado por los efectos combinados de una eyección ventricular rápida, un TSVI disminuido asociado con la presencia de un movimiento anterior sistólico de la válvula mitral (MAS). (2)
Respecto de su expresión clínica, los portadores pueden presentar a cualquier edad episodios de dolor precordial, disnea, palpitaciones y/o síncope. La muerte súbita constituye la complicación más grave y ocurre con una incidencia anual del 2% al 6%.
El tratamiento con betabloqueantes, bloqueantes del calcio o antiarrítmicos como la disopiramida es la estrategia inicial, con el objetivo primario de disminuir el gradiente y con ello los síntomas, sin un efecto claro en la sobrevida.
Pero el gradiente en sí mismo es un marcador pronóstico de sobrevida a largo plazo, tal como lo demuestra el estudio de Maron y colaboradores (3) (Figura 1).
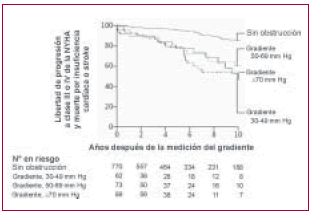
Fig. 1. A menor gradiente, mayor probabilidad de sobrevida libre de eventos a largo plazo. (Tomado de ref. 3).
La miotomía/miectomía quirúrgica se ha realizado por más de 40 años en los pacientes refractarios al tratamiento médico (4-6) y varios centros la tomaron como tratamiento de elección de esta entidad. (5-7) Con ella se obtiene un alivio de los síntomas al lograr disminuir el gradiente, lo cual no sólo mejora la calidad de vida, sino que quizás también altera la historia natural de la enfermedad. Se han publicado tasas de sobrevida a los 5 y los 10 años luego de miotomía/ miectomía del 95% y del 83%, respectivamente. (8)
De todos modos, después de esta intervención se debe continuar con el tratamiento médico para un mejor y más completo control de los síntomas.
Un tratamiento alternativo ha sido la estimulación bicameral con la intención de disminuir la severidad de la obstrucción a nivel del TSVI. Si bien los resultados iniciales fueron alentadores, (9) estudios aleatorizados y controlados aportaron evidencia contradictoria, con reducción incompleta del gradiente, así como una pérdida objetiva de la mejoría clínica en el seguimiento. (10, 11) Un estudio que comparó la cirugía con la estimulación bicameral con puntos finales hemodinámicos y de tolerancia al ejercicio ha demostrado que la cirugía otorga un beneficio mayor que la estimulación secuencial bicameral. (12)
Sigwart, (13) en 1995, fue el primero en describir el efecto de la oclusión y posterior embolización con etanol absoluto del ramo perforante septal en el gradiente de presiones en el TSVI en la MCHO (ASPC). En forma simultánea, dos centros de Alemania comunicaron su experiencia en varios cientos de pacientes. El grupo de Gietzen y colaboradores denominó a esta técnica ablación transcoronaria de la hipertrofia septal (transcoronary ablation of septal hypertrophy [TASH]). (14)
La experiencia más grande en los Estados Unidos la tiene el grupo del Colegio de Medicina de Baylor en Houston, (15) mientras que en Europa el registro alemán de la ASPC ha comunicado un número importante de casos. (16)
En la actualidad, esta técnica se encuentra difundida en todo el mundo, con unos 3.000 pacientes comunicados, según una revisión recientemente publicada. (17)
Pero el problema que se nos plantea es a quiénes y en qué momento se les debe indicar este procedimiento. Cuando nos encontramos con pacientes que a pesar de estar con una medicación adecuada persisten sintomáticos, tenemos la posibilidad de intervenir mecánicamente y así realizar el intento de disminuir la severidad del gradiente, ya que se sabe que esta disminución se acompaña de una mejoría de los síntomas y, como hemos visto, de un aumento en la sobrevida.
La ablación septal percutánea con alcohol (ASPC) surge como una alternativa menos invasiva que la cirugía y de resultados comparables. Se trata de un procedimiento que se realiza por vía percutánea mediante el cual se administra etanol absoluto para producir un infarto controlado del septum interventricular basal (Figura 2), tendiente a disminuir el espesor de éste. El resultado final se expresa en una reducción del gradiente de presiones en el TSVI. (14, 18)

Fig. 2. Resonancia magnética nuclear con gadolinio. Defecto de perfusión a nivel del septum basal. Hospital Italiano de Buenos Aires.
La caída del gradiente se debe inicialmente a un deterioro en la contracción del septum basal, pero posteriormente continúa disminuyendo por un adelgazamiento y fibrosis a este nivel. Este proceso lleva a un aumento en los diámetros del ventrículo izquierdo, caída de la excursión septal, disminución de la insuficiencia mitral y, por lo tanto, la subsiguiente remodelación ventricular. (19)
Sin embargo, hay controversia respecto de la selección correcta de los pacientes, así como un entrenamiento inadecuado por parte de los intervencionistas. Esto ha motivado que algunos grupos con vasta experiencia en el manejo de esta miocardiopatía hayan sugerido que esta técnica debería indicarse sólo en aquellos pacientes con comorbilidades que aumenten el riesgo quirúrgico. (20)
¿Pero cómo seleccionamos adecuadamente a los candidatos? Inicialmente uno debiera indicar este procedimiento a aquellos pacientes que se encuentren refractarios al tratamiento médico, con síntomas de insuficiencia cardíaca (clase funcional III), con hipertrofia septal asimétrica confirmada por ecografía, con el clásico movimiento anterior de la válvula mitral (MAS) y que en el registro Doppler se compruebe un gradiente en reposo de ≥ 30 mm Hg o ≥ 60 mm Hg luego de ser provocado (p. ej., con un extraestímulo, maniobra de Valsalva, ejercicio, etc.).
El segundo punto importante para tener en cuenta es cómo debemos efectuar el procedimiento, si en realidad la ASPC sólo debe estar limitada al subgrupo de pacientes descartados de cirugía o si, por el contrario, se trata de una alternativa válida a la cirugía. Desde su introducción, la ASPC ha tenido modificaciones que han llevado a una disminución significativa en la morbimortalidad, como veremos más adelante.
Este procedimiento se lleva a cabo con las características generales de una intervención coronaria percutánea, pero teniendo en cuenta lo siguiente:
1. Una vez realizada la coronariografía, se obtienen los datos anatómicos respecto de las ramas perforantes septales (el grado de desarrollo, la magnitud del territorio irrigado, la presencia de colaterales, etc.). Pero además podemos identificar la eventual presencia de lesiones coronarias obstructivas, hecho que probablemente nos lleve a descartar el procedimiento en estos pacientes.
2. Se debe colocar un catéter electrodo de marcapasos en el ventrículo derecho, ya que aproximadamente el 20-30% de los pacientes presentan BAV transitorios durante la ablación. En contraste con la cirugía, la ASPC habitualmente provoca un bloqueo de rama derecha. (2)
3. A continuación se prosigue con las etapas de una angioplastia coronaria convencional, heparinización completa, catéter guía, cuerda 0,014", con la que se canaliza en forma selectiva el primer ramo septal o en su defecto el de mayor desarrollo adyacente (se debe evitar el primer ramo septal si es de pequeño calibre y recorrido, ya que habitualmente brinda abundantes colaterales al sistema venoso). Sobre la cuerda se avanza un balón denominado over the wire (OTW) de 1,5 o 2,0 mm de diámetro. Una vez posicionado el balón, se insufla hasta ocluir el ramo deseado con el propósito de eliminar el flujo y evitar la eventual efusión retrógrada. Luego se retira la cuerda, por la luz del balón se inyecta contraste para opacar el territorio distal del ramo comprometido. Éste es un momento muy importante del procedimiento, ya que es cuando se deben evaluar el monto de miocardio en riesgo, las características dinámicas (magnitud de la caída del gradiente), presencia de colaterales hacia otros territorios coronarios, etc. Es aquí donde el eco-Doppler y la experiencia del operador tienen un papel determinante, dado que no se debe continuar si no se observan cambios significativos en el gradiente (dato que también se puede obtener en forma invasiva con medición de presiones simultáneas entre el ventrículo izquierdo y la aorta), pero más aún si se observan trastornos de la motilidad en un territorio extenso que expresa el potencial infarto que puede ocasionar la alcoholización. Es probable que la utilización de eco de contraste haya ayudado a una mejor identificación del territorio comprometido con la consecuente disminución de complicaciones.
4. Previo a decidir la administración del alcohol se debe constatar que el gradiente disminuya en por lo menos un 30%. Habitualmente, la caída es de un 50% o desaparece por completo, tanto el basal como el provocado; generalmente ocurre al minuto de mantener inflado el balón y habiendo inyectado sustancia de contraste. A continuación se inicia la infusión de alcohol absoluto (etanol al 96%), entre 1 y 4 ml, en forma lenta ya que se ha demostrado que la incidencia de bloqueo AV completo se relaciona entre otras cosas con la velocidad de administración.
5. Una vez finalizado el procedimiento, el paciente permanece internado 48 horas en la unidad de cuidados intensivos.
La ASPC se cataloga como exitosa cuando se obtiene una reducción del gradiente en el laboratorio de hemodinamia y se logra un incremento de la creatincinasa como expresión del tamaño del infarto [aproximadamente 1.000 UI, (17) lo que equivale a un área de necrosis del 20% del tamaño del septum o a un 3-10% de la masa del ventrículo izquierdo].
En ocasiones es común observar una disminución progresiva del gradiente en los 6 a 12 meses subsiguientes, momento en que llega a alcanzar el mismo resultado que la cirugía. En otras situaciones se puede obtener una caída del gradiente con un comportamiento bimodal, o sea, una disminución inicial, seguida de un aumento de prácticamente un 50% al día siguiente, con una posterior caída definitiva en los meses siguientes. Esta característica se debería a que una vez producido el infarto éste se acompaña de un proceso inflamatorio con edema intersticial, lo cual lleva a una nueva disminución en el TSVI. Finalmente, una vez consolidada la cicatriz, con la remodelación del septum y del ventrículo izquierdo se obtiene el descenso definitivo del gradiente sin una caída importante en la fracción de eyección del ventrículo izquierdo.
La mejoría de los síntomas y, por lo tanto, de la calidad de vida, es inmediata en la mayoría de los pacientes, con una disminución de la clase funcional (la mayor parte en CF I) y un aumento de la tolerancia al ejercicio y del consumo de oxígeno.
Las complicaciones son relativamente bajas; entre ellas, la mortalidad intraprocedimiento se encuentra en el 0-5%, (17) la mayoría a causa de disección de la arteria descendente anterior, taponamiento cardíaco o shock cardiogénico. La complicación más frecuente es el bloqueo auriculoventricular, que según las series iniciales era cercana al 20-30% y actualmente es de alrededor del 10%. (17) Probablemente se deba a una identificación correcta del monto de miocardio comprometido, a la utilización de balones de mayor diámetro y, como mencionamos, a la velocidad, así como al volumen total del alcohol administrado.
Sin embargo, se discute si el éxito obtenido precozmente en la ASPC se mantiene en el tiempo, especialmente si se coteja con los resultados alcanzados con la miotomía/miomectomía. Aunque hay pocos estudios que comparen directamente la cirugía con la ASPC, y ninguno de ellos es aleatorizado, los ensayos muestran resultados semejantes, aunque quizás la miectomía consiga una reducción inicial mayor en el gradiente en el TSVI.
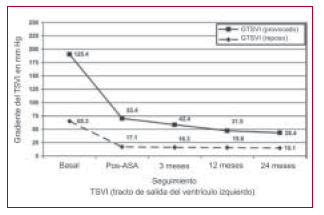
Al observar la condición clínica de los pacientes sometidos a una ASPC, vemos que el gradiente se mantiene menor de 20 mm Hg en un seguimiento a 2 años (Figura 3); existen datos de que estos valores se mantienen más allá de los 5 años. La tolerancia al ejercicio, la clase funcional o la función diastólica sufren una evolución semejante a la del gradiente.
Fig. 3. En el gráfico puede observarse la caída tanto del gradiente en reposo como el provocado en forma aguda y cómo se mantiene en el tiempo. (Tomado de ref. 17).
Si analizamos la mortalidad inicial, así como la evolución alejada, vemos que los datos son comparables.
Hasta el momento no se conoce cuál es el impacto real en la incidencia de muerte súbita, ya que hay quienes sostienen que al provocar una cicatriz la ASPC está sumando un sustrato arritmogénico en una enfermedad que ya lo tiene. En contraste, se han realizado estudios en los que se intentó inducir arritmias ventriculares por reentrada sin éxito. Estos datos son importantes al decidir este tratamiento en una persona joven.
Como conclusión y luego de lo expresado, podríamos afirmar sin lugar a dudas que la ablación septal percutánea es eficaz en la reducción del gradiente en el TSVI en la miocardiopatía hipertrófica y que, en asociación con ello, produce una notoria mejoría en los síntomas de la enfermedad y probablemente una mejoría en la sobrevida.
Es por ello que es una técnica efectiva y segura en los pacientes portadores de esta enfermedad que se encuentren sintomáticos. Pero una vez más quiero reiterar que estos resultados dependen de la selección correcta de los pacientes por tratar, acompañada de una curva de aprendizaje adecuada del grupo intervencionista. Si bien los datos del seguimiento alejado no superan los 10 años, pareciera que los resultados iniciales se mantienen en el tiempo. Se requieren estudios aleatorizados comparados con la miotomía/miectomía para responder esta inquietud.
BIBLIOGRAFÍA
1. Maron BJ. Hypertrophic cardiomyopathy: a systematic review. JAMA 2002;287:1308-20.
2. Maron BJ, McKenna WJ, Danielson GK, Kappenberger LJ, Kuhn HJ, Seidman CE, et al; American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents; European Society of Cardiology Committee for Practice Guidelines. American College of Cardiology/European Society of Cardiology Clinical Expert Consensus Document on Hypertrophic Cardiomyopathy. A report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. Eur Heart J 2003;24:1965-91.
3. Maron MS, Olivotto I, Betocchi S, Casey SA, Lesser JR, Losi MA, et al. Effect of left ventricular outflow tract obstruction on clinical outcome in hypertrophic cardiomyopathy. N Engl J Med 2003; 348:295-303.
4. Morrow AG, Brockenbrough EC. Surgical treatment of idiopathic hypertrophic subaortic stenosis: technic and hemodynamic results of subaortic ventriculomyotomy. Ann Surg 1961;154:181-9.
5. Kirklin JW, Ellis FH Jr. Surgical relief of diffuse subvalvular aortic stenosis. Circulation 1961;24:739-42.
6. Schulte HD, Bircks WH, Loesse B, Godehardt EA, Schwartzkopff B. Prognosis of patients with hypertrophic obstructive cardiomyopathy after transaortic myectomy. Late results up to twenty-five years. J Thorac Cardiovasc Surg 1993;106:709-17.
7. Spirito P, Seidman CE, McKenna WJ, Maron BJ. The management of hypertrophic cardiomyopathy. N Engl J Med 1997;336:775-85.
8. Woo A, Williams WG, Choi R, Wigle ED, Rozenblyum E, Fedwick K, et al. Clinical and echocardiographic determinants of long-term survival after surgical myectomy in obstructive hypertrophic cardiomyopathy. Circulation 2005;111:2033-41.
9. Fananapazir L, Epstein ND, Curiel RV, Panza JA, Tripodi D, McAreavey D. Long-term results of dual-chamber (DDD) pacing in obstructive hypertrophic cardiomyopathy. Evidence for progressive symptomatic and hemodynamic improvement and reduction of left ventricular hypertrophy. Circulation 1994;90:2731-42.
10. Nishimura RA, Trusty JM, Hayes DL, Ilstrup DM, Larson DR, Hayes SN, et al. Dual-chamber pacing for hypertrophic cardiomyopathy: a randomized, double-blind, crossover trial. J Am Coll Cardiol 1997;29:435-41.
11. Maron BJ, Nishimura RA, McKenna WJ, Rakowski H, Josephson ME, Kieval RS. Assessment of permanent dual-chamber pacing as a treatment for drug-refractory symptomatic patients with obstructive hypertrophic cardiomyopathy. A randomized, double-blind, crossover study (M-PATHY). Circulation 1999;99:2927-33.
12. Ommen SR, Nishimura RA, Squires RW, Schaff HV, Danielson GK, Tajik AJ. Comparison of dual-chamber pacing versus septal myectomy for the treatment of patients with hypertropic obstructive cardiomyopathy: a comparison of objective hemodynamic and exercise end points. J Am Coll Cardiol 1999;34:191-6.
13. Sigwart U. Non-surgical myocardial reduction for hypertrophic obstructive cardiomyopathy. Lancet 1995;346:211-4.
14. Gietzen FH, Leuner CJ, Raute-Kreinsen U, Dellmann A, Hegselmann J, Strunk-Mueller C, et al. Acute and long-term results after transcoronary ablation of septal hypertrophy (TASH). Catheter interventional treatment for hypertrophic obstructive cardiomyopathy. Eur Heart J 1999;20:1342-54.
15. Lakkis NM, Nagueh SF, Dunn JK, Killip D, Spencer WH 3rd. Nonsurgical septal reduction therapy for hypertrophic obstructive cardiomyopathy: one-year follow-up. J Am Coll Cardiol 2000;36:852-5.
16. Kuhn H, Seggewiss H, Gietzen FH, Boekstegers P, Neuhaus L, Seipel L. Catheter-based therapy for hypertrophic obstructive cardiomyopathy. First in-hospital outcome analysis of the German TASH Registry. Z Kardiol 2004;93:23-31.
17. Alam M, Dokainish H, Lakkis N. Alcohol septal ablation for hypertrophic obstructive cardiomyopathy: a systematic review of published studies. J Interv Cardiol 2006;19:319-27.
18. Flores-Ramirez R, Lakkis NM, Middleton KJ, Killip D, Spencer WH 3rd, Nagueh SF. Echocardiographic insights into the mechanisms of relief of left ventricular outflow tract obstruction after nonsurgical septal reduction therapy in patients with hypertrophic obstructive cardiomyopathy. J Am Coll Cardiol 2001;37:208-14.
19. van Dockum WG, Beek AM, ten Cate FJ, ten Berg JM, Bondarenko O, Gotte MJ, et al. Early onset and progression of left ventricular remodeling after alcohol septal ablation in hypertrophic obstructive cardiomyopathy. Circulation 2005;111:2503-8.
20. Maron BJ, Dearani JA, Ommen SR, Maron MS, Schaff HV, Gersh BJ, et al. The case for surgery in obstructive hypertrophic cardiomyopathy. J Am Coll Cardiol 2004;44:2044-53.
Antagonista
Alejandro Hita
La respuesta a esta controversia tiene dos aspectos que es necesario analizar; el primero es que la toma de decisiones terapéuticas en la práctica médica tiene sus fundamentos en algunas reglas generales que son excluyentes: tener un firme basamento fisiopatológico, una evidencia médica que la sustente, no provocar daño. El segundo es que en toda decisión terapéutica deberíamos contestarnos con claridad los siguientes puntos: ¿a quién trato?, ¿por qué lo trato? y ¿cómo lo trato? Analizando la problemática planteada bajo esta óptica, la respuesta a la controversia es "no" y su fundamento es lo que expondré como antagonista en los siguientes párrafos.
Aspectos fisiopatológicos: una cuestión inicial sería analizar las causas de muerte en los pacientes con miocardiopatía hipertrófica (MCH) y el papel del componente obstructivo dinámico en esta entidad. En el estudio epidemiológico más importante publicado hasta el presente sobre 744 pacientes con MCH pertenecientes a una población no seleccionada y con un seguimiento a más de 20 años, Maron y colaboradores (1) demuestran una mortalidad menor del 1%/año. De los 744 pacientes con MCH fallecieron 125 (17%), 3 muertes ocurrieron como complicaciones en el perioperatorio de la cirugía miotomia-miectomia, 36 muertes no adjudicables a la patología referida y las 86 restantes relacionadas con la MCH de la siguiente forma: 44 (51,16%) en forma súbita (MS), 31 (36,04%) por insuficiencia cardíaca refractaria y 11 (12,79%) secundarias a stroke (Tabla 1).
Tabla 1. Parámetros clínicos y demográficos y modo de muerte relacionada con la MCH en 86 pacientes

Como puede observarse, la muerte súbita es la principal causa de muerte en esta entidad, no se limita solamente al grupo etario de baja edad y no se demuestra la existencia de correlación entre la presencia del componente obstructivo y la muerte súbita.
Esta misma conclusión se repite en el trabajo más importante que se ha publicado sobre la evolución clínica de los pacientes con MCH y componente obstructivo. (2) En este estudio, sobre 1.101 pacientes con MCH se analizó una subpoblación de 273 pacientes (25%) que presentaban un gradiente instantáneo en reposo superior a 30 mm Hg en el tracto de salida del VI determinado por Doppler continuo. Si bien los pacientes con obstrucción presentaron en el seguimiento mayor probabilidad de muerte relacionada con la MCH que los pacientes sin obstrucción (riesgo relativo 2,0; IC 95%) y mayores probabilidades de tener peor clase funcional o muerte debido a IC y stroke, el valor predictivo positivo de la obstrucción del tracto de salida para la MS fue sólo del 7% y como conclusión los autores consideran que éste es un factor de riesgo menor para MS y que las terapéuticas dirigidas al alivio de la obstrucción deben limitarse sólo a pacientes muy sintomáticos (clase funcional III-IV) que no han respondido a la terapéutica médica.
Por otro lado, la MCH es una patología que tiene una serie de alteraciones fisiopatológicas, sustrato de su evolución y pronóstico; el análisis de distintas publicaciones nos demuestra que es una entidad altamente arritmógena (3) y que en gran parte esta predisposición se relaciona con múltiples focos de necrosis y fibrosis (4) con múltiples mecanismos isquémicos en juego, en parte relacionados con la pérdida de los mecanismos fisiológicos de reserva vasodilatadora coronaria (5) y un pronóstico adverso cuando la MCH se asocia con enfermedad coronaria. (6) Otra evolución frecuente de esta entidad en su camino final a la muerte es la IC refractaria, sobre todo en el grupo etario de mayor edad (7) con una remodelación adversa y dilatación ventricular con deterioro de la función contráctil del VI, función que suele estar alterada con más frecuencia de lo que inicialmente se presumió. (8)
La implementación de una terapéutica como la alcoholización septal, cuyo basamento radica en la generación de un "infarto programado" (no necesariamente controlado), con la creación de una escara subsecuente y el agregado de pérdida de masa miocárdica, no parece ser la mejor opción para resolver la problemática de esta patología, al menos desde el punto de vista fisiopatológico. En primer lugar, no trata la causa de la enfermedad; por lo tanto, es un recurso terapéutico paliativo, no protege de la primera causa de muerte en esta entidad, la MS, sino que por el contrario gatilla muchos de los mecanismos comentados en el párrafo precedente que han demostrado que se encuentran relacionados con una mala evolución de esta entidad, y mediante la generación de un área de fibrosis podría favorecer y/o prolongar en los diferentes grupos etarios el riesgo de MS. De hecho, algunos autores han comunicado la presencia de arritmias graves vinculadas con el procedimiento. (9)
Evidencia médica: la medicina contemporánea y la cardiología en particular han optimizado sus resultados al basar su toma de decisiones en la evidencia médica, ¿cuál es entonces la evidencia que sugiere la utilización de este recurso terapéutico en la MCHO?
Lamentablemente, aún no se dispone de un trabajo aleatorizado controlado que demuestre los beneficios de esta terapéutica contra otras consideradas estándar de calidad como la miomectomía quirúrgica. (10) Los datos existentes de ablación septal con alcohol sólo refieren información con seguimientos no mayores de 6 o 7 años en una entidad en la que la remodelación, especialmente luego de la generación de un infarto, cumple un papel de gran importancia en la evolución alejada. Sin embargo, y a pesar de la falta de evidencia descripta y la ausencia de un basamento fisiopatológico sólido, el número de ablaciones con alcohol realizadas en los últimos años luego de su descripción original en 1995 es de 3.000, (11) lo cual excede con mucho el número de miomectomías quirúrgicas realizadas en los últimos 40 años; esto sugiere una falla en la selección de los pacientes o un margen de escasa prudencia a la hora de la toma de decisiones.
No provocar daño: si somos conscientes de nuestras limitaciones, tendremos la mitad de nuestra decisión bien tomada. Probablemente no disponemos de equipos quirúrgicos con el suficiente entrenamiento en la técnica de la miomectomía quirúrgica y en consecuencia es lógico que su indicación en un paciente concreto no sea una decisión sencilla; esto no es criticable, pero generar indicaciones frecuentes de ablación por alcoholización no es la respuesta correcta a esta problemática. Si observamos los resultados de centros entrenados en ambos procedimientos, podemos ver datos como los de la Tabla 2. (12)
Tabla 2. Comparación entre la miomectomía septal y la ablación con alcohol
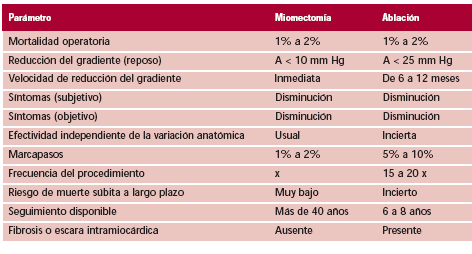
Es claro, como lo establece el consenso europeoamericano del año 2003, que al presente la miomectomía septal continúa siendo la terapéutica estándar para los pacientes con MCHO, síntomas severos y refractariedad al tratamiento médico. (12)
El segundo aspecto que he planteado en esta controversia se basa sobre las preguntas que deberíamos responder una vez que hemos decidido que algo tenemos que hacer con nuestro paciente y en este sentido es importante repasar los siguientes ítems:
¿A quién trato? Como fuera expresado previamente, se trata de una subpoblación de pacientes muy pequeña dentro del marco de la MCH; estos pacientes deben estar muy bien elegidos, es decir, cumplir absolutamente y en forma estricta con todos los criterios de selección: sintomáticos en clase funcional III o IV a pesar de un tratamiento médico adecuado (betabloqueantes, antagonistas cálcicos y disopiramida), claro componente obstructivo, gradiente mínimo de reposo tomado con eco-Doppler continuo de 30 mm Hg y si es con apremio, de 50 mm Hg. El apremio aconsejado es el ejercicio; (12) distintos grupos han seleccionado a sus pacientes sobre la base de otros apremios, como el nitrito de amilo o la dobutamina, con las graves dificultades que ello acarrea ya que no representa la verdadera fisiopatología de la MCH y, por ende, se torna aún más dificultosa la obtención de resultados adecuados. (13) El incumplimiento de estas pautas ha sido uno de los motivos del incremento en el número de procedimientos terapéuticos de ablación realizados.
¿Por qué lo trato? En el momento actual y con la evidencia disponible debemos tener en claro que no existe una terapéutica específica para la MCH; por lo tanto, como con todo tratamiento paliativo, debemos ser mucho más exigentes en la evaluación de sus resultados. La ausencia de información referida a un beneficio concreto en la sobrevida de nuestros pacientes tratados nos deja centrados en el segundo objetivo de nuestra toma de decisiones: la mejoría de la calidad de vida; ésta es la razón por la que la tranquilidad de la toma de decisiones descansa en la selección adecuada de los pacientes ya refractarios a toda terapéutica.
¿Cómo lo trato? Llegados a este punto, resulta indiscutible que la terapéutica gold standard continúa siendo la miomectomía quirúrgica. Nuestra dificultad en disponer de grupos quirúrgicos entrenados en este procedimiento no debe hacer que olvidemos las múltiples dificultades que atraviesan operadores no expertos en la ablación septal con alcohol, generando un infarto, que como expresáramos es programado, pero lamentablemente no controlado. En este sentido es de destacar la variabilidad en la distribución de las arterias perforantes septales (14) con arterias que no irrigan el segmento septal deseado para la terapéutica o que irrigan áreas alejadas del segmento referido con los riesgos consecuentes; éste es otro de los tantos problemas aún no resueltos con la técnica de ablación septal con alcohol, incluso con la ayuda de la utilización de eco de contraste.
Conclusiones: podríamos concluir diciendo con claridad que no todos los pacientes con MCHO sintomáticos con gradiente significativo y refractarios al tratamiento son pasibles de la ablación septal con alcohol, en primer lugar porque las bases fisiopatológicas y la evidencia médica, como hemos visto, no sustentan esta toma de decisiones y en segundo lugar porque muchos pacientes responden bien a un manejo médico adecuado (en el 60% a 80% de los casos), porque la anatomía de su corazón no lo permite (anatomía de las perforantes, espesor septal menor de 18 mm o mayor de 30 mm, etc.), por presentar anomalías frecuentemente asociadas en la MCH como alteraciones mitrales o de músculo papilar que requieren corrección quirúrgica y, finalmente, porque en toda decisión médica la selección adecuada de una decisión surge de elegir el mejor método para el mejor paciente. De esta forma, parece correcto manejarse con prudencia ante esta nueva opción terapéutica y su rédito terapéutico será mucho mejor aprovechado cuando se aplique en pacientes que han sido cuidadosamente seleccionados y que sus condiciones de comorbilidad y mayor edad así lo justifiquen, en tanto que no es aconsejable en ningún caso en las poblaciones de pacientes jóvenes. En otras palabras, que la alcoholización septal represente posiblemente una opción terapéutica en una población seleccionada de pacientes y como alternativa a la cirugía no significa que hoy se pueda considerarla una práctica primaria y estándar de estrategia terapéutica.
BIBLIOGRAFÍA
1. Maron BJ, Olivotto I, Spirito P, Casey SA, Bellone P, Gohman TE, et al. Epidemiology of hypertrophic cardiomyopathy-related death: revisited in a large non-referral-based patient population. Circulation 2000;102:858-64.
2. Maron MS, Olivotto I, Betocchi S, Casey SA, Lesser JR, Losi MA, et al. Effect of left ventricular outflow tract obstruction on clinical outcome in hypertrophic cardiomyopathy. N Engl J Med 2003; 348:295-303.
3. Boriani G, Biffi M, Martignani C. Clinical and therapeutic implications of troponin elevation in cardiac arrest. Am J Cardiol 2004;94:1478.
4. Roberts R, Sigwart U. Current concepts of the pathogenesis and treatment of hypertrophic cardiomyopathy. Circulation 2005; 112:293-6.
5. Cecchi F, Olivotto I, Gistri R, Lorenzoni R, Chiriatti G, Camici PG. Coronary microvascular dysfunction and prognosis in hypertrophic cardiomyopathy. N Engl J Med 2003;349:1027-35.
6. Sorajja P, Ommen SR, Nishimura RA, Gersh BJ, Berger PB, Tajik AJ. Adverse prognosis of patients with hypertrophic cardiomyopathy who have epicardial coronary artery disease. Circulation 2003; 108:2342-8.
7. Harris KM, Spirito P, Maron MS, Zenovich AG, Formisano F, Lesser JR, et al. Prevalence, clinical profile, and significance of left ventricular remodeling in the end-stage phase of hypertrophic cardiomyopathy. Circulation 2006;114:216-25.
8. Chejtman D, Baratta S, Fernández H, Marani A, Ferroni F, Bilabao J y col. Valor clínico del análisis de la fase sistólica de la contracción ventricular con Doppler tisular en la discriminación de hipertrofia fisiológica de formas patológicas. Rev Argent Cardiol 2006;74:129-35.
9. Maron BJ, Shen WK, Link MS, Epstein AE, Almquist AK, Daubert JP, et al. Efficacy of implantable cardioverter-defibrillators for the prevention of sudden death in patients with hypertrophic cardiomyopathy. N Engl J Med 2000;342:365-73.
10. Yacoub MH. Surgical versus alcohol septal ablation for hypertrophic obstructive cardiomyopathy: the pendulum swings. Circulation 2005;112:450-2.
11. Maron BJ. Role of alcohol septal ablation in treatment of obstructive hypertrophic cardiomyopathy. Lancet 2000;355:425-6.
12. Maron BJ, McKenna WJ, Danielson GK, Kappenberger LJ, Kuhn HJ, Seidman CE, et al; Task Force on Clinical Expert Consensus Documents. American College of Cardiology; Committee for Practice Guidelines. European Society of Cardiology. American College of Cardiology/ European Society of Cardiology clinical expert consensus document on hypertrophic cardiomyopathy. A report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. J Am Coll Cardiol 2003;42:1687-713.
13. Nagueh SF, Lakkis NM, He ZX, Middleton KJ, Killip D, Zoghbi WA, et al. Role of myocardial contrast echocardiography during nonsurgical septal reduction therapy for hypertrophic obstructive cardiomyopathy. J Am Coll Cardiol 1998;32:225-9.
14. Singh M, Edwards WD, Holmes DR Jr, Tajil AJ, Nishimura RA. Anatomy of the first septal perforating artery: a study with implications for ablation therapy for hypertrophic cardiomyopathy. Mayo Clin Proc 2001;76:799-802.
RÉPLICA DEL AGONISTA
Estoy completamente de acuerdo con el Dr. Hita en que la toma de decisiones terapéuticas en medicina tiene que estar basada sobre el conocimiento de los mecanismos fisiopatológicos de la enfermedad, una evidencia sustentable y, obviamente, en no provocar daño. También coincidimos en que la mayoría de los pacientes portadores de una miocardiopatía hipertrófica obstructiva se controlan con un tratamiento médico adecuado, pero, ¿qué es lo que debemos hacer en aquellos que no lo logran?
Aquí probablemente disentimos, ya que no sólo debemos intentar mejorar el pronóstico de vida, sino también la calidad de vida. ¿Cómo debemos encarar la situación cuando a pesar del tratamiento médico completo, los síntomas continúan y el eco-Doppler nos sigue informando un gradiente importante? Si bien la evidencia es variada, así como su interpretación, creo sin lugar a dudas que en este punto debemos actuar.
Y en este momento, cuando decidimos "intervenir", que tenemos la opción de la cirugía o el tratamiento endovascular. Es muy importante que el grupo sea multidisciplinario y acorde con su experiencia uno pueda indicar un procedimiento determinado.
Con respecto a la ablación septal percutánea (ASPC) implementada en el mundo hace más de una década (no es un procedimiento novedoso), ha demostrado que es una técnica eficaz y segura. Pero esta aseveración es correcta sólo si se realiza una selección adecuada de los pacientes y se cumple estricta mente con los criterios metodológicos, como lo he comentado.
Finalmente, en un futuro no muy lejano deberíamos contar con una evidencia de mayor peso, especialmente al momento de compararla con la cirugía, y quizás también asociada con otras intervenciones, con el objetivo claro de lograr un impacto en la sobrevida.
Dr. José M. Gabay
RÉPLICA DEL ANTAGONISTA
La prolija y minuciosa descripción del método de ASPC presentado por el Dr. Gabay no debe alejarnos del problema principal de la discusión, es decir, el criterio clínico por el cual decidimos la implementación de una terapéutica invasiva con riesgos. Tomando las palabras del agonista, que la complicación más grave en la MCHO es la muerte súbita, la incidencia de este fenómeno en trabajos poblacionales como el de Maron es sólo del 1% y la correlación con el componente obstructivo tiene un valor predictivo positivo de sólo el 7%, por lo que el componente obstructivo se considera un factor de riesgo menor en la estratificación de riesgo de esta enfermedad.
Que se hayan comunicado 3.000 procedimientos de ASPC en unos pocos años en relación con aproximadamente un tercio de procedimientos indicados con la técnica gold standard de la miomectomía quirúrgica en los últimos 40, sólo expresa un incremento pronunciado en la indicación.
La necesidad de una selección correcta de los pacientes es lógica en un procedimiento que tiene limitaciones importantes a la hora de su realización, entre las que podemos contar, según palabras del propio agonista, una mortalidad intraprocedimiento del 0% al 5% en una patología con mortalidad por muerte súbita del 1% en estudios poblacionales mayores, y con datos de seguimientos de tan sólo 2 a 7 años en una patología con remodelación alejada importante y evolución a la insuficiencia cardíaca; estos aspectos nos dejan más incertidumbres que certezas y nos enfrenta con la necesidad de analizar el segundo punto de beneficio teórico, el relacionado con la mejoría de los síntomas.
La ASPC es una técnica, como expresáramos, de infarto programado pero no controlado y la estandarización del método para obtener el resultado deseado depende en gran medida de la experiencia del centro tratante y de variables anatómicas y funcionales no fácilmente predecibles.
Comparto en pleno gran parte de las conclusiones del Dr. Gabay en el sentido de que se deben seleccionar en forma muy precisa los pacientes para este tipo de procedimientos, el grupo intervencionista debe tener un alto grado de entrenamiento, se requieren aún estudios aleatorizados comparativos con la miotomía/miomectomía para responder nuestras dudas. Es decir, este procedimiento no es para todos los pacientes sintomáticos con MCHO y gradiente significativo.
Dr. Alejandro Hita














