Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.76 n.3 Buenos Aires mayo/jun. 2008
Reubicación de los vasos del cuello y exclusión endovascular de las disecciones y los aneurismas del arco aórtico
Carlos A. Deluca†, 1, Fernando G. Chiminella1, Ramón Gomes Marques1, Alejandro Goldsmit1, Marcelo Cardone1, Marcelo O. Bettinotti MTSAC , 1, Carlos SztejfmanMTSAC , 1, Aldo Pais2, José L. Aquino2, Fabián Donini2, Antonio Piazza2, Adriano Malusardi2
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
† Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
1 Departamento de Cardiología Intervencionista
2 Departamento de Cirugía Vascular, Instituto Médico de Alta Complejidad-Sanatorio Güemes - Clínica Independencia. Buenos Aires, Argentina
Dirección para separatas: Dr. Carlos A. Deluca Pje. Pernambuco 2494 "3" - (1417) Buenos Aires, Argentina Tel. 4957-6777 int 511 e-mail: carlosadeluca@yahoo.com.ar
Recibido: 06/08/2007
Aceptado: 28/01/2008
RESUMEN
El tratamiento endovascular de la aorta descendente le brinda a un grupo de pacientes seleccionados de alto riesgo una alternativa para resolver un problema grave de manera segura y efectiva.
Sólo el 15% de los enfermos tiene un cuello adecuado para el implante respetando la integridad de la arteria subclavia izquierda y su oclusión intencional origina en hasta un 30% isquemia del brazo, síndrome vertebrobasilar o leaks. Además, los pacientes que presentan compromiso del arco aórtico (extensión retrógrada de la disección, porque ésta se origina allí o por aneurisma de ese sector) constituyen una población aún más seleccionada y de mayor riesgo para el tratamiento quirúrgico habitual.
Entre noviembre de 2005 y diciembre de 2006 incluimos 10 pacientes que se presentaban con: 1) disecciones con compromiso de la arteria subclavia izquierda o retrodisecciones hacia el cayado aórtico (n = 7) y 2) aneurismas del cayado aórtico (n = 3). Fueron tratados dentro del período agudo (14 días), todos con un puntaje de riesgo anestésico (ASA) igual a 3 o mayor.
Se utilizó una técnica híbrida, de un solo acto en dos etapas (quirúrgica/endovascular) realizadas en el mismo día. En la fase quirúrgica no se requirió paro cardíaco, circulación extracorpórea ni hipotermia profunda y durante la etapa endovascular se utilizaron prótesis autoexpandibles y es aquí donde se notaron las dificultades técnicas que debieron sortearse para llevar adelante el implante.
Todos los procedimientos resultaron técnicamente exitosos.
Dos pacientes fallecieron, uno en el primer día (taponamiento cardíaco) otro por sepsis en el día 27.
No se registraron complicaciones neurológicas ni vasculares.
La técnica fue factible y efectiva, con una morbimortalidad adecuada para la población en estudio y similar a la de publicaciones con pacientes de las mismas características.
Palabras clave: Aneurisma; Aorta; Disección; Prótesis vascular; Cirugía torácica
Abreviaturas
PTFE Politetrafluoroetileno
TAC Tomografía axial computarizada
TBC Tronco braquiocefálico
SUMMARY
Replacement of Neck Vessels and Endovascular Exclusion of Aortic Arch Dissections and Aneurysms
Endovascular treatment of the descendant aorta is a safe and effective alternative to solve a severe condition in a selected group of high-risk patients.
In only 15% of patients the anatomical relations of the aneurysm neck with the left subclavian artery are adequate for the implant, and the incidence of arm ischemia, vertebrobasilar artery syndrome or leaks related to the left subclavian artery intentionally occluded reaches 30%. In addition, patients with compromise of the aortic arch (due to dissections or aneurysms of the aortic arch) are still a more selected high-risk population for surgical treatment.
Between November 2005 and December 2006 we included 10 patients with: 1) dissections with compromise of the left subclavian artery or dissections towards the aortic arch (n=7) and, 2) aneurisms of the aortic arch (n=3).
All patients had ASA class III or greater, and they were all treated during the acute phase (14 days).
A two-stage (surgical/endovascular) hybrid technique was performed during the same day. The surgical approach was carried out without the need for circulatory arrest, extracorporeal circulation, and deep hypothermia, but endovascular self-expanding stent-graft placement presented a few technical difficulties.
All procedures were technically successful.
Two patients died, one at day 1 (cardiac tamponade) and the other at day 27 (sepsis).
No neurologic or vascular complications were reported.
The procedure was feasible and effective, with morbidity and mortality rates according to the study population and similar to those reported in other studies performed on comparable patients.
Key words: Aneurysm; Aorta; Dissection; Vascular Prosthesis; Chest Surgery
INTRODUCCIÓN
El tratamiento endovascular de la aorta descendente le brinda a un grupo de pacientes seleccionados y de alto riesgo una alternativa para resolver de manera segura y efectiva un problema grave. (1, 2)
Para beneficiarse con esta variante terapéutica, los enfermos deben presentar en los exámenes tomográficos una anatomía favorable, es decir, un cuello libre de patología para el anclaje de la endoprótesis. Sólo entre el 5% y el 15% de las disecciones o aneurismas de la aorta descendente cumplen con el requisito de al menos 15 mm de cuello sano para el implante y por lo tanto el "mundo real" queda excluido de esta forma de tratamiento. (3, 4)
Para que se pueda incluir a un número mayor de pacientes, una forma de resolver el problema planteado es ocluir en forma programada la arteria subclavia izquierda con el dispositivo, lo cual tiene una incidencia de eventos no menor del 30% si se toman en cuenta las tres complicaciones más frecuentes: isquemia del brazo, fugas y síndrome vertebrobasilar por robo de la subclavia.
Y como si lo planteado fuera poco, las formaciones que se extienden hacia el arco o se originan primitivamente en él están clásicamente excluidas del tratamiento endovascular y requieren paro circulatorio, hipotermia profunda y circulación extracorpórea para la corrección quirúrgica.
Con esta trilogía en nuestra cabeza (minoría de enfermos con características anatómicas óptimas, un número considerable de complicaciones al ocluir en forma programada la arteria subclavia izquierda y extensiones al cayado aórtico), decidimos realizar el tratamiento de pacientes de esas características durante la fase aguda del síndrome aórtico (primeros 14 días desde el diagnóstico) con una técnica híbrida quirúrgica y endovascular, vista como un único procedimiento en dos actos en el mismo día, como alternativa para resolver el problema planteado.
MATERIAL Y MÉTODOS
Entre noviembre de 2005 y diciembre de 2006 tratamos 10 enfermos, nueve de sexo masculino, de entre 42 y 73 años (edad media 58 años). Todos presentaban factores comórbidos: enfermedad coronaria difusa con deterioro de la función ventricular (2 casos), diabetes mellitus (4), hipertensión (10), deterioro de la función renal sin requerimiento de hemodiálisis (creatinina sérica ≥ 2 mg/dl) (1) o enfermedad pulmonar obstructiva crónica (VEF1 ≤ 1 L) (4). El puntaje de riesgo anestésico (ASA) fue igual a 3 o mayor en todos los casos.
Como criterios de exclusión se plantearon los riesgos ASA 1 o 2, ausencia de riesgo cardiopulmonar y arterias femorales inadecuadas (de menos de 6 mm de diámetro).
Todos fueron tratados durante los primeros 14 días desde el diagnóstico (7), dentro de las primeras 48 horas.
La evaluación preoperatoria fue un examen tomográfico del cuello, el tórax y el abdomen, con contrate intravenoso y cortes cada 3 mm.
Los primeros siete pacientes se presentaron con disecciones del tipo B (tres agudas con falsa luz permeable y diámetro aórtico mayor de 4 cm y cuatro crónicas reagudizadas con aneurismas asociados mayores de 6 cm), relacionadas con compromiso del arco (retrodisección) o de la arteria subclavia izquierda, lo que no dejaba cuello adecuado para el implante.
Para estos casos se realizó una transposición parcial del arco aórtico, con revascularización con puentes de las arterias carótida y subclavia izquierdas, y luego se implantó la endoprótesis inmediatamente distal al tronco braquiocefálico (zona 1). (5)
En los siguientes tres casos, todos aneurismas del cayado aórtico, el procedimiento quirúrgico fue la transposición completa del arco aórtico con un bypass complejo desde la aorta ascendente y luego la liberación de la prótesis distal a éste (zona 0). En ningún caso se utilizó paro circulatorio, circulación extracorpórea o hipotermia profunda.
Todos los procedimientos se realizaron bajo anestesia general.
Se definió éxito técnico primario al implante de la endoprótesis con cobertura del sitio de entrada en el caso de las disecciones o exclusión completa del aneurisma, ausencia de fugas y supervivencia del paciente.
El protocolo de seguimiento incluyó además del examen clínico, la realización de TAC helicoidal al mes, a los 6 meses y al año.
Los hallazgos satisfactorios en las TAC fueron la ausencia de endoleak, migración, kinking, estenosis o trombosis de la prótesis endovascular, además de descartar la expansión del aneurisma o la trombosis total o parcial de la falsa luz en el caso de las disecciones.
Durante la intervención no realizamos eco transesofágico de rutina, aunque lo preferimos en los casos de reubicación completa debido a la exactitud con que debe ser liberada la prótesis.
El procedimiento se concibió como un único acto en dos etapas, cuyos detalles se describen a continuación.
Etapa quirúrgica (6-8) (Figura 1)

Fig. 1. Esquema que muestra las prótesis individualmente (A), luego de las anastomosis (B) y, por último, in situ (C).
Reemplazo total del arco aórtico
El abordaje de la aorta ascendente, el arco aórtico y los vasos del cuello se efectúa mediante esternotomía mediana. Se reparan el tronco braquiocefálico (TBC), la arteria carótida izquierda y la arteria subclavia izquierda extratorácica. Una vez identificados y reparados dichos vasos, previa heparinización y con clampeo parcial de la aorta ascendente, se procede a realizar la anastomosis proximal del bypass con una prótesis de Dacron "precoagulado" de 10 o 12 mm de diámetro según el diámetro de los vasos supraaórticos.
El primer vaso que se anastomosa es el TBC y es terminoterminal, con clampeo total, el cual debe ser lo más corto posible (en nuestra serie, el clampeo de los vasos del cuello, que implica isquemia cerebral, no excede los 5 minutos). Desde este bypass emergen en forma lateral dos prótesis de 6 u 8 mm de diámetro (confeccionadas previamente), hacia la arteria carótida izquierda y la arteria subclavia homolateral; la primera se anastomosa en forma terminoterminal y con la subclavia se efectúa una anastomosis terminolateral extratorácica luego de pasar por el primer espacio intercostal.
Una vez confeccionado este "nuevo arco aórtico" se ligan a nivel proximal el tronco braquiocefálico, las arterias carótida izquierda y subclavia izquierda.
La anastomosis proximal de la derivación de los vasos del cuello se marca previamente con material radioopaco en forma de O para identificar el sitio de liberación de la endoprótesis (Figura 2).

Fig. 2. La prótesis confeccionada. A. Antes de las anastomosis proximal y distales. B. In situ.
Reemplazo parcial del arco aórtico
En este caso, la derivación del arco se realiza en forma extraanatómica. Se abordan ambas arterias axilares por medio de incisiones en sendos pliegues deltopectorales y para acceder a la arteria carótida izquierda se realiza una cervicotomía homolateral.
Se confecciona un "túnel" en la cara anterior del tórax, por debajo del plano del músculo pectoral mayor, por donde se pasa una prótesis de PTFE anillada, de 6 u 8 mm de diámetro, que permite realizar un bypass entre ambas arterias axilares.
Una vez realizado, a partir de la prótesis que une las mencionadas arterias se realiza un bypass en forma de "Y" o de "T" invertida, con la arteria carótida izquierda, terminoterminal o terminolateral. También en este caso se debe tener en cuenta el tiempo de isquemia cerebral y ligar en forma proximal las arterias carótida y subclavias izquierdas.
Etapa endovascular (Figuras 3 y 4)
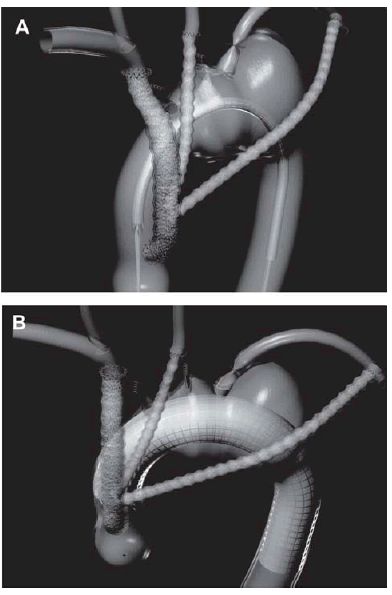
Fig. 3. Esquema que muestra las prótesis ya anastomosadas a la aorta y los vasos del cuello y el ascenso del endograft desde la vía femoral (A) y la resolución final con la endoprótesis desplegada (B).
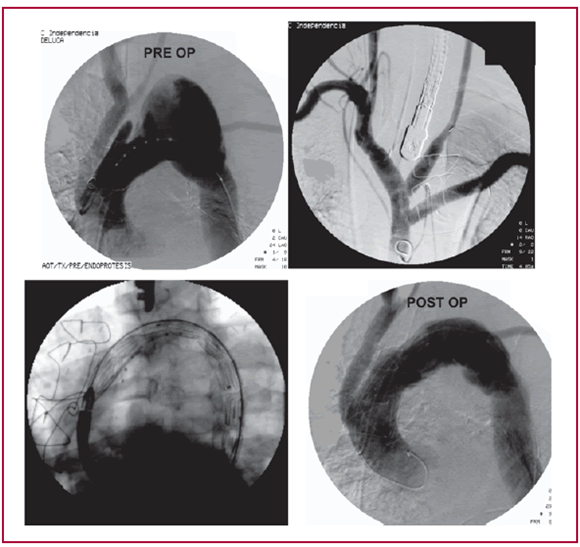
Fig. 4. El procedimiento endovascular paso por paso.
Todas las prótesis se introdujeron luego de la disección de la arteria femoral común; en ningún caso se requirió un acceso ilíaco. Desde el inicio se avanzó un catéter pigtail marcado desde la región femoral contralateral a la elegida para el dispositivo. Con este catéter se tomaron puntos de referencia y se realizaron las angiografías preoperatorias y los controles finales. No se utilizó la vía braquial para referencia o comprobación.
Todos los procedimientos dieron comienzo con la angiograf ía de los bypasses efectuados para constatar su permeabilidad.
Se utiliz ó una dosis de heparina de 80 UI/kg, que se administró inmediatamente antes de la arteriotomía. Luego se avanzó el dispositivo bajo guía fluoroscópica y se liberó en el sitio elegido con una presión media no superior a 60 mm Hg.
En todos los casos, el endograft ascendió sobre una cuerda de extrasoporte Lunderqvist 0,035" y alcanzó el plano valvular aórtico, en tanto que en los tres casos de aneurismas del cayado, en los que el anclaje debió ser más proximal aún, tanto la cuerda como la prótesis que va montada sobre ella protruyeron hacia el ventrículo izquierdo.
Si bien en todos los casos la liberaci ón de la prótesis requiere alta precisión, en la patología más proximal y con la reubicación completa de los vasos, este punto es de especial importancia para no ocluir inadvertidamente el origen del puente efectuado. En nuestro caso, el anillo radioopaco con el que se marcó la sutura proximal del bypass en la aorta fue de gran utilidad.
Se utilizaron 12 endopr ótesis autoexpandibles: tres Zenith TX1® (Cook), todas en el mismo paciente, el primero de la serie, siete Valiant ® (Medtronic) y dos Relay® (Bolton Medical).
RESULTADOS
Procedimiento quirúrgico
Todos los pacientes se recuperaron sin signos de déficit isquémico transitorio o definitivo luego de la reubicación parcial o total de los vasos del cuello.
No se registraron complicaciones vasculares debidas a las anastomosis.
No hubo dehiscencias mecánicas del esternón en los tres pacientes que requirieron esternotomía mediana.
Procedimiento endovascular
En siete de los diez casos se utilizó una sola prótesis autoexpandible por paciente, de 200 mm de largo. En dos pacientes se empleó una única prótesis de 250 mm y en otro, tres prótesis. Con respecto a este último caso, el primero de la serie, se trató una disección tipo B de la manera habitual, respetando el origen de la arteria subclavia con resultado exitoso. A los 15 días del procedimiento, el paciente regresó al hospital con dolor torácico, hipertensión y hemoptisis; se constató una retrodisección hacia el cayado, que requirió la reubicación parcial de los vasos del cuello y el implante de una tercera prótesis.
Todos los implantes fueron técnicamente exitosos. Un paciente con diagnóstico de disección aguda falleció en las primeras 24 horas del posoperatorio debido a retrodisección hacia la aorta ascendente, con derrame pericárdico y taponamiento.
Un paciente portador de un aneurisma del cayado falleció en el día 27 del posoperatorio debido a sepsis con punto de partida pulmonar. Padecía de enfermedad pulmonar obstructiva crónica y se le había realizado una reubicación completa que requirió esternotomía.
Todos los pacientes restantes (seis disecciones y dos aneurismas) se presentaron a control clínico y se les efectuaron exámenes tomográficos al primer mes, al sexto y al año. El tiempo máximo de seguimiento es de un año y medio y el menor es de 6 meses. En este lapso no se registraron fugas ni se requirieron nuevas correcciones. Los dos pacientes con aneurismas presentaron al sexto mes de seguimiento trombosis completa de la formación, sin cambios en los diámetros.
Con respecto a los pacientes con disecciones, los dos casos agudos, sin dilatación, presentaron trombosis completa en el seguimiento. Los otros cuatro casos, dilatados, mostraron trombosis parcial, sin cambios en los diámetros en relación con los encontrados en el preoperatorio.
Ningún paciente fue derivado a tratamiento quirúrgico adicional.
DISCUSIÓN
La reubicación de los vasos del cuello, ya sea parcial o total, con el consiguiente implante de una endoprótesis, resultó un procedimiento factible y eficaz para tratar un grupo de pacientes altamente seleccionados.
El tratamiento quirúrgico habitual del arco aórtico presenta una morbimortalidad elevada (9-12) y a pesar de las constantes mejoras de la técnica aún muestra cifras nada despreciables de deterioro neurológico. (13-15) La combinación de stroke/muerte a los 30 días asciende hasta el 25,6% (media 17,5%).
Se han publicado hasta el momento comunicaciones de casos aislados o pequeñas series de tratamiento en las que este procedimiento combinado se mostró factible y seguro, con porcentajes elevados de éxito técnico primario y buenos resultados en el seguimiento a mediano plazo. (16, 17)
Como medidas adyuvantes del procedimiento global, en ninguno de los casos utilizamos monitorización cerebral, lo cual no generó dificultad alguna y sólo se utilizó eco transesofágico en dos de los tres casos de reubicación completa. Este método complementario de diagnóstico no reveló ningún dato adicional para completar el acto exitosamente.
Si bien la técnica del procedimiento endovascular no difiere de la habitual para la aorta descendente, algunas características especiales son específicas de este sector. Es necesario que la cuerda de extrasoporte se apoye en el seno de Valsalva y, en algunos casos, que ingrese hacia el ventrículo izquierdo.
Las prótesis fueron diseñadas originalmente para el tratamiento de la aorta torácica descendente y por lo tanto su nariz es demasiado larga y puede ingresar hacia el ventrículo izquierdo también; tanto en el caso de la cuerda como en el de la endoprótesis resulta potencialmente peligroso (riesgo de arritmias ventriculares y complicaciones mecánicas por rotura del aparato valvular, subvalvular o por perforación del ventrículo izquierdo).
Para poder generalizar los procedimientos endovasculares sobre el cayado de la aorta, (18) el desarrollo de las prótesis es crucial, ya que deben tener un diseño específico para este sector, con narices más cortas y cuerpos más flexibles. En este sentido, la prótesis Relay de Bolton Medical® está mejor adaptada. Esto se debe a que el cono proximal es más corto y a que utiliza un dispositivo de liberación con un introductor que alcanza sólo la aorta abdominal y el endograft avanza sin cobertura hacia el sitio deseado.
La principal ventaja de esta metodología es su menor invasividad y su aparente menor riesgo. En la comunidad médica, estos hechos se unen inmediatamente al concepto de mejor pronóstico. En el caso particular de los aneurismas y las disecciones de la aorta, el pronóstico parece íntimamente relacionado con los factores comórbidos (19-22) y no con el menor riesgo del procedimiento. En estas patologías pareciera que la sobrevida a mediano plazo estará influida por otras variables que reflejan el estado general del enfermo y su expectativa de vida.
No es materia de análisis de este artículo determinar qué población se beneficiará más con esta estrategia, si el paciente de bajo riesgo y no complicado o, en el otro extremo del espectro, el paciente añoso con múltiples factores comórbidos que es excluido del tratamiento quirúrgico habitual. Está claro que disponemos de una nueva tecnología pero no sabemos aún cuál es el paciente que obtendrá más beneficios con su utilización. (23, 24)
En este contexto de revisión se encuentra también el sitio que el implante de endoprótesis ocupará dentro de las variantes disponibles para el tratamiento de aneurismas y disecciones de la aorta. Quedan pocas dudas de que esta modalidad ha llegado para quedarse y su utilización en pacientes de alto riesgo o con complicaciones (rotura inminente, isquemia visceral, hipertensión intratable) está aceptada. La utilidad de esta estrategia comparada con el tratamiento médico será puesta de manifiesto por estudios en marcha (INSTEAD TRIAL). Hasta ese momento, la permeabilidad de la falsa luz y el diámetro aórtico mayor de 4 cm son datos predictores de peor pronóstico a mediano y largo plazo. (25, 26) Ése fue nuestro criterio de tratamiento en los tres pacientes con disecciones agudas no complicadas.
Finalmente, esta nueva estrategia destinada a resolver casos complejos y de alto riesgo requiere el desarrollo de un equipo terapéutico integrado por técnicos, enfermeros, cirujanos cardiovasculares, cardiólogos intervencionistas, anestesiólogos y cardiólogos clínicos, todos con amplia experiencia en el manejo de urgencias. En nuestro caso, realizamos implantes de endoprótesis de la aorta abdominal desde 1998, iniciamos el programa de tratamiento de la aorta descendente en el año 2000 y desde el 2004 decidimos el tratamiento endovascular en el contexto de urgencia. La realización de procedimientos híbridos como los descriptos es el corolario de una curva de aprendizaje de varios años, que incluyó la formación profesional específica para el entendimiento del cuadro clínico, la anatomía subyacente, la selección de los pacientes y las opciones de tratamiento.
CONCLUSIONES
En esta experiencia de tratamiento combinado de disecciones y aneurismas que comprometen el arco aórtico, la reubicación parcial o total de los vasos del cuello más el implante de una endoprótesis, concebido como un único procedimiento en dos actos en el mismo día, demostró que es técnicamente exitoso y seguro para la población incluida.
El seguimiento a mediano plazo es alentador y similar al de otras series internacionales.
No está claro cuál es el contexto clínico o el paciente ideal para aplicar esta tecnología; la respuesta se desprenderá de futuros trabajos que se encuentran en marcha.
La complejidad de este tipo de tratamiento requiere grupos terapéuticos integrados por cardiólogos intervencionistas y cirujanos cardiovasculares que trabajen estrechamente vinculados en centros de alta especialización.
1. Bergeron P, Mangialardi N, Costa P, Coulon P, Douillez V, Serreo E, et al. Great vessel management for endovascular exclusion of aortic arch aneurysms and dissections. Eur J Vasc Endovasc Surg 2006; 32:38-45. [ Links ]
2. Bertoni HG, Fava MP, Girella GA, Zgrablich C, Ruda Vega P, Salvo GA, et al. Tratamiento endovascular de la aorta torácica descendente. Resultados a mediano plazo. Rev Argent Cardiol 2007;75:96-102. [ Links ]
3. Dake MD. Endovascular stent-graft management of thoracic aortic diseases. Eur J Radiol 2001;39:42-9. [ Links ]
4. Schoder M, Grabenwoger M, Holzenbein T et al. J Thorac Cardiovasc Surg 2006; 131: 380-7. [ Links ]
5. Criado FJ, Clark NS, Barnatan MF. Stent graft repair in the aortic arch and descending thoracic aorta: a 4-year experience. J Vasc Surg 2002;36:1121-8. [ Links ]
6. Kato M, Matsuda T, Kaneko M, Ueda T, Kuratani T, Yoshioka Y, et al. Experimental assessment of newly devised transcatheter stentgraft for aortic dissection. Ann Thorac Surg 1995;59:908-14. [ Links ]
7. Kato M, Kaneko M, Kuratani T, Horiguchi K, Ikushima H, Ohnishi K. New operative method for distal aortic arch aneurysm: combined cervical branch bypass and endovascular stent-graft implantation. J Thorac Cardiovasc Surg 1999;117:832-4. [ Links ]
8. Wheat MW Jr. Current status of medical therapy of acute dissecting aneurysms of the aorta. World J Surg 1980;4:563-9. [ Links ]
9. Tabayashi K, Niibori K, Iguchi A, Shoji Y, Ohmi M, Mohri H. Replacement of the transverse aortic arch for type A acute aortic dissection. Ann Thorac Surg 1993;55:864-7. [ Links ]
10. Okita Y, Ando M, Minatoya K, Kitamura S, Takamoto S, Nakajima N. Predictive factors for mortality and cerebral complications in arteriosclerotic aneurysm of the aortic arch. Ann Thorac Surg 1999;67:72-8. [ Links ]
11. Jacobs MJ, de Mol BA, Veldman DJ. Aortic arch and proximal supraaortic arterial repair under continuous antegrade cerebral perfusion and moderate hypothermia. Cardiovasc Surg 2001;9:396-402. [ Links ]
12. Niinami H, Aomi S, Chikazawa G, Tomioka H, Koyanagi H. Progress in the treatment of aneurysms of the distal aortic arch: approach through median sternotomy. J Cardiovasc Surg (Torino) 2003;44:243-8. [ Links ]
13. Kazui T, Washiyama N, Muhammad BA, Terada H, Yamashita K, Takinami M. Improved results of atherosclerotic arch aneurysm operations with a refined technique. J Thorac Cardiovasc Surg 2001; 121:491-9. [ Links ]
14. Westaby S, Katsumata T. Proximal aortic perfusion for complex arch and descending aortic disease. J Thorac Cardiovasc Surg 1998;115:162-7. [ Links ]
15. Czerny M, Fleck T, Zimpfer D, Dworschak M, Hofmann W, Hutschala D, et al. Risk factors of mortality and permanent neurologic injury in patients undergoing ascending aortic and arch repair. J Thorac Cardiovasc Surg 2003;126:1296-301. [ Links ]
16. Czerny M, Gottardi R, Zimpfer D, Schoder M, Grabenwoger M, Lammer J, et al. Transposition of the supraaortic branches for extended endovascular arch repair. Eur J Cardiothorac Surg 2006; 29:709-13. [ Links ]
17. Bergeron P, Mangialardi N, Costa P, Coulon P, Douillez V, Serreo E, et al. Great vessel management for endovascular exclusion of aortic arch aneurysms and dissections. Eur J Vasc Endovasc Surg 2006; 32:38-45. [ Links ]
18. Melissano G, Tshomba Y, Civilini E, Chiesa R. Disappointing results with a new commercially available thoracic endograft. J Vasc Surg 2004;39:124-30. [ Links ]
19. Eggebrecht H, Herold U, Kuhnt O, Schmermund A, Bartel T, Martini S, et al. Endovascular stent-graft treatment of aortic dissection: determinants of post-interventional outcome. Eur Heart J 2005;26:489-97. [ Links ]
20. Demers P, Miller DC, Mitchell RS, Kee ST, Sze D, Razavi MK, et al. Midterm results of endovascular repair of descending thoracic aortic aneurysms with first-generation stent grafts. J Thorac Cardiovasc Surg 2004;127:664-73. [ Links ]
21. Leurs LJ, Bell R, Degrieck Y, Thomas S, Hobo R, Lundbom J; EUROSTAR; UK Thoracic Endograft Registry collaborators. Endovascular treatment of thoracic aortic diseases: combined experience from the EUROSTAR and United Kingdom Thoracic Endograft registries. J Vasc Surg 2004;40:670-9. [ Links ]
22. Ishida M, Kato N, Hirano T, Cheng SH, Shimono T, Takeda K. Endovascular stent-graft treatment for thoracic aortic aneurysms: short- to midterm results. J Vasc Interv Radiol 2004;15:361-7. [ Links ]
23. Nienaber CA, Skriabina V, Schareck W, Ince H. To stent or not to stent aortic dissection: good news for a chosen few, but who? Eur Heart J 2005;26:431-2. [ Links ]
24. Dobrilovic N, Elefteriades JA. Stenting the descending aorta during repair of type A dissection: technology looking for an application? J Thorac Cardiovasc Surg 2006;131:777-8. [ Links ]
25. Marui A, Mochizuki T, Mitsui N, Koyama T, Kimura F, Horibe M. Toward the best treatment for uncomplicated patients with type B acute aortic dissection: A consideration for sound surgical indication. Circulation 1999;100:II275-80. [ Links ]
26. Onitsuka S, Akashi H, Tayama K, Okazaki T, Ishihara K, Hiromatsu S, et al. Long-term outcome and prognostic predictors of medically treated acute type B aortic dissections. Ann Thorac Surg 2004;78:1268-73. [ Links ]














