Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.77 n.3 Ciudad Autónoma de Buenos Aires mayo/jun. 2009
CIRUGÍA CARDIOVASCULAR/VALVULOPATÍAS
Reemplazo valvular aórtico percutáneo en pacientes de alto riesgo quirúrgico
Fernando A. Cura1, Mariano Albertal1, Lucio Padilla1, Gerardo Nau1, Matías Sztejfman1, Gustavo Avegliano2, Daniel Navia3, Marcelo Trivi2, Ricardo Ronderos2, Jorge Belardi1
1 Servicio de Cardiología Intervencionista y Terapéuticas Endovasculares. Instituto Cardiovascular de Buenos Aires. Buenos Aires, Argentina
2 Servicio de Ultrasonido Cardiovascular, Instituto Cardiovascular de Buenos Aires. Buenos Aires, Argentina
3 Servicio de Cirugía Cardíaca, Instituto Cardiovascular de Buenos Aires. Buenos Aires, Argentina
Recibido: 04/05/2009
Aceptado: 13/05/2009
Dirección para separatas: Dr. Fernando A. Cura Instituto Cardiovascular de Buenos Aires Blanco Encalada 1543 (1428) Buenos Aires, Argentina fcura@icba-cardiovascular.com.ar
RESUMEN
Una proporción importante de pacientes con estenosis aórtica (EAo) grave poseen comorbilidades que incrementan el riesgo de la cirugía de reemplazo valvular aórtico. El implante percutáneo de válvula protésica surge como una alternativa en este grupo de pacientes. Se comunican dos casos de pacientes de edad avanzada portadores de EAo grave a los que se les realizó con éxito el implante percutáneo de una prótesis valvular aórtica CoreValve y se describen los criterios para la selección de pacientes y la técnica de implante percutáneo.
Palabras clave: Válvula aórtica; Cateterismo; Endovascular; Prótesis valvular cardíaca
Abreviaturas
CRVAo Cirugía de reemplazo valvular aórtico
DA Descendente anterior
EAo Estenosis aórtica
VI Ventrículo izquierdo
SUMMARY
Percutaneous Aortic Valve Replacement in High-Risk Patients
A significant proportion of patients with severe aortic stenosis (AS) have comorbidities that increase the risk of surgical aortic valve replacement. Percutaneous implantation of an aortic valve prosthesis emerges as an alternative in this group of patients. We report two cases of elderly patients with severe aortic stenosis that underwent successful percutaneous implantation of CoreValve aortic valve prostheses; in addition, criteria for patient selection and the technique of the procedure are described.
Key words: Aortic Valve; Heart Valve Prosthesis; Catheterization; Endovascular
INTRODUCCIÓN
La estenosis aórtica (EAo) grave es la enfermedad valvular más frecuente en el mundo occidental y su prevalencia crece a medida que aumenta la longevidad de la población. (1) Los pacientes con EAo sintomática poseen una mala calidad de vida y una mortalidad elevada. (2) Hasta el momento, la cirugía de reemplazo valvular aórtico (CRVAo) representa la única terapéutica definitiva capaz de mejorar sustancialmente la sintomatología y su pronóstico a largo plazo. (3) Sin embargo, la presencia de un riesgo quirúrgico excesivo reduce la viabilidad de la CRVAo en aproximadamente el 30% de los pacientes. (1) Es necesario destacar que la presencia de contraindicación quirúrgica se asocia con escasa sobrevida. En este grupo de pacientes, la valvuloplastia percutánea surgió como una posible alternativa terapéutica. No obstante, la tasa elevada de recidiva desalentó su práctica para quedar restringida como puente a la cirugía solamente. (4) El reemplazo valvular percutáneo es una técnica novedosa que se está incorporando con gran entusiasmo en la práctica clínica, en particular en los pacientes con riesgo quirúrgico elevado. (5, 6)
En este trabajo se describen dos casos clínicos, los criterios de selección de pacientes y la técnica empleada.
CASO 1
Mujer de 89 años que presenta disnea a esfuerzos mínimos (clase III de la NYHA) y antecedente de múltiples internaciones por insuficiencia cardíaca descompensada. El ecocardiograma transtorácico 2D, 3D y Doppler mostraron una válvula aórtica trivalva significativamente calcificada con estenosis grave (gradiente máximo de 69 mm Hg y medio de 40 mm Hg y un área valvular de 0,6 cm2) e insuficiencia aórtica moderada (Figura 1 A-C). La fracción de eyección del ventrículo izquierdo fue del 62% y se evidenció una disfunción diastólica de grado III, caracterizada por un patrón diastólico mitral restrictivo y una presión arterial pulmonar sistólica de 52 mm Hg. Se midieron el anillo valvular aórtico, 24 mm, y la distancia anillo-unión sinotubular, 15 mm (Figura 1 A-C). La angiografía coronaria no reveló obstrucciones significativas. El riesgo de mortalidad según EuroScore se estimó en 13,6%. La alternativa quirúrgica se rechazó debido a edad avanzada. Se realizaron diversas evaluaciones angiográficas para determinar la factibilidad del reemplazo valvular aórtico percutáneo (Figura 2 A-B). La paciente fue sometida al implante valvular aórtico por vía percutánea (Figuras 3 A-B y 4 A-C), que resultó satisfactorio (gradiente máximo posimplante de 16 mm Hg e insuficiencia aórtica moderada). Seguidamente, se posdilató la válvula protésica con un balón de 25 mm, lo que redujo ligeramente la regurgitación aórtica (Figura 3 C-D). La evaluación electrocardiográfica luego del procedimiento evidenció conducción AV conservada con un nuevo bloqueo completo de rama izquierda. Durante su internación alternó ritmo propio con el ritmo del marcapasos transitorio durante las siguientes 72 horas y se decidió la colocación de un marcapasos definitivo. El ecocardiograma posoperatorio mostró una posición correcta de la válvula protésica y la presencia de insuficiencia aórtica leve (Figura 5 A-C). La paciente fue dada de alta sin complicaciones mayores y en clase funcional I de la NYHA.

Fig. 1. A. Eco 3D. Cortes multiplanares a nivel de la válvula aórtica. Evaluación de los diámetros aórticos y del área valvular. B. Doppler continuo a través de la válvula aórtica, que muestra un gradiente máximo de 69 mm Hg y medio de 40 mm Hg. C. ETE. Vista longitudinal a 137 grados. Obsérvense las diferentes mediciones realizadas preprocedimiento. A: TSVI. B: Anillo aórtico. C: Senos de Valsalva. D: Unión sinotubular. E: Espesor del tabique interventricular a nivel de la válvula aórtica. D1 y D2: Distancia desde el anillo aórtico hasta la unión sinotubular. ETE: Ecocardiograma transesofágico. ETT: Ecocardiograma transtorácico. AI: Aurícula izquierda. TSVI: Tracto de salida del VI. VI: Ventrículo izquierdo. Ao: Aorta ascendente.

Fig. 2. A. Medición del calibre de las arterias femoral e ilíaca mediante angiografía cuantitativa. B. Aorta con las mediciones necesarias para evaluar la factibilidad del implante valvular percutáneo.

Fig. 3. Posicionamiento (A) y expansión de la prótesis CoreValve (B). (C). Posdilatación de la prótesis. (D). Resultado final. Se observa un reflujo aórtico leve.
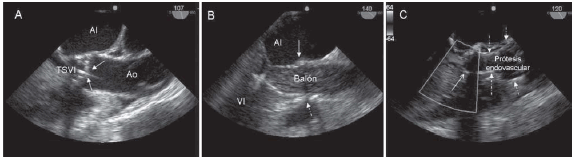
Fig. 4. Monitorización intraprocedimiento mediante ETE. A. Vista longitudinal a 107 grados donde se evidencia el paso de la guía a través de la válvula aórtica (flechas). B. Vista longitudinal a 140 grados donde se observa la insuflación del balón. Las flechas marcan la región del anillo valvular. C. Vista longitudinal a 120 grados. Nótese la prótesis endovascular correctamente posicionada y expandida (flechas discontinuas). Con Doppler color se evidencia la presencia de fuga periprotésica mínima (flecha continua).
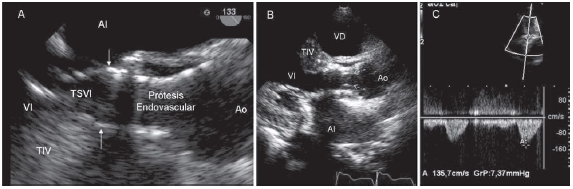
Fig. 5. A. ETE posprocedimiento inmediato. Vista longitudinal a 133 grados donde se evidencia la prótesis endovascular totalmente abierta y correctamente posicionada. Las flechas marcan el borde proximal de la prótesis a nivel del TSVI. B. ETT. Prótesis endovascular en posición correcta. Nótense las valvas finas abiertas durante la sístole (flechas). C. Doppler continuo a través de la prótesis endovascular con un gradiente máximo de 7 mm Hg.
CASO 2
Mujer de 90 años, que presenta disnea progresiva de 2 años de evolución, actualmente en clase III de la NYHA. Su altura es de 1,52 m y su peso es de 59 kg, con un índice de masa corporal de 26. El riesgo quirúrgico se estimó según EuroScore en 14,6%. La evaluación ecocardiográfica reveló una válvula aórtica trivalva calcificada con EAo grave (gradiente transvalvular máximo de 80 mm Hg, medio de 52 mm Hg y un área de 0,75 cm2) e insuficiencia aórtica de grado leve. La fracción de eyección del ventrículo izquierdo fue del 58%. Se evidenció disfunción diastólica de grado II (incremento moderado de las presiones de llenado del VI) y presión sistólica estimada de la arteria pulmonar de 56 mm Hg. Se midieron el diámetro del anillo valvular aórtico, 22 mm, y la distancia anillo-unión sinotubular, 16 mm. Se le realizó una angiografía coronaria que sólo mostró irregularidades en el tercio medio de la DA.
Se le implantó exitosamente por vía percutánea una prótesis 26; se observaron resolución completa del gradiente transvalvular aórtico e insuficiencia aórtica moderada, la cual se redujo sustancialmente luego de la posdilatación con balón de 25 mm. Debido al desarrollo de bloqueo trifascicular a las 24 horas del procedimiento, se procedió a la colocación de un marcapasos definitivo. La evaluación ecocardiográfica prealta mostró una válvula protésica en posición correcta, con gradientes transvalvulares normales e insuficiencia aórtica leve.
REQUERIMIENTOS PARA LA SELECCIÓN DE PACIENTES PARA VÁLVULA AUTOEXPANDIBLE
Para una selección adecuada de los pacientes candidatos al implante valvular percutáneo se requieren ciertos criterios: 1) presencia de EAo sintomática con riesgo quirúrgico elevado, 2) diámetro ecocardiográfico del anillo valvular aórtico ≥ 20 mm y ≤ 27 mm, 3) distancia desde el anillo-unión sinotubular > 14 mm y 4) diámetro de la aorta ascendente a 30 mm del plano valvular < 43 mm. La ecocardiografía 3D permite una medición directa y correcta mediante la técnica multiplanar (Figura 2). (5)
Por otro lado, la evaluación angiográfica (o en su defecto mediante tomografía computarizada con multicorte) resulta fundamental para descartar la presencia de enfermedad coronaria y evaluar las dimensiones de las siguientes estructuras: anillo aórtico valvular, distancia entre anillo valvular y nacimiento de arterias coronarias, diámetro de la aorta ascendente a 30 mm del anillo valvular (Figuras 2 y 3 A-C). Además, la angiografía permite evaluar la factibilidad del avance del dispositivo mediante la determinación de: a) el ángulo entre el ventrículo izquierdo y el nacimiento de la aorta y b) el ángulo entre el cayado aórtico y la aorta descendente. Además, se determinan el grado de tortuosidad del árbol iliofemoral y los diámetros de las arterias femoral, ilíaca externa y común.
DESCRIPCIÓN DE LA PRÓTESIS
La prótesis CoreValve Inc, California, USA, consiste en una bioprótesis de pericardio porcino trivalva que se encuentra suturada en un stent autoexpandible de nitinol (Figura 6). La porción distal de la prótesis que se implanta desde el tracto de salida del ventrículo izquierdo y a nivel del anillo valvular posee una gran fuerza radial, lo que le permite expandirse, excluir valvas calcificadas y evitar la retracción. La porción central está diseñada para evitar la obstrucción de los orígenes coronarios, mientras que la porción proximal se expande hasta afirmarse en la pared de la aorta ascendente, lo que proporciona estabilidad longitudinal junto con una alineación coaxial correcta. Actualmente, el perfil de la prótesis es de 18 Fr. Existen dos tamaños de prótesis de acuerdo con el diámetro del anillo aórtico: 26 mm para anillos de 20 a 23 mm y de 29 mm para anillos de 23 a 27 mm.
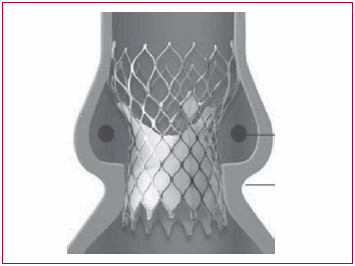
Fig. 6. Esquema de la válvula CoreValve posicionada a nivel del anillo valvular y respetando los orígenes de las arterias coronarias.
DESCRIPCIÓN DEL PROCEDIMIENTO
El procedimiento se realiza bajo control angiográfico, hemodinámico y ecocardiográfico. Algunos grupos experimentados prescinden de la monitorización ecocardiográfica intraprocedimiento. Nosotros creemos que es de utilidad en la evaluación de diámetros, la monitorización durante el ingreso de los catéteres (posibles desgarros de placas arterioscleróticas de la aorta descendente) y para el control poscolocación inmediato, en el que se evalúan la presencia y el grado de la insuficiencia aórtica. Se coloca un marcapasos transitorio que permanece durante 48 horas, ya que existe riesgo de comprometer el sistema de conducción con la consiguiente necesidad de un marcapasos definitivo. El acceso más frecuentemente utilizado es la arteria femoral con la colocación de un introductor de 18 Fr. Se puede acceder por disección arterial o por punción arterial con la utilización de un sistema de cierre percutáneo con sutura. En caso de acceso femoral inadecuado se podría considerar la disección de la arteria subclavia. Se introduce un catéter pigtail por vía femoral o radial para la medición simultánea del gradiente de presiones y para el control angiográfico, colocándolo para el posicionamiento de la prótesis valvular CoreValve.
Luego de determinar el gradiente transvalvular aórtico, se realiza una valvuloplastia con un balón de diámetro similar al del anillo valvular. Posteriormente, se avanza la válvula por vía femoral hasta posicionarla a nivel del anillo valvular (Figura 3). Se libera la válvula retrayendo la vaina liberadora. En caso de que se presentaran estenosis o insuficiencia valvular significativa se puede dilatar la válvula protésica con un balón de mayor diámetro.
DISCUSIÓN
En la actualidad, la presencia de comorbilidades o la edad avanzada limitan la indicación de CRVAo en un gran número de pacientes. (1) Hasta el momento se han implantado dos válvulas protésicas (CoreValve y Edwards LifeScience) en aproximadamente 5.000 pacientes, con éxito creciente. Esta nueva técnica amplía el espectro de pacientes con EAo que pueden beneficiarse con un tratamiento definitivo para la corrección de su enfermedad. Específicamente, el implante de la prótesis CoreValve presenta una tasa de éxito elevada y una tasa baja de complicaciones. (5) Algunas de las complicaciones observadas con esta prótesis, como el accidente cerebrovascular (temporario o permanente) y el trauma vascular ilíaco o femoral, se han subsanado con la reducción del perfil de la prótesis de 25 Fr a 18 Fr. (5) Por otro lado, es frecuente la necesidad del implante de un marcapasos definitivo (20%) debido al desarrollo de bradiarritmias. (7) La presencia de insuficiencia aórtica luego de su implante se debe en la mayoría de los casos a una fuga periprotésica que tiende a retrogradar con el tiempo, ya que la prótesis continúa expandiéndose y se desarrollaría tejido fibrótico perivalvular. En algunos casos, la posdilatación reduce la fuga periprotésica. Otras complicaciones, como el taponamiento cardíaco, la oclusión de los ostia coronarios al implantar la prótesis o un implante muy distal dentro del ventrículo izquierdo o muy proximal en la aorta ascendente, son más frecuentes en manos pocos experimentadas, lo que destaca la necesidad de un entrenamiento riguroso en esta nueva técnica antes de su utilización.
1. Iung B, Baron G, Butchart EG, Delahaye F, Gohlke-Barwolf C, Levang OW, et al. A prospective survey of patients with valvular heart disease in Europe: The Euro Heart Survey on Valvular Heart Disease. Eur Heart J 2003;24:1231-43. [ Links ]
2. Varadarajan P, Kapoor N, Bansal RC, Pai RG. Clinical profile and natural history of 453 nonsurgically managed patients with severe aortic stenosis. Ann Thorac Surg 2006;82:2111-5. [ Links ]
3. Varadarajan P, Kapoor N, Bansal RC, Pai RG. Survival in elderly patients with severe aortic stenosis is dramatically improved by aortic valve replacement: Results from a cohort of 277 patients aged > or =80 years. Eur J Cardiothorac Surg 2006;30:722-7. [ Links ]
4. Otto CM, Mickel MC, Kennedy JW, Alderman EL, Bashore TM, Block PC, et al. Three-year outcome after balloon aortic valvuloplasty. Insights into prognosis of valvular aortic stenosis. Circulation 1994;89:642-50. [ Links ]
5. Grube E, Schuler G, Buellesfeld L, Gerckens U, Linke A, Wenaweser P, et al. Percutaneous aortic valve replacement for severe aortic stenosis in high-risk patients using the second- and current thirdgeneration self-expanding CoreValve prosthesis: device success and 30-day clinical outcome. J Am Coll Cardiol 2007;50:69-76. [ Links ]
6. Piazza N, Grube E, Gerckens U, den Heijer P, Linke A, Luha O, Ramondo A, Ussia G, Wenaweser P, Windecker S, Laborde JC, de Jaegere P, Serruys PW. Procedural and 30-day outcomes following transcatheter aortic valve implantation using the third generation (18 Fr) corevalve revalving system: results from the multicentre, expanded evaluation registry 1-year following CE mark approval. EuroIntervention 2008;4:242-9. [ Links ]
7. Erdogan HB, Kayalar N, Ardal H, Omeroglu SN, Kirali K, Guler M, et al. Risk factors for requirement of permanent pacemaker implantation after aortic valve replacement. J Card Surg 2006;21:211-5. [ Links ]














