Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.77 n.4 Ciudad Autónoma de Buenos Aires jul./ago. 2009
INSUFICIENCIA CARDÍACA
Perfil clínico y funcional de los pacientes con insuficiencia cardíaca sistólica y disfunción renal
Adriana Acosta†, 1, Máximo Migliori1, Nora Vainstein2, Javier C. Marino1, Ramiro Guglielmone4, Marcelo S. TriviMTSAC, 3, 4, Mónica Sultán5, Fernando Brites6, Jorge M. ThiererMTSAC, 1
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
† Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
1 Servicio de Insuficiencia Cardíaca y Trasplante, Instituto Cardiovascular de Buenos Aires
2 Servicio de Lípidos, Instituto Cardiovascular de Buenos Aires
3 Servicio de Cardiología Clínica, Instituto Cardiovascular de Buenos Aires
4 Servicio de Ultrasonido, Instituto Cardiovascular de Buenos Aires
5 Servicio de Cardiología Clínica, Hospital Municipal de San Isidro
6 Facultad de Farmacia de la Universidad de Buenos Aires
Recibido: 11/05/2009
Aceptado: 08/06/2009
Dirección para separatas: Dra. Adriana Acosta Instituto Cardiovascular de Buenos Aires Blanco Encalada 1525 (1428) Buenos Aires, Argentina Fax: (54-11) 4787-7511 e-mail: acosta_adry@yahoo.com.ar
RESUMEN
Introducción
La disfunción renal está fuertemente asociada con la insuficiencia cardíaca crónica. Es una complicación habitual y progresiva de esta condición, con una evolución clínica que fluctúa con la clase funcional y el tratamiento farmacológico.
Objetivos
Definir la prevalencia y el perfil clínico y funcional de pacientes con disfunción renal en el contexto de insuficiencia cardíaca con baja fracción de eyección.
Material y métodos
En 132 pacientes con insuficiencia cardíaca y fracción de eyección < 40% se midió la depuración de creatinina. Se definió disfunción renal a una depuración de creatinina < 60 ml/ min. Se realizaron analítica sanguínea, ecocardiograma, bioimpedanciometría y caminata de 6 minutos.
Resultados
La prevalencia de disfunción renal fue del 43,2% (57 pacientes). Comparados con el resto, en estos pacientes hubo mayor prevalencia de sexo femenino, mayor edad y menos frecuentemente etiología coronaria. En el laboratorio tuvieron valores menores de hemoglobina, albúmina, ferritina y triyodotironina y mayor prevalencia de troponina T dosable. Fueron menores el índice de masa corporal (IMC), la tasa metabólica basal, la masa muscular y el ángulo de fase, mientras que la relación agua extracelular/agua corporal total fue mayor. La distancia recorrida en la prueba de 6 minutos fue menor. Respecto del tratamiento, sólo difirió el uso de betabloqueantes y amiodarona. En el análisis multivariado, la edad, el nivel de NT-proBNP, la presencia de troponina T positiva y la masa muscular como variable continua fueron predictores independientes de disfunción renal en pacientes con insuficiencia cardíaca sistólica.
Conclusiones
La disfunción renal es frecuente en pacientes con insuficiencia cardíaca con baja fracción de eyección y se vincula con características distintivas que pueden contribuir a explicar el cuadro clínico.
Palabras clave: Insuficiencia cardíaca; Insuficiencia renal; Impedancia eléctrica; Composición corporal
Abreviaturas:
ARA Bloqueantes de los receptores de angiotensina
DR Disfunción renal
Fey Fracción de eyección
IC Insuficiencia cardíaca
IECA Inhibidores de la enzima convertidora de la angiotensina
NT-proBNP Fragmento N terminal del propéptido natriurético cerebral
T3 Triyodotironina
T4 Tiroxina
TSH Hormona estimulante del tiroides
VSG Velocidad de sedimentación globular
SUMMARY
Clinical and Functional Profile of Patients with Systolic Heart Failure and Renal Dysfunction
Background
Renal dysfunction is strongly associated with chronic heart failure, and is a frequent and progressive complication of this condition, with clinical outcomes which depend on the functional class and pharmacological treatment.
Objectives
To define the prevalence and the clinical and functional profile of patients with renal dysfunction in the setting of heart failure with depressed ejection fraction.
Material and Methods
Creatinine clearance was measured in 132 patients with heart failure and an ejection fraction <40%. Renal dysfunction was defined as a creatinine clearance <60 ml/min. Patients underwent routine lab tests, echocardiogram, bioelectrical impedance analysis and 6-minute walk test.
Results
The prevalence of renal dysfunction was 43.2% (57 patients).
Among these patients, there was a greater prevalence of women and elder subjects, yet the prevalence of coronary artery disease was low. Lab tests showed lower levels of hemoglobin, albumin, ferritin and triiodothyronine, and greater prevalence of measurable levels of troponin T. Body mass index (BMI), basal metabolic rate, muscle mass and phase angle were lower, while the ratio of extracellular water to total body water was greater in patients with renal dysfunction. The distance walked in the 6-minute test was lower. The use of beta blockers and amiodarone was the only difference in therapy. At multivariate analysis, age, NTproBNP level, the presence of positive troponin T and muscle mass as a continuous variable were independent predictors of renal dysfunction in patients with systolic heart failure.
Conclusions
Renal dysfunction is frequent in patients with heart failure with depressed ejection fraction and is associated with distinctive features that may contribute to explain the clinical picture.
Key words: Heart Failure; Renal Failure; Electrical Impedance; Body Composition
INTRODUCCIÓN
La insuficiencia cardíaca (IC) es la patología cardiovascular de mayor crecimiento en los últimos años. (1-3) La disfunción renal (DR) es una complicación habitual y progresiva de esta condición, con una evolución clínica que fluctúa con la clase funcional y el tratamiento farmacológico. (1-5)
La presencia de DR ha demostrado que es un predictor independiente de peor pronóstico en la IC. (5-7) Los mecanismos probablemente involucrados serían la coexistencia de comorbilidades, el aumento de toxicidad por procedimientos diagnósticos y terapéuticos, la aterosclerosis acelerada y el menor uso de fármacos con eficacia comprobada en pacientes con ambas entidades. (3-7)
Los estudios multicéntricos no representan el total de la población de los pacientes con IC. Generalmente se incluyen pacientes de sexo masculino, más jóvenes, con disfunción sistólica y escasa tasa de comorbilidad. (8) Así, los pacientes con DR quedan casi totalmente excluidos de los estudios, lo cual limita la evidencia clínica.
El objetivo de este estudio fue definir la prevalencia y el perfil clínico y funcional de los pacientes con DR en el contexto de la IC con disfunción sistólica.
MATERIAL Y MÉTODOS
Durante el período comprendido entre agosto de 2006 y abril de 2008 se incluyeron consecutivamente 132 pacientes ambulatorios mayores de 18 años con diagnóstico de IC crónica de cualquier etiología, fracción de eyección (Fey) £ 40%, tratamiento completo para IC y estabilidad clínica 90 días previos a la selección.
Se definió DR a la presencia de una depuración (clearance) de creatinina < 60 ml/min/m2, según las guías de la National Kidney Foundation. (9, 10) La depuración de creatinina se calculó con una muestra de orina recolectada durante 24 horas y la creatinina plasmática.
Se recabó el antecedente de diabetes mellitus, hipertensi ón, dislipidemia y comorbilidades (enfermedad pulmonar obstructiva crónica, neoplasias, discrasia sanguínea, asma, hipotiroidismo, hipertiroidismo y osteoporosis). El diagnóstico de IC y su etiología se basaron sobre el criterio del médico tratante y los datos de la historia clínica.
Se efectuó laboratorio: hematología, química sanguínea, perfil hormonal (T3, T4 y TSH) y biomarcadores (troponina T y NT-proBNP).
Se consideró troponina T positiva cuando los valores séricos basales eran mayores de 0,01 ng/ml.
Se definió microalbuminuria a valores de albuminuria de 30-300 mg/24 horas en una muestra de orina de 24 horas.
Se realizó ecocardiograma Doppler color transtorácico (ecógrafo modelo Philips IE-33) desde ventana paraesternal izquierda (eje largo y corto) y apical del ventrículo izquierdo (cuatro y dos cámaras). La Fey se determinó por el método de Simpson.
La evaluación de la composición corporal se efectuó con el método de la bioimpedancia eléctrica (bioimpedanciómetro de cuatro canales modelo BioScan MSR-916, Maltron International Ltd.). Esta técnica se basa en la resistencia que ofrecen el agua y los tejidos corporales al paso de una corriente eléctrica de baja intensidad. Para ello se colocaron dos electrodos en la mano y la muñeca y otros dos en el pie y el tobillo derechos. Este estudio se realizó en el consultorio con el paciente en decúbito supino con una preparación mínima: 6 horas de ayuno, no realizar ejercicios extenuantes en las 12 horas previas, evacuar orina y no poseer objetos metálicos sobre el cuerpo.
La capacidad funcional se evaluó con la prueba de la caminata de 6 minutos.
Análisis estadístico
Las variables continuas se expresaron como media ± desviación estándar o mediana y rango intercuartil 25-75 según su distribución fuera normal o no, respectivamente. La comparación se realizó con la prueba de la t de Student en el caso de variables continuas con distribución normal y con la prueba de Wilcoxon en el caso de distribución no normal.
Las variables categóricas se expresaron como porcentajes y la comparación entre grupos se realizó con la prueba de chi cuadrado.
Las variables diferentes entre los pacientes con DR y sin DR con valor de p < 0,10 se ingresaron en un modelo multivariado para definir las asociadas independientemente con DR.
RESULTADOS
La edad media de los pacientes fue de 63,4 ± 11,5 años, con predominio del sexo masculino. La etiología de la IC fue principalmente isquémica; la Fey media fue del 27,5% ± 7,6% y la mayoría se encontraba en clase funcional I-II (Tabla 1).
Tabla 1. Características generales de la población y de pacientes con DR y sin DR

La media de depuración de creatinina fue de 70,6 ± 35,5 ml/min. La prevalencia de DR fue del 43,2% (57 pacientes). Para determinar las características de los pacientes con DR, la población se dividió en dos grupos según la depuración de creatinina: grupo con DR (57 pacientes, 43,2%) y grupo sin DR (75 pacientes, 56,8%).
La prevalencia de sexo femenino fue más elevada en el grupo con DR. Se observó además mayor edad, prevalencia de etiología no isquémica y tendencia a presentar más comorbilidades (Tabla 1).
La hemoglobina, la albúmina, la ferritina y la T3 fueron más bajas, pero hubo niveles más elevados de potasio, troponina T, velocidad de sedimentación globular (VSG) y NT-proBNP (Tabla 2). En cuanto a la medicación, sólo se observaron diferencias significativas en cuanto la utilización de betabloqueantes y amiodarona (Tabla 3).
Tabla 2. Resultados de laboratorio de la población y de pacientes con DR y sin DR

Tabla 3. Tratamiento farmacológico de la población y de pacientes con DR y sin DR

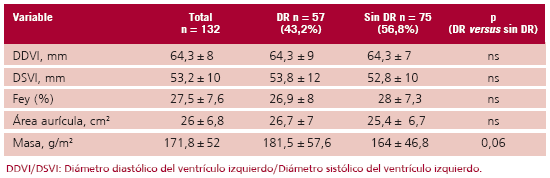
No se evidenciaron diferencias significativas en los datos obtenidos por ecocardiograma Doppler color. Hubo tendencia a una masa ventricular mayor en los pacientes con DR (Tabla 4).
Tabla 4. Resultados del ecocardiograma de la población y de pacientes con DR y sin DR
El análisis de la bioimpendancia mostró que el índice de masa corporal, la masa muscular, la masa proteica, el ángulo de fase y tasa metabólica basal fueron menores en el grupo con DR, en tanto que sucedió lo contrario con la relación agua extracelular / agua corporal total.
Los pacientes con DR recorrieron una distancia menor en la prueba de la caminata de 6 minutos (Tabla 5).
Tabla 5. Resultados de bioimpedancia y de la prueba de la caminata de la población total y de pacientes con DR y sin DR

En el análisis multivariado, la edad, el nivel de NTproBNP (expresado en forma logarítmica), la presencia de troponina T positiva y la masa muscular como variable continua fueron predictores independientes de DR en pacientes ambulatorios con IC con disfunción sistólica (área bajo la curva ROC 0,87) (Tabla 6 y Figura 1).
Tabla 6. Predictores de DR en pacientes con IC

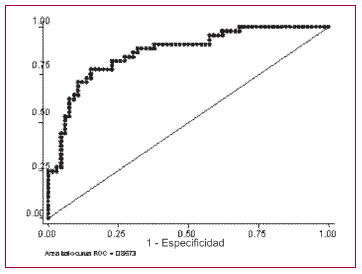
Fig. 1. Curva ROC de predictores de disfunción renal en insuficiencia cardíaca.
DISCUSIÓN
La codependencia de riñón y corazón a menudo hace difícil delimitar la relación de causalidad en pacientes con DR e IC crónica. (1-3, 6, 7) La DR es un factor pronóstico generalmente subestimado en la IC que se asocia con cambios en la fisiología vascular e intravascular: anormalidades en los sistemas coagulación/fibrinólisis, calcificación vascular anormal, disfunción endotelial, hiperhomocisteinemia, resistencia a la insulina, niveles elevados de proteína C reactiva y VSG, desequilibrio endotelina/óxido nítrico, alteraciones electrolíticas (hiperpotasemia e hipermagnesemia) e hiperactividad del sistema nervioso simpático y del sistema renina-angiotensina-aldosterona. (4, 5, 7, 11, 12) Estas alteraciones, sumadas a una función ventricular deteriorada, podrían determinar peor evolución con aumento de la tasa de eventos cardiovasculares. (4, 7, 11)
En nuestra serie, la prevalencia de DR en pacientes con IC crónica fue semejante a la comunicada en publicaciones internacionales (30-50% aproximadamente). (1-3, 12, 13)
En el grupo con DR, la edad media fue mayor que en los pacientes con función renal conservada, lo que podría responder a la caída fisiológica de la tasa de filtración glomerular dependiente de la edad (0,8 ml/ min/1,73 m2 por año a partir de los 30 años). (9, 10)
El porcentaje de mujeres fue más alto en este grupo, no obstante que el sexo masculino fue más prevaleciente en ambos grupos. En estudios previos se han observado diferencias en la farmacocinética de los diuréticos del asa dependientes del sexo. Las mujeres requieren dosis más elevadas que los hombres para obtener una misma respuesta natriurética. Esta situación podría provocar mayor depleción de volumen plasmático y activación neurohormonal, que contribuye al deterioro progresivo de la función renal y cardíaca. (14, 15) En nuestra serie, cuando se analizó el porcentaje de agua corporal total de las mujeres, éste fue menor.
La enfermedad coronaria y la enfermedad renal tienen muchos factores de riesgo en común, por lo que la etiología coronaria de la disfunción sistólica es más frecuente en pacientes con DR. (1-3) Sin embargo, esta asociación no se observó en nuestra serie.
Cuando se analizaron las variables de laboratorio, la hemoglobina y la ferritina fueron más bajas en los pacientes con DR, lo que indica mayor tendencia a anemia ferropénica, anemia asociada con enfermedades inflamatorias crónicas y/o anemia dilucional. Como lo demuestran estudios anteriores, la anemia se asocia tanto con IC como con DR. (12, 16, 17) En nuestra serie, la prevalencia de anemia fue del 17,4% (21% en pacientes con DR y 15% en pacientes sin DR, sin diferencia significativa). La interrelación entre anemia, DR e IC no está completamente esclarecida. Se han sugerido varias hipótesis: isquemia crónica y fibrosis del intersticio renal, incremento de citocinas circulantes (como el factor de necrosis tumoral alfa), hemodilución por expansión plasmática más frecuente en pacientes con DR y efectos adversos de ciertos fármacos (enalapril, diuréticos, betabloquenates, antiarrítmicos y digoxina). (18, 19) Sin embargo, Bansal y colaboradores sugieren que la anemia sería un reflejo de mayor gravedad de la IC; de esta forma, los pacientes con estadios más avanzados serían más susceptibles a la progresión de la DR y menor hematocrito. (16)
La microalbuminuria, marcador de disfunción endotelial, constituye un factor de riesgo para el desarrollo y la progresión de la DR. Paradójicamente, no encontramos diferencias en la presencia de microalbuminuria en ambos grupos. Esto podría responder a que los dos grupos de pacientes estaban en tratamiento con IECA/ARA en igual porcentaje y se encontraban clínicamente estables.
Si bien los niveles de potasio en ambos grupos estuvieron dentro de los parámetros normales, fueron más elevados en el grupo con DR. La insuficiencia renal es un factor predisponente para el desarrollo de hiperpotasemia, lo que podría limitar el uso de ciertos fármacos como espironolactona e IECA/ARA, situación que no ocurrió en nuestra serie.
Las elevaciones de troponina T y BNP en cualquier momento del seguimiento de pacientes con IC se asocian con eventos adversos; (20-22) la monitorización de estos biomarcadores permite evaluar mejor el riesgo. En nuestra serie, los niveles de BNP y de troponina T fueron más elevados en los pacientes con DR, lo cual indica mayor deterioro miocárdico y peor pronóstico. En un estudio español, el BNP en pacientes con DR presentó niveles superiores a los de la población general y se consideró un marcador de enfermedad cardiovascular e hipertrofia ventricular izquierda. En pacientes con IC se halló una correlación inversa entre los niveles de BNP y la depuración de creatinina debido a que el BNP está influido por la tasa de filtración glomerular, la masa parenquimatosa y la función tubular.
El significado clínico de la VSG en la IC es controversial y en la DR no está establecido. (23, 24) En nuestro estudio, fue más elevada en el grupo de pacientes con DR; sin embargo, el valor fue menor que el comunicado en trabajos previos. La VSG elevada podría responder a la mayor edad, a la prevalencia de anemia y a la morfología alterada de los eritrocitos en enfermedades crónicas.
En los pacientes con enfermedades crónicas graves y bajo tratamiento con múltiples drogas se pueden observar cambios en el metabolismo y concentraciones periféricas de las hormonas tiroideas. (25-27) El grupo con DR presentó niveles de T3 más bajos, tal vez relacionados con disminución de la conversión periférica de T4 en T3, alteraciones en el transporte de las hormonas asociado con proteínas y efectos secundarios al uso de amiodarona. Esta disfunción tiroidea sería un factor agravante en la progresión de la IC y la DR.
La masa del ventrículo izquierdo determinada por ecocardiograma fue mayor en pacientes con DR (p = 0,06). Este hallazgo tiene varias causas: cambios hemodinámicos compensatorios de la anemia, isquemia-fibrosis-remodelación miocárdica, dilatación ventricular por sobrecarga hídrica, situaciones que son más frecuentes en pacientes con DR. (16, 19)
En los últimos años se ha observado un avance en la terapéutica farmacológica de la IC que ha incrementado la sobrevida de los pacientes. Algunas de estas drogas presentan efectos beneficiosos en pacientes con DR a pesar de cierto grado de elevación de los niveles séricos de creatinina. De esta forma, la DR habitualmente se considera una contraindicación relativa para ciertas terapias. Así, existen diferencias en el tratamiento de la IC con dependencia de la presencia de DR. McAlister y colaboradores observaron que a medida que disminuye la depuración de creatinina, lo mismo sucede con la prescripción de betabloqueantes, IECA y espironolactona. (2) En nuestro grupo con DR, la prescripción de amiodarona fue mayor y la de betabloqueantes fue menor. Esta situación se debería probablemente a un estadio de IC más avanzado, mayor frecuencia de arritmia ventricular por trastornos electrolíticos, intolerancia a los betabloqueantes por hipotensión y menor etiología no coronaria en los grupos con DR.
Existe suficiente evidencia para considerar a la composición corporal como un marcador sistémico de gravedad en enfermedades crónicas, como IC e insuficiencia renal. (28-30) La pérdida involuntaria de peso (caquexia) se relaciona con aumento de morbimortalidad independientemente de la gravedad de la enfermedad. Considerando los resultados de la bioimpedancia, los pacientes con DR tenían un índice de masa corporal menor a expensas de una masa proteica menor y, por lo tanto, menor masa muscular. Esta situación, sumada a los niveles de albúmina sérica bajos, sugiere un estado nutricional desfavorable, a veces infravalorado en estos pacientes. Cuando se analizó el agua corporal, los resultados de ambos grupos fueron similares, pero el porcentaje de agua extracelular en el grupo con DR fue significativamente más elevado, reflejo de la mayor dificultad en el manejo del balance hidroelectrolítico que estos pacientes presentan.
Un tercio de nuestra población se encontraba en CF III-IV distribuida homogéneamente en los dos grupos. A pesar de este hallazgo, cuando se evaluaron objetivamente los pacientes con la prueba de la caminata de 6 minutos, aquellos con DR recorrieron una distancia menor; esto podría responder al hecho de que eran pacientes más añosos, más anémicos, con peor estado nutricional, menor masa muscular y peor acondicionamiento físico. En un subgrupo del estudio DIG (31) en el que se efectuó caminata de 6 minutos, los pacientes ubicados en los dos cuartiles inferiores de depuración de creatinina presentaron mayor edad, predominancia de mujeres, una cantidad mayor de internaciones por IC, clase funcional III-IV, más uso de diuréticos y la distancia recorrida en la caminata fue menor.
Limitaciones
Debemos mencionar que nuestro estudio tiene una serie de limitaciones. En primer lugar, la depuración de creatinina se obtuvo con una muestra de orina recolectada en 24 horas, que tiene una serie de inconvenientes: si la recolección de orina es incompleta, subestima el valor de depuración de creatinina; por otro lado, en el paciente con caída de la tasa de filtración glomerular, la secreción de creatinina se incrementa como mecanismo compensatorio, lo que sobrestima la depuración de creatinina. Asimismo, esta serie de pacientes pertenece a un grupo de cardiólogos especialistas en IC. No se realizó screening de patología renal: sedimento urinario, evaluación de la estructura renal, fondo de ojo y arteria renal. Por último, nuestros datos se obtuvieron de pacientes con disfunción sistólica y no pueden extrapolarse a los pacientes con insuficiencia cardíaca y función sistólica conservada.
CONCLUSIONES
La DR es frecuente en pacientes con IC con Fey baja y se vincula con características distintivas que pueden contribuir a explicar el peor pronóstico: edad, troponina T y BNP elevados y menor masa muscular.
Agradecimientos
Agradecemos la colaboración de Lucrecia Álvarez Saavedra, secretaria de Investigación de la Fundación Cardiovascular de Buenos Aires, de Irene Monte, técnica del Servicio de Ergometría y Consumo de Oxígeno del Instituto Cardiovascular de Buenos Aires, y de Marcela Sutton y César Sutton del Laboratorio del Instituto Cardiovascular de Buenos Aires.
1. Schiffrin EL, Lipman ML, Mann JF. Chronic kidney disease: effects on the cardiovascular system. Circulation 2007;116:85-97. [ Links ]
2. McAlister FA, Ezekowitz J, Tonelli M, Armstrong PW. Renal insufficiency and heart failure: prognostic and therapeutic implications from a prospective cohort study. Circulation 2004;109:1004-9. [ Links ]
3. Ezekowitz J, McAlister FA, Humphries KH, Norris CM, Tonelli M, Ghali WA, et al; APPROACH Investigators. The association among renal insufficiency, pharmacotherapy, and outcomes in 6,427 patients with heart failure and coronary artery disease. J Am Coll Cardiol 2004;44:1587-92. [ Links ]
4. Dries DL, Exner DV, Domanski MJ, Greenberg B, Stevenson LW. The prognostic implications of renal insufficiency in asymptomatic and symptomatic patients with left ventricular systolic dysfunction. J Am Coll Cardiol 2000;35:681-9. [ Links ]
5. Hillege HL, Girbes AR, de Kam PJ, Boomsma F, de Zeeuw D, Charlesworth A, et al. Renal function, neurohormonal activation, and survival in patients with chronic heart failure. Circulation 2000;102:203-10. [ Links ]
6. Butler J, Forman DE, Abraham WT, Gottlieb SS, Loh E, Massie BM, et al. Relationship between heart failure treatment and development of worsening renal function among hospitalized patients. Am Heart J 2004;147:331-8. [ Links ]
7. Maxwell AP, Ong HY, Nicholls DP. Influence of progressive renal dysfunction in chronic heart failure. Eur J Heart Fail 2002;4:125-30. [ Links ]
8. Dahlström U. Frequent non-cardiac comorbidities in patients with chronic heart failure. Eur J Heart Fail 2005;7:309-16. [ Links ]
9. Levey AS, Coresh J, Balk E, Kausz AT, Levin A, Steffes MW, et al; National Kidney Foundation. National Kidney Foundation practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Ann Intern Med 2003;139:137-47. [ Links ]
10. National Kidney Foundation. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis 2002;39:S1-266. [ Links ]
11. Hillege HL, Nitsch D, Pfeffer MA, Swedberg K, McMurray JJ, Yusuf S, et al; Candesartan in Heart Failure: Assessment of Reduction in Mortality and Morbidity (CHARM) Investigators. Renal function as a predictor of outcome in a broad spectrum of patients with heart failure. Circulation 2006;113:671-8. [ Links ]
12. Obialo CI. Cardiorenal consideration as a risk factor for heart failure. Am J Cardiol 2007;99:21D-24D. [ Links ]
13. Silverberg DS, Wexler D, Iaina A, Schwartz D. The interaction between heart failure and other heart diseases, renal failure, and anemia. Semin Nephrol 2006;26:296-306. [ Links ]
14. CohenN, Ilgiyaev E, Almoznino-SarafianD, Alon I, Shteinshnaider M, Chachashvily S, et al. Sex-related bedside clinical variables associated with survival of older inpatients with heart failure. Eur J Heart Fail 2004;6:781-6. [ Links ]
15. Wenger NK. Women heart failure and heart failure therapies. Circulation 2002;105:1526-8. [ Links ]
16. BansalN, Tighiouart H,Weiner D, Griffith J, Vlagopoulos P, Salem D, et al. Anemia as a risk factor for kidney function decline in individuals with heart failure. Am J Cardiol 2007;99:1137-42. [ Links ]
17. Mitchell JE. Emerging role of anemia in heart failure. Am J Cardiol 2007; 99:15D-20D. [ Links ]
18. Celik T, Iyisoy A, Kursaklioglu H, Gungor M, Yuksel UC. Anemia and cardio-renal syndrome: a deadly association? Int J Cardiol 2008;128:255-6. [ Links ]
19. Berl T, Henrich W. Kidney-heart interactions: epidemiology, pathogenesis, and treatment. Clin J Am Soc Nephrol 2006;1:8-18. [ Links ]
20. Potluri S, VenturaHO, Mulumudi M, Mehra MR. Cardiac troponin levels in heart failure. Cardiol Rev 2004;12:21-5. [ Links ]
21. Miller WL, Hartman KA, Burritt MF, Burnett JC Jr, Jaffe AS. Troponin, B-type natriuretic peptides and outcomes in severe heart failure: differences between ischemic and dilated cardiomyopathies. Clin Cardiol 2007;30:245-50. [ Links ]
22. Miller WL, Hartman KA, Burritt MF, Grill DE, Rodeheffer RJ, Burnett JC Jr, et al. Serial biomarker measurements in ambulatory patients with chronic heart failure: the importance of change over time. Circulation 2007;116:249-57. [ Links ]
23. Brouillard M, Reade R, Boulanger E, Cardon G, Dracon M, Dequiedt P, et al. Erythrocyte sedimentation rate, an underestimated tool in chronic renal failure. Nephrol Dial Transplant 1996; 11:2244-7. [ Links ]
24. Sharma R, Rauchhaus M, Ponikowski PP, Varney S, Poole-Wilson PA, Mann DL, et al. The relationship of the erythrocyte sedimentation rate to inflammatory cytokines and survival in patients with chronic heart failure treated with angiotensin-converting enzyme inhibitors. J Am Coll Cardiol 2000;36:523-8. [ Links ]
25. Van den Berghe G. Euthyroid sick syndrome. Curr Opin Anaesthesiol 2000;13:89-91. [ Links ]
26. Hamilton MA, Stevenson LW, Luu M,Walden JA. Altered thyroid hormone metabolism in advanced heart failure. J Am Coll Cardiol 1990;16:91-5. [ Links ]
27. Schmidt-Ott UM, Ascheim DD. Thyroid hormone and heart failure. Curr Heart Fail Rep 2006;3:114-9. [ Links ]
28. Uszko-Lencer NH, Bothmer F, van Pol PE, Schols AM. Measuring body composition in chronic heart failure: a comparison of methods. Eur J Heart Fail 2006;8:208-14. [ Links ]
29. Kistorp C, Faber J, Galatius S, Gustafsson F, Frystyk J, Flyvbjerg A, et al. Plasma adiponectin, body mass index, and mortality in patients with chronic heart failure. Circulation 2005;112:1756-62. [ Links ]
30. Das SR, Drazner MH, Dries DL, Vega GL, Stanek HG, Abdullah SM, et al. Impact of body mass and body composition on circulating levels of natriuretic peptides: results from the Dallas Heart Study. Circulation 2005;112:2163-8. [ Links ]
31. Mahon NG, Blackstone EH, Francis GS, Starling RC 3rd, Young JB, Lauer MS. The prognostic value of estimated creatinine clearance alongside functional capacity in ambulatory patients with chronic congestive heart failure. J Am Coll Cardiol 2002;40:1106-13. [ Links ]














