Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.77 n.5 Ciudad Autónoma de Buenos Aires sept./oct. 2009
CIRUGÍA CARDIOVASCULAR
Registro multicéntrico de disección aórtica aguda. Estudio RADAR. Resultados preliminares
Claudio HigaMTSAC, Javier Guetta†, Raúl A. BorracciMTSAC, Raúl Meribilhaa, María Pía Marturano†, Ricardo Marenchino, Mariano Benzadón, Pablo Comignani, Gustavo Bastianelli, Juan José FuselliMTSAC, en representación de los investigadores del estudio RADAR. Área de Investigación y Consejo de Emergencias Cardiovasculares de la Sociedad Argentina de Cardiología
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
† Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
Recibido: 19/06/2009
Aceptado: 04/08/2009
Dirección para separatas: Dr. Claudio Higa Sociedad Argentina de Cardiología Azcuénaga 980 (1115) Buenos Aires, Argentina
RESUMEN
Introducción
El síndrome aórtico agudo (SAA) representa aún hoy una de las más serias afecciones cardiovasculares debido a su alta morbilidad y mortalidad, por lo que el diagnóstico precoz es de vital importancia.
Objetivos
El Registro de la Sociedad Argentina de Cardiología de Disecciones AóRticas Agudas (RADAR) tiene por objetivo analizar las modalidades de presentación, el diagnóstico, el tratamiento y la mortalidad del SAA a través de un registro continuo de esta enfermedad poco prevaleciente.
Material y métodos
Desde febrero de 2007 hasta abril de 2009, 12 centros enrolaron 95 pacientes consecutivos admitidos con diagnóstico de SAA, de los que se obtuvieron las características clínicas basales, los estudios complementarios, el tipo de tratamiento y la evolución clínica.
Resultados
El 68% fueron hombres, la edad media fue de 58,8 ± 13,9 años, el 78% fueron disecciones aórticas de tipo A y el 22% de tipo B. El 84% de los pacientes eran hipertensos, el 28% tabaquistas y el 24% dislipidémicos. El dolor precordial o dorsal estuvo presente en el 85,1%. La mediana global del intervalo síntomas - inicio de la intervención fue de 18 horas (12-72). El 89% de las disecciones de tipo A y el 15% de las de tipo B recibieron tratamiento quirúrgico. Los betabloqueantes se utilizaron en el 64,7% de los casos, el nitroprusiato de sodio en el 47,4%, el ácido acetilsalicílico en el 15,8%, los anticoagulantes en el 3,2% y los trombolíticos en el 3,2%. La mortalidad global fue del 32,6%. La mortalidad en las disecciones de tipo A fue del 37,8% (31% en los operados versus 87,5% en los no operados; p = 0,01). La mortalidad de las disecciones de tipo B fue del 14% en los operados y del 12% en los no operados (p = ns). Se observó un patrón de variación horaria circadiana con respecto al horario del inicio de los síntomas, con un pico en las horas matinales. El análisis de regresión logística mostró que las variables independientes asociadas con la mortalidad hospitalaria fueron la edad mayor de 70 años y el ingreso con hipotensión arterial o shock.
Conclusiones
A pesar de los avances técnicos, la mortalidad global de los SAA sigue siendo elevada. Su detección requiere un alto nivel de sospecha por parte del médico para un diagnóstico y un tratamiento tempranos. Esta modalidad de registro continuo y multicéntrico permite una aproximación más real a la problemática de esta grave enfermedad en nuestro medio, a fin de optimizar su enfoque diagnóstico y terapéutico.
Palabras clave: Aorta; Disección aórtica; Registro; Mortalidad; Cirugía cardiovascular
Abreviaturas
ECG Electrocardiograma
SAA Síndrome aórtico agudo
TA Tensión arterial
SUMMARY
Multicenter Registry of Acute Aortic Dissection. The RADAR Study. Preliminary Results
Background
Acute aortic syndrome (AAS) still represents one of the most severe cardiovascular conditions due to its high mortality and morbidity; for this reason, it is extremely important to perform an early diagnosis of the disease.
Objectives
The Registro de la Sociedad Argentina de Cardiología de Disecciones AóRticas Agudas (RADAR registry) was designed to analyze the modalities of clinical presentation, diagnosis, treatment and mortality of AAS through a continuous registry of this not very prevalent disease.
Material and Methods
From February 2007 to April 2009, 95 patients consecutively admitted to 12 centers with a diagnosis of AAS were enrolled; basal clinical characteristics, complementary studies, type of treatment and clinical outcomes were obtained.
Results
Most patients were men (68%), mean age was 58.8±13.9 years, 78% were type A aortic dissections and 22% were type B. Eighty four percent of patients had hypertension, 28% were current smokers and 24% had dyslipemia. Chest pain or dorsal pain was present in 85.1% of cases. Global median time interval from onset of symptoms to intervention was 18 hours (12-72). Surgery was performed in 89% of type A and in 15% of type B dissections. Beta blockers were used in 64.7% of cases, sodium nitroprusside in 47.4%, aspirin in 15.8%, oral anticoagulant agents in 3.2% and thrombolytic drugs in 3.2%. Global mortality was 32.6%. Mortality rate of type A dissection was 37.8% (31% in patients undergoing surgery versus 87.5% in absence of surgical treatment; p=0.01). Dissection type B had mortality rates of 14% versus 12%, respectively (p=ns). A pattern of circadian variation regarding onset of symptoms was observed, with a peak in the morning hours. Logistic regression analysis showed that the independent variables associated with in-hospital mortality were age >70 years and the presence of hypotension or shock at admission.
Conclusions
Mortality from AAS is still high despite technical progress. Physicians should be alert to detect this condition in order to perform early diagnosis and treatment. This type of continuous and multicenter registry allows a more real approach to the problem related to this severe disease in our environment in order to optimize diagnostic and therapeutic strategies.
Key words: Aorta; Aortic Dissection; Registry; Mortality; Cardiovascular Surgery
INTRODUCCIÓN
El síndrome aórtico agudo (SAA) es un cuadro clínico que agrupa distintos procesos de la pared aórtica y representa una de las afecciones cardiovasculares más serias y de mayor riesgo, que puede alcanzar una mortalidad del 50% en las primeras 48 horas sin tratamiento (1) o del 15% al 30% con tratamiento quirúrgico, según las series publicadas. (2, 3) Está constituido por tres entidades: la disección aórtica, el hematoma intramural y la úlcera penetrante. (4) El SAA afecta aproximadamente a 20-40 casos/millón de habitantes/año, (5, 6) de los cuales el 80% son disecciones, el 15% son hematomas intramurales y el 5% son úlceras penetrantes.
Si bien en los últimos años se ha logrado una mejor comprensión de la fisiopatología de los SAA, sumado esto a los avances en el diagnóstico por imágenes y a las nuevas modalidades terapéuticas, la mortalidad sigue siendo elevada debido a la gravedad de la enfermedad y al retraso en el diagnóstico.
Varios grupos han publicado recientemente información sobre los factores de riesgo preoperatorios y el pronóstico de la enfermedad. (3, 7-14) No obstante, la mayoría de estos datos provienen de estudios retrospectivos con escaso número de pacientes recolectados en períodos cortos, sin diferenciar la disección de tipo A de la de tipo B. (9-12) En otras ocasiones, las series son más grandes, pero con pacientes recolectados en períodos demasiado largos (15 a 20 años), lo cual no hace comparables los resultados. Por el contrario, otros estudios son multicéntricos, pero con el sesgo de haber incluido pacientes atendidos en centros de alta complejidad, (3, 7, 8) lo que impide extrapolar los resultados a los del mundo real.
El Registro de Disecciones Aórticas Agudas (RADAR) tuvo como objetivo analizar las modalidades de presentación, diagnóstico, tratamiento y mortalidad del SAA en centros con cirugía cardíaca de la Ciudad Autónoma de Buenos Aires a través de un registro continuo.
MATERIAL Y MÉTODOS
Desde febrero de 2007 hasta abril de 2009 se incluyeron en forma prospectiva en un registro continuo pacientes de ambos sexos mayores de 18 años, con diagnóstico de disección aórtica o SAA de hasta 14 días de evolución que fueron atendidos en 12 centros de la ciudad de Buenos Aires. El diagnóstico se obtuvo a partir de los datos clínicos recolectados de la historia clínica, por los hallazgos de estudios por imágenes (radiografía de tórax, aortograma, tomografía computarizada, resonancia magnética y ecocardiograma) o por los hallazgos post mortem. Se excluyeron los pacientes con diagnóstico de disección aórtica de origen traumático. La decisión de que el registro fuera de carácter continuo se basó en la baja incidencia de las disecciones aórticas, por lo que se llevaron a cabo relevamientos periódicos en los centros. El registro fue coordinado en forma conjunta por el Área de Investigación y el Consejo de Emergencias de la Sociedad Argentina de Cardiología. El protocolo fue aprobado por el Comité de Bioética de la Sociedad Argentina de Cardiología y por las autoridades de cada centro participante; por otro lado, los pacientes y/o sus familiares firmaron el consentimiento informado previo a la inclusión en el registro. Los datos se recolectaron de las historias clínicas hospitalarias mediante el llenado de un formulario estructurado que contenía 104 variables correspondientes a campos de tipo epidemiológico y antecedentes clínicos, hallazgos del examen físico, resultados de estudios por imágenes y evolución clínica. Se definió crisis hipertensiva a la elevación de la tensión arterial (TA) por encima de 180/120 mm Hg, complicada con disfunción de órgano blanco, lo que requería la reducción inmediata de la TA para prevenir o limitar el daño de dicho órgano. La hipotensión/shock se definió con valores de TA sistólica < 90 mm Hg o volumen minuto urinario < 0,5 ml/kg/h. Se consideró síncope a la pérdida transitoria de la conciencia y del tono postural, de inicio relativamente rápido y recuperación espontánea, cuyo mecanismo subyacente fuera la hipoperfusión cerebral global. Por último, se definió insuficiencia renal aguda a un aumento del 50% del valor basal (para previos anormales), un valor de creatinina > 2 mg/dl para valores previos normales o al requerimiento de hemodiálisis.
Análisis estadístico
Las variables cualitativas se expresaron como porcentajes y las cuantitativas como medias y desviaciones estándar o medianas con sus respectivos intervalos intercuartiles 25- 75%, de acuerdo con las características de las distribuciones; la normalidad de estas últimas se evaluó con una prueba de bondad de ajuste. La comparación de la mortalidad se realizó con la prueba de chi cuadrado. Se realizó un análisis de regresión logística en el que la mortalidad hospitalaria fue la variable dependiente. Para el análisis cronobiológico del horario de inicio de los síntomas de disección aórtica se graficó la distribución de frecuencia para cada hora del día y se ajustó mediante una curva suavizada. Se consideraron significativos los valores de p menores de 0,05. Para este análisis se utilizó el software estadístico SPSS versión 13.0 (Chicago, Illinois).
RESULTADOS
Desde febrero de 2007 a abril de 2009 se incluyeron en el registro 95 pacientes con diagnóstico de SAA. El 68% (64 pacientes) eran hombres y la edad media fue de 58,8 ± 13,9 años. En el 78% (74 casos), las disecciones aórticas fueron de tipo A y en el 22% (21 casos) fueron de tipo B. En la Tabla 1 se describe el perfil clínico según el tipo de disección. Entre los fumadores, el 59% (31 casos) eran tabaquistas activos y el 31% (15 casos) ex fumadores. En un caso (1,2%), por anatomía patológica se detectó una aortitis (sifilítica) y en 5 casos (5,3%) se informó síndrome de Marfan. Un caso de disección estuvo relacionado con cirugía previa y otro con lesión iatrogénica por cateterismo. El 42% de los pacientes (40 casos) fueron derivados de otros centros, en su mayor parte por motivos relacionados con la falta de complejidad para efectuar su diagnóstico y/o tratamiento.
Tabla 1. Características clínicas de la población según el tipo de disección aórtica aguda

Presentación clínica, radiológica y electrocardiográfica
El dolor precordial o dorsal estuvo presente en el 85% (80 casos) de los pacientes, que en el 30% (28 casos) presentó un carácter migratorio. El 4,2% (4 casos) debutó con episodios de síncope. En el momento de la presentación clínica, el 10,5% (10 casos) presentaba crisis de hipertensión arterial, mientras que el 11,6% (11 casos) ingresó con un cuadro de hipotensión o shock. En el 7,4% (7 casos) se detectó taponamiento cardíaco, el 7,4% (7 casos) desarrolló insuficiencia renal, coma el 9,5% (9 pacientes), ausencia o déficit de pulso el 6,3% (6 casos), isquemia periférica el 7,4% (7 casos), isquemia medular el 6,3% (6 casos) y accidente cerebrovascular el 3,2% (3 casos).
Al ingreso, las radiografías de tórax mostraron imágenes de ensanchamiento mediastínico en el 67% (65 casos) de los pacientes (67,6% –50 casos– en las de tipo A versus 75% –15 casos– en las de tipo B).
El electrocardiograma fue normal o inespecífico en el 82% (77 casos) de la población, presentando signos de isquemia o infarto en el 10,5% (8 casos) (10,8% –10 casos– en las de tipo A y 10% –2 casos– en las de tipo B).
Hallazgos de los estudios por imágenes
En el 69% (66 casos) del total de los pacientes se realizó un ecocardiograma transtorácico, que fue positivo para el diagnóstico de disección en el 66% (43 casos), sospechoso en el 28% (19 casos) y negativo en el 6% (4 casos). El ecocardiograma transesofágico se realizó en el 60% (57 casos) de los pacientes, que fue positivo en el 96% de ellos (55 casos). Fue sospechoso sólo en el 1,7% (1 caso) y negativo en el mismo porcentaje. La tomografía computarizada de tórax se utilizó en el 67% de los pacientes (64 casos), con resultado positivo en el 85% (55 casos), sospechoso en el 12% (8 casos) y negativo en el 1,5% (1 caso). Sólo en el 8,4% (8 casos) se realizaron estudios de resonancia magnética para su diagnóstico, que fue positivo en el 85% de los casos (7 casos). En el 13% (14 casos), la evaluación se efectuó mediante cateterismo, que resultó positivo en el 92% (13 casos). Se realizó un solo estudio en el 40% (38 casos), mientras que en el 52% (49 casos) se necesitaron dos estudios. Las combinaciones de estudios más frecuentes fueron la del ecocardiograma transtorácico con la tomografía computarizada (26%, 24 casos) y la del ecocardiograma transtorácico y el ecocardiograma transesofágico (21%, 20 casos). En el 13% (12 casos) se realizó ecocardiograma transesofágico con tomografía computarizada; en todos los casos, ambos estudios fueron positivos. El 48,9% (36 casos) de las disecciones de tipo A presentaron insuficiencia aórtica de grado moderado a grave versus el 5% en las de tipo B. En el 29,7% (22 casos) de las disecciones de tipo A, el diámetro aórtico fue mayor de 6 cm versus el 5% en las de tipo B (1 caso). Se encontró permeabilidad de la falsa luz en el 58% (64 casos) de las disecciones de tipo A y en el 25% (5 casos) de las de tipo B. La falsa luz se halló parcialmente trombosada en el 14,9% de las disecciones de tipo A (11 casos) y en el 20% de las de tipo B (4 casos). Se observó trombosis total de la falsa luz en el 4,1% (3 casos) de las disecciones de tipo A y en el 30% de las disecciones de tipo B (6 casos). La úlcera penetrante se detectó en el 1,4% (1 caso) de las disecciones de tipo A y en el 10% (2 casos) de las de tipo B. El hematoma intramural se encontró en el 9,5% (7 casos) de las disecciones de tipo A y en el 30% (6 casos) de las disecciones de tipo B.
Cronobiología e intervalo entre los síntomas y el diagnóstico
En la Figura 1 se muestra la distribución de frecuencias del momento del día de aparición de los primeros síntomas de la disección. La información sobre la hora de inicio de los síntomas estuvo disponible en el 75% de los pacientes (72/95). Estos datos se obtuvieron por referencias del propio paciente, familiares o testigos. Los horarios se incluyeron en un análisis del ritmo circadiano de los horarios de inicio luego de la categorización por cada hora del día. La información sobre el intervalo entre el inicio de los síntomas y el comienzo de la intervención estuvo disponible en el 70% de la población, el cual fue de 14 horas (4-48) para todo tipo de disección. En las disecciones de tipo A, la mediana del intervalo de tiempo entre la aparición de los síntomas y el inicio de la intervención fue de 12 horas (4-48) y en las disecciones de tipo B dicho intervalo fue de 16 horas (6-56).

Fig. 1. Curva de la variación circadiana del inicio de los síntomas de disección aórtica.
Manejo y terapéuticas utilizadas
En forma global, el 74% (71 casos) de los pacientes fueron intervenidos quirúrgicamente. De las disecciones de tipo A operadas (89%, 66 casos), se realizó reemplazo de la aorta ascendente en el 92,6% (61 casos), reemplazo del cayado aórtico en el 21,8% (17 pacientes), reemplazo de la aorta descendente en el 10,6% (7 casos) y técnica de elephant trunk en el 6,1% (4 casos). Con respecto al tratamiento de la insuficiencia aórtica asociada, en el 19,7% (13 casos) se realizó resuspensión de las comisuras aórticas y en el 48,5% (32 casos) se efectuó reemplazo valvular aórtico. Se asoció cirugía de revascularización miocárdica en el 13% (9 casos) y reimplante coronario en el 37,9% (25 casos). La estrategia o combinación quirúrgica utilizada con más frecuencia en las disecciones de tipo A fueron el reemplazo valvular aórtico con tubo aórtico como único procedimiento (50%, 31 casos), seguido del reemplazo valvular aórtico con tubo aórtico y reimplante coronario (37%, 25 casos).
Con respecto al tratamiento farmacológico, los betabloqueantes se utilizaron en el 67,4% de los pacientes (64 casos), el nitroprusiato de sodio en el 47,4% (45 casos), el ácido acetilsalicílico en el 15,8% (15 casos), los anticoagulantes en el 3,2% (3 casos) y los trombolíticos en el 3,2% (3 casos). De esto se desprende que una quinta parte de la población (19%) recibió algún tipo de terapéutica antitrombótica/trombolítica.
En el 35% (7 casos) de las disecciones de tipo B se implantó una endoprótesis, mientras que en el 15% (3 casos) se realizó cirugía directa, ya sea reemplazo de la aorta descendente (15%, 3 casos) o fenestración quirúrgica (10%, 2 casos).
Evolución intrahospitalaria
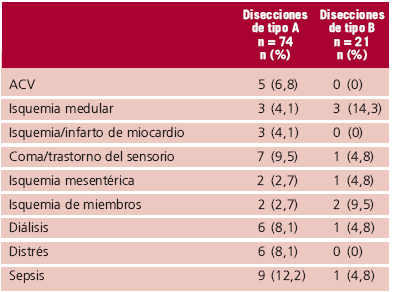
La mortalidad global fue del 32,6% (31 casos). La mortalidad en las disecciones de tipo A fue del 37,8% (28 casos): 31% en los operados (21 casos) versus 87,5% en los no operados (7 casos); p = 0,01. Dentro de las disecciones de tipo A, la mortalidad de los que se presentaron con hipotensión/shock o taponamiento cardíaco fue significativamente mayor que en los que no tuvieron esa presentación, 66% versus 28% (p = 0,004). En cambio, no se detectaron diferencias significativas entre los pacientes derivados de otros centros versus los ingresados directamente al centro tratante, 33% versus 36% (p = ns) ni entre los que ingresaron dentro de las 12 horas de evolución de los síntomas versus los que ingresaron más allá de ese tiempo: 36% versus 34% (p = ns). Por su parte, la mortalidad en las disecciones de tipo B fue del 14% (3 casos): 1 caso de 5 operados (20%) y 2 de 16 no operados (12%) (p = ns). En la Tabla 2 se muestran las principales complicaciones intrahospitalarias según el tipo de disección.
Tabla 2. Complicaciones intrahospitalarias según el tipo de disección
Predictores de mortalidad intrahospitalaria
En el análisis univariado, las variables correspondientes al momento de la presentación asociadas con mortalidad hospitalaria fueron edad > 70 años, hipotensión arterial/shock al ingreso, insuficiencia renal aguda, déficit de pulso, isquemia periférica, isquemia intestinal, accidente cerebrovascular, hipertensión arterial, insuficiencia aórtica de grado moderado a grave, hematoma intramural y úlcera penetrante. Luego del ajuste por medio del análisis de regresión logística, las variables asociadas independientemente con mortalidad fueron hipotensión arterial/shock al ingreso (OR 10,1 IC 95% 1,4-73, p = 0,02) y edad > 70 años (OR 7,7 IC 95% 2,2-27; p = 0,001).
DISCUSIÓN
La primera disección descripta en la literatura médica fue la del rey Jorge II de Inglaterra en el año 1760. El médico real, el Dr. Frank Nicholls, (15) realizó la necropsia en la que describió la presencia de hemopericardio y dilatación de la aorta ascendente con rotura de la íntima y la consiguiente extravasación de sangre entre sus capas. Un año más tarde, Morgagni (16) describió una disección de la aorta con rotura en la cavidad pericárdica y efectuó una serie de consideraciones interesantes al respecto. Este caso era el del rey Jorge II de Inglaterra, al que no menciona explícitamente, pero dice que el lector "identificará con facilidad". Gurin (17) practicó en 1935 la primera intervención quirúrgica, en la que realizó una fenestración en la arteria ilíaca. La era moderna de abordaje directo la inició Johns en 1953 al conseguir la sutura directa de la íntima. La reparación abierta de la disección de tipo B la llevaron a cabo De Bakey y Cooley (18) en 1953 y la de la aorta ascendente la realizó Morris (19) en 1963. En 1999, Dake (20) utilizó por primera vez una endoprótesis para tratar una disección aguda de la aorta.
El conocimiento acerca de la incidencia del síndrome aórtico agudo es limitada; algunos estudios sugieren una incidencia de 2,6 a 3,5 casos por 100.000 personas/año. (21)
Dado que es un proceso patológico de toda la aorta, su espectro clínico es muy variado y los síntomas pueden simular otras afecciones más comunes, como infarto agudo de miocardio o accidente cerebrovascular, y los hallazgos del examen físico pueden estar ausentes o sugerir otras patologías.
A pesar del adelanto en nuevas técnicas diagnósticas, la mortalidad no ha disminuido y el diagnóstico continúa siendo dificultoso y requiere un alto índice de sospecha por parte del médico.
RADAR es un registro multicéntrico sobre SAA en centros hospitalarios terciarios de nuestro medio, de carácter continuo y como tal es el primero llevado a cabo a nivel local.
El retraso en el diagnóstico puede ser mayor de 24 horas en el 39% de los casos; (22) en el Registro Español de Síndromes Aórticos (RESA), (23) el 70% de los pacientes tuvo confirmación diagnóstica dentro de las primeras 24 horas. Esta variable tiene implicaciones en la evolución, ya que a más precocidad en el diagnóstico, peor es el pronóstico de la población en estudio.
Al comparar nuestros resultados con los del International Registry of Acute Aortic Dissection (IRAD) (3) y del RESA, (23) podemos observar que la población es relativamente más joven que la de otros registros, 58 versus 60,9 años en el IRAD y 63,1 años en el RESA, que la proporción de hombres es intermedia con respecto a los dos registros en cuestión (68% versus 77,5% y 65,3%, respectivamente). Al igual que en otras series y registros, la radiografía de tórax fue normal en más del 30% de los pacientes. (3, 23, 24) Realizar el diagnóstico diferencial entre SAA y síndrome coronario agudo es un problema habitual en la práctica y dado que la estrategia terapéutica es totalmente diferente, es necesario un diagnóstico seguro. La manifestación de dolor torácico con ECG normal orienta a pensar más en SAA; sin embargo, aproximadamente el 10% de los pacientes presentaron anormalidades en el ECG compatibles con isquemia/necrosis al ingreso y el 19% recibió alguna estrategia antitrombótica/trombolítica. (5, 6, 25)
En cuanto a los métodos de diagnóstico por imágenes utilizados, la resonancia magnética nuclear, si bien posee mayor sensibilidad y especificidad, (26) se utilizó rara vez, tal vez debido a falta de disponibilidad, imposibilidad de monitorizar al paciente adecuadamente o incompatibilidad en cuanto al ingreso de pacientes con dispositivos metálicos previamente implantados. Algo similar sucedió con la aortografía que constituía el patrón oro previo y sin embargo fue reemplazada por otras técnicas como la ecocardiografía y la tomografía computarizada.
En nuestra serie se requirieron dos estudios diagnósticos en el 52% de los casos, similar a lo ocurrido en el RESA, que muestra que fue necesario realizar dos estudios en el 53,2%.
La mortalidad global fue del 32,9%, en tanto que fue del 27,4% en el IRAD (3) y del 35,4% en el RESA. (23) Como es de esperar, la mayor mortalidad ocurre en las primeras horas desde el inicio de los síntomas, lo que refuerza la necesidad de un rápido diagnóstico para el tratamiento urgente.
Otro aspecto interesante es que en el IRAD se realizó tratamiento médico en el 28% de los SAA de tipo A y éstos presentaron una mortalidad del 58%. En el RESA se efectuó tratamiento médico en el 20% de los SAA de tipo A, con una mortalidad de 71,2% y en nuestra serie, el 11% de los SAA de tipo A se trataron médicamente, con una mortalidad del 87%. Si bien la tasa de tratamiento médico en los SAA de tipo A en el IRAD fue mayor que la del Registro Español (23) y que la de nuestra serie, lo que sugiere una selección mayor de los casos quirúrgicos, llama la atención la baja mortalidad observada, del 58%.
Existe evidencia sobre la presencia de ritmo circadiano en la ocurrencia de eventos cardiovasculares.
En nuestro registro se halló una frecuencia mayor entre las 9:00 y las 11:00 am, además de otros dos picos entre las 3:00 y las 5:00 am y entre las 15:00 y las 17:00 pm.
Gallerani y colaboradores (27) publicaron una variación significativa del ritmo circadiano en los SAA, con un pico inicial durante las horas de la mañana entre las 8:00 y las 10:00 am y otro por la tarde, aproximadamente a las 8:00 pm.
Sumiyoshi y colaboradores, (28) en Japón, hallaron una frecuencia mayor de disecciones en horas de la mañana, aunque con menor significación estadística, con un segundo pico entre las 5:00 y las 7:00 pm.
En el IRAD también se halló un pico matinal entre las 8:00 y las 9:00 am.
Este patrón matinal, semejante al de otras patologías cardiovasculares, sugiere mecanismos fisiopatológicos similares que pueden ser responsables del desencadenamiento de estos eventos. El incremento de la tensión arterial, de la frecuencia cardíaca, de la actividad simpática, del tono vascular basal y de la actividad protrombótica muestra un ritmo circadiano que se correlaciona con el de los eventos cardiovasculares, por lo que pueden ser los disparadores de la rotura aórtica en las primeras horas de la mañana. (29, 30)
Respecto de los predictores de mortalidad intrahospitalaria, nuestros resultados son en parte consistentes con el modelo del IRAD: edad mayor de 70 años y la presentación con hipotensión arterial/shock. Posiblemente, con la inclusión de un número mayor de casos podamos identificar otras variables como las halladas también en ese estudio: dolor migratriz, cirugía cardíaca previa, signos de isquemia o infarto en el ECG, taponamiento cardíaco o déficit de pulso.
Limitaciones
Si bien el Registro SAC de Disecciones AóRticas Agudas es la primera y más grande experiencia al respecto realizada en nuestro país, posee algunas limitaciones.
Los centros involucrados en el registro son centros terciarios de referencia, de mediano a alto volumen de cirugía aórtica y sólo de la ciudad de Buenos Aires.
Sólo se incluyeron a los pacientes que ingresaron vivos al hospital y algunos datos se obtuvieron de las historias clínicas.
Si bien en los pacientes que recibieron manejo médico no hubo confirmación diagnóstica por anatomía patológica, la evaluación fue realizada en centros de referencia con técnicas de diagnóstico por imágenes con aceptable sensibilidad y especificidad.
CONCLUSIONES
Pese a que en los últimos años se incrementaron el aporte de la tecnología en los estudios por imágenes y su disponibilidad, la detección de esta mortal enfermedad, aún en la actualidad, depende del grado de sospecha clínica presente en el momento del contacto con el personal de la salud, sobre todo teniendo en cuenta su baja prevalencia en comparación con otras causas de síntomas precordiales como los coronarios o la embolia pulmonar. Posiblemente éste sea uno de los puntos que debemos enfocar y mejorar. Vale la pena señalar una vez más que la mortalidad comparando distintas series no deja lugar a dudas de que la disección aórtica sigue siendo una entidad muy grave, cuyo desenlace es la muerte en uno de cada tres casos. Con las limitaciones anteriormente referidas, este tipo de registros continuos nos permitirá conocer cada día más su estado actual en cuanto a evolución, formas de presentación, estrategias diagnósticas utilizadas, procedimientos quirúrgicos y percutáneos a los que se somete a los pacientes, un número mayor de variables predictoras de mortalidad que puedan ser de utilidad a la hora de tomar decisiones en pacientes de alto riesgo y el interesante comportamiento cronobiológico, dentro de otros futuros aspectos que el desarrollo del estudio nos permitirá conocer e investigar, con la sola intención de aproximarnos más a la problemática que rodea a esta enfermedad en nuestro medio.
INVESTIGADORES PRINCIPALES DEL ESTUDIO RADAR (por orden alfabético del centro participante)
- Alemán, Hospital: Pablo Comignani, Blas Mancini, Claudio Higa.
- Argerich, Hospital: Gustavo Bastianelli, Alberto Bartolomé, Sandro Belforte, Walter Esteban, Jorge Estrada, Victorio Picone.
- Bazterrica, Clínica: Miguel Rubio, Raúl A. Borracci, Víctor Mauro, Carlos Barrero.
- CEMIC: Javier Guetta, Diego Arakaki, Juan José Fuselli.
- del Sol, Clínica: Juan Gagliardi.
- FLENI: Hernán Cohen Arazi, Silvina Waldman, Carlos Nojek.
- Fundación Favaloro: María Pía Marturano, Raúl Merbilhaa, Roberto Favaloro.
- Güemes, Sanatorio: Ricardo Villaroel, Ariel Sosa.
- Instituto Cardiovascular de Buenos Aires: Mariano Benzadón, Fernando Botto, Daniel Navia.
- Italiano, Hospital: Ricardo Marenchino, Daniel Bracco.
- de los Arcos, Sanatorio: Félix Ramírez, Sergio Muryan, Alfredo Larraburu.
- Santa Isabel, Clínica: Yanina Castillo Costa.
Agradecimientos
El de siempre: a Liliana Capdevila por su capacidad, cooperación y afectividad.
1. Anagnostopoulos CE, Prashakar MJ, Kittle CF. Aortic dissections and dissecting aneurysms. Am J Cardiol 1972;30:263-73. [ Links ]
2. Miller DC, Mitchell RS, Oyer PE, Stinson EB, Jamieson SW, Shumway NE. Independent determinants of operative mortality for patients with aortic dissections. Circulation 1984;70:I153-64. [ Links ]
3. Hagan PG, Nienaber CA, Isselbacher EM, Bruckman D, Karavite DJ, Russman PL, et al. The International Registry of Acute Aortic Dissection (IRAD): new insights into an old disease. JAMA 2000; 283:897-903. [ Links ]
4. Vilacosta I, Román JA. Acute aortic syndrome. Heart 2001;85:365-8. [ Links ]
5. Tsai TT, Nienaber Ch, Eagle KA. Acute aortic syndromes. Circulation 2005;112:3802-13. [ Links ]
6. Khan IA, Nair CK. Clinical, diagnostic, and management perspectives of aortic dissection. Chest 2002;122:311-28. [ Links ]
7. Mehta RH, Suzuki T, Hagan P, Bossone E, Gilon D, Llovet A, et al; International Registry of Acute Aortic Dissection (IRAD) Investigators. Predicting death in patients with acute type A aortic dissection. Behalf of the International Registry of Acute Aortic Dissection (IRAD) investigators. Circulation 2002;105:200-6. [ Links ]
8. Trimarchi S, Nienaber CA, Rampoldi V, Myrmel T, Suzuki T, Bossone E, et al. Role and results of surgery in acute type B aortic dissection: insights from the International Registry of Acute Aortic Dissection (IRAD). Circulation 2006;114:I357-64. [ Links ]
9. Umaña JP, Lai DT, Mitchell RS, Moore KA, Rodriguez F, Robbins RC, et al. Is medical therapy still the optimal treatment strategy for patients with acute type B aortic dissection? J Thorac Cardiovasc Surg 2002;124:896-910. [ Links ]
10. Bavaria JE, Brinster DR, Gorman RC, Woo YJ, Gleason T, Pochettino A. Advances in the treatment of acute type A dissection: an integrated approach. Ann Thorac Surg 2002;74:S1848-52. [ Links ]
11. Ehrlich MP, Ergin MA, McCullough JN, Lansman SL, Galla JD, Bodian CA, et al. Results of immediate surgical treatment of all acute type A dissections. Circulation 2000;102:III248-52. [ Links ]
12. Kallenbach K, Oelze T, Salcher R, Hagl C, Karck M, Leyh R, et al. Evolving strategies for treatment of acute aortic dissection type A. Circulation 2004;110:II243-9. [ Links ]
13. Evangelista A, Mukherjee D, Mehta R, O'Gara P, Fattori R, Cooper JM, et al; International Registry of Aortic Dissection (IRAD) Investigators. Acute intramural hematoma of the aorta a mystery in evolution. Circulation 2005;111:1063-70. [ Links ]
14. Suzuki T, Metha R, Ince H, Nagai R, Sakomura Y, Weber F, et al; International Registry of Aortic Dissection. Clinical profiles and outcomes of acute type B aortic dissection in the current era: lessons from the International Registry of Aortic Dissection (IRAD). Circulation 2003;108:II312-7. [ Links ]
15. Nicholls F. Observations concerning the body of his late majesty, October 26, 1760. Philos Trans R Soc Lond A 1761;52:265-74. [ Links ]
16. Morgagni GB. De sedibus et causis morborum per anatomen indagatis. Venecia; 1761. [ Links ]
17. Gurin D, Bulmer JW, Derby R. Dissecting aneurysms of the aorta: diagnosis and operative relief of acute arterial obstruction due to this cause. NY State J Med 1935;35:1200-2. [ Links ]
18. De Bakey ME, Cooley DA. Successful resection of aneurysm of thoracic aorta and replacement by graft. J Am Med Assoc 1953; 152:673-6. [ Links ]
19. Morris Jr GC, Henly WS, De Bakey ME. Correction of acute dissecting aneurysm of aorta with valvular insufficiency. JAMA 1963;184:63-4. [ Links ]
20. Dake MD, Kato N, Mitchell RS, Semba CP, Razavi MK, Shimono T, et al. Endovascular stent-graft placement for the treatment of acute aortic dissection. N Engl J Med 1999;340:1546-52. [ Links ]
21. Bickerstaff LK, Pairolero PC, Hollier LH, Melton LJ, Van Peenen HJ, Cherry KJ, et al. Thoracic aortic aneurysms: a population-based study. Surgery 1982;92:1103-8. [ Links ]
22. Klompas M. Does this patient have an acute thoracic aortic dissection? JAMA 2002;287:2262-72. [ Links ]
23. Evangelista A, Padilla F, López-Ayerbe J, Calvo F, López-Pérez JM, Sánchez V, et al. Spanish Acute Aortic Syndrome Study (RESA). Better diagnosis is not reflected in reduced mortality. Rev Esp Cardiol 2009;62:255-62. [ Links ]
24. von Kodolitsch Y, Nienaber CA, Dieckmann C, Schwartz AG, Hofmann T, Brelenfeld C, et al. Chest radiography for the diagnosis of acute aortic syndrome. Am J Med 2004;116:73-7. [ Links ]
25. Hansen MS, Nogareda GJ, Hutchison SJ. Frequency of and inappropriate treatment of misdiagnosis of acute aortic dissection. Am J Cardiol 2007;99:852-6. [ Links ]
26. Shiga T, Wajima Z, Apfel C, Inoue T, Ohe Y. Diagnostic accuracy of transesophageal echocardiography, helical computed tomography, and magnetic resonance imaging for suspected thoracic aortic dissection: systematic review and meta-analysis. Arch Intern Med 2006;166:1350-6. [ Links ]
27. Gallerani M, Portaluppi F, Grandi E, Manfredini R. Circadian rhythmicity in the occurrence of spontaneous acute dissection and rupture of thoracic aorta. J Thorac Cardiovasc Surg 1997;113:603-4. [ Links ]
28. Sumiyoshi M, Kojima S, Arima M, Suwa S, Nakazato Y, Sakurai H, et al. Circadian, weekly, and seasonal variation at the onset of acute aortic dissection. Am J Cardiol 2002;89:619-23. [ Links ]
29. Mehta RH, Manfredini R, Hassan F, Sechtem U, Bossone E, Oh JK, et al; International Registry of Acute Aortic Dissection (IRAD) Investigators. Chronobiological patterns of acute aortic dissection. Circulation 2002;106:1110-5. [ Links ]
30. Portaluppi F, Manfredini R, Fersini C. From a static to a dynamic concept of risk: the circadian epidemiology of cardiovascular events. Chronobiol Int 1999;16:33-49. [ Links ]














