Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista argentina de cardiología
On-line version ISSN 1850-3748
Rev. argent. cardiol. vol.78 no.4 Ciudad Autónoma de Buenos Aires July/Aug. 2010
CARDIOLOGÍA PEDIÁTRICA
Cirugía de Rastelli: impacto adverso de la comunicación interventricular no relacionada con los grandes vasos en los resultados quirúrgicos
Claudia N. Villalba1, Marcela I. Woloszyn2, Mariela D. Mouratian3, Jorge Barreta4, Juan P. LauraMTSAC, 5, Horacio FaellaMTSAC, 6, Horacio CapelliMTSAC, 7
Servicio de Cardiología - Hospital de Pediatría "Prof. Dr. Juan P. Garrahan". Buenos Aires, Argentina
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
1 Jefa de Residentes de Cardiología
2 Becaria de Cardiología
3 Médica Asistente del Servicio de Cardiología
4 Médico Principal de Cirugía Cardiovascular
5 Jefe del Servicio de Cirugía Cardiovascular
6 Jefe del Servicio de Hemodinamia
7 Jefe del Servicio de Cardiología
Recibido: 27/07/2009
Aceptado: 01/03/2010
Dirección para separatas: Dr. Horacio Capelli Libertador 2630 (1425) Buenos Aires Tel. 011-4801-3586 Fax: 011-4806-9251 e-mail: horaciocapelli027@hotmail.com
RESUMEN
Introducción
La evolución de los pacientes operados con técnica de Rastelli revela que se trata de un procedimiento quirúrgico complejo no exento de morbilidad y mortalidad a mediano y a largo plazos. Las complicaciones serían, aparentemente, más frecuentes cuando la comunicación interventricular (CIV) es anatómicamente remota o no relacionada con la aorta.
Objetivo
Evaluar el impacto de la localización anatómica de la CIV en la cirugía de Rastelli.
Material y métodos
Se incluyeron 47 pacientes con una media (X) de seguimiento posquirúrgico de 6 años (15 meses-14 años). Los pacientes se subdividieron en: grupo I, CIV relacionada con la aorta (n = 29) y grupo II, CIV remota o no relacionada (n = 18).
Resultados
En el posquirúrgico inmediato, las reoperaciones (p = 0,05) fueron más frecuentes en el grupo II, en el cual se observó también una tendencia a mayor frecuencia de arritmias (p = 0,06).
Luego de una X = 3 años (1 día-13 años) posquirúrgicos se realizaron 27 reoperaciones en 22 pacientes. Se cerró CIV residual en 11 pacientes a una X = 1 mes. En 8 de ellos, la CIV era remota (p =0,007). Desarrollaron estenosis subaórtica que requirieron cirugía 6 pacientes a una X = 5 años.
Se reemplazó el conducto ventrículo derecho-arteria pulmonar en 12 pacientes a una X = 5 años. La mortalidad en el período posquirúrgico inmediato fue del 6% (3 pacientes). La mortalidad global fue del 17,2% (n = 8); 7 pacientes tenían CIV no relacionada (p = 0,003).
Conclusiones
La CIV remota en la cirugía de Rastelli se asocia con: 1) mayor mortalidad, 2) mayor frecuencia de reoperaciones en el posquirúrgico inmediato y 3) tendencia a mayor frecuencia de arritmias en el posquirúrgico inmediato.
Palabras clave Abreviaturas: Cirugía cardíaca; Ventrículo derecho con doble salida; Transposición de los grandes vasos; Estenosis pulmonar
SUMMARY
The Rastelli Procedure: Adverse Impact in Surgical Outcomes of a Ventricular Septal Defect Noncommitted to the Great Arteries
Background
The Rastelli procedure is complex surgical procedure with marked morbidity and mortality in the medium and long-term follow-up. These adverse outcomes seem to be more frequent when the ventricular septal defect (VSD) is anatomically remote or noncommitted to the aorta.
Objective
To evaluate the impact of the anatomical location of the VSD on the outcomes of the Rastelli procedure.
Material and Methods
A total of 47 patients were included with a mean follow-up of 6 years after surgery (15 months-14 years). Patients were divided into two groups: group I (committed VSD, n=29) and group II (remote or noncommitted VSD, n=18).
Results
During the immediate postoperative period, reoperations and arrhythmias were more frequent in group II (p=0.05 and p=0.06, respectively).
After a mean follow-up of 3 years (1 day-13 years) following surgery, 22 patients underwent 27 reoperations. A residual VSD was closed in 11 patients at a mean of 1 month, 8 of which were remote VSD (p=0.007). Six patients developed subaortic stenosis requiring surgery at a mean of 5 years.
The right ventricleto-pulmonary artery conduit was replaced in 12 patients at a mean of 5 years. Immediate postoperative mortality was 6% (3 patients). Global mortality was 17.2% (n=8); 7 patients had noncommitted VSD (p=0.003).
Conclusions
Remote VSD in patients undergoing the Rastelli procedure is associated with: 1) increased mortality, 2) greater incidence of reoperations in the immediate postoperative period, and, 3) a trend towards greater incidence of arrhythmias in the immediate postoperative period.
Key words: Cardiac Surgery; Double Outlet Right Ventricle;Transposition of the Great Arteries; Pulmonary Stenosis
Abreviaturas
ARM Asistencia respiratoria mecánica
ASP Anastomosis subclaviopulmonar
BAV Bloqueo auriculoventricular
CEC Circulación extracorpórea
CIA Comunicación interauricular
CIV Comunicación interventricular
DSVD Doble salida del ventrículo derecho
EP Estenosis pulmonar
RIVA Ritmo idioventricular acelerado
TGV Transposición de los grandes vasos
VD-AP Ventrículo derecho-arteria pulmonar
X Media
INTRODUCCIÓN
Giancarlo Rastelli propuso en 1969 la cirugía que hoy lleva su nombre para el tratamiento quirúrgico de pacientes con transposición de los grandes vasos (TGV) con comunicación interventricular (CIV) y estenosis pulmonar (EP). (1-3) Posteriormente, este procedimiento quirúrgico también se aplicó a otras cardiopatías, como doble salida del ventrículo derecho (DSVD) con estenosis pulmonar. (4)
El gran beneficio de esta técnica es que preserva dos ventrículos funcionantes (corrección biventricular) y la aorta queda conectada con el ventrículo izquierdo. (5) Se trata de un procedimiento quirúrgico complejo no exento de morbilidad a mediano y a largo plazos. (6) Las complicaciones más frecuentes son la presencia de una CIV residual, el desarrollo de obstrucción al tracto de salida del ventrículo izquierdo, estenosis o insuficiencia del conducto entre el ventrículo derecho y la arteria pulmonar (VD-AP) (7-9) y las arritmias ventriculares. (10)
La tunelización del ventrículo izquierdo hasta la aorta que emerge del ventrículo derecho es técnicamente más fácil cuando la CIV está relacionada con los grandes vasos. Por el contrario, cuando la CIV tiene una posición anatómica remota respecto de los vasos, como sucede en un tercio de los casos, la cirugía es técnicamente más dificultosa. En este último grupo de pacientes se puede optar por una variante de corrección biventricular: cirugía de Nikaidoh (traslocación aórtica con reconstrucción de ambos tractos de salida) (7, 11, 12) o una corrección univentricular mediante cirugía de Fontan-Kreutzer (bypass del ventrículo derecho).
A pesar de que uno de los factores determinantes para la elección de la mejor opción quirúrgica en este grupo es la posición anatómica del defecto interventricular, así como la presencia de inserciones subvalvulares tricuspídeas y/o mitrales en los bordes del defecto que dificulten o impidan la tunelización del ventrículo izquierdo hacia la aorta, (13-17) no hemos encontrado referencias en la bibliografía acerca de la evolución de la cirugía de Rastelli en función del tipo de CIV. Por ello, el objetivo del presente estudio fue evaluar el impacto de la localización anatómica de la CIV en los resultados posquirúrgicos inmediatos y en la evolución a corto y a mediano plazos de la cirugía de Rastelli.
MATERIAL Y MÉTODOS
Estudio de diseño cohorte retrospectivo, en el que se incluyeron 47 pacientes operados con la técnica de Rastelli entre enero de 1989 y diciembre de 2007 en el Hospital de Pediatría Prof. Dr. Juan P. Garrahan.
Se excluyeron los pacientes con transposición congénitamente corregida de los grandes vasos que requirieron, además de cirugía Rastelli, un switch auricular asociado, DSVD y TGV con CIV asociados con atresia pulmonar con mala anatomía del árbol vascular pulmonar y pacientes perdidos en el seguimiento.
La edad media de cirugía fue de 4 años (15 meses-8 años). El peso medio fue de 14 kg (6,300-22 kg).
Se identificaron dos variantes anatómicas: TGV en 24 pacientes y DSVD en 23. La obstrucción a la salida del ventrículo derecho fue secundaria a estenosis pulmonar en 41 pacientes y atresia pulmonar en 6. La CIV fue subaórtica en 23 pacientes (49%), subpulmonar en 3 (6,4%), subarterial (doblemente relacionada) en 3 (6,4%), muscular en 9 (19%) y del inlet en 9 pacientes (19%). Los pacientes se subdividieron en dos grupos, de acuerdo con la relación de la CIV con los grandes vasos: grupo I, CIV relacionada (29 pacientes) y grupo II, CIV no relacionada (18 pacientes). Se consideró CIV relacionada a la ubicada en posición subaórtica o subarterial y a aquellos defectos perimembranosos o musculares suficientemente próximos a la aorta que en la evaluación ecocardiográfica no daban la impresión de que dificultarían la tunelización desde el ventrículo izquierdo hasta la aorta originada en el ventrículo derecho. Por el contrario, se consideró CIV no relacionada a la ubicada en el inlet, como también a la muscular en posición remota respecto de la aorta.
Las anomalías asociadas fueron ductus arterioso permeable en 16 pacientes, arco aórtico derecho en 7, comunicación interauricular (CIA) en 6, anomalía coronaria en 6, doble sistema cava superior en 7, yuxtaposición de orejuelas en 3, situs inversus con dextrocardia en 3, straddling tricuspídeo en 3, displasia tricuspídea en 2, anillo vascular en 1, canal auriculoventricular completo en 1 paciente.
El diagnóstico se realizó en base a los hallazgos clínicos, radiológicos, electrocardiográficos y fundamentalmente ecocardiográficos y angiográficos.
Los procedimientos paliativos preoperatorios incluyeron septostomía auricular con balón y anastomosis subclavio-pulmonar (ASP). Requirieron septostomía auricular 11 pacientes a una edad media de 3,4 meses (1 día de vida-14 meses). Se realizaron 42 ASP en 38 pacientes a una edad media de 6,4 meses (1 día de vida-30 meses) y consistieron en ASP izquierda en 28, ASP derecha en 6 y ambas en 4 pacientes.
Las características de la población estudiada se describen en la Tabla 1.
Tabla 1. Características de la población operada con técnica de Rastelli

Técnica quirúrgica
En los 47 pacientes se realizó esternotomía mediana, bypass cardiopulmonar con canulación de ambas cavas y solución cardiopléjica. El tiempo medio del bypass fue de 186,76 min (83-420) y el tiempo medio de clampeo aórtico fue de 91,86 min (44-187).
En todos los casos la CIV se tunelizó hacia la aorta utilizando parche de Dacron.
Para la reconstrucción del tracto de salida del ventrículo derecho se utilizó homoinjerto aórtico en 18 pacientes, homoinjerto pulmonar en 22 y tubo de pericardio en 7. Se realizaron además procedimientos asociados en 32 pacientes: ampliación de CIV en 16, resección del septum infundibular en 13, cierre de CIA en 3, plástica de tronco y/o ramas pulmonares en 3, plástica tricuspídea en 2, desinserción de cuerdas tricuspídeas en 2 y plástica mitral en 1.
Seguimiento
Todos los pacientes incluidos en el presente trabajo fueron seguidos desde el egreso hospitalario hasta el final del estudio con una media de seguimiento posquirúrgico de 6 años (15 meses-14 años).
Todos fueron evaluados en nuestra institución mediante examen fisico, telerradiografía de tórax, electrocardiograma, ecocardiograma Doppler color, ergometría y Holter de 24 horas. Requirieron además cateterismos cardíacos 20 pacientes.
Análisis estadístico
Para el almacenamiento de los datos se utilizó el programa Microsoft Office Excel 2003®. El análisis se realizó con el paquete estadístico del programa Statistix 8.0®.
Para todas las variables se estableció la distribución de frecuencias y/o porcentajes en relación con el total de casos y de acuerdo con ello, los valores se expresaron como proporciones, media y desviación estándar o mediana y rango intercuartil.
Para las variables continuas se utilizaron la prueba de la t o la de Mann-Whitney según correspondiera. Para las proporciones se emplearon la prueba exacta de Fischer o la de chi cuadrado. Se consideró diferencia significativa una p < 0,05.
El cálculo de OR se realizó con sus respectivas bandas de confianza del 95%.
Para calcular la sobrevida a mediano plazo se utilizó el método de Kaplan-Meier.
RESULTADOS
Tiempo de circulación extracorpórea y clampeo aórtico
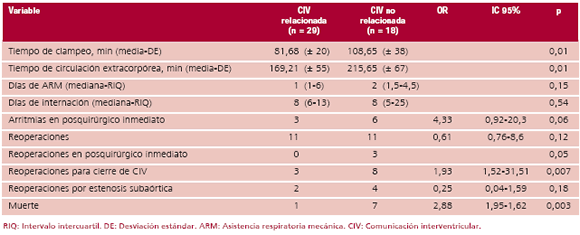
La media de bypass y clampeo aórtico fue de 169,21 min (± 55) y 81,68 min (± 20), respectivamente, para el grupo I (CIV relacionada) y de 215,65 (± 67) y 108,65 min (± 38), respectivamente, para el grupo II (CIV no relacionada) (p = 0,01).
Días de asistencia respiratoria mecánica y de internación
La mediana de tiempo de asistencia respiratoria mecánica (ARM) y de internación fueron de 1 día (1-6 días) y 8 días (6-13 días) para el grupo I y de 2 días (1,5-4,5 días) y 8 días (5-25 días) para el grupo II (p = 0,15 y p = 0,54, respectivamente).
Mortalidad
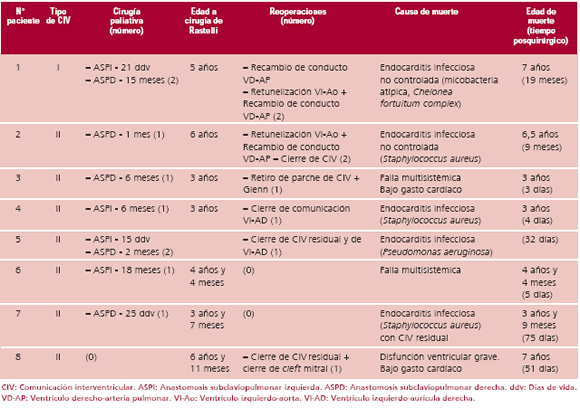
Durante el posquirúrgico inmediato murieron por falla multisistémica 3 pacientes (6%) en un tiempo medio de 4 días (3-5 días). Las cinco defunciones restantes se produjeron a una media de 5 meses (2-17 meses), de lo que resulta que la mortalidad de la evolución a mediano plazo fue del 10,6%. Siete de los 8 pacientes fallecidos tenían una CIV remota (p = 0,003) (Tabla 2).
Tabla 2. Análisis de la mortalidad
Sobrevida
La sobrevida global, con un seguimiento medio de 6 años (15 meses-14 años) después de la cirugía correctora, fue del 82,8%; fue mayor en el grupo de pacientes con CIV relacionada (p = 0,003) (Figura 1).

Fig. 1. Sobrevida después de la cirugía de Rastelli en los dos grupos comparados.
Arritmias
En el posquirúrgico inmediato presentaron arritmias 9 pacientes: bloqueo auriculoventricular (BAV) 4, taquicardia de la unión 3 y ritmo nodal 2. Observamos una tendencia a mayor frecuencia de arritmias en el grupo II (6 pacientes) que en el grupo I (3 pacientes) (p = 0,06) y no encontramos relación con la ampliación de la CIV durante la cirugía (p = 0,64). Dos de los 4 pacientes con BAV mencionados requirieron la colocación de un marcapasos definitivo; ambos pertenecían al grupo II (p = 0,14).
En la evolución alejada, un paciente presentó un episodio de taquicardia ventricular con imagen de bloqueo de rama izquierda a los 3 años de la cirugía de Rastelli, que tuvo como sustrato hemodinámico subyacente estenosis grave del homoinjerto con presión en el ventrículo derecho del 80% de la sistémica. La arritmia no se repitió luego del recambio del homoinjerto y de la normalización de la presión en el ventrículo derecho. Otro paciente presentó ritmo nodal con ritmo idioventricular acelerado (RIVA) a los 8 años de la cirugía correctora. Ambos pacientes pertenecían al grupo II (p = 0,14).
Reintervenciones
Luego de un período medio de 3 años (1 día-13 años) de la cirugía correctora se realizaron 39 reintervenciones: 12 cateterismos intervencionistas en 9 pacientes y 27 reoperaciones en 22.
Cateterismos intervencionistas
Los cateterismos intervencionistas realizados consistieron en angioplastia con balón del homoinjerto estenótico en 9 pacientes, angioplastia con balón de ramas pulmonares estenóticas en 2, colocación de stent en ramas pulmonares en 2, embolización de colaterales aortopulmonares en 1, de la vena cava superior izquierda persistente en 1 y cierre de comunicación ventrículo izquierdo-aurícula derecha en 1 (Figura 2).
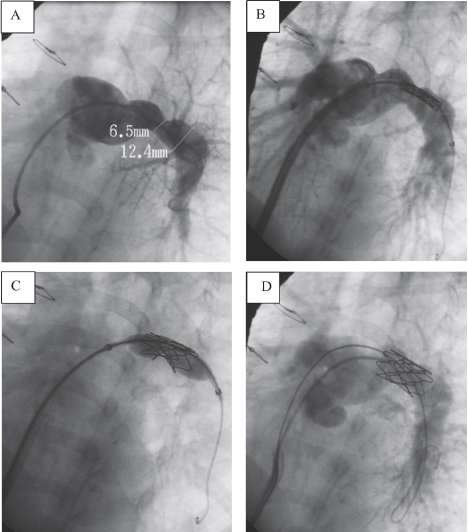
Fig. 2. Paciente con DSVD con CIV y EP con antecedente de anastomosis subclaviopulmonar izquierda a los 7 meses de edad, operado con técnica de Rastelli a los 3 años y 7 meses de edad, que requirió a los 7 meses posquirúrgicos dilatación de rama pulmonar derecha y colocación de stent en rama pulmonar izquierda. Las angiografías ilustran este último procedimiento.
Reoperaciones
Las causas de reoperación fueron cierre de la CIV, resección de estenosis subaórtica y/o retunelización de ventrículo izquierdo-aorta y reemplazo del conducto VD-AP.
En el posquirúrgico inmediato fueron reoperados 3 pacientes (6%): retunelización de ventrículo izquierdo-aorta en 1 y cierre de la CIV en 2. Los 3 pacientes tenían CIV no relacionada (p = 0,05).
Requirieron reoperación para cierre de la CIV 11 pacientes (23%) en un tiempo medio de 1 mes (1 día-6 meses). En 8 de estos pacientes, la CIV era no relacionada (p = 0,007). La CIV fue secundaria al desarrollo de endocarditis infecciosa en 6 pacientes.
Desarrollaron estenosis subaórtica significativa que requirió cirugía 6 pacientes (12,8%) a una media de 5 años (2-9 años). Cuatro de estos pacientes pertenecían al grupo II (p = 0,31) (Figura 3).

Fig. 3. Imagen ecocardiográfica de un paciente con DSVD con CIV y EP operada con técnica de Rastelli a los 3 años y 7 meses de edad que desarrolló estenosis subaórtica grave a los 5 años posquirúrgicos. En este paciente, la CIV era subaórtica. A la izquierda (A y B), en un eje largo paraesternal izquierdo, obsérvese la estenosis subaórtica y la angulación anterior y derecha del túnel aorta-ventrículo izquierdo. A la derecha (C), en una vista apical de cinco cámaras, se registra el gradiente de estenosis subaórtica grave.
Se reemplazó el conducto VD-AP en 12 pacientes (25%) en un tiempo medio de 5 años (3 meses-13 años). Las indicaciones de recambio fueron estenosis en 7, insuficiencia en 2, endocarditis infecciosa en 2, estenosis e insuficiencia en 1.
De los 12 pacientes que requirieron recambio del conducto VD-AP, 5 tenían CIV no relacionada (p = 0,78). Con respecto al tipo de conducto reemplazado, 6 fueron homoinjertos aórticos recambiados a una X de 40 ± 22 meses, 5 homoinjertos pulmonares a una X de 40 ± 23 meses y 1 tubo de pericardio a 137 meses. No encontramos una diferencia significativa en la durabilidad de los dos tipos de homoinjertos utilizados entre el ventrículo derecho y la arteria pulmonar (p = 0,56).
Los resultados se resumen en la Tabla 3.
Tabla 3. Resultados de la cirugía de Rastelli
DISCUSIÓN
El tratamiento convencional de la TGV con CIV y E P, así como de la DSVD con E P, es la cirugía de Rastelli. (2, 18) La evolución clínica a mediano y a largo plazos revela que estos pacientes no están exentos de complicaciones, así como de la necesidad de reintervenciones. (8, 9, 19) Éstas serían, aparentemente, más frecuentes en pacientes con CIV en posición anatómica remota respecto de la aorta. Tanto es así que, en presencia de este tipo de CIV, algunos centros prefieren no forzar una cirugía biventricular, sino seguir el camino de la corrección univentricular.
En este trabajo retrospectivo, donde hemos comparado la evolución de los pacientes con cirugía de Rastelli que tenían CIV relacionada con la aorta con aquellos que tenían CIV no relacionada, confirmamos contundentemente que la CIV remota influye en forma adversa en los resultados. De hecho, en este subgrupo de pacientes de nuestra serie fueron mayores la mortalidad, el requerimiento de reoperaciones tempranas, la incidencia de CIV residual, la presencia de arritmias y el desarrollo de estenosis subaórtica que en los pacientes con CIV relacionada con los grandes vasos.
En cuanto a la mayor mortalidad, creemos que es atribuible a la mayor complejidad quirúrgica, lo que conlleva un tiempo de circulación extracorpórea (CEC) y de clampeo aórtico más prolongados.
De igual manera, la mayor incidencia de reoperaciones en el posquirúrgico inmediato evidencia resultados hemodinámicos subóptimos vinculados a un procedimiento quirúrgico técnicamente más demandante.
La mayor incidencia de CIV residual está vinculada a la complejidad de la tunelización de la aorta hacia el ventrículo izquierdo, que requiere la utilización de parches de mayor longitud y con peculiar disposición espacial intraventricular para poder acceder a la aorta que se encuentra visiblemente alejada del defecto interventricular. Por otro lado, muchos de estos pacientes tienen una CIV muscular del inlet con la cual el cirujano es muy cauteloso para preservar el haz de conducción, lo que a veces contribuye también a una incidencia mayor de CIV residuales.
En coincidencia con lo descripto en otras series, (4, 20) la tendencia a mayor frecuencia de arritmias y/o BAV en el posquirúrgico inmediato no estuvo relacionada con la ampliación de la CIV como procedimiento quirúrgico adicional y consideramos que estuvo vinculada al mayor trauma e inflamación de la zona perinodal, como consecuencia de una cirugía más laboriosa, así como a la localización anterosuperior del haz de conducción en los pacientes con CIV muscular del inlet. De hecho, los dos pacientes que requirieron marcapasos definitivo tenían una CIV muscular ubicada en el tracto de entrada ventricular.
Contrariamente a lo referido en otras series, (4, 21) en el presente estudio las arritmias alejadas no constituyeron una complicación significativa, ya que fueron documentadas en apenas el 4,2% a 5 años de seguimiento.
El desarrollo de estenosis subaórtica es una complicación descripta en la cirugía de Rastelli que en nuestra población mostró una incidencia del 12,7% en un tiempo medio de 5 años, similar a la hallada en la bibliografía. Si bien en los casos con CIV remota la incidencia fue mayor, como consecuencia de la persistencia de una CIV restrictiva no suficientemente ampliada o de un tracto de salida del ventrículo izquierdo elongado y angulado en forma anterior, esta diferencia no fue significativa. Probablemente esto se deba a que se trata de un evento adverso multifactorial cuya presentación también puede resultar de hipertrofia muscular del septum conal o de la formación de un diafragma fibroso generado a partir de la discontinuidad mitroaórtica preexistente, como aconteció en dos de nuestros pacientes que tenían CIV relacionada con la aorta.
La necesidad de recambio del conducto VD-AP por estenosis o insuficiencia es un evento prácticamente inevitable en la evolución de la cirugía de Rastelli, puesto que responde a la historia natural de los homoinjertos y esto es independiente de la posición anatómica de la CIV. En nuestra serie, esta complicación afectó al 25% de los pacientes en un tiempo medio de 5 años, frecuencia semejante a la descripta en algunos trabajos (20, 22) y menor que la mencionada en otros y sin diferencias entre los dos grupos comparados. Cabe señalar, sin embargo, que los conductos de pericardio fueron los que tuvieron una incidencia menor de reoperación.
En nuestro Hospital se está desarrollando desde junio de 2005 una experiencia inicial de la cirugía descripta por Nikaidoh, que consiste en la traslocación de los grandes vasos evitando de esta manera la compleja tunelización de una CIV remota hacia la aorta.
Se operaron 7 pacientes con esta técnica. En todos los casos, la traslocación aórtica se realizó con reimplante coronario y conexión ventrículo derecho-arteria pulmonar con homoinjerto aórtico (3 pacientes) y pulmonar (4 pacientes).
Con este procedimiento quirúrgico no tuvimos mortalidad. Ningún paciente presentó CIV residual y todos evolucionaron con ambos tractos de salida ventricular sin obstrucción significativa. Dados los resultados subóptimos obtenidos con la técnica de Rastelli en los pacientes con CIV remota y los alentadores resultados preliminares con la técnica descripta por Nikaidoh, nos parece que esta última sería el procedimiento quirúrgico de elección para los pacientes con CIV alejada de los grandes vasos.
CONCLUSIONES
La presencia de CIV remota, no relacionada con la aorta, en pacientes con cirugía de Rastelli se asocia con: 1) mayor mortalidad, 2) mayor frecuencia de reoperaciones en el posquirúrgico inmediato, 3) tendencia a mayor frecuencia de arritmias en el posquirúrgico inmediato.
En este subgrupo de pacientes, con CIV no relacionada con los grandes vasos, la cirugía de Nikaidoh surge como una mejor opción en términos hemodinámicos inmediatos y potenciales complicaciones a mediano y a largo plazos. Cuando esta alternativa no es posible, debe considerarse la corrección univentricular.
1. Backer CL, Mavroudis C. The Rastelli Operation. Operative Techniques. J Thorac Cardiovasc Surg 2003;8:121-30. [ Links ]
2. Rastelli GC. A new approach to anatomic repair of transposition of the great arteries. Mayo Clin Proc 1969;44:1-12. [ Links ]
3. Morel VO, Jacobs J P, Quintessenza JA. Surgical management of the transposition with ventricular septal defect and obstruction to the left ventricular outflow tract. Cardiol Young 2005;15:102-5. [ Links ]
4. Kreutzer C, De Vive J, Oppido G, Kreutzer J, Gauvreau K, Freed M, et al. Twenty-five year experience with Rastelli repair for transposition of the great arteries. J Thoracic Cardiovasc Surg 2000;120: 211-23. [ Links ]
5. Sato Y, Ayusawa M, Komatsu S, Matsumoto N, Ichikawa M, Yoda S, et al. MCDT evaluation of a double oulet right ventricle after the Rastelli procedure. Int J Cardiol 2007;117:430-2. [ Links ]
6. Hu S, Liu Z, Li S, Shen X, Wang X, Liu J, et al. Strategy for biventricular outflow tract reconstruction: Rastelli, REV or Nikaidoh procedure?. J Thorac Cardiovasc Surg 2008;135:331-8. [ Links ]
7. Yeh TJ, Ramaciotti C, Leonard S, Roy L, Nikaidoh H. The aortic translocation (Nikaidoh) procedure: Midterm results superior to the Rastelli procedure. J Thorac Cardiovasc Surg 2007;133:461-9. [ Links ]
8. Giardini A, Donti A, Gargiulo G, Formigari R, Bonvicini M, Picchio F. Trascatheter residual ventricular septal defect closure after Rastelli operation. Cathet Cardiovasc Interv 2005;64:209-12. [ Links ]
9. Vouhé PR, Tamisier D, Leca F, Ouaknine R, Vernant F, Neveux JY. Transposition of the great arteries, ventricular septal defect, and pulmonary outflow tract. J Thorac Cardiovasc Surg 1992;103:428-36. [ Links ]
10. Capelli H, Faella H. Cardiopatías congénitas. En: Bertolasi CA, Barrero C, Gimeno G, Liniado G, Mauro V, editores. Transposición completa de los grandes vasos. Buenos Aires: Editorial Médica Panamericana; 2000. p. 2507-14. [ Links ]
11. Morell VO, Jacobs J P, Quintessenza JA. Aortic translocation in the management of the transposition of the great arteries with ventricular septal defect and pulmonary stenosis: results and follow-up. Ann Thorac Surg 2005;79:2089-92. [ Links ]
12. Hu SS, Li SJ, Wang L, Wang LQ, Xiong H, Li LH, et al. Pulmonary and aortic translocation in the management of transposition of the great arteries with ventricular septal defect and left ventricular outflow tract obstruction. J Thorac Cardiovasc Surg 2007;133:1090-2. [ Links ]
13. Imamura ES, Morikawa T, Tatsuno K, Konno S, Arai T, Sakakibara S. Surgical consideration of ventricular septal defect associated with complete transposition of the great arteries and pulmonary stenosis: with special reference to the Rastelli operation. Circulation 1971;44:914-23. [ Links ]
14. Huhta JC, Edwards WD, Danielson GK, Feldt RH. Abnormalities of the tricuspid valve in complete transposition of the great arteries with ventricular septal defect. J Thorac Cardiovasc Surg 1982;83: 569-76. [ Links ]
15. Villagra F, Quero-Jimenez M, Maitre-Azcarate MJ, Gutierrez J, Brito JM. Transposition of the great arteries with ventricular septal defect: Surgical considerations concerning the Rastelli operation. J Thorac Cardiovasc Surg 1984;88:1004-11. [ Links ]
16. Kurosawa H, Van Mierop LH. Surgical anatomy of the infundibular septum in transposition of the great arteries with ventricular septal defect. J Thorac Cardiovasc Surg 1986;91:123-32. [ Links ]
17. Niinami H, Imai Y, Swatari K, Hoshino S, Ishihara K, Aoki M. Surgical management of tricuspid malinsertion in the Rastelli operation: Conal Flap Method. Ann Thorac Surg 1995;59:1476-80. [ Links ]
18. Rastelli GC, McGoon DC, Wallace RB. Anatomic correction of transposition of the great arteries with ventricular septal defect and subpulmonary stenosis. J Thorac Cardiovasc Surg 1969;58:545-52. [ Links ]
19. Brown JK, Ruzmetov M, Okada Y, Vijay P, Turrentine M W. Surgical results in patients with double oulet right ventricle: a 20-year experience. Ann Thorac Surg 2001;72:1630-5. [ Links ]
20. Hörer J, Schreiber C, Dworak E, Cleuziou J, Prodan Z, Vogt M, et al. Long-term results after the Rastelli repar for transposition of the great arteries. Ann Thorac Surg 2007;83:2169-75. [ Links ]
21. Dearani JA, Danielson GK, Puga FJ, Mair DD, Schleck CD. Late results of the Rastelli operation for transposition of the great arteries. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu 2001;4:3-15. [ Links ]
22. Takeuchi K, Murakami A, Sekiguchi A, Hirata Y, Maeda K, Kitahori K, et al. Fate of equine pericardial roll conduit for Rastelli operation during long-term follow-up. Congenit Heart Dis 2007;2:121-4. [ Links ]














