Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. vol.80 no.3 Ciudad Autónoma de Buenos Aires jun. 2012
EPIDEMIOLOGÍA
Grasa epicárdica y su asociación con el HOMA-IR y el grosor íntima-media carotídeo
Association Between Epicardial Fat, HOMA-IR and Carotid Intima-media Thickness
Julio O. Cabrera-Rego1, Julio C. Gandarilla-Sarmientos1, Abel del Busto-Mesa2, Juan Valiente-Mustelier1
1 Departamento de Ecocardiografía - Instituto Nacional de Cardiología y Cirugía Cardiovascular. La Habana, Cuba
2 Instituto Nacional de Endocrinología. La Habana, Cuba
Recibido: 02/06/2011
Aceptado: 21/09/2011
Dirección para separatas:
Dr. Julio O. Cabrera Rego
Avenida 17 esquina Paseo, Nº 702 Vedado, Plaza de La Revolución Ciudad La Habana, Cuba (CP 10400) Tel. 537-8382661 - Fax: 537-8344435
e-mail: jocabrera@infomed.sld.cu
RESUMEN
Introducción
La grasa epicárdica se considera actualmente como un verdadero órgano endocrino y su determinación ecocardiográfica ha surgido como un nuevo parámetro de fácil adquisición en la evaluación del riesgo cardiometabólico.
Objetivo
Determinar la asociación entre la grasa epicárdica, la presencia de insulinorresistencia y el grosor íntima-media carotídeo.
Material y métodos
Se realizó un estudio transversal en 239 pacientes con sospecha de trastornos en el metabolismo de los carbohidratos en colaboración entre el Instituto Nacional de Endocrinología y el Instituto Nacional de Cardiología y Cirugía Cardiovascular. Se incluyeron variables clínicas (edad, sexo, antecedentes de tabaquismo, presión arterial sistólica y diastólica), antropométricas (circunferencia de la cintura e índice de masa corporal), bioquímicas (glucemia, colesterol total, C-HDL, C-LDL, triglicéridos, insulina en ayunas y HOMA-IR) y ultrasonográficas (grosor íntima-media carotídeo).
Resultados
La glucemia, la grasa epicárdica y la circunferencia de la cintura fueron las variables que mostraron, en ese orden, una asociación significativa e independiente con la presencia de un HOMA-IR > 2,6. La grasa epicárdica mostró también una correlación positiva y significativa con los niveles de insulinemia en ayunas (r = 0,536; p = 0,0001) y con el HOMA-IR (r = 0,512; p = 0,001). La correlación entre la grasa epicárdica y el grosor íntima-media carotídeo fue superior en los pacientes insulinorresistentes (r = 0,523; p = 0,0001), en comparación con los pacientes con valores de HOMA-IR < 2,6 (r = 0,173; p = 0,029). La grasa epicárdica ≥ 4,9 mm tuvo una sensibilidad del 85% y una especificidad del 75% en la predicción de insulinorresistencia, con un área bajo la curva ROC de 0,815 [IC 95% (0,759-0,871)].
Conclusiones
La grasa epicárdica mostró una asociación significativa e independiente con la presencia de insulinorresistencia y una correlación significativa con el grosor íntima-media carotídeo en el grupo de pacientes con HOMA-IR > 2,6.
Palabras clave: Grasa epicárdica; Resistencia a la insulina; Aterosclerosis
Abreviaturas
CCin Circunferencia de la cintura
HTA Hipertensión arterial
C-HDL Colesterol unido a lipoproteínas de alta densidad
IMC Índice de masa corporal
C-LDL Colesterol unido a lipoproteínas de baja densidad
PAD Presión arterial diastólica
GIM Grosor íntima-media
PAS Presión arterial sistólica
HOMA-IR Homeostatic model assessment-insulin resistance (modelo homeostático de evaluación de la resistencia a la insulina)
Abstract
Association Between Epicardial Fat, HOMA-IR and Carotid Intima-media Thickness
Background
Epicardial fat is currently considered a real endocrine organ that can be easily determined by echocardiography, emerging as a novel parameter for the estimation of cardiometabolic risk.
Objective
To determine the association between epicardial fat, insulin resistance and carotid intima-media thickness.
Methods
The Instituto Nacional de Endocrinología and the Instituto Nacional de Cardiología y Cirugía Cardiovascular conducted a cross-sectional study on 239 patients with suspected disorders of carbohydrate metabolism. Clinical variables (age, gender, smoking habits, systolic and diastolic blood pressure), anthropometric measurements (waist circumference and body mass index), biochemical determinations (blood glucose, total cholesterol, HDL-C, LDL-C, triglycerides, fasting insulin levels and HOMA-IR) and echocardiographic variables (carotid intima-media thickness) were included.
Results
A significant and independent association was found between blood glucose, epicardial fat and waist circumference, in that order, and HOMA-IR >2.6. Epicardial fat also showed a positive and significant correlation with fasting insulin levels (r=0.536; p=0.0001) and HOMA-IR (r=0.512; p=0.001).
The correlation between epicardial fat and carotid intimamedia thickness was greater in insulin resistant patients (r=0,523; p=0.0001), compared to patients with HOMA-IR <2.6 (r=0.173; p=0.029). Epicardial fat thickness ≥4.9 mm had a sensitivity of 85% and a specificity of 75% to predict insulin resistance, with an area under the ROC curve of 0.815 (95% CI 0.759-0.871).
Conclusions
Epicardial fat had a significant an independent association with insulin resistance and a significant correlation with carotid intima-media thickness in the group of patients with HOMA-IR >2.6.
Key words: Epicardial Fat; Insulin Resistance; Atherosclerosis
INTRODUCCIÓN
La determinación ecocardiográfica de la grasa epicárdica ha surgido como un nuevo parámetro de fácil adquisición en la evaluación del riesgo cardiometabólico. (1) Este depósito graso visceral es considerado actualmente como un verdadero órgano endocrino, responsable de la producción de citocinas proinflamatorias y proaterogénicas como el factor de necrosis tumoral a, la interleucina 6, la visfatina, la leptina, la omentina, el inhibidor-1 del activador tisular del plasminógeno, las angiotensinas y las adipocinas (adiponectina) con propiedades antiinflamatorias y antiaterogénicas. (2)
La relación entre la grasa epicárdica y los niveles de insulina y adiponectina plasmáticas han sugerido que debe considerarse como un tejido adiposo altamente insulinorresistente, (3) el cual se ha asociado inversamente con la sensibilidad a la insulina (4) y con marcadores subrogados de insulinorresistencia como el HOMA-IR [del inglés, homeostatic model assessment-insulin resistance (modelo homeostático de evaluación de la resistencia a la insulina)]. (5) A ello se añaden las ventajas de la grasa epicárdica en relación con medidas antropométricas relacionadas con la insulinorresistencia como la circunferencia de la cintura (CCin) en la estimación del tejido adiposo visceral. (3)
Algunas investigaciones han postulado algunas diferencias étnicas en relación con el grosor de la grasa epicárdica y su actividad metabólica. (6-8) En pacientes hispanos se ha demostrado previamente su asociación con la presencia de enfermedad arterial coronaria significativa (9) y diversos marcadores de aterosclerosis subclínica en pacientes asintomáticos. (10) No obstante, la asociación entre la grasa epicárdica y los niveles de HOMA-IR, indicativos de insulinorresistencia, así como el grosor íntima-media (GIM) carotídeo en este grupo de pacientes, no se ha establecido bien en nuestra región.
MATERIAL Y MÉTODOS
Población en estudio
Se incluyeron 239 pacientes con sospecha de trastornos en el metabolismo de los carbohidratos por presencia de uno o más de los siguientes factores de riesgo: 1) índice de masa corporal (IMC) > 27 (kg m2), 2) familiares diabéticos de primer grado, 3) antecedentes obstétricos de diabetes gestacional y/o macrosomía, 4) antecedentes de alteraciones previas a la glucosa y 5) hipertensos con niveles de triglicéridos> 150 mg/dl y C-HDL (colesterol unido a lipoproteínas de alta densidad) > 35 mg/dl, estudiados en el Instituto Nacional de Endocrinología, en el período de enero de 2009 a junio de 2010. El estudio se condujo de acuerdo con las guías propuestas en la Declaración de Helsinki y fue aprobado por el Comité de Ética de nuestra institución. Todos los pacientes brindaron su consentimiento informado antes del inicio de la investigación.
Diseño del estudio
Las variables clínicas, antropométricas y hemoquímicas de interés fueron adquiridas por un especialista en endocrinología en el Centro de Atención al Diabético perteneciente al Instituto Nacional de Endocrinología. Posteriormente, los pacientes fueron citados al Laboratorio de Ecocardiografía del Instituto Nacional de Cardiología y Cirugía Cardiovascular para la realización de un examen ecocardiográfico transtorácico y carotídeo, ambos en un período no mayor de dos semanas posteriores al diagnóstico. Aquellos con antecedentes de enfermedad cardiovascular conocida, insuficiencia renal crónica y bajo tratamiento con estatinas fueron excluidos del estudio.
Protocolo de las variables incluidas en el estudio
Variables clínicas y antropométricas: se incluyeron edad, sexo, antecedentes de tabaquismo, presión arterial sistólica (PAS) y diastólica (PAD), peso, talla e IMC y CCin. La presión arterial se determinó con un esfigmomanómetro aneroide con columna de mercurio, con el brazalete colocado en el brazo izquierdo, después de 5 minutos de descanso con el sujeto sentado. A cada paciente se le realizaron dos tomas de presión arterial, mediando aproximadamente 10 minutos entre la primera y la segunda toma, promediándose ambos valores.
Variables hemoquímicas: en todos los participantes, la extracción (10 ml) se realizó por punción en la vena cubital y la sangre se colocó en un tubo con EDTA, un tubo con heparina y un tubo con gel seco para suero. Se incluyeron glucemia en ayunas, colesterol total, C-HDL, C-LDL (colesterol unido a lipoproteínas de baja densidad) y triglicéridos. Para la determinación de la glucemia, el colesterol total y los triglicéridos se emplearon los reactivos RapiGluco-Test, Colestest y Monotriglitest, respectivamente, producidos en el EPB"Carlos J. Finlay", La Habana, Cuba. La glucemia fue procesada en un equipo Eppendorf mediante método enzimático colorimétrico y el colesterol y los triglicéridos en un equipo Hitachi 7170 A, Tokio, Japón. Para las variables C-HDL y C-LDL, se emplearon los reactivos C-HDL Inmuno FS y LDL-C Select FS, respectivamente, mediante determinación cuantitativa in vitro en suero o plasma en equipos fotométricos (prueba inmunoturbidimétrica), fabricados por DiaSys Diagnostic Systems GmbH, Holzheim, Alemania.
Las determinaciones hormonales de insulinemia se realizaron utilizando kits diagnósticos proporcionados por el CENTIS. La insulina se determinó por método de radioinmunoensayo [insulina por radioinmunoanálisis (Coat- A-CountInsulin -DPC-) en fase sólida por competencia] con una sensibilidad de 5 mUI/ml y un rango de normalidad de 5-35 mUI/ml con un coeficiente de variación interensayo e intraensayo del 6,2% y 7,1%, respectivamente. En el caso del radioinmunoanálisis, el coeficiente de variación del control de calidad oscila habitualmente en nuestro laboratorio entre el 6% y el 9%, rango característico de este tipo de método inmunorradiológico.
El índice de resistencia a la insulina empleado fue el HOMA-IR (homeostatic model assessment-insulin resistance), calculado a partir de los valores iniciales de glucosa e insulina siguiendo el modelo homeostático (HOMA), de acuerdo con la fórmula: RI = [insulinemia ayunas (mUI/ml) × glucemia ayunas (mmol/L)] / 22,5. El valor de referencia estandarizado en el laboratorio del Instituto Nacional de Endocrinología es 2,6, validado por Arranz y colaboradores, (11, 12) por lo que cifras superiores son indicadoras de insulinorresistencia.
Protocolo de las variables ecocardiográficas
Grasa epicárdica: los exámenes ecocardiográficos se realizaron en un equipo Philips iE33 2006, versión 2.0.1.420 con transductor S5-1 con arreglo de fase de 1,3-3,6 MHz provisto de imagen armónica. El estudio fue realizado por dos observadores con nivel III de experiencia de la Sociedad Americana de Ecocardiografía, quienes en ningún momento conocieron los datos del paciente.
La grasa epicárdica se determinó mediante medición en modo bidimensional en las vistas eje largo paraesternal tomando como referencia de corte el plano valvular aórtico (Figura 1 A) y el eje corto paraesternal a nivel de los músculos papilares (Figura 1 B). Para la determinación de la grasa epicárdica anterior al ventrículo derecho se promediaron los valores obtenidos de las vistas eje largo y corto paraesternal. La grasa epicárdica se midió en el período telesistólico del ciclo cardíaco. La grasa epicárdica se definió como el espacio ecolúcido (con elementos ecorrefringentes en su interior indicativos de grasa) entre la línea ecodensa del pericardio visceral y el epicardio de la pared ventricular derecha. Los coeficientes de correlación y la variabilidad intraobservador e interobservador de nuestro Laboratorio de Ecocardiografía muestran una buena reproducibilidad, según comunicaciones previas. (9)

Fig. 1. Evaluación ecocardiográfica de la grasa epicárdica. A. Eje largo paraesternal. Medición a nivel del anillo valvular aórtico. B. Eje corto paraesternal a nivel de los músculos papilares. Grasa epicárdica (flechas). AO: Aorta. VI: Ventrículo izquierdo. VD: Ventrículo derecho. AI: Aurícula izquierda.
Grosor íntima-media carotídeo: se colocó al paciente en decúbito supino con ligera lateralización del cuello, ubicándose un transductor lineal con frecuencia de 7,5 MHz en posición longitudinal con respecto a la arteria carótida común en la posición laterosuperior del cuello por dentro del músculo esternocleidomastoideo, con la señal del electrocardiograma activada para obtener imágenes vasculares al final de la diástole, visualizándose con una profundidad de 4 cm.
Para la determinación del GIM se examinó la arteria carótida común en un segmento de 10 mm distal a la emergencia del bulbo carotídeo. Las mediciones se realizaron mediante el software QLAB, que emplea un programa semiautomático de detección de bordes (Figura 2). La medición del GIM se adquiría si el éxito en la detección era mayor del 95%. Los percentiles carotídeos de la arteria carótida común derecha e izquierda se determinaron de acuerdo con la edad, el sexo y la raza del paciente según los datos brindados por el Bogalusa Heart Study (13) y el estudio MESA (Multi-Ethnic Study of Atherosclerosis). (14) En presencia de discrepancia entre los percentiles encontrados para ambas arterias carótidas, se adjudicó al paciente el percentil de mayor valor.

Fig 2. Medición del grosor íntima-media carotídeo. Las líneas son trazadas usando el software Q-Lab para la detección semiautomática de bordes.
Análisis estadístico
Para el procesamiento estadístico se utilizó el programa SPSS versión 13.0 (SPSS Inc., Chicago, Ill, USA). Se determinaron la distribución y la asociación de las características generales de los pacientes en estudio de acuerdo con el sexo, expresando las variables categóricas en números absolutos y porcentaje y las continuas en valores medios y desviación estándar. En el análisis univariado se aplicaron la prueba de chi cuadrado para las variables categóricas y la prueba de la t de Student para las continuas. Se estableció asociación significativa si p < 0,05.
Se realizó un análisis multivariado entre las variables clínicas, antropométricas, hemoquímicas y ultrasonográficas y la presencia de HOMA-IR > 2,6, mediante regresión logística binaria para cada una de las variables con p < 0,20 en relación con este marcador subrogado de insulinorresistencia en el análisis univariado, con el objetivo de establecer su independencia del resto de los factores de riesgo cardiometabólico incluidos en el estudio. Incluimos además el cálculo del odds ratio con un intervalo de confianza del 95%. Se determinó el valor de corte de grasa epicárdica con mejor sensibilidad y especificidad en la predicción de insulinorresistencia, mediante el cálculo del área bajo la curva ROC. Para comparar las curvas ROC se aplicó la prueba de homogeneidad de áreas por el método de chi cuadrado mediante el programa EPIDAT versión 3.1.
Se determinó además la correlación de la grasa epicárdica con la insulinemia en ayunas, el HOMA-IR y el GIM carotídeo de acuerdo con la presencia o no de insulinorresistencia, utilizando el coeficiente de correlación de Pearson. Se consideró asociación significativa entre las variables si p < 0,05.
RESULTADOS
Características generales de la población en estudio
En la Tabla 1 se exponen las características generales de la muestra estudiada.
Tabla 1. Características generales de la población en estudio

Se incluyeron un total de 239 pacientes con sospecha de trastornos en el metabolismo de los carbohidratos: 143 (59,8%) mujeres, edad media 54,7 ± 8,9 vs. 55,5 ± 9,4 para mujeres y hombres, respectivamente, 79 (33,1%) con presencia de insulinorresistencia y 84 (35,7%) con GIM ≥ 75 percentil.
El rango de grasa epicárdica fue de 1,0 mm hasta un máximo de 12,5 mm, con un grosor medio general en el grupo de estudio de 4,7 ± 2,1 mm.
Resulta de interés señalar que los valores medios de C-LDL y triglicéridos de la población en estudio se encontraban por encima de los valores normales de referencia.
Variables clínicas, antropométricas, hemoquímicas y ecocardiográficas de acuerdo con la presencia de insulinorresistencia (Tabla 2)
Tabla 2. Asociación de variables clínicas, antropométricas, hemoquímicas y ecocardiográficas de acuerdo con la presencia de insulinorresistencia según HOMA-IR
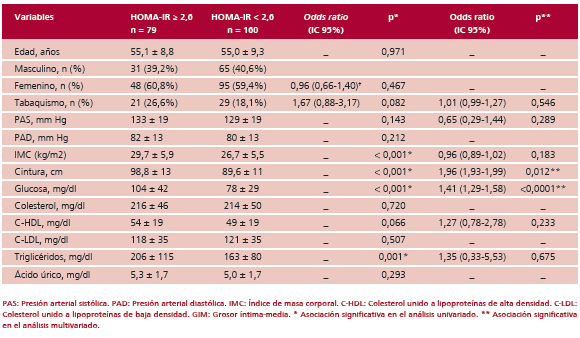
El IMC, la CCin, la glucemia, los triglicéridos, la grasa epicárdica y el GIM carotídeo mostraron, en ese orden, una asociación significativa con la presencia de insulinorresistencia en el análisis univariado. Finalmente, la glucemia, la grasa epicárdica y la CCin fueron las variables que mostraron una asociación significativa e independiente con la presencia de un HOMA-IR > 2,6. La grasa epicárdica ≥ 4,9 mm mostró una sensibilidad del 85% y una especificidad del 75% en la detección de insulinorresistencia, con un área bajo la curva de 0,840 (IC 95% 0,785-0,896), significativamente superior a la mostrada por la CCin [0,776, IC 95% (0,710-0,841); p = 0,039] (Figura 3).
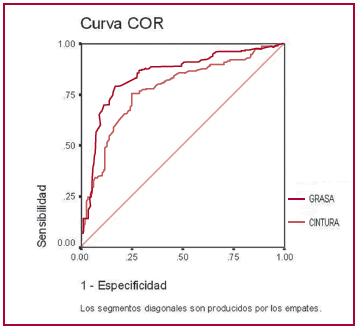
Fig 3. Área bajo la curva para la grasa epicárdica y la circunferencia de la cintura en la predicción de insulinorresistencia.
Correlación de la grasa epicárdica con la insulinorresistencia y el GIM carotídeo La grasa epicárdica mostró una correlación positiva y significativa con los niveles de insulinemia en ayunas (r = 0,536; p < 0,0001) (Figura 4) y con el HOMA-IR (r = 0,512; p = 0,001). Se demostró además una correlación significativa entre la grasa epicárdica y el GIM carotídeo en los pacientes insulinorresistentes (r = 0,523; p < 0,0001) (Figura 5 A), la cual fue superior en comparación con los pacientes con valores de HOMA-IR < 2,6 (r = 0,173; p = 0,029) (Figura 5 B).
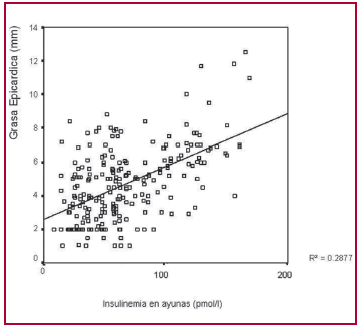
Fig 4. Correlación entre la grasa epicárdica y los valores de insulinemia en ayunas.

Fig 5. Correlación entre la grasa epicárdica y el grosor íntima-media carotídeo según presencia o no de insulinorresistencia.
DISCUSIÓN
Los hallazgos más importantes de nuestro estudio fueron: 1) la grasa epicárdica mostró una correlación positiva y significativa con los niveles de insulinemia en ayunas y el HOMA-IR y 2) una correlación significativa más fuerte con el GIM carotídeo en el grupo de pacientes insulinorresistentes.
Grasa epicárdica y su asociación con la presencia de insulinorresistencia
La grasa epicárdica está compuesta principalmente por adipocitos y macrófagos, ambos con propiedades secretoras e importantes acciones autocrinas, paracrinas y endocrinas. (15) Recientemente se ha demostrado el papel de las adipocinas como reguladores de la sensibilidad a la insulina. De ellos, el factor de necrosis tumoral alfa, la interleucina 6 y la leptina se han señalado como los miembros más prominentes de esta familia de citocinas proinflamatorias producidos por la grasa epicárdica en su contribución con la presencia de insulinorresistencia. (16) Igualmente, se ha descripto que los niveles de adiponectinas se encuentran típicamente reducidos en los pacientes con insulinorresistencia (17) y que esta disminución se comporta como un predictor de diabetes y esteatosis hepática. (18)
Iacobellis y colaboradores fueron los primeros en demostrar, en un estudio que incluyó un total de 30 pacientes obesos, una correlación significativa entre el grosor de la grasa epicárdica y los niveles de insulina en ayunas (r = 0,59; p = 0,01) y a los 120 minutos (r = 0,45; p = 0,03). (5) En otro estudio posterior, este autor comunicó un incremento proporcional y significativo del grosor de la grasa epicárdica en pacientes sensibles, resistentes y altamente resistentes a la insulina (5,4 mm vs. 9,5 mm vs. 11,0 mm; p < 0,001). (4)
Aydin y colaboradores estudiaron 50 pacientes con síndrome metabólico con el objetivo de demostrar la asociación entre la función endotelial y la grasa epicárdica. Demostraron una correlación significativa de la grasa epicárdica con la glucemia en ayunas (r = 0,307; p = 0,020), la insulina en ayunas (r = 0,376; p = 0,002), el HOMA-IR (r = 0,370; p = 0,002) y la dilatación mediada por flujo (R2 = 0,247; p = 0,001), un marcador ultrasonográfico de estadios tempranos de aterosclerosis. (19)
La grasa epicárdica también ha mostrado una asociación significativa con la presencia de síndrome metabólico. Ahn y colaboradores demostraron no sólo una correlación significativa de la grasa epicárdica con los niveles de glucosa e insulina en ayunas y el HOMAIR, sino también un grosor significativamente mayor en el grupo de pacientes no diabéticos con síndrome metabólico (3,5 vs. 1,6 mm; p < 0,001). (20) Recientemente se conoció un resultado similar en cuanto a la presencia de valores significativamente mayores de grasa epicárdica en pacientes diabéticos tipo 1 con criterios de síndrome metabólico (6,15 ± 0,34 mm vs. 4,96 ± 0,25 mm; p = 0,006). (21)
La sensibilidad y la especificidad de la grasa epicárdica en la predicción de insulinorresistencia referidas por algunos autores son similares a las encontradas en nuestra investigación; sin embargo, los valores de corte para nuestro grupo de estudio son menores que los utilizados por otros. (4, 22) Iacobellis y colaboradores demostraron que la grasa epicárdica mayor de 9,5 mm en hombres y de 7,5 mm en mujeres tenía una sensibilidad del 85,0% y 82,0% y una especificidad del 63,0% y 62,0%, respectivamente, en la predicción de resistencia a la insulina [área bajo la curva de 0,792 (IC 95 % 0,725-0,848)]. En ese estudio, el rango de grasa epicárdica fue desde 1,1 mm hasta 22,6 mm. (4) Por otro lado, en un estudio realizado en niños obesos (edad media 10,2 ± 2,5 años), la grasa epicárdica mayor de 4,1 mm mostró un área bajo la curva de 0,750 ± 0,06 (p = 0,001) con una sensibilidad del 90% y una especificidad del 61% en la predicción de insulinorresistencia. (22)
En otros estudios, los valores medios de grasa epicárdica en pacientes con insulinorresistencia o síndrome metabólico han sido mayores [(9,87 mm, (3) 8,0 mm, (23) 6,16 mm (19) y 6,15 mm (21)] en comparación con el nuestro (5,3 mm). Al respecto, resulta interesante mencionar que se han señalado algunas diferencias étnicas en relación con la cantidad de grasa epicárdica, la cual parece que es menor en pacientes hispanos. Alexopoulos y colaboradores encontraron diferencias importantes en el volumen de la grasa epicárdica cuantificada mediante tomografía computarizada, que resultó menor en los hispanos, incluso en comparación con los pacientes de raza negra (caucásicos 96 ± 44 ml vs. asiáticos 71 ± 32 ml vs. negros 56 ± 28 ml vs. hispanos 54 ± 17 ml; p < 0,001). (24)
En el primer estudio que demostró una asociación significativa entre la grasa epicárdica y la presencia de enfermedad coronaria significativa en pacientes hispanos, los valores medios de grasa epicárdica encontrados también fueron menores que los hallados en la bibliografía para este grupo de pacientes. (9)
Grasa epicárdica y su correlación con el GIM carotídeo
Iacobellis y colaboradores fueron también los primeros autores que demostraron una correlación significativa entre la grasa epicárdica y el GIM carotídeo. En un estudio que incluyó un total de 60 pacientes portadores del virus de la inmunodeficiencia humana y lipodistrofia secundaria a antirretrovirales, el grupo de pacientes con síndrome metabólico y lipodistrofia mostró valores significativamente mayores de grasa epicárdica y GIM carotídeo en comparación con aquellos sin lipodistrofia (8,0 vs. 6,5 mm, p < 0,01 y 0,71 vs. 0,66 mm, p < 0,01, respectivamente). En este estudio, la grasa epicárdica mostró además una correlación significativa con los niveles de insulina en ayunas (r = 0,65; p < 0,01). (23)
Abaci y colaboradores demostraron en niños obesos una correlación significativa entre la grasa epicárdica y el GIM carotídeo (r = 0,343; p = 0,02). (22) En un estudio que incluyó un total de 459 pacientes hipertensos, la grasa epicárdica > 7 mm se asoció significativamente con un GIM carotdeo mayor y con parámetros de rigidez arterial en comparación con aquellos con grosor ≤ 7 mm. (25) Por último, Rego y colaboradores encontraron en 300 pacientes asintomáticos que la grasa epicárdica mostró una asociación significativa con el GIM carotídeo, la calcificación arterial coronaria, el radio ApoB/ApoA1 elevado y la estratificación de riesgo cardiovascular según puntaje de Framingham. (10)
Diversos estudios han mostrado que el radio leptina/ adiponectina (ambas adipocinas relacionadas con la insulinorresistencia) se asocia significativamente con el GIM carotídeo (26-28) y otros marcadores ultrasonográficos de aterosclerosis, como la dilatación mediada por flujo y la distensibilidad carotídea. (27) Igualmente, en algunas investigaciones se ha referido que los niveles incrementados de insulina son predictores de cambios aterogénicos en estadios más tempranos que la propia hiperglucemia. (29) Basados en estas evidencias, podríamos deducir que el incremento significativo de la grasa epicárdica en los pacientes con insulinorresistencia y su correlación con la insulina en ayunas y el HOMA-IR podrían explicar la correlación superior encontrada entre la grasa epicárdica y el GIM carotídeo en el grupo de pacientes con resistencia a la insulina.
Se pueden señalar como limitaciones de nuestro estudio el diseño de corte transversal y el uso del HOMA-IR como parámetro subrogado de insulinorresistencia. La totalidad de los estudios precedentes presentan características similares. No obstante, se ha señalado la necesidad de conducir estudios prospectivos en relación con la grasa epicárdica, con la finalidad de demostrar su valor predictivo de eventos cardiovasculares o su variación en relación con modificaciones de parámetros cardiometabólicos durante el seguimiento. (2) La insulinorresistencia, según el Consenso de Síndrome Metabólico de 2005 de la Federación Internacional de Diabetes, se puede determinar con el clamp euglucémico hiperinsulinémico (patrón oro), pero es un método invasivo y complejo para la práctica clínica. En su reemplazo, empleamos el índice HOMA-IR, un modelo matemático simple, de bajo costo y apto para estudios poblacionales. (30)
CONCLUSIONES
La determinación ecocardiográfica de la grasa epicárdica puede ser una herramienta útil en la estratificación de riesgo cardiometabólico, al demostrar su asociación significativa e independiente con la presencia de insulinorresistencia y una correlación significativa con el GIM carotídeo superior en el grupo de pacientes con HOMA-IR > 2,6. Serán necesarios futuros estudios prospectivos, multiétnicos y con muestras más amplias para generalizar estos resultados.
1. MacGavock J, Víctor RU, Roger H, Szczepaniak LS. Adiposity of the heart, Revisited. Ann Int Med 2006;114:517-24. [ Links ]
2. Iacobellis G, Willens HJ. Echocardiographic epicardial fat: a review of research and clinical applications. J Am Soc Echocardiogr 2009;22:1417-8. [ Links ]
3. Iacobellis G, Ribaudo MC, Assael F, Vecci E, Tiberti C, Zappaterreno A, et al. Echocardiographic epicardial adipose tissue is related to anthropometric and clinical parameters of metabolic syndrome: a new indicator of cardiovascular risk. J Clin Endocrinol Metab 2003;88:5163-8. [ Links ]
4. Iacobellis G, Willens HJ, Barbaro G, Sharman AM. Threshold values of high risk echocardiographic epicardial fat thickness. Obesity (Silver Spring) 2008;16:887-92. [ Links ]
5. Iacobellis G, Leonetti F. Epicardial adipose tissue and insulin resistance in obese subjects. J Clin Endocrinol Metab 2005;90:6300-2. [ Links ]
6. Howard JW, Gómez-Marín O, Chirinos JA, Goldberg R, Lowery MH, Iacobellis G. Comparison of epicardial and pericardial fat thickness assessed by echocardiography in African American and non-Hispanic white men: a pilot study. Ethn Dis 2008;18:311-6. [ Links ]
7. Alexopoulos N, McLean DS, Janik M, Arepalli ChD, Stillman AE, Raggi P. Epicardial adipose tissue and coronary artery plaque characteristics. Atherosclerosis 2010;210:150-4. [ Links ]
8. Divers J, Wagenknecht LE, Bowden DW, Carr J, Hightower RC, Register TC, et al. Ethnic differences in the relationship between pericardial adipose tissue and coronary artery calcified plaque: African-American-Diabetes Heart Study. J Clin Endocrinol Metab 2010;95:5382-9. [ Links ]
9. Mustelier JV, Rego JO, González GA, Sarmiento JC, Riverón BV. Echocardiographic parameters of epicardial fat deposition and its relation to coronary artery disease. Arq Bras Cardiol 2011;97:122-9. [ Links ]
10. Rego JO, Iacobellis G, Sarmientos JC, Mustelier JV, Aquiles EW, Rodríguez VM, et al. Epicardial fat thickness correlates with ApoB/ ApoA1 ratio, coronary calcium and carotid intima media thickness in asymptomatic subjects. Int J Cardiol 2011;151:234-36. [ Links ]
11. Arranz C, Álvarez A, Perich P, González R. Relación de la sensibilidad a la insulina determinada con diferentes índices con el síndrome metabólico en hombres con glicemia en ayunas normal. Rev Asociación Latinoam Diabetes 2007;15:120. [ Links ]
12. Arranz C, González R, Álvarez A, Rodríguez B, Reyes A. Criterios de referencia para los indicadores de secreción de insulina y de los parámetros lipídicos en una población mixta hospitalaria. Rev Cubana Endocrinol 2010;21:1-12. [ Links ]
13. Tzou WS, Douglas PS, Srinivasan SR, Bond MG, Tang R, Chen W, et al. Distribution and predictors of carotid artery intima-media thickness in young adults: the Bogalusa Heart Study. Prev Cardiol 2007;10:181-9. [ Links ]
14. O'Leary DH, Polak JF, Kronmal RA, Manolio TA, Burke GL, Wolfson SK. Carotid-artery intima and media thickness as a risk factor for myocardial infarction and stroke in older adults: Cardiovascular Health Study Collaborative Research Group. N Engl J Med 1999;340:14-22. [ Links ]
15. Matsuzawa Y. Therapy insight: adipocytokines in metabolic syndrome and related cardiovascular disease. Nat Clin Pract Cardiovasc Med 2006;3:35-42. [ Links ]
16. Mazurek T, Zhang L, Zalewski A, Mannion JD, Diehl JT, Arafat H, et al. Human epicardial adipose tissue is a source of inflammatory mediators. Circulation 2003;108:2460-6. [ Links ]
17. Abbasi F, Chu JW, Lamendola C, McLaughlin T, Hayden J, Reaven GM, et al. Discrimination between obesity and insulin resistance in the relationship with adiponectin. Diabetes 2004;53:585-90. [ Links ]
18. Bajaj M, Suraamornkul S, Piper P, Hardies LJ, Glass L, Cersosimo E, et al. Decreased plasma adiponectin concentrations are closely related to hepatic fat content and hepatic insulin resistance in pioglitazone-treated type 2 diabetic patients. J Clin Endocrinol Metab 2004;89:200-6. [ Links ]
19. Aydin H, Toprak A, Deyneli O, Yazici D, Tarçin Ö, Sancak S, et al. Epicardial fat tissue thickness correlates with endothelial dysfunction and other cardiovascular risk factors in patients with metabolic syndromes. Metabolic Syndrome and Related Disorders 2010;8:229-34. [ Links ]
20. Ahn GS, Lim HS, Joe DY, Kang SJ, Choi BJ, Choi SY, et al. Relationship of epicardial adipose tissue by echocardiography to coronary artery disease. Heart 2008;94:e7. [ Links ]
21. Momesso DP, Bussade I, Epifanio MA, Schettino CD, Russo LA, Kupfer R. Increased epicardial adipose tissue in type 1 diabetes is associated with central obesity and metabolic syndrome. Diabetes Res Clin Pract 2011;91:47-53. [ Links ]
22. Abaci A, Tascilar ME, Saritas T, Yozgat Y, Yesilkaya E, Kilic A, et al. Threshold value of subepicardial adipose tissue to detect insulin resistance in obese children. Int J Obes 2009;33:440-6. [ Links ]
23. Iacobellis G, Pellicelli AM, Sharma AM, Grisorio B, Barbarini G, Barbaro G. Relation of subepicardial adipose tissue to carotid intima-media thickness in patients with human immunodeficiency virus. Am J Cardiol 2007;99:1470-2. [ Links ]
24. Alexopoulos N, McLean DS, Janik M, Arepalli CD, Stillman AE, Raggi P. Epicardial adipose tissue and coronary artery plaque characteristics. Atherosclerosis 2010;210:150-4. [ Links ]
25. Natale F, Tedesco MA, Mocerino R, de Simone V, Di Marco GM, Aronne L, et al. Visceral adiposity and arterial stiffness: echocardiographic epicardial fat thickness reflects, better than waist circumference, carotid arterial stiffness in a large population of hypertensives. Eur J Echocardiogr 2009;10:549-55. [ Links ]
26. Norata GD, Raselli S, Grigore L, Garlaschelli K, Dozio E, Magni P, et al. Leptin:adiponectin ratio is an independent predictor of intima media thickness of the common carotid artery. Stroke 2007;38:2844-6. [ Links ]
27. Saarikoski LA, Huupponen RK, Viikari JS, Marniemi J, Juonala M, Kähönen M, et al. Adiponectin is related with carotid artery intima-media thickness and brachial flow-mediated dilatation in young adults- the Cardiovascular Risk in Young Finns Study. Ann Med 2010;42:603-11. [ Links ]
28. Takamura N, Hayashida N, Hagane K, Kadota K, Yamasaki H, Abiru N, et al. Leptin to high-molecular-weight adiponectin ratio is independently correlated with carotid intima-media thickness in men, but not in women. Biomarkers 2010;15:340-4. [ Links ]
29. Fang J, Zhang JP, Luo CX, Yu XM, Lu LQ. Carotid intimamedia thickness in childhood and adolescent obesity relations to abdominal obesity, high triglyceride level and insulin resistance. Int J Med Sci 2010;7:278-83. [ Links ]
30. Ascaso JF, González-Santos P, Mijares AH, Rojas AM, Marín LM, Núñez-Cortés JM, et al. Diagnóstico de síndrome metabólico. Adecuación de los criterios diagnósticos en nuestro medio. Recomendaciones del foro HDL. Resumen ejecutivo. Rev Clin Esp 2006;206:576-82. [ Links ]














