Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. vol.83 no.5 Ciudad Autónoma de Buenos Aires oct. 2015
ARTÍCULO ORIGINAL
Crioablación con balón en fibrilación auricular paroxística. Experiencia inicial
Balloon Cryoablation for Paroxysmal Atrial Fibrillation. Initial Experience
José L. GonzálezMTSAC, Néstor GalizioMTSAC, Alejandro A. Palazzo†, Federico Robles, Guillermo Carnero, Mauricio Mysuta
Hospital Universitario Fundación Favaloro. Buenos Aires, Argentina
MTSAC Miembro Titular de la Sociedad Argentina de Cardiología
† Para optar a Miembro Titular de la Sociedad Argentina de Cardiología
Dirección para separatas: Dr. Alejandro A. Palazzo - Hospital Universitario Fundación Favaloro - Av. Belgrano 1782 - (C1093AAS) Buenos Aires, Argentina - Tel. (54-11) 4378-1200/1300 int. 3660/3650 - e-mail: alejandropalazzo@hotmail.com
Recibido: 08/04/2015
Aceptado: 14/07/2015
RESUMEN
Introducción: El aislamiento eléctrico de las venas pulmonares constituye la piedra angular en el tratamiento curativo de pacientes con fibrilación auricular paroxística (FAP) recurrente y sintomática. La crioablación con balón (CAB) es una alternativa a la radiofrecuencia, con disminución de los tiempos del procedimiento y de radioscopia.
Objetivos: Describir los resultados inmediatos y la experiencia inicial en las primeras intervenciones de CAB de FAP en nuestro hospital.
Material y métodos: Entre noviembre de 2013 y febrero de 2015, 23 pacientes fueron intervenidos con una CAB de FAP. Previo al procedimiento se les realizó una angiotomografía con reconstrucción de la aurícula izquierda y las venas pulmonares.
Resultados: La edad promedio de los pacientes fue de 53 ± 11 años, 19 eran varones, el diámetro de la aurícula izquierda fue de 40 ± 7 mm, la FEVI fue de 58% ± 8%. El CHA2DS2VASc promedio fue de 0,6. La duración promedio de los procedimientos fue de 169 ± 47 minutos, con un tiempo de radioscopia de 39 ± 17 minutos. Se logró el aislamiento en 89/91 venas pulmonares (97,8%); en 2 pacientes se debió completar la lesión con radiofrecuencia. Un paciente (4,34%) presentó parálisis diafragmática transitoria, con recuperación espontánea a los 30 minutos. No hubo otras complicaciones. Con una mediana de seguimiento de 9,2 meses, 21 pacientes (91,3%) permanecieron en ritmo sinusal.
Conclusiones: En esta experiencia inicial, la CAB de FAP se mostró como una técnica segura y eficaz en pacientes seleccionados. Presentó un éxito agudo alto en el aislamiento de las venas pulmonares. Durante el seguimiento, la tasa de recurrencia fue baja. Resta esperar los resultados del seguimiento extendido para conocer su impacto real.
Palabras clave: Fibrilación auricular; Ablación con catéter; Criocirugía; Electrofisiología
ABSTRACT
Background: Pulmonary vein isolation is the cornerstone for the treatment of patients with recurrent and symptomatic paroxysmal atrial fibrillation (PAF). Balloon cryoablation (BCA) is an option to radiofrequency with shorter procedural and fluoroscopy times.
Objectives: The aim of this study was to describe the immediate outcomes and the initial experience in the first BCA procedures for PAF in our hospital.
Methods: Between November 2013 and February 2015, 23 patients underwent BCA for PAF. A computed tomography angiography with reconstruction of the left atrium and pulmonary veins was performed before the procedure.
Results: Mean age was 53±11 years, 19 patients were men, left atrial dimension was 40±7 mm and LVEF was 58%±8%. Average CHA2DS2VASc score was 0.6. The average procedural time was 169±47 minutes, with a fluoroscopy time of 39±17 minutes. Isolation of the pulmonary veins was achieved in 89/91 pulmonary veins (97.8%), and 2 patients required additional radiofrequency catheter ablation. One patient (4.34%) presented transient paralysis of the diaphragm with spontaneous recovery after 30 minutes. No further complications were observed. After a median follow-up of 9.2 months, 21 patients (91.3%) remained with sinus rhythm.
Conclusions: In this initial experience, BCA for PAF proved to be a safe and effective technique in selected patients. A high acute success rate was achieved for pulmonary vein isolation. During follow-up, the recurrence rate was low. The real impact of the procedure will be known when long-term outcomes become available.
Keywords: Atrial Fibrillation; Catheter Ablation; Cryosurgery; Electrophysiology
Abreviaturas
ACV Accidente cerebrovascular
AI Aurícula izquierda
Angio-TAC Angiotomografía computarizada
AVP Aislamiento de las venas pulmonares
CAB Crioablación con balón
ECG Electrocardiograma
FA Fibrilación auricular
FAP Fibrilación auricular paroxística
FEVI Fracción de eyección del ventrículo izquierdo
RF Radiofrecuencia
RIN Razón internacional normatizada
TIE Temperatura intraesofágica
INTRODUCCIÓN
La fibrilación auricular (FA) es la arritmia de mayor prevalencia (1-2%) en la población general y aumenta 5 veces el riesgo de accidentes cerebrovasculares (ACV), alterando la calidad de vida y aumentando la morbimortalidad de los pacientes afectados. (1, 2) El aislamiento eléctrico de las venas pulmonares (AVP) u otros focos gatillo constituye un tratamiento con intención curativa de los pacientes con fibrilación auricular paroxística (FAP) que continúan sintomáticos con tratamiento médico, además de disminuir el número de hospitalizaciones y potencialmente aumentar su sobrevida. (3-5)
El AVP mediante radiofrecuencia (RF) punto por punto mostró un éxito considerable en el tratamiento de la FAP, (6, 7) pero se asocia con un riesgo de complicaciones mayores tales como embolias, taponamiento cardíaco, lesión de órganos o estructuras vecinas (esófago, nervio frénico, aorta) y estenosis de las venas pulmonares. (6-10) Además, el procedimiento es complejo, insume tiempo y los resultados a largo plazo dependen en gran medida de la experiencia del operador en lograr una lesión lineal sin solución de continuidad. (11)
La crioablación con balón (CAB) de FAP es una tecnología introducida recientemente que evidenció principalmente disminución de los tiempos del procedimiento y de fluoroscopia, con una eficacia similar a la obtenida por R F. (11, 12) Además, la lesión por frío mostró que es menos trombogénica (menor lesión endotelial), con lesiones más delimitadas que dan mayor estabilidad al catéter al quedar adherido a la superficie de contacto. (13-16) En lo inherente a seguridad, no demostró superioridad respecto de la R F, agregando incluso una complicación casi exclusiva, la lesión del nervio frénico, reportada con una prevalencia del 11% al 24%, que en algunos casos puede producir parálisis diafragmática permanente. (11, 17, 18)
El objetivo de este estudio fue describir los resultados inmediatos de las primeras intervenciones con esta tecnología en nuestro hospital.
MATERIAL Y MÉTODOS
Entre noviembre de 2013 y febrero de 2015 se realizaron 23 procedimientos de CAB en 23 pacientes con diagnóstico de FAP sintomática y refractaria al tratamiento farmacológico (al menos una droga antiarrítmica) que habían presentado más de dos episodios en los últimos 3 meses.
La selección de los pacientes para CAB se realizó mediante método de imágenes [angiotomografía computarizada (angio-TAC)] con reconstrucción de la aurícula izquierda (AI) y las venas pulmonares (VP). Dos operadores evaluaron los resultados excluyendo a los pacientes con anatomía desfavorable, como ostium común de diámetro superior al balón, borde entre la orejuela izquierda y VP izquierdas agudo y profundo o múltiples venas de fino calibre.
Se excluyeron los pacientes con AI ≥ 5 cm, fracción de eyección del ventrículo izquierdo (FEVI) ≤ 40%, insuficiencia cardíaca en clase funcional III o más, enfermedad coronaria con necesidad de tratamiento invasivo, antecedentes de ACV en los 6 meses previos.
Todos los pacientes se encontraban anticoagulados con warfarina con una RIN estable entre 2 y 3 por lo menos 1 mes antes de la CAB. Se rotó a heparina de bajo peso molecular los días previos al procedimiento. Las drogas antiarrítmicas se suspendieron antes de la CAB. Ambas se reiniciaron a las 8 horas de finalizado el procedimiento y se mantuvieron por un período de 3 meses.
No se realizó ecografía transesofágica previa en ningún caso.
El procedimiento se realizó con anestesia general, evitando el uso de relajantes musculares, con control invasivo de la presión arterial y temperatura intraesofágica (TIE). La punción transeptal fue guiada por fluoroscopia con un set de punción convencional. Tras el abordaje de la AI se avanzó una cuerda de 0,035” de diámetro y 260 cm de longitud a la VP superior izquierda, luego de lo cual se realizó el intercambio por la vaina Flexcath sobre la que finalmente se avanzó el catéter balón y por su interior el catéter guía de mapeo circular (Achieve marca Medtronic Inc.). Durante todo el abordaje de la AI se mantuvo un tiempo de coagulación activado de entre 250 y 300 segundos. Se consideró tiempo total del procedimiento al tiempo transcurrido desde el ingreso del paciente a la sala de hemodinamia hasta el vendaje de los sitios de punción.
Para la ablación se utilizó catéter balón de 28 mm de primera o segunda generación (Artic Front y Artic Front Advance Medtronic Inc., respectivamente).
Ante de iniciar la CAB se colocó un catéter de mapeo circular en el interior de cada VP buscando la presencia de potenciales eléctricos en forma espontánea. En ritmo sinusal se buscó la captura de la AI al estimular desde el interior de cada V P. La presencia de alguno de estos dos elementos indicó la necesidad de realizar el aislamiento de esa V P. Se insufló el catéter balón en el interior de la AI y, usando como guía el catéter de mapeo circular localizado en el interior de la V P, se avanzó el balón contra el ostium de esta. En los primeros 20 casos se realizó una serie de dos aplicaciones de 240 segundos por cada VP tras la oclusión completa evidenciada por una venografía sin fuga de contraste y por un descenso de la temperatura del balón de -30 °C en 30 segundos. En los últimos 3 casos se realizó una serie de una sola aplicación por V P.
Durante las aplicaciones se controló la TIE y ante un descenso de esta menor o igual a 25 °C se detuvo la aplicación (Figura 1).

Fig. 1. Venografía de la vena pulmonar superior izquierda. Se observa la inyección de contraste luego de la oclusión mediante el catéter balón de la vena pulmonar superior izquierda, sin signos de fuga. Nótese la cercanía del termómetro intraesofágico al sitio de aplicación de crioterapia.
En las aplicaciones en las venas derechas se realizó monitoreo del nervio frénico, con estimulación de alta salida (20 mV a 1.200 mseg) y captura diafragmática (contracción del diafragma) mediante un catéter colocado en la cara derecha de la vena cava superior. Al perder o disminuir la contracción diafragmática, se interrumpía inmediatamente la aplicación (Figura 2).
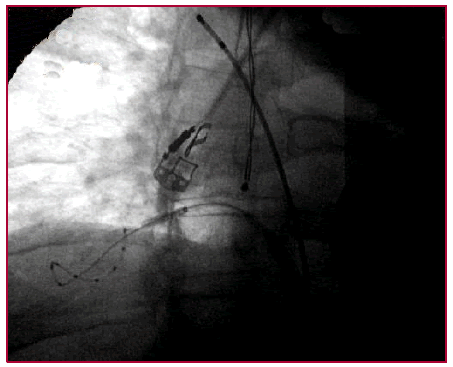
Fig. 2. Venografía de la vena pulmonar inferior derecha. Se observa la inyección de contraste luego de la oclusión mediante el catéter balón de la vena pulmonar inferior derecha. Se puede ver el catéter guía circular de mapeo, desplegado, y totalmente distal al ostium, sirviendo en este caso como soporte para el adecuado contacto del balón con el ostium de la vena pulmonar inferior derecha. Se observan, además, la ubicación del catéter bipolar en la vena cava superior (sitio en el cual se realiza estimulación para evidenciar la captura frénica) y la cercanía del termómetro intraesofágico al sitio de aplicación de crioterapia.
Posterior a la CAB de cada VP se buscó, en forma inmediata y a los 30 minutos, la desaparición de los potenciales y la presencia en ritmo sinusal de bloqueo bidireccional (ausencia de potenciales de VP e incapacidad de capturar la AI desde el ostium de la VP), considerándose estos hallazgos como éxito primario.
El seguimiento de los pacientes se realizó por consultorios externos: clínico + electrocardiograma (ECG) a las 48 horas y a los 30 días, clínico + ECG + monitoreo ambulatorio electrocardiográfico (ECG Holter) de 3 canales de 48 horas a los 3, 6 y 12 meses.
La medicación antiarrítmica y anticoagulante fue reinstaurada en el posoperatorio inmediato y se mantuvo durante los primeros 3 meses (período considerado de blanking tras una intervención de FA), suspendiéndose ambas luego de ese plazo. Se definió recurrencia a la presencia de FA en el seguimiento de al menos 30 segundos en cualquiera de los controles luego de la intervención (ECG o ECG Holter).
Análisis estadístico
Los resultados se expresan en términos de media ± desviación estándar o porcentaje de pacientes, mediana e intervalo intercuartil. La eficacia del procedimiento se evaluó como éxito en el AVP y ausencia de FA en el seguimiento.
Consideraciones éticas
El protocolo fue revisado y aprobado por el Comité Institucional de Bioética. Todos los pacientes firmaron un consentimiento informado antes de la CAB.
RESULTADOS
La edad promedio de los pacientes fue de 53 ± 11 años, 19 eran varones. El CHA2DS2VASc promedio fue de 0,6. El diámetro promedio de la AI fue de 40 ± 7 mm y la FEVI fue de 58% ± 8%. El 95% de los pacientes tenían 4 VP separadas en su desembocadura en la AI y un paciente tenía un tronco común izquierdo (Tabla 1).
Tabla 1. Características basales

Se utilizó el catéter Artic Front en 12 pacientes (52%) y Artic Front Advance en 11 (48%).
La duración promedio de los procedimientos fue de 169 ± 47 minutos, con un tiempo de radioscopia de 39 ± 17 minutos, observándose una tendencia a la disminución de ambos tiempos al aumentar el número de casos y mejorar la experiencia del operador (Figura 3).

Fig. 3. Relación entre el tiempo del procedimiento y número de casos.
El tiempo de internación en todos los casos fue de 1 día.
Se logró el aislamiento eléctrico y bloqueo bidireccional con CAB en 89 de 91 VP (97,8%). En 2 pacientes se debió completar el aislamiento de la VP con RF y catéter irrigado de 4 mm usando radioscopia: en un paciente en la VP inferior derecha y en el otro en la VP inferior izquierda.
Un paciente (4,34%) presentó parálisis diafragmática transitoria mientras se realizaba la CAB de la VP superior derecha (usando un balón de segunda generación), sin que impidiera el logro del aislamiento y con recuperación espontánea después de 30 minutos. En 2 pacientes (utilizando balón de segunda generación) se observó un marcado descenso de la TIE al realizar la CAB de la VP inferior izquierda, interrumpiéndose la aplicación para evitar el daño esofágico; igualmente se consiguió el aislamiento eléctrico y sin complicaciones en el seguimiento.
Durante una mediana de seguimiento de 9,2 meses (IIC 25%-75% = 5,5), el 91,3% de los pacientes se mantuvieron libres de FA (Tabla 2).
Tabla 2. Resultados de la serie

DISCUSIÓN
La CAB de FAP es una tecnología dirigida a facilitar la técnica de aislamiento de las VP en algunos casos difícil de lograr. En nuestra casuística se logró un aislamiento en el 97,8% de las V P, resultado similar a los publicados en la literatura internacional (Andrade y colaboradores, éxito primario promedio del 98,4%) (11) y a los conseguidos mediante la RF en nuestro país. (19, 20)
Solo una fracción de los pacientes en esta serie cumplió un seguimiento mayor de un año. La publicaciones internacionales no encontraron diferencias en la recurrencia de arritmia al año de una ablación usando RF o una CAB con balón de primera generación (RF 77% vs. CAB 72%); (21) sin embargo, el uso de CAB de segunda generación evidenció recientemente una tasa menor en la recurrencia de FA al compararla con la RF en el seguimiento alejado (76% vs. 60%, respectivamente). (22)
El tiempo promedio del procedimiento fue similar a los ya reportados, a pesar incluso de ser el inicio de la curva de aprendizaje. El estudio comparativo FAST-PVI (ablación de FA por métodos de navegación no radioscópico vs. CAB) con más 400 procedimientos en 9 centros de Alemania, diseñado para evaluar costos hospitalarios y tiempos de procedimiento, mostró que la CAB es más rápida disminuyendo los tiempos totales un 36%, con un tiempo promedio de laboratorio de 262 minutos para la navegación 3D versus 170 minutos para la CAB. (23)
En esta serie se observó un 4,3% de parálisis transitoria del nervio frénico usando un balón de segunda generación. Con los balones de primera generación, las primeras publicaciones del grupo de Packer y colaboradores (17) en 163 pacientes en el estudio STOP AF describieron una incidencia de parálisis frénica transitoria del 11,2% (menos del 1% permanente), que con el advenimiento de la monitorización del diafragma mediante estimulación durante la aplicación disminuyó a un 6%. (11) Con el uso de los balones de segunda generación se ha reportado un incremento del porcentaje de parálisis frénica (19,5%), recomendándose un mayor cuidado en las aplicaciones en las venas derechas, alejándose del ostium y permitiendo una pequeña fuga de contraste. (18)
En dos pacientes se debió suspender la aplicación por descenso marcado de la TIE, sin que impidiera en el tiempo de aplicación completar el aislamiento de forma exitosa. En la literatura se describen la ocurrencia de una fístula auriculoesofágica con balones de primera (24) y segunda generación. (25) Con balones de segunda generación se observó un incremento del porcentaje de úlceras esofágicas, el cual fue directamente proporcional al descenso de la TIE. (26)
En dos pacientes no se logró realizar el aislamiento, debiéndose completar la lesión con R F. En ambos el hallazgo se observó utilizando un balón de primera generación; en un caso en la VP inferior derecha, la cual presentaba una ramificación proximal al ostium con una orientación diferente, mientras que en el otro ocurrió en la VP inferior izquierda, sin poder identificarse la razón. Entre las limitaciones en conseguir el aislamiento se publicaron, utilizando balón de primera generación, las asociadas con variantes anatómicas en las VP y la AI (un borde profundo y agudo entre la orejuela izquierda y la VP superior izquierda, una separación angosta en la carina de las VP izquierdas o, en la VP inferior derecha, la presencia de una ramificación proximal al ostium con una orientación diferente, y un ángulo agudo entre el ostium y la vena), que se comportan como obstáculos y predictores de falla en el aislamiento (27) y hacen necesaria la selección previa con métodos de imágenes. Tal vez algunas de estas limitaciones se vean superadas con el uso de los balones de segunda generación, cuyo poder se incrementa al utilizar 8 inyectores y logra lesionar con todo el hemisferio anterior y no en el ecuador como su antecesor.
Limitaciones
El tiempo de seguimiento en esta serie fue corto, sobre todo al considerar además el período de blanking de los primeros 3 meses posteriores a una ablación de FA en el que la presencia o la ausencia de arritmias no confieren pronóstico alguno. En esta serie se realizó una selección de los casos previa angio-TAC, por lo que los resultados se limitan a pacientes que reúnan características similares.
CONCLUSIONES
En esta experiencia inicial, la CAB de FAP se mostró como una técnica segura y eficaz en pacientes seleccionados. Presentó un éxito agudo alto en el aislamiento de las V P. Durante el seguimiento, la tasa de recurrencia fue baja. Resta esperar los resultados del seguimiento extendido para conocer el impacto real de esta intervención.
Declaración de conflicto de intereses
Los autores declaran que no poseen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la web/ Material suplementario).
1. Wolf PA, Abbott RD, Kannel WB. Atrial fibrillation: a major contributor to stroke in the elderly. The Framingham Study. Arch Intern Med 1987;147:1561-4. http://doi.org/d8mjkr [ Links ]
2. Wang TJ, Larson MG, Levey D, Vasan RS, Leip E P, Wolf PA, et al. Temporal relations of atrial fibrillation and congestive heart failure and their joint influence on mortality: the Framingham Heart Study. Circulation 2003;107:2920-5. http://doi.org/c2m7hq [ Links ]
3. Bunch TJ, Crandall BG, Weiss J P, May HT, Bair TL, Osborn JS, et al. Patients treated with catheter ablation for atrial fibrillation have long-term rates of death, stroke, and dementia similar to patients without atrial fibrillation. J Cardiovasc Electrophysiol 2011;22:839-45. http://doi.org/cvv6fs [ Links ]
4. Piccini J P, Lopes RD, Kong MH, Hasselblad V, Jackson K, Al-Khatib SM. Pulmonary vein isolation for the maintenance of sinus rhythm in patients with atrial fibrillation: a meta-analysis of randomized, controlled trials. Circ Arrhythm Electrophysiol 2009;2:626-33. http://doi.org/c8bq9n [ Links ]
5. Wokhlu A, Monahan KH, Hodge DO, Asirvatham SJ, Friedman PA, Munger TM, et al. Long-term quality of life after ablation of atrial fibrillation the impact of recurrence, symptom relief, and placebo effect. J Am Coll Cardiol 2010;55:2308-16. http://doi.org/dpz4rv [ Links ]
6. Natale A, Raviele A, Arentz T, Calkins H, Chen SA, Haissaguerre M. Venice Chart international consensus document on atrial fibrillation ablation. J Cardiovasc Electrophysiol 2007;18:560-80. http://doi.org/ck3982 [ Links ]
7. Calkins H, Brugada J, Packer DL, Cappato R, Chen SA, Crijms HJ. HRS/EHRA/ECAS expert Consensus Statement on catheter and surgical ablation of atrial fibrillation: recommendations for personnel, policy, procedures and follow-up. Heart Rhythm 2007;4:816-61. http://doi.org/frdqkg [ Links ]
8. Dagres N, Hindricks G, Kottkamp H, Sommer P, Gaspar T, Bode K. Complications of atrial fibrillation ablation in a high-volume center in 1,000 procedures: still cause for concern? J Cardiovasc Electrophysiol 2009;20:1014-9. http://doi.org/bmd87g [ Links ]
10. Cappato R, Calkins H, Chen SA, Davies W, Lesaka Y, Kalman J. Updated worldwide survey on the methods, efficacy, and safety of catheter ablation for human atrial fibrillation. Circ Arrhythm Electrophysiol 2010;3:32-8. http://doi.org/fcn658 [ Links ]
11. Calkins H, Reynolds MR, Spector P, Sondhi M, Xu Y, Martin A. Treatment of atrial fibrillation with antiarrhythmic drugs or radiofrequency ablation: two systematic literature reviews and meta-analyses. Circ Arrhythm Electrophysiol 2009;2:349-61. http://doi.org/djsfz2 [ Links ]
12. Andrade J, Khairy P, Guerra P, Deyyell M, Rivard L, Dubuc M. Efficacy and safety of cryoballoon ablation for atrial fibrillation: A systematic review of published studies. Heart Rhythm 2011;8:1444-51. http://doi.org/fscbq7 [ Links ]
13. Linhart M, Bellmann B, Mittmann-Braun E, Schrichel J W, Bitzen A, Andrié R, et al. A Comparison of cryoballoon and radiofre-quency ablation of pulmonary veins in 40 patients with paroxysmal atrial fibrillation: A case-control study. Cardiovasc Electrophysiol 2009;20:1343-8. http://doi.org/bfhpb7 [ Links ]
14. Khairy P, Chauvet P, Lehmann J, Lambert J, Macle L, Tanguay J F. Lower incidence of thrombus formation with cryoenergy versus radiofrequency catheter ablation. Circulation 2003;107:2045-50. http://doi.org/c6j2fm [ Links ]
15. Khairy P, Dubuc M. Transcatheter cryoablation part I: preclinical experience. Pacing Clin Electrophysiol 2008;31:112-20. http://doi.org/d5t2fk [ Links ]
16. Lemola K, Dubuc M, Khairy P. Transcatheter cryoablation part II: clinical utility. Pacing Clin Electrophysiol 2008;31:235-44. http://doi.org/c6wdw4 [ Links ]
17. Sarabanda AV, Bunch TJ, Johnson SB, Mahapatra S, Milton M, Leite L. Efficacy and safety of circumferential pulmonary vein isolation using a novel cryothermal balloon ablation system. J Am Coll Cardiol 2005;46:1902-12. http://doi.org/dnpdtt [ Links ]
18. Packer D, Kowall RC, Wheelam KR, Irwin J, Ruskin J. Cryoballoon ablation of pulmonary veins for paroxysmal atrial fibrillation: first results of the North American Arctic Front (STOP AF) pivotal trial. J Am Coll Cardiol 2013;61:1713-23. http://doi.org/f2m68n [ Links ]
19. Casado-Arroyo R, Chierchia GB, Conte G. Phrenic nerve paralysis during cryoballoon ablation for atrial fibrillation: A comparison between the first- and second- generation balloon. Heart Rhythm 2013;10:1318-24. http://doi.org/578 [ Links ]
20. Labadet C, Dubner S, Hadid C, Azocar D, Di Toro D, Valsechi C. Eficacia y seguridad de la ablación por radiofrecuencia en pacientes con fibrilación auricular. Rev Argent Cardiol 2014;82:285-91. http://doi.org/576 [ Links ]
21. Scazzuso F, Rivera S, Sammartino, V, Albina G, Laiño R, Giniger A. Aislamiento de las venas pulmonares como tratamiento de la fibrilación auricular. Rev Argent Cardiol 2012;80:21-6. [ Links ]
22. Kojodjojo P, O’Neill MD, Lim PB, Malcolm-Lawes L, Whinnett ZI, Salukhe T V. Pulmonary venous isolation by antral ablation with a large cryoballoon for treatment of paroxysmal and persistent atrial fibrillation: medium-term outcomes and non-randomised comparison with pulmonary venous isolation by radiofrequency ablation. Heart 2010;96:1379-84. http://doi.org/cnzzh2
23. Aryana A, Singh SM, Kowalski M, Pujara D, Cohen A, Singh SK. Acute and Long-term outcomes of ablation of atrial fibrillation using the second-generation cryoballon versus open-irrigated radiofrequency: A multicenter experience. J Cardiovasc Electrophysiol 2015 Apr 27 [Epub ahead of print] http://doi.org/577 [ Links ]
24. Klein G, Lickfett L, Schreieck J. Comparison of ‘Anatomically designed’ and ‘Point-by-point’ Catheter Ablations for Human Atrial Fibrillation in terms of procedure timing and costs in German hospitals. FAST-PVI Study. Europace 2015;17:1030-7. http://doi.org/579
25. Stockigt F, Schirckel J W, Andrié R, Licfett L. Atrioesophageal fistula after cryoballon pulmonary vein isolation. J Cardiovasc Electrophysiol 2012;23:1254-7. http://doi.org/58b [ Links ]
26. Lim HW, Cogert GA, Cameron CS, Cheng VY, Sandler DA. Atrio-esophageal fistula during cryoballoon ablation for atrial fibrillation. J Cardiovasc Electrophysiol 2014;25:208-13. http://doi.org/58c [ Links ]
27. Fürnkranz A, Bordignon S, Schmidt B, Böhmig M, Böhmer MC, Bode F, et al. Luminal esophageal temperature predicts esophageal lesions after second-generation cryoballoon pulmonary vein isolation. Heart Rhythm 2013;10:789-93. http://doi.org/58d [ Links ]
28. Knecht S, Kuhne M, Altmann D. Anatomical predictors for acute and mid-term success of cryoballoon ablation of atrial fibrillation using the 28 mm balloon. J Cardiovasc Electrophysiol 2013;24:132-8. http://doi.org/58f [ Links ]














