INTRODUCCIÓN
La insuficiencia mitral (IM) representa alrededor del 25% del total de las valvulopatías 1, en su fase avanzada es, además, un fuerte predictor de mortalidad. 2 Como tratamiento, actualmente se prefiere la cirugía de reparación valvular al reemplazo de la válvula mitral, pero el número de casos en los que se opta por esta práctica sobre el total de casos en los que potencialmente se podría aplicar es muy bajo: se estima que es de un 50% 3, y muchos lo atribuyen a que se trata de una población con alta incidencia de comorbilidades entre las cuales merecen destacarse la edad avanzada, la mala función ventricular izquierda, el antecedente de cirugía cardíaca previa, la radioterapia en mediastino, la enfermedad renal, la fragilidad u otras comorbilidades. Debido a ello, la cirugía a menudo es descartada frente a este tipo de pacientes. 4,5
En los pacientes con alto riesgo, el tratamiento médico suele ser eficaz en la etapa inicial de la enfermedad. Con el correr del tiempo, sin embargo, comienza el deterioro de la función ventricular y renal; se incrementan a menudo las internaciones y también se eleva el riesgo de muerte, y se vuelve necesario recurrir a una intervención. Cuando la cirugía no es factible, la estrategia percutánea es una alternativa válida. 6
El tratamiento percutáneo destinado al agarre (clipado o grasping) de ambas valvas, técnica conocida como “edge-to-edge” en la literatura en inglés, remeda a la cirugía introducida por el Dr. O. Alfieri hace ya varios años, y se realiza con un dispositivo llamado MitraClipTM (Abbott Vascular, Santa Clara, California). El estudio EVEREST II 7 demostró la factibilidad y seguridad de esta técnica, que llevó a una mejoría significativa en la clase funcional (CF), comparable con la lograda mediante cirugía a 5 años de seguimiento, a expensas de una mayor necesidad de reintervención, sobre todo dentro de los 6 primeros meses de efectuado el tratamiento percutáneo.
Luego de ese estudio clínico, hubo múltiples publicaciones que dieron cuenta de mejores resultados con procedimientos de menor duración, producto de la “curva de aprendizaje” tanto en la selección de los pacientes como en el procedimiento en sí mismo. Además, la llegada del ecocardiograma Doppler 3D no solo permitió hacer una mejor selección de los casos, sino que ha sido vital para la optimización de la técnica y, por ende, de los resultados.
MATERIAL Y MÉTODOS
Desde marzo de 2016 hasta octubre de 2018 se incluyeron en forma consecutiva 12 pacientes portadores de IM grave y sintomáticos, con alto riesgo para cirugía o que eran inoperables y que recibieron reparación de la válvula mitral por cateterismo (PMVR) con MitraClip® . Todos se encontraban con tratamiento médico óptimo completo tolerable.
En todos los pacientes se realizó ecocardiografía transesofágica 2D-3D. La cuantificación de la insuficiencia se realizó de acuerdo con las guías específicas. 8 Se definió insuficiencia mitral grave orgánica (primaria) como aquella que presentaba un orificio regurgitante efectivo (ORE) ≥0,4 cm², y funcional (secundaria) como aquella que presentaba un ORE ≥ 0,2 cm2.
Se adquirieron imágenes volumétricas por ecocardiografía tridimensional. 9
La insuficiencia mitral orgánica incluyó pacientes con un “flail” ≤ 15 mm de ancho y ≤ 10 mm de altura; la insuficiencia mitral funcional incluyó pacientes con una profundidad de la coaptación desde el anillo mitral ≤ 10 mm y una altura de la coaptación entre las valvas ≥ 2 mm. Todos los pacientes debían tener un área valvular mitral ≥ 4 cm² estimada por planimetría y un gradiente medio ≤ 5 mmHg.
Se utilizaron los criterios de selección del estudio EVEREST para evaluar la factibilidad técnica del procedimiento
Se consideró “éxito del implante” (EI) frente a la presencia de IM leve o moderada al finalizar el procedimiento y “éxito del procedimiento a 30 días” (EP) frente al EI en ausencia de eventos adversos mayores (muerte, IAM, ACV, necesidad de cirugía valvular, derrame pericárdico, taponamiento o sangrado mayor)
El procedimiento fue realizado bajo anestesia general y las drogas usadas fueron propofol, remifentanilo y dexmedotomidina como coadyuvante debido a la utilización del ETE.
El acceso utilizado fue el venoso femoral derecho; en 10 casos se utilizó para el cierre una sutura percutánea con técnica de Preclose (Prostar XLTM 10Fr, Abbott Vascular, Santa Clara, California) y en 2 se utilizó la sutura cutánea compresiva con Vycril 3-0 (haciendo el punto compresivo llamado “figure 8”).
Luego se realizó una punción transeptal alta guiada con ETE; se realizó anticoagulación con heparina sódica 10.000 UI. Posteriormente se avanzó la vaina de Mullins colocándose un catéter de tipo Pig Tail 5 Fr en la aurícula izquierda para obtener un registro de la curva y de las presiones durante el procedimiento y el catéter guía dirigible (CGD) del MitraClip de 24 French.
El procedimiento se realizó bajo control con ETE 2D y 3D, y una vez confirmado el correcto grasping (> 4 mm de cada valva) y una reducción de la IM a ≤ 2+, se procedía a la liberación del clip. En caso de no lograrse, se implantaba un segundo clip o los que fuesen necesarios.
El catéter Pig Tail permitía monitorear la onda V auricular y sus presiones para determinar el impacto hemodinámico del procedimiento. Usualmente se observa que un buen clipado de las valvas lleva a una reducción marcada de la onda V y las presiones de la AI. Esto hoy puede ser realizado a través de un puerto lateral del nuevo CGD. Además, se evaluaba el flujo de las venas pulmonares, para una mejor evaluación de la IM residual.
Se analizó la calidad de vida de los pacientes antes del procedimiento y a los 6 meses de seguimiento con la escala Kansas City Cardiomyopathy Questionnaire (KCCQ). 10
El seguimiento fue realizado por el cardiólogo clínico, el cardiólogo intervencionista y el ecocardiografista en forma presencial. Al mes, a los 6 meses, al año y luego una vez por año se efectuó un eco-Doppler Luego del alta, recibieron tratamiento médico completo a dosis tolerables.
RESULTADOS
La media para la edad de los sujetos incluidos en la serie, que incluyó 7 hombres y 5 mujeres, fue de 74,1±8,9 años. Las comorbilidades o condiciones presentes fueron las siguientes: hipertensión y dislipidemia (n = 10); fibrilación auricular (n = 5); EPOC (n = 4); tabaquismo (n = 4); cirugía cardíaca previa (n = 4); infarto previo (n = 3); diabetes (n = 3), ATC previa (n = 2); marcapaso definitivo (n = 2). La eGFR fue de 73,8 ± 34,8 ml/m2; dicho parámetro fue < 60 ml/m2 en 2 enfermos y 1 se encontraba en diálisis. Ningún paciente había presentado ACV con anterioridad.
Todos estaban en CF III-IV, con antecedentes de internaciones por insuficiencia cardíaca dentro del año previo. En el ecocardiograma, el diámetro diastólico del ventrículo izquierdo (DDVI) fue de 61,8 ± 6,4 mm, el diámetro sistólico (DSVI) de 46,3 ± 2,1 mm y la fracción de eyección del ventrículo izquierdo (FEVI) de 50 ± 11%. La IM era degenerativa en 7 pacientes y funcional en 5.
La evaluación de riesgo por el Heart Team mostró que el EuroSCORElog fue de 9,6 ± 6,8; el STS score para mortalidad fue de 16,1 ± 13,5 y el STS score para la morbimortalidad fue de 22,8 ± 17,7.
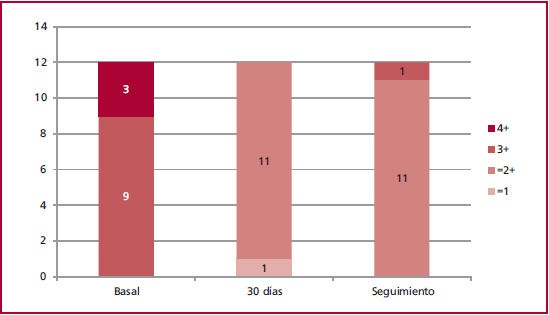
Se logró EI en todos los pacientes (Figura 1 y 2), en 7 de ellos se logró con el implante de 1 solo clip, mientras que 5 requirieron 2 clips en el mismo procedimiento. El gradiente transvalvular mitral posimplante fue de 3,6 ± 0,2 mmHg. La IM residual posprocedimiento fue leve (≤ 2+) en 11 pacientes y mínima en 1. No hubo muertes ni IAM, derrame pericárdico, taponamiento cardíaco, ACV, sangrado mayor, transfusión, necesidad de reintervención, cirugía de urgencia o conversión quirúrgica ni en la hospitalización ni luego del alta. La estadía hospitalaria fue de 1,9 ± 0,8 días (rango: 1-3 días).

Fig. 1 Insuficiencia mitral grave funcional (a-b-c); insuficiencia trivial luego del implante de dos clips (d-e-f)
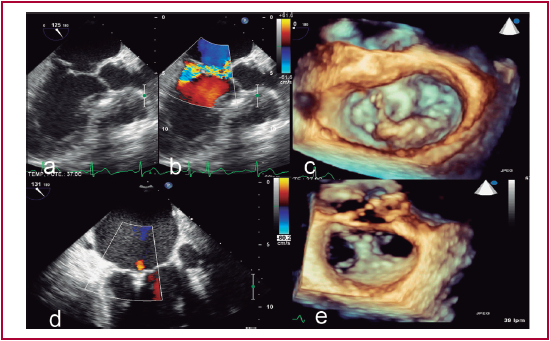
Fig. 2 Insuficiencia mitral grave de causa orgánica (a-b-c); insuficiencia trivial luego del implante de un clip (d-e)
El EP se alcanzó en todos los enfermos, ya que todos mantuvieron el EI sin que se presentara ningún efecto adverso mayor ni reinternación por insuficiencia cardíaca. Todos pasaron a CF I-II.
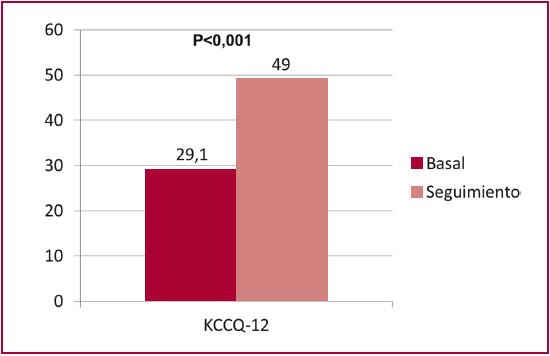
El seguimiento clínico se realizó en todos los pacientes con un tiempo medio de 8,8 ± 6,7 meses (rango: 1-30 meses), lapso durante el cual ocurrieron 2 muertes: una debido a una neumonía al octavo mes y la otra luego de un reemplazo valvular aórtico por cateterismo (TAVI) a 30 meses del seguimiento y no relacionada con IM o fallo del clip. No hubo ACV, IAM o cirugía valvular mitral o reintervención. Todos se encontraban en CF I-II (Figura 3). Un paciente (el mismo que luego recibió TAVI y falleció) requirió internación por insuficiencia cardíaca por disfunción ventricular crónica mientras mantenía IM < 2. En el eco-Doppler cardíaco en el seguimiento, 11 pacientes tenían IM leve y 1 moderada a grave (Figura 4). Hubo mejoría en la calidad de vida en el seguimiento en comparación con la situación basal (29,09 vs. 48,97; p > 0,001) (Figura 5).
DISCUSIÓN
En esta serie inicial, el tratamiento percutáneo de la IM grave sintomática en pacientes con alto riesgo quirúrgico fue factible y seguro. Quedó demostrado que luego de un procedimiento exitoso, la estadía hospitalaria es corta y el enfermo logra una mejoría clínica significativa y también en su calidad de vida, con una baja tasa de reinternación por insuficiencia cardíaca a 30 días y en el seguimiento a corto plazo.
La curva de aprendizaje se vio reflejada en los tiempos que demandó el procedimiento, que fue de alrededor de 2 horas en los primeros casos y de alrededor de 1 hora en los últimos.
El procedimiento parece complejo y el dispositivo poco amigable al inicio; se destaca la importancia de una buena coordinación entre el ecocardiografista, el intervencionista y el anestesiólogo.
Un buen comienzo es de vital importancia para logar un buen resultado de manera relativamente sencilla. Para ello, la punción transeptal debe ser realizada con la guía del ETE, ya que una punción en un lugar inadecuado puede complicar mucho el manejo del CGD y el sistema de entrega del clip.
Dentro de las posibles complicaciones se señala el desprendimiento parcial del clip luego de la liberación (“detachment”), que fue reportado en los primeros estudios. 11 No obstante, cabe señalar que en la medida que los operadores adquirieron más experiencia, esta complicación técnica disminuyó drásticamente. Ningún paciente de nuestra serie sufrió esa complicación.
La evaluación de la cantidad de tejido de la valva que ha sido atrapada por los brazos del clip queda a cargo del ecografista, quien, luego de asegurarse de que es la correcta, autoriza al intervencionista a la liberación final del clip. Cuando no existe tal seguridad, el clip debe ser abierto y reposicionado.
El tratamiento médico en la IM grave secundaria con fracción conservada ha demostrado ser eficaz; sin embargo, se ha observado que estos pacientes tienen alta mortalidad con el paso del tiempo. Esto fue analizado por Barakat et al. 12, quienes analizaron 400 sujetos con IM grave y fracción de eyección ≥ 60%. En el seguimiento a 12 meses y a 3 años, la mortalidad fue del 19,1% y 26,3%, respectivamente. Además, estos individuos requirieron con frecuencia internaciones por insuficiencia cardíaca y a menudo debieron someterse a tratamiento de ablación por cateterismo de la fibrilación auricular, terapia de resincronización cardíaca, angioplastia, colocación de dispositivos de asistencia ventricular o trasplante cardíaco.
Como ya hemos indicado, las guías de tratamiento13 recomiendan la cirugía de reparación o reemplazo para los pacientes con IM grave sintomática, pero el número de enfermos que efectivamente son intervenidos es bajo respecto del número total de casos en los que se presenta esta patología. 14
Con el objeto de paliar este déficit y ofrecer un tratamiento menos invasivo se han introducido diversas tecnologías para la reparación o el reemplazo de la válvula mitral por cateterismo; el MitraClipTM es una de las primeras, además de ser la más utilizada (más de 60 000 casos en todo el mundo hasta 2017) y la primera registrada en un estudio aleatorizado versus la cirugía.
El EVEREST II 6, que incluyó 279 pacientes, fue el primer estudio aleatorizado (proporción 2:1) que analizó esta estrategia versus la cirugía. Ese estudio mostró que, en la etapa inicial, los enfermos que recibieron MitraClipTM tuvieron menos complicaciones, en especial, sangrado, pero requirieron más cirugía dentro de los primeros 6 meses. En el seguimiento a 5 años, el punto final combinado de sobrevida libre de mortalidad, cirugía e insuficiencia mitral grave fue del 44,2% vs. 64,3% (p = 0,01) a favor de la cirugía. Esto fue consecuencia de una mayor incidencia de IM 3+ o 4+ (12,3% vs. 1,8%; p = 0,02) y de necesidad de cirugía (27,9% vs. 8,9%; p = 0,003). La cirugía luego del MitraClipTM fue, en la mayoría de los casos (78%), dentro de los primeros 6 meses; luego de este período, la evolución fue similar en ambos grupos. No hubo diferencias en la mortalidad a 5 años (20,8% vs. 26,8%) y se mantuvieron la CF y la calidad de vida
Es interesante destacar que cuando se hizo este estudio clínico no estaba disponible en la práctica diaria el ETE en 3D, lo cual, sin lugar a dudas, puede haber influido en los resultados, así como también la técnica empleada, por ejemplo, el uso de múltiples clips para logar una reducción máxima de la IM.
Kortlandt y col. 15 realizaron un interesante análisis en el que se comparó la evolución de 1036 sujetos con IM sintomática; 568 de ellos recibieron MitraClip, 173 cirugía y 295 tratamiento médico. Si bien las características clínicas fueron similares, los que recibieron MitraClip tenían menor fracción de eyección del VI y sus scores quirúrgicos eran más altos (STS scores: 7,7 para MitraClipTM; 2,7 para el grupo cirugía y 3,5 para el de tratamiento médico). En el seguimiento a 5 años, la sobrevida fue menor en los que recibieron tratamiento médico y fue similar entre los grupos que recibieron MitraClipTM y cirugía, pero debemos tener en cuenta que la edad era mayor, la función ventricular izquierda era menor y tenían mayor riesgo quirúrgico aquellos que recibieron la estrategia percutánea.
Los pacientes con alto riesgo para cirugía, como los de nuestra serie, generan una gran dificultad para el manejo y esto fue analizado en el estudio EVEREST II High Risk Registry 16, que incluyó 351 pacientes con un STS score >12. Al año de seguimiento hubo una reducción muy importante de la IM: el 84% tenía una IM ≤ 2+. También hubo una reducción significativa de los diámetros ventriculares, el 83% se encontraba en clase funcional I-II, y eso estuvo acompañado de una disminución de la necesidad de internaciones por insuficiencia cardíaca, con mejoría en la calidad de vida y en los test de evaluación mental. La sobrevida libre de mortalidad fue del 77,2% y libre de cirugía valvular mitral, del 97,8%.
Uno de los grandes desafíos que presenta el tratamiento de la IM grave, ya sea funcional o secundaria, es cuando se asocia a deterioro de la función ventricular izquierda. Si bien en estudios previos se ha reportado una evolución similar, pero con más reinternaciones por insuficiencia cardíaca en el grupo bajo tratamiento médico convencional 17,18, actualmente contamos con dos estudios aleatorizados que analizan la estrategia invasiva por cateterismo y el tratamiento médico convencional.
El primero de ellos es el MITRA FR 19, que incluyó 152 individuos sintomáticos con IM secundaria divididos en dos grupos: quienes recibieron MitraClipTM + tratamiento médico vs. quienes recibieron tratamiento médico óptimo solo. El punto final primario de eficacia (PFE) fue mortalidad de cualquier causa y rehospitalización por insuficiencia cardíaca no planeada a 12 meses. La media para la edad de los pacientes fue de 70 años y el resto de las características fueron similares al comparar grupos; la fracción de eyección fue de 33%, el área del orificio regurgitante efectivo (AORE) de 31 mm2 y el score de riesgo EuroScore II de 6. Se logró éxito del implante en el 95,8% de los casos. Al año de seguimiento, el PFE fue similar para ambas ramas de tratamiento (54,6% vs. 51,3%; p = 0,53); además, tampoco hubo diferencia en términos de mortalidad ni de nuevas reinternaciones por insuficiencia cardíaca.
Debemos tener en cuenta que en el citado estudio hubo una pérdida importante de los datos ecocardiográficos y de dosaje del BNP, así como de aquellos referidos a calidad de vida y evolución clínica en el seguimiento al año. También hay que tener presente que el requerimiento mínimo para los operadores era de tan solo 5 casos previos, aunque estaba permitida la asistencia por expertos (proctoring).
El otro estudio importante es el COAPT, que aleatorizó 614 pacientes con IM moderada o grave sintomáticos y con alto riesgo quirúrgico (STS score > 8), 302 recibieron MitraClip y 312 tratamiento médico óptimo. El PFE fueron todas las hospitalizaciones por insuficiencia cardíaca a 24 meses. No hubo diferencia entre los grupos en cuanto a la edad (71 años), la presencia de fibrilación auricular (más de la mitad de los enfermos), la etiología isquémica (60%). La fracción de eyección fue del 31,3% y el área del orificio efectivo regurgitante (AORE) de 40 mm2. El éxito del implante fue del 97%. El PFE estuvo a favor de los que recibieron MitraClip (35,8 vs. 67,9; p<0,001; HR [95% CI] = 0,53 [0,40-0,66]; p < 0,001), con un número necesario a tratar a 24 meses (NNT 24 m) de 3,1 [95% CI: 1,9-8,2], además este grupo presentó menor mortalidad (29,1% vs. 46,1%; p < 0;001; HR [95% CI] = 0,62 [0,46-0,82]; p < 0,001), con NNT 24 m = 5,9 [95% CI: 3,9-11,7] y mejoría significativa en la clase funcional, la calidad de vida y el test de marcha de los 6 minutos. En el análisis ecocardiográfico, el tratamiento con MitraClip preservó más la función ventricular izquierda y tuvo menor regurgitación mitral y mejor remodelado ventricular izquierdo.
El tratamiento invasivo también disminuyó la necesidad de asistencia ventricular o trasplante cardíaco en el seguimiento (4,4% vs. 9,5%; HR [95%CI] = 0,37 [0,17-0,81]; p = 0,01). Se debe resaltar que un tercio del grupo de tratamiento médico también recibió terapia de resincronización.
Las posibles explicaciones para las diferencias entre estos dos estudios, tan discutidas en la comunidad médica, son varias. En primer lugar, en el COAPT el tratamiento médico estuvo a cargo de especialistas en insuficiencia cardíaca y los enfermos recibieron tratamiento médico con dosis máximas toleradas antes de la aleatorización, por lo que ingresaron al estudio los que presentaban IM grave refractaria; esto no ocurrió en el MITRA FR. Además, en el MITRA FR los pacientes presentaron menos insuficiencia cardíaca (CF I-II), más internaciones por insuficiencia cardíaca, valores más altos del BNP y con un mayor volumen de fin de diástole. En segundo lugar, hubo diferencia en el área efectiva del orificio regurgitante, que fue mayor en el COAPT (41 ± 15 mm2 vs. 31 ± 10 mm2), con un volumen de fin de diástole menor, y, en tercer lugar, hubo más pacientes del COAPT que recibieron más de un clip. Todo esto puede explicar la diferencia entre ambos estudios con resultados tan dispares. 20
Además, hay análisis que demostraron que es muy importante intervenir a los enfermos antes de que comience el deterioro de la función ventricular y la dilatación ventricular, ya que cuando ello ocurre, comienza a aparecer el deterioro de la función renal 21 y la fibrilación auricular 22, generando un fuerte impacto negativo en el pronóstico.
Si bien está demostrado que la presencia de IM ≥ 2+ se asocia con mala evolución clínica, no debemos olvidarnos del gradiente residual luego del implante; esto fue analizado por Neuss y col. 23, quienes evaluaron a 200 pacientes, 50 de los cuales presentaban un gradiente posimplante de MitraClip > 5 mmHg. Estos autores observaron que no había diferencia en las características clínicas basales de los grupos, pero el análisis de Kaplan-Meier en el seguimiento mostró mayor mortalidad cuando el gradiente era > 5 mmHg medido en forma invasiva o > 4,4 mmHg por ecocardiografía. Es por ello que el límite al número total de clips a implantar con el objeto de eliminar o reducir al máximo la IM se basa en dicho gradiente residual. En nuestra serie, el gradiente medio al finalizar el procedimiento fue de 3,6 ± 0,2 mmHg y en ningún caso superior a 5 mmHg.
La IM secundaria debido a la dilatación de ventrículo izquierdo se asocia a una dilatación del anillo mitral; en este grupo de individuos, la cirugía realiza la reparación mitral con la utilización de anillos mitrales protésicos asociada a la reparación valvular y del aparato subvalvular. Con el desarrollo tecnológico, es probable que en el futuro dispongamos de anillos mitrales percutáneos asociados a clips para tratar a este grupo de pacientes, en los que la dilatación futura del anillo podría alterar el resultado inicial logrado.
En nuestro grupo, con gran experiencia en el “approach minimalista” para la reparación valvular o de la aorta, hemos tratado de disminuir al máximo la invasividad en estos pacientes y si bien el uso de anestesia general es muy necesario para el confort y para poder tolerar durante un período largo la sonda transesofágica de la ecografía; hemos limitado la utilización de vías centrales o catéteres en la vía urinaria, ya que ello otorga mayor confort a los pacientes y favorece una deambulación precoz.
CONCLUSIÓN
En esta serie inicial de un solo centro, la reparación valvular de la válvula mitral por cateterismo con MitraClipTM en pacientes con alto riesgo quirúrgico portadores de insuficiencia mitral grave sintomática fue factible y segura, con una significativa mejoría clínica a 30 días y en el seguimiento, con mejoría en la calidad de vida. Estos hallazgos, que incluyen la curva de aprendizaje de todo el equipo, muestran resultados similares a las grandes series internacionales.