INTRODUCCIÓN
La enfermedad cardiovascular es la principal causa de mortalidad en la mayoría de los países, con un enorme impacto económico y sanitario. 1
La terapia con estatinas reduce aproximadamente en un 22% la incidencia de eventos coronarios mayores por cada 1 mmol/l (≈ 39 mg/dl) de colesterol unido a las lipoproteínas de baja densidad (C-LDL) que disminuye. 2 Sin embargo, aun cuando los pacientes estén correctamente medicados con estatinas e inclusive alcancen las metas lipídicas recomendadas por las diferentes guías, los eventos cardiovasculares siguen ocurriendo. El riesgo cardiovascular remanente una vez conseguido el objetivo de C-LDL con el uso apropiado de estatinas se conoce como “riesgo cardiovascular residual”. 3 Este riesgo residual se debe, en gran medida, a otros factores lipídicos diferentes del C-LDL pero con potencial acción aterogénica, como son las lipoproteínas ricas en triglicéridos. 4,5
Sin embargo y más allá del riesgo residual “lipídico”, se han propuesto otros mecanismos para explicar el riesgo cardiovascular remanente. En dicho contexto, la inflamación es considerada un factor relevante en el proceso de la aterosclerosis, en la aparición de los eventos cardiovasculares clínicos y en el riesgo cardiovascular residual. 6 Por lo tanto, las terapias antiinflamatorias dirigidas a la inflamación de la placa aterosclerótica podrían contribuir a la estabilización de la placa y a la prevención de los eventos tromboembólicos. 7,8
En los últimos años se ha propuesto a la colchicina como una potencial opción terapéutica en el marco de la enfermedad coronaria. 9 A través de la unión a las proteínas a-tubulina y b-tubulina, la colchicina tiene múltiples propiedades antiinflamatorias, incluida la inhibición de la polimerización de los microtúbulos, la afectación del rodamiento de los leucocitos y de la adhesión endotelial, la inhibición del inflamasoma NLRP y la disminución en la secreción de citocinas. 10
Varios metaanálisis han evaluado la asociación entre el uso de colchicina y los eventos cardiovasculares. 11,12,13,14 Sin embargo, los resultados sobre la asociación entre el uso de colchicina y la incidencia de infarto agudo de miocardio (IAM) fueron heterogéneos. Más aún, en el ensayo clínico COLCOT, que fue uno de los estudios que incluyeron mayor número de pacientes, si bien se evidenció una reducción del punto final combinado de eventos cardiovasculares, esto fue principalmente a expensas de una reducción del accidente cerebrovascular (ACV) y de la hospitalización urgente por angina inestable, y no por una disminución en el riesgo de IAM. 15 Asimismo, recientemente se han publicado dos nuevos ensayos clínicos y ha surgido la necesidad de actualizar y clarificar la información. 16,17
El objetivo principal del presente metaanálisis fue evaluar el efecto de la colchicina en la incidencia de IAM en pacientes con enfermedad aterosclerótica establecida. Por otro lado, analizar el impacto de dicha droga sobre la incidencia de ACV y la mortalidad cardiovascular fue el objetivo secundario.
MATERIAL Y MÉTODOS
Extracción de datos y evaluación de la calidad: El metaanálisis se realizó de acuerdo con la declaración PRIS-MA para informar revisiones sistemáticas. 18 Se realizó una búsqueda en la literatura para identificar ensayos clínicos que evaluaran la terapia con colchicina, publicados entre enero de 1990 y septiembre de 2020. Dos revisores independientes realizaron búsquedas en las bases de datos electrónicas PubMed/Medline, EMBASE, Scielo y Cochrane Clinical Trials usando los términos “colchicine”, “major cardiovascular events”, “myocardial infarction”, “coronary heart disease”, “stroke”, “cardiovascular mortality”, “mortality” y “cardiovascular risk”. Los estudios elegidos fueron aquellos ensayos clínicos aleatorizados que informaron los datos sobre los eventos cardiovasculares y que evaluaron el efecto de la colchicina en poblaciones con enfermedad aterosclerótica clínica (enfermedad coronaria, enfermedad cerebrovascular, enfermedad vascular periférica). En el caso de estudios que evaluaron pacientes con cirugía cardíaca, se seleccionaron aquellos en los cuales los pacientes con enfermedad coronaria representaron >50% del total de la población incluida.
El punto final primario del estudio fue la incidencia de IAM. La ocurrencia de ACV y la mortalidad cardiovascular se consideraron puntos finales secundarios.
Se evaluó el riesgo potencial de sesgos para todos los ensayos incluidos utilizando la herramienta Cochrane desarrollada para este propósito (Rob 2). 19 Esta herramienta evalúa el sesgo en cinco dominios diferentes: sesgo que surge de la asignación al azar, sesgo debido a desviaciones de la intervención prevista, sesgo debido a datos de resultado faltantes, sesgo en la medición del resultado y sesgo en la selección del resultado informado. Cada dominio se calificó como de “alto riesgo de sesgo”, de “bajo riesgo de sesgo” o con “algunas preocupaciones”.
El protocolo fue revisado y aprobado por el Comité Asesor del Consejo de Epidemiología y Prevención Cardiovascular de la Sociedad Argentina de Cardiología.
Análisis estadístico: Se estimó el efecto sumario del uso de colchicina sobre los puntos finales previamente comentados. Las medidas del tamaño del efecto se expresaron como odds ratios (OR) y se calculó el estadístico I2 para cuantificar la heterogeneidad y la inconsistencia entre los ensayos. Se eligió un modelo de efectos fijos o aleatorios, dependiendo del valor de I2 (<40% o >40%, respectivamente). Para comparar el efecto promedio entre los subgrupos, utilizamos la prueba Z. El nivel de significación estadística se estableció en 0,05 (análisis de dos colas). Para el análisis se utilizó el software estadístico R. 20
Análisis del sesgo de publicación: Se creó un gráfico de embudo utilizando el error estándar (SE) por log OR. Asimismo, se realizaron las pruebas de Harbord y Peters, ajustadas por el número de estudios incluidos.
Análisis de sensibilidad: El análisis de sensibilidad consiste en replicar los resultados del metaanálisis, excluyendo en cada paso cada uno de los estudios incluidos en la revisión. Si los resultados obtenidos son similares, tanto en la dirección como en la magnitud del efecto, se considera que el análisis es robusto.
RESULTADOS
En total, 9 estudios que evaluaron el uso de colchicina fueron seleccionados para el análisis cuantitativo. 15,16,17,21,22,23,24,25,26 Siete trabajos fueron elegidos y considerados para el análisis del punto final primario, incluyendo 11914 pacientes. 15,16,17,21,22,25,26 Un total de 5966 sujetos se analizaron en la rama colchicina y 5948 pacientes en el grupo placebo. Ocho ensayos clínicos que incluyeron 12275 pacientes fueron elegidos para el análisis de ACV. 15,16,17,21,22,24,25,26 Asimismo, ocho estudios que informaron la mortalidad cardiovascular (12111 pacientes) fueron tenidos en cuenta para el análisis de dicho punto final secundario. 15,16,17,21,22,23,25,26 El diagrama de flujo del proceso de selección de los estudios puede observarse en la Figura 1.
Todos los estudios evaluados fueron ensayos aleatorizados. La calidad de los estudios incluidos en el presente metaanálisis se resume en la Figura 2.
Cuatro de los estudios evaluados incluyeron pacientes con enfermedad coronaria estable, mientras que otros cuatro evaluaron sujetos luego de un síndrome coronario agudo. Un estudio incluyó pacientes con diabetes que serían sometidos a una angioplastia coronaria y otros dos estudios evaluaron pacientes sometidos a una cirugía cardíaca. El tiempo medio de seguimiento osciló entre 1 y 28,6 meses.
Las características de los estudios incluidos pueden observarse en la Tabla 1.
TABLA 1 Características de los estudios incluidos en el análisis.
| Estudio | Rama colchicina (dosis diaria) | N | Rama control | n | Población | Seguimiento (meses) |
|---|---|---|---|---|---|---|
| Raju et al. 21 | 1 mg | 40 | Placebo | 40 | SCA o ACV isquémico | 1 |
| LoDoCo 31 | 0,5 mg | 282 | Cuidado usual | 250 | Enfermedad coronaria estable | 24 |
| Deftereos et al. 23 | 1 mg | 100 | Placebo | 96 | Diabéticos con necesidad de angioplastia coronaria | 6 |
| COPPS-2 24 | 0,5 a 1 mg (según el peso) | 180 | Placebo | 180 | Postcirugía cardíaca. | 3 |
| Meurin et al. 25 | 1 mg | 98 | Placebo | 99 | Postcirugía cardíaca con derrame pericárdico | 6 |
| COLIN 26 | 1 mg | 23 | Placebo | 21 | SCA | 1 |
| COLCOT 35 | 0,5 mg | 2366 | Placebo | 2379 | SCA | 22,6 |
| LoDoCo-2 22 | 0,5 mg | 2762 | Placebo | 2760 | Enfermedad coronaria estable | 28,6 |
| COPS 17 | 1 mg x 1 mes, luego 0,5 mg | 396 | Placebo | 399 | SCA | 12 |
ACV: accidente cerebrovascular; SCA: síndrome coronario agudo
Este metaanálisis demostró que la terapia con colchicina se asoció a un menor riesgo de IAM (OR: 0,76; IC 95%: 0,62-0,92; I2 = 15%) (Figura 3). Asimismo, se observó una reducción significativa en la incidencia de ACV (OR: 0,48; IC 95%: 0,30-0,76; I2 = 0%), sin un efecto significativo en la mortalidad cardiovascular (OR: 0,71; IC 95%: 0,49-1,05; I2 = 32%) con la intervención farmacológica (Figura 4).
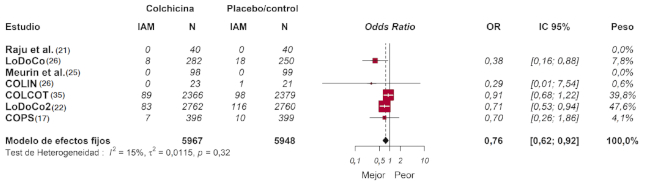
Fig. 3 Efecto de la terapia con colchicina sobre la incidencia de infarto agudo de miocardio. Modelo de efectos fijos, odds ratio, intervalo de confianza 95% y estadístico I2

Fig. 4 Efecto de la terapia con colchicina sobre la incidencia de accidente cerebrovascular (A) y mortalidad cardiovascular (B). Modelo de efectos fijos, odds ratio, intervalo de confianza 95% y estadístico I2
La evaluación gráfica y analítica sugiere ausencia de sesgo de publicación (Figura 5).
El análisis de sensibilidad muestra que los resultados son robustos (Figura 6).
DISCUSIÓN
En este metaanálisis observamos que el tratamiento con colchicina comparado con placebo se asoció a un menor riesgo de IAM. Por otro lado, el uso de dicho fármaco también se asoció a un menor riesgo de ACV, sin ser significativa la reducción de la mortalidad cardiovascular.
Existe evidencia que respalda y confirma el rol de la inflamación en el proceso fisiopatológico de la aterosclerosis. 27 Dentro de los múltiples mecanismos moleculares involucrados en el proceso inflamatorio, se encuentra la participación activa de los inflamasomas. Los inflamasomas son complejos de proteínas de alto peso molecular que se forman en el compartimento citosólico en respuesta a diferentes estímulos. 28 Entre los más estudiados en el contexto de la aterosclerosis se ubica el complejo de señalización multiproteico citosólico llamado inflamasoma NLRP3, que sirve como plataforma para la activación de la caspasa-1 y favorece la síntesis de las citocinas proinflamatorias, como la interleucina (IL)-1β , la IL-18, e, indirectamente, la IL-6. 29
Se han descrito al menos cuatro supuestos mecanismos de inhibición del inflamasoma NLRP3 por la colchicina: 1) inhibición del gen MEFV que da como resultado la inhibición del receptor-pirina; 2) inhibición del ensamble citoplásmico del inflamasoma debido a la interferencia de la tubulina; 3) bloqueo directo de la caspasa-1; 4) inhibición de la formación de poros mediados por P2X7, lo que genera una disminución del flujo de salida de K+. El resultado final es la disminución de la síntesis de la forma activa de la IL-1β. 30 Por otro lado, un subestudio proteómico del ensayo clínico LoDoCo-2 demostró que el efecto antiinflamatorio de la colchicina en pacientes con enfermedad coronaria crónica se explicaría no solo por su efecto sobre el inflamasoma, sino también por su efecto sobre la función de los neutrófilos. 31
La colchicina no es el único fármaco con efecto antiinflamatorio que se ha evaluado en el contexto de la prevención cardiovascular. El estudio CANTOS demostró que el tratamiento antiinflamatorio anti IL-1β con canakinumab en pacientes con IAM previo redujo significativamente la tasa de eventos cardiovasculares comparado con placebo. 32 Sin embargo, en el estudio CIRT, que evaluó el uso de bajas dosis de metotrexato en pacientes con enfermedad aterosclerótica estable, no se observó una reducción en los niveles de IL-1β, IL-6 o proteína C reactiva y, consecuentemente, no se demostró una reducción de los eventos cardiovasculares con la medicación en comparación con el placebo. 33
A pesar de toda la evidencia disponible sobre cuestiones fisiopatológicas que explicarían el potencial beneficio de la colchicina sobre la incidencia de IAM, los ensayos clínicos previamente publicados han mostrado resultados contradictorios. Quizás el beneficio más robusto sea el observado en términos de incidencia de ACV. 14 Si bien los eventos cerebrovasculares y coronarios tienen bases fisiopatológicas en común, el potencial impacto de la colchicina sobre la ocurrencia de fibrilación auricular podría ser un mecanismo adicional en la protección de eventos isquémicos cerebrales. 34
Nuestro metaanálisis tuvo como objetivo principal clarificar si existe o no una asociación significativa entre el uso de la colchicina y la incidencia de IAM, incorporando los últimos ensayos clínicos recientemente publicados.
Cuando analizamos los dos estudios clínicos que han incluido más pacientes, los resultados fueron distintos. En el estudio COLCOT, que incluyó 4745 pacientes luego de un síndrome coronario agudo, no se observó una diferencia significativa en la incidencia de IAM con el uso de 0,5 mg diarios de colchicina. 15 Sin embargo, un subanálisis del estudio COLCOT mostró que el beneficio fue mayor en los pacientes que recibieron colchicina en los primeros tres días posteriores al IAM en comparación con los sujetos que recibieron la medicación entre los días 4 y 30. 35 Por otro lado, el recientemente publicado ensayo LoDoCo-2, que incluyó 5522 sujetos con enfermedad coronaria estable, reportó una disminución significativa del 30% en la ocurrencia de IAM luego de administrar la misma dosis de colchicina. 16 En la misma línea, los resultados del estudio LoDoCo, que incluyó pacientes con enfermedad coronaria estable, mostraron una reducción significativa en la incidencia de eventos coronarios agudos con el uso de colchicina 22, mientras que el estudio COPS, que fue desarrollado en pacientes con un síndrome coronario agudo reciente y usó una dosis más elevada de colchicina durante el primer mes (1 mg), no evidenció un beneficio clínico en la incidencia de IAM. 17
A priori, la intuición nos dice que los pacientes luego de un síndrome coronario agudo están más inflamados, por lo que debería ser la población más beneficiada por la intervención farmacológica. Sin embargo, la discordancia entre lo hipotetizado basándonos en la fisiopatología y los resultados observados en los ensayos clínicos no está del todo aclarada. En general, una alta proporción de pacientes estaban medicados con estatinas en todos los estudios. Sin embargo, la doble antiagregación (aspirina más otro antiagregante plaquetario) fue mucho más elevada en los estudios que incluyeron pacientes con cuadros coronarios agudos.
¿La eficacia de la colchicina es mayor en estados de menor inflamación, pero constante? En la etapa aguda de la enfermedad, ante un estado protrombótico mayor, ¿podría la medicación antiagregante o anticoagulante atenuar el efecto de la colchicina? Es claro que no contamos con las respuestas definitivas a estos interrogantes, teniendo en cuenta que, además, las diferencias podrían explicarse por cuestiones estadísticas (falta de poder en los estudios más pequeños) o simplemente por azar. Determinar si el impacto de la colchicina difiere en las distintas poblaciones escapa al objetivo de nuestro trabajo y deberá analizarse en futuras investigaciones.
El resultado principal de nuestro metaanálisis, luego de analizar toda la información disponible a la fecha en forma conjunta, demostró que el uso de colchicina se asoció a una reducción del 24% en la incidencia de IAM. Asimismo, el efecto beneficioso sobre la incidencia de ACV fue reconfirmado. Finalmente, no encontramos una asociación entre el uso de colchicina y una menor mortalidad cardiovascular, aunque sí se observó una tendencia no significativa a favor del fármaco antiinflamatorio. El menor número de eventos reportados para este punto final primario en comparación con la incidencia de IAM (105 vs. 430) podría explicar la ausencia de significación estadística.
Este metaanálisis presenta varias limitaciones. En primer lugar, se observó heterogeneidad clínica (características de las poblaciones, diferentes dosis de colchicina, diferente seguimiento). Sin embargo, en el análisis de la variable principal, la heterogeneidad estadística fue baja y los resultados fueron robustos al realizar el análisis de sensibilidad. En segundo lugar, el análisis incluyó solo los datos globales de cada ensayo sin tener datos individuales. Tercero, nuestro análisis incluyó pocos estudios y el número de eventos fue pequeño en muchos de ellos. Por último, los datos del estado inflamatorio durante el seguimiento fueron escasamente reportados en los estudios evaluados. Consecuentemente, no pudimos evaluar si la asociación entre el uso de la colchicina y la menor incidencia de IAM se modificaría al considerar el nivel de los marcadores inflamatorios alcanzados con la terapia farmacológica.
CONCLUSIÓN
Nuestro análisis mostró que el uso de colchicina en pacientes con enfermedad cardiovascular aterosclerótica se asoció a una reducción significativa en la incidencia de IAM. Asimismo, en comparación con el grupo placebo, los eventos cerebrovasculares fueron significativamente menos frecuentes en el grupo de pacientes que utilizaron colchicina. Sin embargo, no encontramos una reducción significativa en la mortalidad cardiovascular con el uso de esta droga antiinflamatoria. La incorporación de la colchicina dentro del arsenal terapéutico de la enfermedad cardiovascular deberá ser discutida y considerada por las futuras guías de práctica clínica.



















