INTRODUCCIÓN
Aunque la infección por influenza humana generalmen te se limita al tracto respiratorio, se han descrito múltiples complicaciones cardíacas. 1 Las enfermedades cardiovasculares (ECV) y la influenza se han asociado durante mucho tiempo debido a una superposición en la incidencia máxima de cada enfermedad durante los meses de invierno. 2 Los estudios epidemiológicos observaron un aumento en las muertes cardiovascu lares (CV) durante las epidemias de Influenza, lo que indica que las complicaciones CV de la infección por influenza, incluida la exacerbación de la insuficiencia cardíaca (IC), la cardiopatía isquémica aguda y, con menos frecuencia, otras manifestaciones CV (accidente cerebrovascular, arritmias cardíacas, tromboembolismo venoso, o miocarditis), contribuyen de manera importante a la morbilidad y la mortalidad durante esta infección. 3
La relación entre enfermedad cardíaca e influenza es compleja: puede ocurrir por la vía inflamación-trombosis, efectos directos del virus sobre el miocardio, o por exacerbación de enfermedad CV existente. 4 En cuanto a los eventos vasculares, los mecanismos que se han postulado para explicar este aumento del riesgo incluyen la precipitación de la ruptura de la placa, la disfunción endotelial, la reactivación de otras infecciones latentes que conducen a la ruptura de la placa, el estímulo procoagulante, la taquicardia y la vasodilatación asociadas a la fiebre y los trastornos metabólicos relacionados con la infección, incluida la elevación de los niveles de triglicéridos y glucemia. 5,6
La vacunación contra la influenza (VI) es una estrategia bien establecida para reducir la enfermedad y la mortalidad relacionada con la Influenza en pacientes con ECV. 7,8 Con base en gran parte en estudios observacionales y ensayos clínicos aleatorizados, se ha encontrado que la vacunación está asociada con reducciones significativas de la mortalidad por todas las causas y eventos cardíacos adversos mayores. 9-12
Actualmente, la Organización Mundial de la Salud, el Centro para el Control y la Prevención de Enfer medades, la Asociación Estadounidense del Corazón/ Colegio Estadounidense de Cardiología y la Sociedad Europea de Cardiología recomiendan la vacunación anual contra la influenza para pacientes con ECV establecida. 13-15 En 2021, la Sociedad Interamericana de Cardiología publicó un consenso sobre VI y ECV, 16 donde se citaron el metaanálisis más reciente con cuatro ensayos clínicos aleatorizados que mostró que la VI se asoció con una reducción de los eventos cardiovasculares, 17 y otro metaanálisis basado en datos observacionales de los pacientes con IC, que tuvo hallazgos consistentes. 18
Debido a la reciente publicación de dos nuevos ensayos clínicos en los últimos dos años, decidimos realizar un metaanálisis actualizado de ensayos clínicos aleatorizados sobre el impacto de la VI en la mortalidad y los resultados CV en pacientes con ECV.
OBJETIVO
Nuestro objetivo primario fue realizar una revisión sistemática y un metaanálisis de ensayos clínicos aleatorizados para evaluar el efecto de la VI sobre la mortalidad en pacientes con enfermedad CV. Como objetivo secundario se evaluó el efecto de la VI sobre mortalidad CV, el infarto de miocardio y eventos adversos cardiovasculares mayores (MACE) entre los pacientes con IC y enfermedad de las arterias coronarias (EAC).
MATERIAL Y MÉTODOS
Nos adherimos a la declaración Preferred Reporting Items for Systematic Reviews and Meta- Analyses (PRISMA) al realizar e informar esta revisión sistemática. 19
Métodos de búsqueda para la identificación de estudios
Se realizaron búsquedas sistemáticas para identificar ar tículos utilizando MEDLINE (base de datos PubMed), la Biblioteca Cochrane y la Plataforma de Registro de Ensayos Clínicos Internacionales publicados hasta abril de 2022. Se usaron los términos: “influenza”, “vacuna contra la influenza”, “vacuna”, “infarto de miocardio”, “enfermedad de las arterias coronarias”, “síndrome coronario agudo”, “insuficiencia cardíaca” y “enfermedad cardíaca congestiva” como palabras clave o términos MeSH en el título o el resumen.
Realizamos búsquedas manuales en la lista de referencias de todas las publicaciones relevantes para asegurar la captura completa de los artículos relevantes, y también revisamos presentaciones recientes en congresos cardiovasculares internacionales.
Selección de estudios para inclusión
Dos revisores (LMB, EJZ) examinaron de forma independiente los títulos y resúmenes para identificar artículos potencialmente relevantes. Las discrepancias en el juicio se resolvieron después de la discusión. Los artículos de texto completo se incluyeron en esta revisión si cumplían con todos estos criterios de inclusión: (1) ensayos clínicos aleatorizados que compararon la vacunación contra la influenza con placebo o ninguna intervención cuando se informaron datos sobre uno de los resultados; (2) proporcionaron datos sobre la efectividad de la vacunación contra la influenza en pacientes con IC o EAC en comparación con un grupo de control no vacunado; (3) la vacunación contra la influenza se administró dentro del año posterior a la inscripción en el estudio; (4) publicación en idioma inglés o español.
Se excluyeron los artículos duplicados, los estudios que incluyeron pacientes con diferentes dosis de vacunación contra la influenza sin una rama sin vacunación, y todos los ensayos controlados no aleatorios.
Tipos de participantes
Se incluyeron participantes mayores de 18 años con ECV es tablecida: IC, o enfermedad de las arterias coronarias (EAC): angina estable o inestable e infarto de miocardio con y sin elevación del segmento ST.
Resultados de interés
El criterio de valoración principal fue la mortalidad por todas las causas, mientras que el criterio de valoración secundario fue la mortalidad CV, el infarto de miocardio y eventos ad versos cardiovasculares mayores (MACE) entre los pacientes con IC y EAC, vacunados y no vacunados.
Extracción y manejo de datos
Dos revisores realizaron la extracción de datos de forma independiente y todos los desacuerdos se resolvieron mediante discusión o arbitraje. Se extrajeron los siguientes datos sistemáticamente.
- Características del ensayo: diseño, duración, región, ámbito, año de publicación.
- Intervención: tipo y método de vacunación, intervención de control.
- Participantes: número de participantes, criterios de inclusión y exclusión, número total y número en los grupos de comparación, características basales (edad, sexo, factores de riesgo cardiovascular, medicación cardiovascular).
- Resultados: resultados primarios y secundarios según el ensayo, infarto de miocardio o reinfarto, angina inestable, muerte por causas cardiovasculares y resultados relacionados.
Las discrepancias en la extracción de datos se resolvieron mediante discusión con otro de los autores (ASL).
Análisis de subgrupos
Se realizó un análisis de subgrupos para comparar los efectos de la vacunación sobre la mortalidad en los pacientes con IC y EAC.
Evaluación de sesgos
Dos investigadores evaluaron de forma independiente el riesgo de sesgo. Se evaluó la evidencia de sesgo de los ensayos controlados aleatorios con la herramienta Cochrane de riesgo de sesgo, 20,21 con evaluación de los siguientes criterios: generación de secuencias aleatorias (adecuación del método), ocultamiento de la asignación, cegamiento de los participantes y el personal, manejo de datos de resultados incompletos, abandonos/pérdidas durante el seguimiento, análisis por intención de tratar, informe selectivo, similitud al inicio, cualquier otro sesgo observado.
Medidas del efecto del tratamiento
Todos los resultados de interés fueron resultados dicotómicos y se presentaron como cocientes de riesgos (RR) en el último seguimiento informado.
Evaluación de la heterogeneidad
La heterogeneidad entre los estudios se cuantificó con la métrica I2, que es independiente del número de estudios en un metaanálisis, y la estadística Chi2, con niveles de significación establecidos en el valor de p = 0,1. Un valor de I2 >50% se consideró como heterogeneidad significativa entre los estudios. 22
Síntesis de datos
Sobre la base de la prueba de heterogeneidad, el RR agrupado se calculó mediante el modelo de efectos fijos cuando no había heterogeneidad, mientras que se adoptó el modelo de efectos aleatorios cuando existía heterogeneidad.
Análisis estadístico
Todos los resultados de interés fueron resultados dicotómicos y se presentaron como cocientes de riesgos (RR) e interva los de confianza del 95% (IC95%) en el último seguimiento informado.
Todos los valores de p fueron de dos colas y p<0,05 se consideró estadísticamente significativo.
Se estimó el sesgo de publicación en caso de que encontráramos más de 10 estudios mediante la inspección visual del gráfico en embudo (funnel plot). Se utilizó la prueba de regresión de Egger para examinar la asimetría del gráfico en embudo. 23
El proceso de selección se realizó con el gerente de referencia Rayyan QCRI 24. Todos los datos de los estudios incluidos se extrajeron en Review Manager (RevMan 5.3).
RESULTADOS
Resultados de la búsqueda
Se identificaron 957 estudios a través de una búsqueda bibliográfica, entre los cuales se seleccionaron 527 y se excluyeron 486 después de una revisión inicial de títulos y resúmenes. Las 41 publicaciones restantes se revisaron en texto completo y se evaluaron según los criterios de inclusión. Finalmente, se seleccionaron 6 ensayos para el análisis cuantitativo. 25-30
El proceso de búsqueda y selección se representa en un diagrama de flujo PRISMA (Figura 1)
Características de los estudios incluidos
Se analizaron un total de seis ensayos clínicos, inclui dos 9316 pacientes. Cinco ensayos incluyeron pacientes con EAC (FLUVACS, FLUCAD, IVCAD, IAMI y Phrommintikul et al), y el ensayo IVVE pacientes con IC. El seguimiento medio fue de 16 ± 9,7 meses. En la Tabla 1 se resumen las características principales de los ensayos. En la Tabla 1 del material suplementario se encuentra la descripción de cada estudio incluido en el metaanálisis.
Riesgo de sesgo en los estudios incluidos
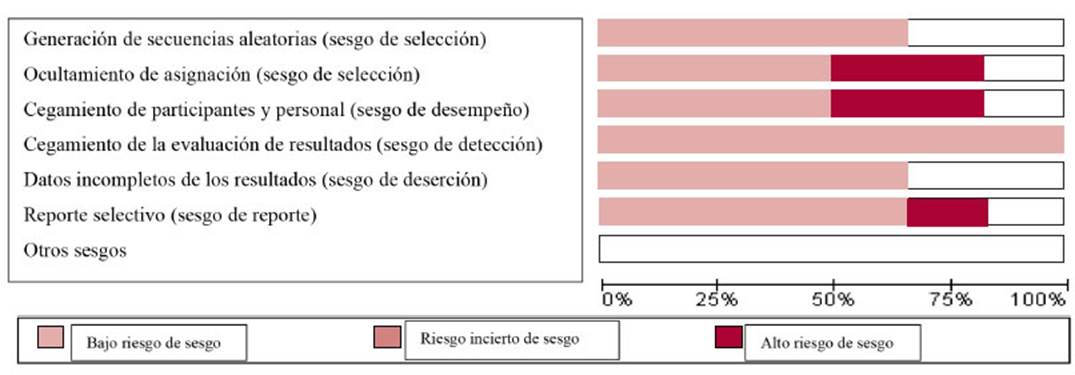
El riesgo general de sesgo de los estudios incluidos se muestra en la figura 1 del material suplementario, y el riesgo de sesgo de cada estudio incluido se muestra en la figura 2 del material suplementario.
Efectos de la vacuna contra la Influenza
Criterio de valoración principal: Mortalidad por todas las causas
La vacuna contra la influenza se asoció con una reducción de la mortalidad en comparación con el control: RR 0,67 (IC95% 0,47-0,95), p=0,03; I2=53 % (Figura 2).

Fig. 2 Forest plot del riesgo de mortalidad por todas las causas en pacientes con vacuna contra la influenza versus placebo
Criterio de valoración secundario: Mortalidad cardiovascular, infarto de miocardio y MACE
La VI se asoció con una reducción de la mortalidad cardiovascular en comparación con el control: RR 0,64 (IC95% 0,44-0,94), p = 0,02; I2 = 54% (Figura 3), así como también con la reducción de MACE: RR 0,69 (IC95% 0-53-0,90), p = 0,007; I2 = 68% (Figura 4). El uso de la vacuna antigripal se asoció con una reducción no estadísticamente significativa de infarto de miocardio en comparación con el control: RR 0,82 (IC95% 0,60-1,12), p = 0,57; I2 = 0% (Figura 5).

Fig. 3 Forest plot del riesgo de mortalidad cardiovascular en pacientes con vacuna contra la influenza frente a placebo
Análisis de subgrupos
Se realizó un subanálisis de la mortalidad global com parando la VI vs. control, estratificado por antecedente de EAC e IC. Este efecto no fue consistente entre las dos poblaciones de estudio: en IC, RR 0,91 (IC95% 0,80- 1,02; p = 0,1) y en EAC RR 0,56 (IC 95% 0,41-0,76; p = 0,0002), p para interacción = 0,004. (Figura 3 del material suplementario)
DISCUSIÓN
En este metaanálisis actualizado de ensayos clínicos controlados, que incluyó 9316 pacientes con EAC o IC, la VI se asoció con una reducción significativa de la mortalidad por todas las causas, la mortalidad cardio vascular y los MACE. En pacientes que recibieron la vacuna, se halló una reducción numérica en el infarto agudo de miocardio, no estadísticamente significativa.
La información acerca de la asociación entre Influenza y ECV es contundente, pero sus mecanismos se encuentran en estudio, siendo el modelo inflamación-trombosis el más reconocido. Otros factores, como la mayor demanda metabólica debido al aumento adrenérgico y la respuesta CV hiperdinámica, así como el compromiso potencial de la oxigenación debido a una infección pulmonar también parecen cumplir un rol importante. 31,32
Desde que el estudio pionero realizado en Argentina por Gurfinkel y colaboradores se publicó en 2004, 25 y luego se incorporó como principal y única evidencia en las normativas del CDC en Estados Unidos en 2009, 33 la VI se estableció -aunque gradualmente- como una estrategia de prevención de eventos CV.
La incertidumbre acerca de la validez externa, la reproducibilidad en diferentes regiones, climas, países de altos y bajos recursos, así como la seguridad del uso en contexto de un evento agudo o la eficacia en sujetos con IC, fueron algunos limitantes reconocidos del uso ampliado de la VI, que motivaron al desarrollo de los nuevos ensayos clínicos aquí evaluados.
Adicionalmente, a pesar que la recomendación de VI tiene larga data, su aceptación sigue siendo subóptima. De los pacientes con EAC en EE. UU. solo el 50% recibió la VI, con disparidades sustanciales según determinantes socioeconómicos. 34 Del mismo modo, un tercio de los hospitalizados por IC no recibió VI. 35
Comparamos los resultados de nuestro metaanálisis con los previamente publicados. Una revisión Cochrane de 2015 de los cuatro ensayos de prevención secundaria incluyó a 1682 pacientes con ECV y encontró una re ducción de mortalidad CV (RR 0,45; IC95% 0,26- 0,76), pero no así de IAM. 36 Más recientemente, en 2021, un metaanálisis de estos mismos cuatro ensayos aleatorizados, así como de 12 estudios observacionales, que incluyeron un total de más de 237 000 pacientes con ECV, encontró que la vacunación contra la influenza se asoció con reducciones significativas del riesgo de mortalidad por todas las causas, mortalidad CV, y MACE en una mediana de seguimiento de 20 meses. 17
Creemos que los principales hallazgos de este metaanálisis son que confirma que se mantiene el beneficio de reducción de mortalidad total y mortalidad cardiovascular al incluir nuevos ensayos clínicos aleatorizados que reunieron más de 7000 sujetos, así como una tendencia a la reducción del riesgo de infarto de miocardio. Se mantiene también el beneficio en reducción de eventos incluyendo en el metaanálisis dos poblaciones previamente no evaluadas: sujetos con un evento coronario reciente (IAMI), así como sujetos con insuficiencia cardíaca (IVVE).
En relación con el estudio IAMI, 29 la indicación de VI en sujetos con enfermedad coronaria se encontra ba avalada por diferentes ensayos clínicos y metaanálisis previos; sin embargo, los autores plantearon como estrategia la indicación durante una hospitalización por evento coronario agudo, demostrando la seguridad y eficacia de esta estrategia. La indicación desde la hospitalización es una estrategia reconocida para incrementar la adhesión a la vacunación, y en un estudio previo hemos evaluado que esta estrategia se asoció con mayor tasa de vacunación efectiva en comparación con la prescripción desde consultorios. 37 Por ello, una posible estrategia clave para aumentar la aceptación sería incluir la vacunación contra la Influenza como parte del checklist al alta del síndrome coronario agudo. El checklist garantiza la prescripción de farmacoterapias basadas en evidencia, 38 y agregar la vacuna es clave para normalizar la vacuna como parte de la terapia estándar de atención.
Nuestro metaanálisis evidenció una tendencia a la reducción del infarto de miocardio en los sujetos que recibieron VI. Los ensayos clínicos individuales incluidos presentaron en relación con este desenlace la misma dirección. Es posible que una de las limitaciones para confirmar definitivamente la asociación sea el número de sujetos evaluados en los ensayos clínicos.
Con respecto a la VI para sujetos con IC, uno de los principales limitantes en la generación de evidencia acerca de la utilidad de la VI fue la superposición con otras indicaciones formales, principalmente la edad: tres cuartas partes de los sujetos con IC tienen indicación de VI sólo por presentar más de 65 años, y en el otro extremo, sólo 3 a 6% de los sujetos con IC son menores de 50 años. 39 El estudio más recientemente presentado y que forma parte de este metaanálisis es el IVVE, 30 donde los investigadores incluyeron más de 5129 pacientes con IC, con características peculiares: la edad promedio era de 57 años, y los pacientes provenían de países de bajos y medianos recursos económicos de Asia y África. Los autores del estudio IVVE reportan que durante los picos de circulación de influenza se reportó reducción en los desenlaces como mortalidad total, cardiovascular, y MACE, mientras que al analizar en conjunto todo el tiempo de duración del estudio la reducción de eventos fue tendencial. Ello, opuesto a considerarse un resultado neutral, refuerza la asocia ción fisiopatológica y fortalece la indicación de la VI en esta población. Al incluir los resultados globales de este estudio en nuestro metaanálisis, los beneficios en reducción de eventos mantuvieron la misma dirección y magnitud de efecto.
Las características mencionadas en el párrafo an terior podrían explicar las diferencias que hallamos en el análisis estratificado de subgrupos de acuerdo con la enfermedad CV de base. Sin embargo, mediante este metaanálisis no podemos discernir cuántos de los sujetos reclutados por EAC tenían IC concomitante y viceversa, o si el beneficio es mayor o no en los sujetos que tienen ambas condiciones clínicas.
Para tomar conciencia de la magnitud de los hallazgos sobre la efectividad de la VI en la reducción de eventos en pacientes con ECV, se pueden comparar los resultados con los de tratamientos farmacológicos clásicos como las estatinas, betabloqueantes e inhibidores de la enzima convertidora de angiotensina (IECA). 40 Cada uno de ellos, en los metaanálisis de los ensayos capitales, disminuyó la mortalidad cardiovascular: la RR fue de 24% en el caso de las estatinas, 41 de 23% con betabloqueantes, 42, y de un 16% con los IECA. 43 En forma similar, la cesación tabáquica reduce 39% el riesgo de ECV. 44
Las fortalezas de esta revisión incluyen una extensa investigación bibliográfica sistemática y la inclusión exclusiva de ensayos clínicos aleatorizados con bajo riesgo de sesgo. Se encontró heterogeneidad baja en los resultados primarios y secundarios analizados, probablemente debido al diseño similar del ensayo, la población incluida y la definición de los resultados.
Sin embargo, esta revisión tiene limitaciones. No fue posible evaluar el sesgo de publicación debido al bajo número de estudios incluidos en el metaanálisis. La pandemia COVID-19 tuvo un impacto en el reclutamiento, seguimiento y en la circulación de influenza, que afectó a los dos últimos y grandes ensayos clínicos aleatorizados; sin embargo, el beneficio en reducción de los eventos principales se sostuvo. El número de ensayos clínicos incluidos es escaso, y existe gran variabilidad en el número de sujetos incluidos, así como en sus características basales; a pesar de ello la reducción de eventos tuvo la misma dirección, aunque con relevante diferencia en la magnitud del efecto. Finalmente, los datos del estudio IVVE no fueron publicados aún en una revista indizada al momento del cierre de este análisis, y provienen de la presentación en un congreso científico, por lo que potencialmente podría haber una modificación en sus resultados o interpretación diferente a la que hemos utilizado para este análisis.
CONCLUSIÓN
En este metaanálisis de seis ensayos controlados alea torizados, la vacunación contra la influenza se asoció con una reducción del riesgo relativo del 33% y del 36% en la mortalidad por todas las causas y cardiovascular, respectivamente en pacientes con ECV.
En las últimas décadas se ha acumulado evidencia a favor de los efectos cardioprotectores de la vacuna contra la influenza en pacientes con enfermedad cardiovascular establecida.
Intentamos promover un consenso, a partir del mayor nivel de evidencia, con respecto a los beneficios persistentes de la vacuna contra la influenza en pacientes con ECV, con la inclusión de dos nuevos ensayos clínicos en EAC e IC, donde se confirma la asociación de la vacunación con la reducción de riesgo en sujetos con ECV. El presente metaanálisis puede ayudar a los profesionales de la salud a recomendar firmemente la vacunación contra la influenza para la prevención secundaria de los eventos cardiovasculares.