Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Boletín de la Sociedad Argentina de Botánica
On-line version ISSN 1851-2372
Bol. Soc. Argent. Bot. vol.47 no.1-2 Córdoba Jan./June 2012
PALEOBOTÁNICA Y PALINOLOGÍA
El origen y diversificación del crecimiento cambial atípico en plantas fósiles: procesos del desarrollo involucrado
Josefina Bodnar1,2 y Eliana Paula Coturel1,3
1 CONICET
2 División Paleobotánica, Museo de La Plata, Facultad de Ciencias Naturales y Museo, Universidad Nacional de La Plata, Paseo del Bosque s/n, B1900FWA, La Plata, Argentina. jbodnar@fcnym.unlp.edu.ar
3 Sección Paleopalinología, Museo Argentino de Ciencias Naturales "Bernardino Rivadavia", Ángel Gallardo 470, C1405DJR, Buenos Aires, Argentina. elianacoturel@gmail.com
Resumen: En el registro fósil encontramos una serie de morfologías, cuyo origen sólo puede ser inferido a partir de los estudios ontogenéticos. De este modo, la comprensión de los procesos del desarrollo en plantas y el patrón resultante es de suma importancia en Paleobotánica. En este trabajo, se presenta la relación que existe entre los procesos del desarrollo y los diversos patrones observados en el crecimiento secundario de las plantas fósiles. Se estudiaron superficies pulidas, peels y cortes petrográficos de troncos silicificados correspondientes a Lycopsida, Sphenopsida, Medullosales, Corystospermales y Cycadales. Se identificaron una variedad de patrones cambiales, que pueden ser reunidos en dos grupos principales: patrón en espiral y variantes cambiales (e.g. unifacialidad, fragmentación radial y tangencial de elementos vasculares, polixilia, orientación inversa y sistema vascular medular). La aparición del patrón en espiral estuvo relacionada con el origen del clado de las Lygnophyta. Las variantes cambiales caracterizan grupos particulares, y han experimentado una diversificación evolutiva muy importante, vinculada con eventos del desarrollo.
Palabras clave: Evo-devo; Paleobotánica; Cámbium; Tejidos vasculares secundarios.
Summary: Origin and diversification of atypical cambial growth in fossil plants: developmental processes involved. We found a series of morphologies in the fossil record whose origin can only be inferred by means of ontogenetic studies. Therefore, comprehension of plant developmental processes and their resultant patterns are extremely important in Paleobotany. In this contribution, we exposed the relation between developmental processes and the different patterns observed in fossil plant secondary growth. Polished surfaces, peels and thin slides of silicified trunks belonging to Lycopsida, Sphenopsida, Medullosales, Corystospermales and Cycadales, were studied. We identified a diversity of cambial patterns which can be clustered in two main groups: whirling pattern and cambial variants (e.g. unifacial, radial and tangential fragmentation of vascular elements, polyxyly, inverse orientation and medullary system). The appearance of whirling pattern was related to the origin of the Lygnophyta clade. The cambial variants characterize specific groups and have undergone a significant evolutionary diversification linked with developmental events.
Key words: Evo-devo; Paleobotany; Cambium; Secondary vascular tissues.
INTRODUCCIÓN
La comprensión de los procesos fisiológicos y el patrón que generan en los diferentes estadios ontogenéticos de las plantas es de suma importancia para la Paleobotánica, dado que en el registro fósil encontramos preservada una serie de morfologías y sólo a partir de los estudios actuales podemos inferir su origen. La importancia de este conocimiento radica en que estas mismas estructuras son utilizadas posteriormente para inferir la evolución de cada linaje: una mala interpretación de los caracteres que se observan provocaría, por ejemplo, errores en la elección y/o uso de datos para análisis filogenéticos.
Desde hace varias décadas ha cobrado impulso el estudio de las hormonas que regulan el crecimiento de los tejidos meristemáticos presentes en las plantas vasculares. Entre ellas, se sabe que las auxinas son clave para el desarrollo del cámbium y sus tejidos derivados. Estas fitohormonas poseen un transporte polar desde las hojas hasta los tallos, y cualquier disrupción en éste provoca un patrón característico en la estructura del leño. Más específicamente, la presencia de una rama o nudo causa una disrupción del flujo de auxinas, y genera un patrón en espiral característico. En este patrón el conjunto de traqueidas, elementos de vaso y radios leñosos se curva formando un remolino. Esta morfología ha sido reconocida en leños devónicos pertenecientes a los ancestros de las lignofitas (Rothwell & Lev-Yadun, 2005).
La verificación de la presencia de estos patrones es fundamental para poder establecer homologías en los procesos ontogenéticos entre las plantas actuales y fósiles: en el caso de este trabajo, en el desarrollo del cámbium vascular. Una vez establecidas estas homologías afirmamos nuestra base para estudiar cómo las alteraciones de los procesos ontogenéticos intervienen en la evolución biológica, modificando el marco de un estudio fisio-histológico a otro dentro de lo que se denomina Biología Evolutiva- del Desarrollo (Evo-Devo) (Bateman y DiMichele, 2002). Otro paso fundamental hacia la comprensión de la evolución de las plantas es una estimación detallada de su filogenia. El conocimiento de las relaciones filogenéticas es necesario para evaluar las hipótesis evo-devo, puesto que la decisión entre escenarios evolutivos opuestos depende de la ontogenia asumida como basal (Olson, 2007).
Un cambio evo-devo es "cualquier alteración genética expresada fenotípicamente que se produce en el ancestro, y que modifica profundamente la forma y/o el tamaño de cualquier estadio ontogenético en el descendiente" (Bateman, 1994). Estos cambios incluyen a la heterocronía (cambio en la tasa relativa o el ritmo del desarrollo) y la heterotopía (cambio en el patrón espacial de los procesos del desarrollo) (ambos términos, Haeckel, 1866). Existe una extensa bibliografía sobre la Biología Evo-Devo (Bodnar, en prensa) que se encuentra principalmente en idioma inglés.
La presencia de crecimiento secundario por medio del cámbium vascular caracteriza a Lygnophyta, Isoetales y Sphenopsida. Se acepta que el crecimiento secundario típico es aquel generado por un cámbium bifacial, único, centrífugo y uniforme. Los casos que se apartan de este modelo son considerados patrones atípicos. Dentro de estos últimos se reconocen a la unifacialidad, fragmentación radial y tangencial de elementos vasculares, polixilia, tejidos vasculares centrípetos y sistema vascular medular.
En este trabajo se da a conocer el hallazgo del patrón en espiral en el leño fósil de Protojuniperoxylon ischigualastense Bonetti 1966 emend. Bodnar et Artabe 2007 (Coniferales), proveniente de la Formación Ischigualasto (Triásico Superior), en la Hoyada de Ischigualasto, provincia de San Juan. A su vez, se presenta y ajusta la terminología en castellano para los estudios evo- devo. Finalmente, se realiza una interpretación sobre el origen y diversificación de los patrones atípicos o variantes del cámbium vascular.
MATERIAL Y MÉTODO
Los materiales estudiados corresponden a troncos silicificados de diferentes procedencias geográficas y estratigráficas. El número de colección y el sitio donde se encuentran depositados están detallados en la Tabla 1. Para este análisis se examinaron, en total, 40 ejemplares.
Tabla 1. Material estudiado.

Referencias: Colecciones: (1) División Científica de Paleobotánica, Museo de La Plata, UNLP; (2) Colección didáctica, Cátedra de Paleobotánica UNLP; (3) Colección Paleobotánica de la Facultad de Ciencias Exactas y Naturales y Agrimensura, UNNE; (4) Colección Nacional de Paleobotánica, Museo Argentino de Ciencias Naturales"Bernardino Rivadavia"; (5) Colección de Paleobotánica del Museo de Ciencias Naturales de San Juan.
Se estudiaron superficies pulidas, peels y cortes petrográficos, de los tres planos de corte utilizados en histología (transversal, longitudinal radial y longitudinal tangencial). Las superficies pulidas fueron observadas bajo lupa binocular Nikon, modelo SM6 y fotografiadas con cámaras digitales Canon Powershot S40 y Olympus FE-150. Las ilustraciones fueron efectuadas bajo cámara clara y mediante papel transparente sobre las fotografías. Los peels y cortes petrográficos fueron estudiados bajo lupa binocular Nikon, modelo SM6, con microscopios ópticos Leitz Wetzlar Ortholux y Microscopio Nikon Eclipse 50i, y fotografiados con sistema Leica DC 150 y cámaras digitales Canon Powershot S40 y Nikon DS-Fi1.
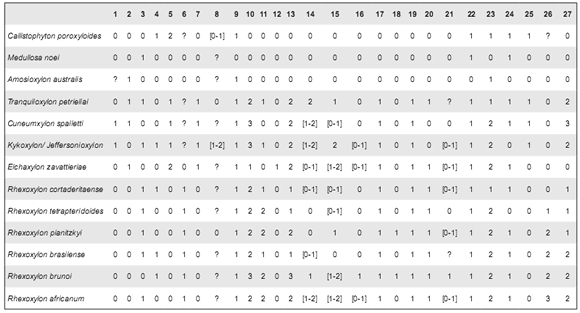
Para estudiar la evolución de los patrones cambiales en un marco filogenético, se realizó un análisis de las relaciones filogenéticas de las plantas vasculares, sobre la base de hipótesis previas (Kenrick & Crane, 1997; Nixon et al., 1994; Rothwell & Nixon, 2006; Hilton & Bateman, 2006). Las matrices utilizadas en dichos trabajos fueron reevaluadas y modificadas para elaborar una matriz de 51 taxones y 182 caracteres (Tablas 2 y 3), que fue analizada con TNT 1.1 (Goloboff et al., 2008) bajo el algoritmo de Wagner, aplicando TBR (100 réplicas, 10 árboles salvados por réplica) y calculando un árbol de consenso estricto. Además, se elaboró una hipótesis filogenética sobre las relaciones entre algunos integrantes de las Corystospermaceae, a partir de una matriz de 13 taxones y 27 caracteres (Tabla 4), la que fue analizada con TNT 1.1, bajo enumeración implícita.
Tabla 2. Lista de caracteres utilizados para el análisis filogenético de las plantas vasculares. Tomados y modificados de Stevenson (1990), Kenrick & Crane (1997), Hilton & Bateman (2006) y Rothwell & Nixon (2006).




Tabla 3. Matriz de datos utilizada en el análisis filogenético de las plantas vasculares.
Tabla 4. Lista de caracteres utilizados para el análisis filogenético de los taxones de troncos de Corystospermaceae.

RESULTADOS
Descripción de los ejemplares revisados
Se presenta la descripción de los siguientes tipos de crecimiento secundario: patrón en espiral, bifacialidad, unifacialidad, fragmentación radial y tangencial de elementos vasculares, polixilia, tejidos vasculares centrípetos y sistema vascular medular (ver Cuadro 1). Estos fueron observados en los ejemplares mencionados en la Tabla 1. En el caso de Eligodendron branisae Archangelsky et de la Sota 1966, se confirma la ausencia de tejido vascular secundario.
Cuadro 1. Clasificación de los patrones cambiales atípicos de acuerdo a este trabajo.

Patrón en espiral
El patrón en espiral ha sido reconocido en los ejemplares del leño de Protojuniperoxylon ischigualastense Bonetti 1966 emend. Bodnar et Artabe 2007 (LPPBpm 368). En vista longitudinal tangencial, se observó que una traza de 3,84 mm de alto y 1,08 mm de ancho máximo, y de contorno romboidal (Fig. 1.A). En su mayor parte está constituida por células parenquimáticas. Se pueden reconocer en la traza tres zonas: una externa, una media y una interna (Fig. 1.A). La zona externa es la que está inmediatamente a continuación del leño caulinar, y está formada por traqueidas axiales y radios de contorno sinuoso (Fig. 1.B, 1.C). Muchos radios se bifurcan o fusionan (Fig. 1.B). Entre las traqueidas, hay dos tipos: traqueidas cortas (de 0,19 a 0,33 mm de longitud) y traqueidas largas (cuya longitud no pudo medirse). Las traqueidas muestran un recorrido sinuoso, en algunos casos las traqueidas cortas se pliegan sobre los radios (Fig. 1.B, 1.C). En otros casos las traqueidas largas muestran una disminución abrupta de su diámetro radial (Fig. 1.B). En la zona media de la traza no se diferencian radios y traqueidas axiales, sino que todas las células están dispuestas de manera radial (Fig. 1.D, 1.E, 1.F). Entre estas células, la gran mayoría son células parenquimáticas radiales de diversos diámetros. Algunas son isodiamétricas y otras son rectangulares y comprimidas. En muchos casos, éstas presentan su pared primaria desprendida (Fig. 1.G). Las traqueidas radiales están presentes de manera escasa y aislada (Fig. 1.D, 1.E, 1.F). Se pueden reconocer por sus paredes gruesas y las punteaduras areoladas en sus paredes terminales (Fig. 1.D, 1.E, 1.F). La zona interna presenta casi exclusivamente células parenquimáticas radiales pequeñas, isodiamétricas y algunas con contenidos oscuros probablemente resinosos (Fig. 1.H).

Fig. 1. Protojuniperoxylon ischigualastenese. (Corte Tangencial). A: Vista general de la traza, mostrando la zona externa (E), media (M) e interna (I). Escala: 1 mm. B: Radios bifurcados (R), una traqueida girante (G) y traqueidas de lumen reducido (T). Escala: 200 μm. C: Torsión de una traqueida. El recuadro señala las punteaduras radiales que como consecuencia de la torsión se pueden observar en el plano tangencial. Escala: 150 μm. D: Traqueidas radiales de la zona media de la traza, se observan las punteaduras de las paredes terminales de las traqueidas. Escala: 60 μm. E: Traqueidas radiales de la zona media (recuadro) y traqueida girante de la zona externa, con detalle de las punteaduras de la pared radial (P). Escala: 120 μm. F: Traqueidas radiales de la zona media, mostrando las punteaduras de las paredes terminales. Escala: 100μm. G: Traqueida girante, y desprendimiento de la pared primaria de una célula parenquimática de la zona media. Escala: 100 μm. H: Detalle de la zona interna de la traza. Escala: 200 μm.
Bifacialidad
Se ha podido estudiar este carácter en dos representantes del grupo de las Sphenopsida: Sphenophyllum sp. (Familia Sphenophyllaceae, Orden Sphenophyllales) y Nododendron suberosum Artabe et Zamuner 1991 (Familia Apocalamitaceae, Orden Equisetales).
Sphenophyllum presenta una estela protostélica, un xilema secundario de gran desarrollo que se diferencia en dos tipos (uno cuyas traqueidas son de mayor calibre y otro cuyas traqueidas son de menor calibre) y un floema secundario de poco espesor, cuyo detalle celular no se ha podido observar en los materiales analizados (Fig. 2.A). Al parecer estaría conformado por fibras floemáticas que han colapsado durante la diágenesis (Fig. 2.B).

Fig. 2. Sphenophyllum sp. (Corte Transversal). A: Vista general del tallo. Escala: 500 μm. B: Detalle de A, la flecha señala la capa de floema secundario entre el xilema secundario y la corteza. Escala: 250 μm. Nododendron suberosum (Impresión-Compresión del diafragma nodal). C: Vista del cilindro vascular secundario. Escala: 5 mm. D: Detalle de C, mostrando la presencia de floema secundario (F, capa más oscura) y xilema secundario (X). Escala: 2,5 mm. Lepidodendron sp. (Corte Transversal). E: Vista del cilindro vascular. Escala: 500 μm. F: Detalle de E, el recuadro indica la zona de tejido interpretado como parénquima secundario. Escala: 250 μm. G: Detalle de E, mostrando la presencia de parénquima de origen cortical en la posición que debería ocupar el floema secundario entre xilema y corteza. Escala: 125 μm. Arthropitys comunnis (Corte Transversal). H: Cilindro vascular secundario. Escala: 1 mm. I: Detalle de H, mostrando la ausencia de floema secundario entre xilema y corteza. Escala: 250 μm.
Nododendron suberosum Artabe et Zamuner 1991, tiene un desarrollo uniforme de xilema y floema secundarios, cómo se puede observar en la Fig. 2.C y 2.D.
Unifacialidad
Esta rasgo fue reconocido en los ejemplares de Lepidodendron sp., Lepidophloios sp. y Stigmaria ficoides (Sternberg) Brongniart 1822 (Familia Lepidodendraceae, Orden Lepidodendrales, Clase Lycopsida), y Arthropitys comunis (Binney) Renault 1876 (Familia Calamitaceae, Orden Equisetales, Clase Sphenopsida).
Los ejemplares observados de Lepidodendron sp. (Fig. 2.E) presentan una estela sifonostélica, con médula mixta, y un xilema secundario de escaso desarrollo (hileras de hasta 12 traqueidas de espesor). Cada 1, 2 o 3 hileras se observa el desarrollo de un radio parenquimático (Fig. 2.F). En posición externa al xilema aparece un tejido mal preservado, con células de sección transversal redondeada y de paredes gruesas (Fig. 2.F). Este tipo de tejido ha sido considerado parénquima secundario derivado de actividad meristemática cortical (Lemoigne, 1966; Eggert & Kanemoto, 1977). Las células de esta zona son isodiamétricas y no presentan ninguna evidencia de haber sido generadas por un cámbium (Eggert & Kanemoto, 1977), por lo que se verifica la ausencia total de foema secundario
En Lepidophloios sp., se advierte un mayor desarrollo del xilema secundario respecto de Lepidodendron sp. En la posición más externa el xilema es de menor calibre y pueden encontrarse anillos colapsados de traqueidas. En posición externa al xilema se ha preservado un tejido que posee células de pared contorneada, de lumen más pequeño que aquel de las traqueidas del xilema secundario (Fig. 2.G). Estas células se disponen en radios irregulares. Tampoco en este caso se reconocen células típicas del floema secundario.
Stigmaria ficoides posee un xilema secundario bien desarrollado, pero no se observa la porción extraxilemática.
En el caso de Arthropitys comunis, el xilema secundario se halla bien fragmentado radialmente por la presencia de amplios parenquimáticos. Nuevamente, no se observa un tejido diferenciado asignable al floema secundario (Fig. 2.H, 2.I).
Fragmentación radial de elementos vasculares
Los ejes de Arthropitys (Equisetales), Medullosa (Medullosales), y Rhexoxylon, Tranquiloxylon y Cuneumxylon (Corystospermales) tienen un cilindro vascular secundario disecto radialmente.
El xilema secundario en Arthropitys comunis está segmentado en sectores separados por radios parenquimáticos secundarios de espesor importante. Estos radios están constituidos exclusivamente por células parenquimáticas (Fig. 3.A).

Fig. 3. Arthropitys comunnis (Corte Transversal). A: Detalle del cilindro vascular secundario, fragmentado por radios parenquimáticos. Escala: 500 μm. Medullosa noei (Corte Transversal). B: Vista de un segmento vascular secundario, consituido por xilema centrífugo (F) y centrípeto (C). Escala: 5 mm. Rhexoxylon cortaderitaense (Superfcie transversal pulida). C: Vista general del tallo, donde se observan la fragmentación del cilindro vascular por la presencia de radios parenquimatosos. Escala: 2 cm. E: Detalle de la región medular del tallo, mostrando la médula (M), los tejidos vasculares secundarios centrípetos (C), parénquima de dilatación (D) y tejidos vasculares centrífugos (F). Escala: 1 cm. R. pianitzkyi (Corte Radial). D: Detalle de las células que componen los radios parenquimatosos: nidos escleróticos (N) y cavidades secretoras (S) . Escala: 250 μm. R. cortaderitaense (Corte Radial). F: Vista del parénquima de dilatación (D) que separa el xilema centrípeto (C) del centrífugo (F). También se observa la médula (M). Escala: 1 mm.
Los tallos de Medullosa noei Steidtmann 1937, presentan varios segmentos vasculares, cada uno de ellos formado por un simpodio de xilema primario con dos polos protoxilemáticos, rodeado de xilema y floema secundarios (Fig. 3.B). Estos segmentos vasculares se encuentran inmersos en tejido parenquimatoso que se continúa entre la médula y la corteza.
Los troncos de Rhexoxylon cortaderitaense (Menéndez) Bodnar 2008, R. pianitzkyi Archangelsky et Brett 1961 emend. Brett 1968, R. brasiliense Herbst et Lutz 1988, R. brunoi Artabe, Brea et Zamuner 1999, Tranquiloxylon petriellai Herbst et Lutz 1995 y Cuneumxylon spalletti Artabe et Brea 2003 muestran el cilindro vascular secundario fragmentado en cuñas por radios parenquimatosos de 0,2 a 2,5 cm de ancho en las especies del género Rhexoxylon, y de 0,003 a 0,36 cm de ancho en los otros dos géneros. Probablemente esta diferencia se deba a que en Rhexoxylon, al menos, los radios parenquimatosos crecen en espesor independientemente de la circunferencia del eje (Fig. 3.C).
Los radios parenquimatosos son radios secundarios constituidos por células parenquimáticas isodiamétricas, idioblastos y nidos escleróticos (=grupos de esclereidas) (Fig. 3.D).
Fragmentación tangencial de elementos vasculares
En Rhexoxylon, los tejidos vasculares centrípetos (ver más adelante) están separados de los centrífugos por un tejido parenquimatoso que ha recibido la denominación de parénquima de dilatación (Fig. 3.E, 3.F). Está constituido por células semejantes a las de los radios parenquimatosos (células parenquimáticas, nidos escleróticos e idioblastos).
Polixilia
El cilindro vascular secundario de Rhexoxylon, Tranquiloxylon y Cuneumxylon (Corystospermales), y Neochamberlainia (Cycadales) muestra más de un ciclo de xilema y floema. Estos ciclos de xilema y floema secundarios pueden formar anillos o estar interrumpidos y conformar arcos aislados discordantes o concordantes.
Rhexoxylon cortaderitaense, R. pianitzkyi, R. brasilense y R. brunoi presentan en sus cuñas de tejidos vasculares secundarios ciclos adicionales de floema aislados de manera poco frecuente (Fig. 4.C). En Tranquiloxylon petriellai estos ciclos son también interrumpidos lateralmente pero mucho más frecuentes (Fig. 4.B). Por otro lado, en Cuneumxylon spalletti hay al menos tres ciclos sucesivos de floema y xilema secundarios que conforman verdaderos anillos concéntricos.

Fig. 4. Neochamberlainia pteridospermoidea (Superfcie transversal pulida). A: Cilindro vascular secundario, formado por tres ciclos de xilema y floema. Escala: 1 cm. D: Detalle del xilema secundario centrípeto. Escala: 2 mm Tranquiloxylon petriellai (Superfcie transversal pulida). B: Vista general del cilindro vascular secundario, fragmentado por radios parenquimatosos (P), donde se observan arcos discontinuos de floema incluido (F). Escala: 2 cm. Rhexoxylon brasilense (Superfcie transversal pulida). C: Detalle de una cuña de tejido vascular secundario, mostrando varios ciclos consecutivos de xilema y floema (F), y la fragmentación por radios parenquimatosos (P). Escala: 4 cm. F: Sistema vascular medular. Escala: 2 cm. E: Detalle de F. Escala: 2 cm.
Neochamberlainia pteridospermoidea (Artabe, Zamuner et Stevenson) Artabe, Zamuner et Stevenson 2010, por otra parte, presenta tres bandas concéntricas de floema y xilema secundarios, entre cada una de las cuales hay una zona parenquimática (Fig. 4.A). En este caso, estos anillos de tejidos vasculares son continuos, a diferencia de los presentes en Cuneumxylon spalletti que tienen una interrupción por la presencia de radios parenquimatosos.
Tejidos vasculares centrípetos
Los troncos de Medullosa (Medullosales), Rhexoxylon (Corystospermales) y Neochamberlainia (Cycadales) además de los tejidos vasculares secundarios centrífugos, presentan tejidos vasculares secundarios centrípetos que han crecido hacia la médula. Esta característica también ha sido llamada polixilia centrípeta (Artabe et al., 2005).
En Medullosa noei el xilema secundario rodea completamente cada segmento de xilema primario, desarrollando una porción centrífuga y una porción centrípeta (Fig. 3.B). El cilindro vascular secundario en las especies analizadas de Rhexoxylon presenta un sector centrífugo de mucho mayor desarrollo y un sector centrípeto mucho más reducido, pero que no rodean completamente a los simpodios de xilema primario, dejando libre la región lateral de los polos de protoxilema (Fig. 3.E).
En Neochamberlainia el xilema centrípeto se encuentra en arcos aislados y de poco espesor (Fig. 4.D).
Sistema vascular medular
También en Rhexoxylon se puede observar la presencia de dos sistemas vasculares secundarios independientes: el sistema vascular cilíndrico, conformado por grandes cuñas de xilema y floema centrífugos, y el sistema vascular medular, constituido por haces perimedulares dobles, cada uno con una porción centrípeta y una porción centrífuga (Fig. 4.E, 4.F).
Procesos ontogenéticos. Clasificación de los patrones cambiales
Los patrones cambiales estudiados pueden ser reunidos en dos grupos principales: variaciones anatómicas locales, las que aparecen en zonas localizadas del tallo y se detectan en el leño a nivel celular; y por otro lado, las variantes cambiales, observándose a lo largo de gran parte de los ejes, se detectan a nivel orgánico cambiando la anatomía general del tronco y caracterizan a grupos taxonómicos particulares (Cuadro 1).
Variaciones anatómicas locales del cámbium
Dentro de este grupo se incluye al patrón en espiral presente en las trazas rameales de géneros actuales y fósiles, pudiéndose determinar los cambios morfológicos que ocurren en las células del xilema secundario.
El patrón en espiral comprende cambios continuos en el arreglo de las traqueidas en capas sucesivas del leño, lo que indica que cambios análogos han ocurrido en el cámbium. Las variaciones en la orientación celular en las áreas espiraladas ocurren con una gran rapidez, por esta razón es difícil establecer patrones dominantes (Larson, 1994). Los trabajos de Sachs & Cohen (1982), Sachs (1984), Hejnowicz & Kurczynska (1987), Lev-Yadun & Aloni (1990), Kurczynska & Hejnowicz (1991) y Larson (1994) sugieren que el patrón en espiral se desarrolla en las zonas de bifurcación de dos o más ramas, en zonas de ramificación y en regiones donde se perturbe el desarrollo normal del cámbium (heridas).
Se sabe que la diferenciación vascular estaría regulada por el flujo polar de las auxinas, que transcurre desde las hojas o desde una fuente localizada hacia las raíces. En el desarrollo del patrón en espiral, el bloqueo del transporte polar de las auxinas causaría divergencia y hasta una total inversión de la polaridad de las señales, alterando la diferenciación de los vasos (Larson, 1994) (Fig. 5).

Fig. 5. Esquema mostrando la dirección del flujo de las auxinas en el interior de una planta.
Las traqueidas y vasos que se desarrollan en una zona alterada se presentan en disposición circular ("vasos circulares"); y suelen ser cortos, lo cual indicaría una mayor frecuencia de divisiones anticlinales en la región específica del cámbium en la que se originan. La disposición circular se explica por el recorrido circular del flujo que promueve la diferenciación de estos vasos. El patrón en espiral se incrementa continuamente con el aumento de la circunferencia del tallo. Los estudios realizados sobre leños tumorosos han conducido a la conclusión de que el mecanismo productor de este patrón sería resultado del crecimiento intrusivo propio de las traqueidas. Las células aparecen reorientadas respecto de la condición normal, sea en un patrón espiral o bifurcado. Las bifurcaciones se generan en los ápices de las iniciales fusiformes cuando el crecimiento de la célula resulta obstaculizado por el extremo de otra célula o radio. Si ocurren en las paredes radiales, elápice de crecimiento se introduce entre las paredes radiales de células pertenecientes a dos grupos adyacentes. Si, en cambio, ocurre en el lateral, el extremo de crecimiento se introduce entre las paredes tangenciales de otras células, creando espirales localizados. Las células del medio de la región espiralada son severamente distorsionadas con algunos extremos celulares que se curvan 180º (Larson, 1994).
El patrón en espiral observado y descripto en el leño Protojuniperoxylon ischigualastense correspondería a la salida de una rama.
Variantes del cámbium
Estas variaciones se registran en linajes particulares. Se observaron cinco tipos de variantes cambiales: 1-unifacial, 2-actividad diferencial, 3- actividad remanente, 4- cámbiumes sucesivos y 5-orientación inversa, que producen los patrones de unifacialidad, fragmentación radial y tangencial de los elementos vasculares, polixilia y tejidos vasculares centrípetos, respectivamente. La combinación de la actividad remanente, los cámbiumes sucesivos y la orientación inversa tiene como resultado el desarrollo de un sistema vascular medular. En el Cuadro 2 se aclara qué tipo de variante se encuentra en cada grupo taxonómico estudiado.
Para comprender el origen y la evolución de estos tipos de desarrollo cambial, tenemos que discernir los procesos ontogenéticos implicados en cada uno de ellos. En este trabajo, el crecimiento secundario típico es referido como bifacial. Éste abarca las siguientes etapas (Fig. 6):
Cuadro 2. Distribución de las variantes cambiales en diferentes grupos taxonómicos.


Fig. 6. Diagrama mostrando la actividad típica del cambium bifacial en una protostela (arriba) y en una eustela (abajo). Ver el texto para la explicación.
A partir del procámbium localizado entre los polos protoxilemáticos de una protostela (Fig. 6.A, arriba) y dentro de los haces vasculares de una eustela (Fig. 6.A, abajo), se desarrollan el cámbium s.s. de las protostelas y el cámbium fascicular de las eustelas.
Se diferencia un pericámbium en los polos de una protostela (Fig. 6.B, arriba) y un cámbium interfascicular entre los haces vasculares primarios de una eustela (Fig. 6.B, abajo). El primero deriva de las células del periciclo, mientras que el segundo deriva de las células parenquimáticas ubicadas entre los fascículos vasculares. En las espermatofitas, se considera que el cámbium recién está completamente formado luego de que el parénquima interfascicular se diferencia en células fusiformes (Larson, 1994).
Se forma así un anillo cambial completo, que genera xilema secundario hacia el centro del eje y floema secundario hacia la periferia.
La totalidad de los tejidos vasculares secundarios va creciendo hacia la corteza, es decir, en sentido centrífugo (Fig. 6.C, arriba y abajo).
Un sistema experimental novedoso fue empleado por Ko et al. (2004) para estudiar la regulación molecular de la formación del xilema secundario en Arabidopsis; provocando que en el eje de la inflorescencia se diferencie un cámbium mediante la inducción por peso. Esto es una evidencia de que los genes que regulan el crecimiento secundario no son exclusivos de las especies arbóreas sino que están presentes también en las herbáceas, las que tendrían el potencial de desarrollar crecimiento secundario de acuerdo a las circunstancias (Groover, 2005).
Si bien el cámbium bifacial caracteriza el clado de las Lygnophyta, se ha reconocido en representantes de las Sphenophyta, específicamente en la familia Sphenophyllaceae (Sphenophyllales) y en la familia Apocalamitaceae (Equisetales). El primer caso es de formas lianescentes o trepadoras, pero siempre con un hábito muy delicado. El segundo caso, está constituido por formas arbustivas a arbóreas. Las esfenofitas con crecimiento secundario se extinguieron en el Mesozoico. Actualmente, sólo sobreviven las esfenofitas herbáceas. Es aceptado que el cámbium bifacial de las Sphenophyllaceae y Apocalamitaceae se desarrollaba de la misma manera que el cámbium bifacial de las lignofitas, a partir del procámbium. En el caso de las Apocalamitaceae se desarrolla un cámbium bifacial típico a partir de una eustela. En cambio, en Sphenophyllaceae hay un crecimiento desigual del xilema secundario:
A partir del cámbium localizado entre los polos protoxilemáticos de la protostela se desarrollan hileras de células xilemáticas secundarias de lumen amplio.
A partir del pericámbium localizado en los polos protoxilemáticos de la protostela se desarrollan hileras de células xilemáticas secundarias de lumen reducido.
Esto se distingue de lo que llamamos actividad diferencial del cámbium en el sentido de que ambos cámbiumes producen células conductoras, si bien con características diferentes.
Se podría concluir, de acuerdo con las relaciones filogenéticas expresadas en la Fig. 12, que el origen del cámbium bifacial en las Sphenophyta es independiente con respecto a su aparición en las Lygnophyta. La desaparición del carácter en las Sphenophyta más allá del Mesozoico temprano tal vez responda a que resultaba una adaptación para los linajes de las Apocalamitaceae y Sphenophyllaceae en un momento geológico determinado.
Cámbium unifacial (unifacialidad): Parecería ser un carácter distintivo del clado de las Isoetales, excepto porque dos familias dentro del Orden Equisetales tienen también crecimiento secundario por cámbium unifacial. En la actualidad no existen cámbiumes que actúan de manera unifacial, por lo que se teoriza cómo es la forma de actuar de este cámbium en las formas fósiles. El cámbium bifacial produce tanto xilema como floema secundarios, y las iniciales cambiales pueden dividirse tanto periclinal como anticlinalmente. El cámbium unifacial produce sólo xilema secundario, y las iniciales cambiales sólo se dividirían en la cara periclinal interna (Donoghue, 2005) (Fig. 7).

Fig. 7. Diferencias entre el cambium bifacial y el cambium unifacial. El cambium bifacial produce tanto xilema como floema secundarios, y las iniciales cambiales son capaces de dividirse tanto periclinalmente (produciendo células que se diferencian en tejidos secundarios) como anticlinalmente (produciendo nuevas iniciales cambiales). El cambium unifacial produce solo xilema secundario y las iniciales cambiales se dividen sólo periclinalmente, limitando la expansión del cilindro cambial y la producción de leño (Modificado de Donoghue, 2005).
Actividad diferencial del cámbium (elementos vasculares fragmentados radialmente): La actividad diferencial es una forma de desarrollo cambial que se encuentra presente en numerosas plantas actuales, mayormente en angiospermas. Es típico de lianas como Aristolochia, Vitis, Anredera, donde el cámbium interfascicular forma amplios radios de tejido parenquimático. En muchas leguminosas herbáceas como Medicago sativa (alfalfa), Lotus corniculatus y Lamiáceas (Coleus), el cámbium interfascicular forma principalmente esclerénquima hacia adentro y una pequeña cantidad de foema con escasos elementos cribosos hacia afuera (Fig. 8).
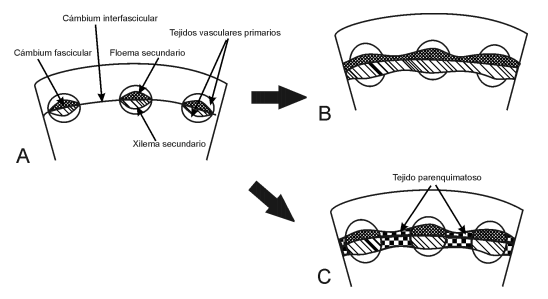
Fig. 8. Esquemas comparando la actividad normal y diferencial del cámbium. A: Desarrollo, a partir del procambium, del cámbium fascicular. Éste genera xilema y floema secundarios. B: En un tallo con actividad normal del cámbium, se diferencia, a partir del parénquima entre los haces vasculares primarios, un cámbium interfascicular. Éste forma también xilema y floema secundarios. C: En un tallo con actividad diferencial del cámbium, en cámbium interfascicular forma tejidos parenquimáticos y/o esclerenquimáticos secundarios (=tejido parenquimatoso).
En el pasado este tipo de actividad cambial se registraba en todas las especies de Medullosa (Medullosales), Pentoxylon (Pentoxylales) y los géneros Rhexoxylon, Cuneumxylon, Tranquiloxylon y seguramente Jeffersonioxylon (Corystospermales), Hermanophyton (Hermanophytales), Amosioxylon (Austrocalyxaceae) y las Calamitaceae.
Actividad remanente del cámbium (elementos vasculares fragmentados tangencialmente): La fragmentación tangencial de los elementos axiales del cilindro vascular secundario está íntimamente relacionada con la polixilia tanto centrífuga como centrípeta. Esto es así porque al parecer hay una separación de tejido parenquimático lignificado entre los sucesivos ciclos de xilema y floema secundarios. Este tejido parenquimático en el caso de la polixilia centrífuga podría ser en realidad el mismo floema secundario que sólo esté conformado por parénquima floemático (Artabe & Brea, 2003).
En el caso de la polixilia centrípeta, la capa de tejido parenquimático estaría vinculada a un tipo de cámbium, denominado remanente. Este cámbium genera una capa de tejido parenquimático (=parénquima de dilatación, sensu Brett, 1968; Zamuner, 1991) que separa los tejidos vasculares centrípetos de los centrífugos. Tendría su origen en la reactivación mitótica de las células del parénquima leñoso del xilema centrípeto.
Cámbiumes supernumerarios o sucesivos (polixilia): Los cámbiumes supernumerarios, o también llamados sucesivos, conducen a la presencia de varios ciclos de xilema y floema secundarios, de dirección de crecimiento normal.
En las primeras etapas de desarrollo del tronco, hay un cilindro cambial, el que cesaría su actividad luego de funcionar por dos o tres años. Posteriormente un segundo cilindro de cámbium se forma a partir de las células parenquimáticas corticales más internas. Estas células parenquimáticas pasan por divisiones periclinales para dar origen a células que se lignifican, abaxialmente, y células cambiales, adaxialmente. Las células cambiales se dividen periclinalmente dando origen a haces vasculares individuales con xilema y floema secundarios. Más tarde este cámbium fascicular queda unido por un cámbium interfascicular. A lo largo de la vida de la planta se irán generando de este modo cámbiumes que formarán sucesivos anillos de xilema y floema (Rajput y Rao, 2003) (Fig. 9). Muchos autores utilizan el término polixilia (e. g. Rao, 1974; Stevenson, 1990; Taylor et al., 2009) o polixilia centrífuga (e. g. Hermsen et al., 2006; Artabe et al., 2005) para este patrón.

Fig. 9. Desarrollo de los sucesivos ciclos de cambium y los tejidos vasculares asociados (foema secundario en gris, xilema secundario en negro) en el tallo de Cocculus hirsutus (Menispermaceae) (Modifcado de Rajput y Rao, 2003).
Carlquist (2007a) realizó una interpretación diferente para el desarrollo de la polixilia, en la que existiría una zona externa (master cámbium) activa mitóticamente de manera ininterrumpida, que genera capas de cámbium en dirección centrípeta.
Los cámbiumes sucesivos están presentes en muchas familias de angiospermas, e.g. Acanthaceae, Aizoaceae, Amaranthaceae, Chenopodiaceae, Combretaceae, Convolvulaceae, Loganiaceae, Menispermaceae, Nyctaginaceae, Verbenaceae (Balfour, 1965; Schmitz et al., 2008; Grosso, 2006; Rajput, 2001, 2002; Terrazas et al., 2011; den Outer & van Veenendaal, 1995; van Veenendaal & den Outer, 1993; Rajput & Rao, 2003; Jacques & De Franceschi, 2007; Carlquist, 2004, 2007b; Schweingruber, 1992, 2007) y en algunos representantes de las gimnospermas vivientes, como Gnetum y Welwitschia (Carlquist & Gowans, 1995; Carlquist, 1996) , las Cycadaceae y algunas Zamiaceae (Terrazas, 1991; Greguss, 1968).
En el registro fósil se observa que la polixilia estaba generalizada en las pteridospermas y cycadales (Nishida et al., 1991; Artabe & Stevenson, 1999; Artabe et al., 1999, 2004, 2005; Artabe & Brea, 2003; Zhang et al., 2006; Hermsen et al., 2006; Taylor et al., 2009).
Orientación inversa (tejidos vasculares centrípetos): La producción de floema y xilema secundarios centrípetos se debe a un cámbium atípico, que recibe la denominación de cámbium inverso, porque produce tejidos vasculares hacia la médula (dirección opuesta a la observada en un crecimiento secundario normal). El desarrollo del cámbium inverso está íntimamente relacionado con la presencia de haces primarios bicolaterales. Este tipo de haces presenta floema a ambos lados del xilema. El cámbium fascicular se encuentra entre el xilema y el floema externo; según Strasburger (2004) también hay algún cámbium entre el xilema y el floema interno. Actualmente, se lo puede hallar en el tallo de ciertas dicotiledóneas, en algunos casos caracterizando familias enteras, en otras ocasiones restringido a ciertos géneros o especies (Metcalfe & Chalk, 1950, 1983; Hayden & Hayden, 1994). Los ejemplos mejor conocidos incluyen las Cucurbitaceae, las familias del Orden Myrtales, y varias familias de astéridas (Hayden & Hayden, 1994). Cabe destacar que el desarrollo de cámbium en la porción más interna de los haces bicolaterales no se conoce para Cucurbitaceae y Myrtales, pero sí ocurre en algunos miembros de las Apocynaceae, Asclepiadacaeae, Convolvulaceae, Gentianaceae, Logarriaceae, Solanaceae y las familias no astéridas de las Polygonaceae y Euphorbiaceae. Entre estas familias, la producción de xilema inverso que resulte en la formación de haces medulares centrípetos ha sido mencionada esporádicamente (Hayden & Hayden, 1994).
En el caso de la Euphorbiaceae Croton glandulosus Linnaeus 1753, el origen del cámbium vascular localizado entre las células más jóvenes del metaxilema y el floema externo procede de manera totalmente normal. Sin embargo, ocurre un desarrollo atípico entre el protoxilema y el floema interno. La actividad combinada de los cámbiumes normal e inverso transforma el sistema vascular de la planta desde una eustela de haces bicolaterales a un cilindro vascular de xilema y floema secundarios con el agregado de haces medulares "anómalos". Estos haces medulares consisten en las células originales de floema primario interno más los tejidos vasculares adicionales. El meristema responsable del crecimiento secundario perimedular se presenta como cordones discretos de cámbium originados entre los primeros elementos del protoxilema y las células más externas del floema primario interno. El crecimiento secundario perimedular está restringido a los haces medulares (Fig. 10). Las células de las regiones interfasciculares se mantienen inactivas o, en los tallos viejos y robustos, estallan por la proliferación de células formadas en la porción interna del haz bicolateral (Hayden & Hayden, 1994).

Fig. 10. Diagrama mostrando la actividad inversa del cámbium. A: En una eustela con haces bicolaterales, se desarrolla, a partir del procambium, un cámbium fascicular "normal" y un cámbium fascicular inverso. B: El cámbium fascicular "normal" comienza a desarrollar xilema secundario hacia el centro del tallo y floema secundario hacia la periferia. El cámbium inverso comienza a generar xilema secundario externamente y floema secundario internamente. C: Comienza la actividad del cambium interfascicular, que sólo actúa de manera centrífuga, por lo que se genera un ciclo de tejidos vasculares secundarios que va creciendo de manera centrífuga. El cámbium inverso origina arcos de tejidos vasculares secundarios centrípeto aislados, que van creciendo hacia la médula.
Si evaluamos esta variante cambial en un sentido estratigráfico, observamos que en el pasado la presencia de cámbium inverso era más generalizada que en al actualidad. En todas las especies del género Medullosa (Medullosales), los géneros Rhexoxylon y Elchaxylon (Corystospermales), Pentoxylon (Pentoxylales), Lioxylon, Fascivarioxylon, Neochamberlainia, Worsdellia y Menucoa (Cycadales) se observan tejidos vasculares secundarios centrípetos que han crecido hacia la médula. De éstos, sólo Lioxylon y Fascivarioxylon tienen un ciclo continuo de xilema centrípeto (Jain, 1962; Zhang et al. 2006).
Puesto que las Medullosales, Corystospermales y Pentoxylales se extinguieron, sólo el linaje de las Cycadales dentro de las gimnospermas conserva en la actualidad el desarrollo del cámbium inverso. Asimismo, el xilema centrípeto en formas vivientes de las Cycadales es esporádico, distinguiéndose en la región basal de algunas especies de Macrozamia, Lepidozamia, Encephalartos y Cycas (Artabe et al., 2005).
De los estudios anatómicos sobre el desarrollo de los tejidos vasculares centrípetos en medullosales, corystospermas y cycadales (Bancroft, 1913; Walton, 1923; Archangelsky & Brett, 1961; Zamuner, 1991; Artabe & Brea, 2003; Artabe et al., 2005; Bodnar, 2008) se puede concluir que el crecimiento de los haces medulares y el xilema centrípeto es semejante a lo que fue descripto para angiospermas vivientes.
Sistema vascular medular: En las plantas con desarrollo de tejidos vasculares centrípetos se puede dar una complejización mucho mayor de los tallos, por el desarrollo de ciclos adicionales de cámbium normal e inverso. Esto culmina en la conformación de dos sistemas vasculares secundarios, que coexisten en un mismo tronco: el sistema medular y el sistema cilíndrico. El sistema medular se ha registrado en formas pérmicas de Medullosales, en Cycadales fósiles (Charmorgia, Fascivarioxylon, Neochamberlainia, Worsdellia, Centricycas y Menucoa) y actuales (Lepidozamia, Encephalartos y Macrozamia) y en Corystospermales (Rhexoxylon). Entre las angiospermas, un ejemplo es el explicado previamente de Croton glandulosus (Euphorbiaceae).
El sistema medular tiene su origen en los tejidos vasculares secundarios centrípetos (=cámbium inverso). Está conformado por uno o más ciclos de haces dobles perimedulares con una porción centrípeta y una porción centrífuga. Una vez separados los tejidos centrípetos de los centrífugos, en el borde externo de los centrípetos aparece un nuevo ciclo de tejidos centrífugos, constituyendo haces perimedulares dobles. Sólo cuando hay haces perimedulares dobles, con una porción centrípeta y una porción centrífuga, se habla de un sistema vascular medular independiente del cilíndrico.
Su desarrollo ha sido intensamente estudiado en el género Rhexoxylon por diferentes autores (Archangelsky & Brett, 1961; Zamuner, 1991; Artabe & Brea, 2003; Bodnar, 2008). Como ocurre en muchas plantas con haces primarios bicolaterales, en las etapas tempranas del crecimiento de los tallos de Rhexoxylon el cilindro vascular secundario consta de un ciclo vascular centrífugo-centrípeto. La actividad del cámbium se torna asimétrica, con un mayor desarrollo de los tejidos centrífugos que los centrípetos. El xilema (y floema) centrípeto se separa del centrífugo por el desarrollo de tejidos parenquimatosos (=actividad remanente) entre ellos. En todas las especies de Rhexoxylon -excepto R. cortaderitaense- durante las etapas tardías, en el borde externo del xilema (y floema) centrípeto comienza a desarrollarse xilema (y floema) centrífugo (=polixilia). Por esto, en la etapa madura, el cilindro vascular secundario consta de un sistema medular, formado por uno a más ciclos de haces perimedulares dobles centrípeto- centrífugos (Fig. 11).

Fig. 11. Evolución del sistema medular, mediante la comparación de las secuencias de desarrollo de tres taxones de Corystospermales. A: Elchaxylon zavattierae. B: Rhexoxylon cortaderitaense. C: Rhexoxylon piatnizkyi. Blanco → parénquima y esclerénquima, Gris claro → tejidos vasculares centrífugos (producidos por el cámbium normal), Gris oscuro → tejidos vasculares centrípetoos (producidos por el cámbium inverso). En el primer estadio (a), dos anillos cambiales, alrededor de los haces vasculares primarios, dan origen a cantidades iguales de tejidos vasculares centrífugos (anillo cambial normal) y centrípetos (anillo cambial inverso). En la fase siguiente (b) los anillos cambiales producen un desarrollo diferencial en la parte centrífuga. La fase adulta de A (Elchaxylon zavattierae) consiste en un cilindro vascular de tejidos vasculares secundarios centrífugos más un ciclo de tejidos vasculares centrípetos. En la ontogenia de los descendientes (B y C) se agregan etapas (peramorfosis). En el estadio (b) de Rhexoxylon cortaderitaense y R. pianitzkyi, el tejido vascular centrípeto se separa del centrífugo debido al desarrollo de parénquima de dilatación entre ellos (resultado de la actividad del cámbium remanente). La fase adulta de R. cortaderitaense (B.c) consiste en un ciclo de grandes cuñas de tejidos vasculares secundarios separado por una barra tangencial de parénquima de un ciclo de tejidos vasculares centrípetos. El desarrollo de R. pianitzkyi (C) se alarga aún más y en una etapa ulterior, tejidos vasculares centrífugos crecen en el margen interno de los tejidos vasculares centrípetos generando un ciclo de haces perimedulares dobles (C.d).
DISCUSIÓN
LOS MODELOS EVOLUTIVOS
Los patrones observados en el flujo de las auxinas, descriptos tanto para las espermatofitas actuales como en el leño de Archaeopteris (progimnosperma del Devónico Tardío), sustentan firmemente la premisa de que los tejidos vasculares secundarios en todas las lignofitas, habrían sido regulados por los mismos mecanismos de control genético y fisiológico (Rothwell & Lev-Yadun, 2005). En la hipótesis filogenética presentada en la Fig. 12 el patrón en espiral aparece como una sinapomorfía de todas las lignofitas.

Fig. 12. Hipótesis de las relaciones filogenéticas de plantas vasculares. La figura presenta el consenso estricto de los 15 árboles más parsimoniosos obtenidos a partir del análisis la matriz de la Tabla 3, y muestra el mapeo de los caracteres relacionados con la actividad del cámbium.
Por otro lado, si consideramos las variantes cambiales estudiadas con respecto a su posición en el árbol filogenético de las plantas vasculares (Fig. 12), podemos concluir que cada una fue adquirida de manera independiente en cada linaje, lo que ya había sido señalado por Carlquist (1988). A pesar de ello, los procesos ontogenéticos implicados son comparables, como se sugiere más adelante en este trabajo. Además, el origen y diversificación de cada una de las variantes, podría tener una íntima relación con eventos heterocrónicos y heterotópicos.
La heterocronía y la heterotopía (incluyendo a la homeosis) tradicionalmente han sido consideradas cambios evo-devo. Bateman (1994) define un cambio evo-devo como cualquier cambio genético expresado fenotípicamente, que se produce en un linaje y que altera profundamente la forma y/o el tamaño de cualquier estadio ontogenético del descendiente en relación al ancestro.
La heterocronía es el cambio en la tasa relativa y el ritmo del desarrollo del descendiente en relación con el ancestro (Haeckel, 1866; de Beer, 1958). Incluye dos tipos de patrones: pedomorfosis y peramorfosis.
La pedomorfosis es la retención de caracteres juveniles ancestrales en la fase adulta del descendiente (Garstang, 1928). Este patrón puede ser alcanzado mediante tres procesos: post-desplazamiento, progénesis y neotenia. Post-desplazamiento significa el retraso del punto de inicio del desarrollo de ciertas estructuras (Alberch et al., 1979), y progénesis implica la aceleración en la maduración sexual con respecto al desarrollo somático (=punto de finalización temprano) (Giard, 1887). La neotenia es la desaceleración de la tasa de desarrollo (Kollman, 1885).
En cambio, la peramorfosis es la presencia de la morfología adulta ancestral en un estadio juvenil del descendiente, lo que resulta en un descendiente que tiene una morfología más diferenciada que la del ancestro (Alberch et al., 1979). Puede ser causada por tres procesos: predesplazamiento, hipermorfosis y aceleración. Predesplazamiento es el comienzo temprano del desarrollo de una estructura en comparación con el desarrollo del organismo entero (Alberch et al., 1979). La hipermorfosis consiste en la extensión del período juvenil de crecimiento, causada por un retraso en la maduración sexual (de Beer, 1930). Por último, la aceleración es el incremento en la tasa de desarrollo morfológico (Cope, 1887).
El segundo tipo de cambio evo-devo es la heterotopía o cambio en el patrón espacial de los procesos del desarrollo (Haeckel, 1866). De acuerdo a Baum & Donoghue (2002) hay dos tipos de heterotopía: homeoheterotopía, que es la transferencia de la identidad genética entre los tejidos u órganos preexistentes, y neoheterotopía, que es la aparición de tejidos u órganos en una posición nueva. Según Baum & Donoghue (2002), homeosis -definida por Bateson (1894) como el reemplazo de una estructura por otra- es la categoría de homeoheterotopía en la que todos los aspectos de identidad de una estructura son conferidas a la estructura receptora.
Teniendo en cuenta estos términos, se pueden trazas los siguientes modelos para el origen y diversificación de las variantes cambiales.
Unifacialidad
De acuerdo a las hipótesis filogenéticas propuestas para las plantas vasculares (Fig. 12), el cambium unifacial de Lycophyta no es homólogo al cámbium unifacial que está presente en algunas Euphyllophyta, evolucionó independientemente en cada linaje (Fig. 12).
Tanto las licofitas como las esfenofitas arborescentes, caracterizadas por el cambium unifacial, están totalmente extintas. Tal vez el cámbiun unifacial que existe hoy en día es el que presenta el género Isoetes, que además es el único representante del clado de las licofitas arbóreas que vive en la actualidad. Sin embargo, la actividad del cámbium vascular del tallo de Isoetes no sería del todo equivalente al cámbium unifacial, ya que externamente genera tejido cortical e internamente tejido vascular compuesto por traqueidas y tubos cribosos entremezclados, el que recibe el nombre de tejido prismático.
De acuerdo a las hipótesis filogenéticas de Kenrick & Crane (1997), el cambium bifacial aparece en la base del clado de las Sphenophyta, por lo que el cambium unifacial de las Archaeocalamitaceae y Calamitaceae sería derivado de áquel. Pero ¿cómo se habría originado este tipo de cámbium que sólo produce xilema secundario? En este caso las células cambiales detendrían las divisiones en la cara periclinal externa, lo que no se sabe es si está interrupción es progresiva o repentina en el desarrollo. En general, para cualquier planta con desarrollo de cámbium bifacial, lo normal es que se produzca menos floema secundario que xilema secundario. Esto ocurre porque en el crecimiento secundario por cada capa de células xilemáticas no se desarrolla una capa de células floemáticas. Esta proporción es, por lo menos, que cada dos capas de xilema se produce una de floema. Si este porcentaje aumenta en detrimento del floema, o sea, que en el crecimiento el cámbium se saltee cada vez más etapas en las que se genera una capa de células del floema, podemos visualizar el origen del cámbium unifacial a partir de un cambium bifacial. Esta deleción de etapas se podría producir por la aceleración de la tasa de crecimiento, y por ende podría corresponder a un proceso heterocrónico, en particular a un patrón peramórfico.
Desde el punto de vista del registro geológico, el cámbium unifacial de las licofitas y esfenofitas arborescentes se origina después (Devónico Tardío) que el cámbium bifacial (Devónico Medio/Tardío) que aparece por primera vez en las progimnospermas (Lignofitas). Las Lepidodendrales, Pleuromeiales, Isoetales, Archaeocalamitaceae y Calamitaceae consiguen la arborescencia y el aumento del diámetro por crecimiento primario epidogenético, más que por el cámbium unifacial. No se produjo diversificación significativa de este carácter, además estos clados sufrieron una marcada declinación. Por esto, es plausible pensar que la arborescencia alcanzada mediante el cámbium bifacial haya sido clave en el éxito ulterior de las lignofitas.
Fragmentación radial de elementos vasculares (actividad diferencial del cámbium)
La actividad diferencial del cambium, así como las variantes cambiales que siguen, se han originado a partir del un cambium bifacial típico (ver Fig. 6 y Fig. 12).
El proceso ontogenético implicado en el origen de la actividad diferencial es un cambio en la función del cámbium interfascicular, que en vez de generar tejidos vasculares secundarios conductores (células xilemáticas y floemáticas), forma un tejido de relleno y/o sostén, conocido como parenquimatoso (células parenquimáticas, esclerenquimáticas e idioblastos). En el marco de la biología evo-devo, este es un reemplazo de un tipo tisular por otro, es decir, un cambio homeótico. Las formas carboníferas de Medullosales (Medullosa noei, M. steinii, M. endocentrica, M. thomsoni, M. primaeva) muestran sistemas vasculares cilíndricos constituidos por segmentos separados, como resultado de que el cámbium interfascicular forma abundante parénquima secundario. En las formas pérmicas, se puede ver una disminución de la fragmentación de los elementos vasculares. Así en Medullosa solmsii está formado por 8 a 12 segmentos vasculares, en M. leuckharti hay 4 segmentos vasculares, y en M. stellata y M. porosa el sistema cilíndrico no es disecto.
La topología del cladograma de Corystospermaceae obtenido en el presente análisis es coherente con las series de transformación propuestas por Artabe & Brea (2003) y Artabe & Zamuner (2007): la serie cuneumxyloide (Cuneumxylon y Tranquiloxylon), caracterizada por el xilema primario endarco, cuñas centrífugas de xilema secundario separadas por radios parequimatosos y polixilia centrífuga, y la serie rhexoxyloide (Rhexoxylon y Elchaxylon), donde se observa la presencia de xilema primario mesarco, cuñas de xilema secundario centrífugo separadas por radios parenquimatosos, polixilia centrífuga, xilema secundario centrípeto y haces perimedulares dobles. La única diferencia entre esta propuesta y nuestra hipótesis filogenética es que en la última Elchaxylon aparece como basal a los dos linajes, por lo que la condición ancestral del resto de las corystospermas es la de un cilindro vascular secundario no disecto.
Polixilia (cámbiumes supernumerarios o sucesivos)
La polixilia centrífuga implica la aparición de meristemas secundarios nuevos. Con respecto a la condición ancestral, que es la existencia de un único cambium, este patrón puede ser interpretado como un evento heterotópico.
En las dos series de transformación evolutiva propuestas por Artabe et al. (2005) para el clado Zamiaceae-Encephalartoidea dentro de las cycadales (Encephalarteae y Diooea) hay un incremento de la polixilia centrífuga: se irían agregando cámbiumes hasta llegar al máximo observado (seis en Brunoa).
Por otro lado, en la hipótesis evolutiva planteada para el cilindro vascular secundario de las corystospermas por Artabe & Brea (2003) se observa también un incremento de la polixilia centrífuga en las dos series de transformación principales (rhexoxyloide y cuneumxyloide).
Orientación inversa (cámbium inverso)
El desarrollo de un cámbium inverso (también denominado polixilia centrípeta ya que involucra la adición de un anillo cambial) corresponde, como el caso anterior, a la aparición de meristemas secundarios nuevos, y puede ser interpretada como un evento heterotópico.
Dentro de las Medullosales se aprecia una complejización de los tallos por aumento de la actividad inversa del cámbium. Las formas carboníferas como Medullosa noei, M. endocentrica y M. steinii, exhiben un anillo cambial centrípeto y otro centrífugo. Por otra parte, las especies pérmicas muestran una organización más complicada: M. stellata y M. porosa presentan dos ciclos de tejidos vasculares centrípetos y dos centrífugos (Fig. 13). Worsdell (1896, 1906) sugirió que las Cycadales habrían derivado de las medullosas por pérdida progresiva de los tejidos vasculares centrípetos. Posteriormente Artabe et al. (2005) al comparar los tallos fósiles de cycadales con los actuales, notaron que la cantidad de xilema centrípeto disminuye gradualmente desde Fascivarioxylon (Jurásico) hacia Neochamberlainia-Worsdellia (Cretácico) hasta Menucoa (Cenozoico) y por último en las formas vivientes, donde el carácter se vuelve relictual.

Fig. 13. Único árbol más parsimonioso obtenido a partir del análisis la matriz de la Tabla 5, indicando la evolución del sistema vascular secundario en las Corystospermales.
En la base de la filogenia de las corystospermas (Fig. 13) se separa Elchaxylon zavattieriae del resto de los taxones de troncos. Los ejes adultos de Elchaxylon tienen un ciclo de tejidos centrípetos unido a los centrífugos. Luego, en el cladograma, se distinguen dos linajes derivados (i.e. cuneumxyloide y rhexoxyloide) en donde se observan los siguientes patrones: una pérdida de los elementos vasculares centrípetos en el primero, y un aumento de la cantidad de estos elementos en el segundo.
Fragmentación tangencial de los elementos vasculares (actividad remanente del cambium)
Entre el xilema secundario centrífugo y centrípeto, aparecen tejidos de relleno y/o sostén (=parénquima de dilatación) en forma de arcos, que son producidos por células parenquimáticas del mismo leño que reanudan su actividad meristemática. En la ontogenia típica no hay tejido en la posición que ocupa el parénquima de dilatación en los tallos de corystospermas. Por esto, este evento puede ser explicado vía heterotopía.
La fragmentación tangencial de los elementos vasculares se observa sólo en el linaje rhexoxyloide, de la hipótesis filogenética propuesta en este trabajo (Fig. 13). Elchaxylon zavattieriae tiene los tejidos centrípetos unidos a los centrífugos porque no se desarrolla parénquima de dilatación.
Sistema vascular medular
El sistema medular ha sido estudiado en profundidad en las Corystospemales. Caracteriza a todas las especies del género Rhexoxylon, excepto a R. cortaderitaense (la especie más basal del género, de acuerdo a la filogenia presentada). En las etapas tempranas del desarrollo de esta especie, el cilindro vascular secundario consta de un ciclo vascular centrífugo-centrípeto. La actividad del cámbium se torna asimétrica, con un mayor desarrollo de los tejidos centrífugos respecto de los centrípetos. El xilema (y floema) centrípeto se separa del centrífugo por el desarrollo de tejidos parenquimatosos (=actividad remanente) entre ellos. Aquí culmina el desarrollo de los tallos de R. cortaderitaense, que, si bien siguen creciendo en espesor, no sufren más diferenciaciones morfológicas. En las restantes especies de Rhexoxylon durante las etapas tardías, en el borde externo del xilema (y floema) centrípeto comienza a desarrollarse xilema (y floema) centrífugo. Por esto, en la etapa madura, el cilindro vascular secundario consta de un sistema medular, formado por uno a más ciclos de haces perimedulares dobles centrípeto-centrífugos.
Entre las formas con sistema medular, R. tetrapteridoides es la menos compleja. Las ontogenias de los otras especies muestran un incremento progresivo en la complejidad del sistemamedular, evidenciado en un aumento del número de ciclos de haces perimedulares. Esto indicaría una adición de estadios ontogenéticos con respecto a R. cortaderitaense. R. tetrapteridoides se encuentra basal con respecto a R. brasilense, R. pianitkzyi, R. africanum y R. brunoi. Estas especies presentan etapas del desarrollo adicionales en comparación con la ontogenia de R. tetrapteridoides, ya que muestran el crecimiento de un nuevo ciclo de tejido vascular centrípeto en todas las cuñas centrífugas. Dicha transformación (R. tetrapteridoides → R. brasilense, R. pianitkzyi, R. africanum y R. brunoi), se podría interpretar como un patrón heterocrónico, en particular peramórfico.
CONCLUSIONES
A partir del panorama expuesto en este trabajo, podemos concluir que las variaciones anatómicas puntuales nos dan indicios de los procesos que subyacen al desarrollo del cámbium. El hallazgo del patrón en espiral en leños triásicos es una evidencia a favor de que los mismos procesos fisiológicos que regulan el crecimiento de leños actuales han existido a lo largo del registro geológico, apoyando las ideas de Rothwell & Lev-Yadun (2005).
Con respecto a las variantes cambiales, podemos concluir que existió una divergencia principal entre el cámbium unifacial presente en las lycophytas y el cámbium bifacial de las lignofitas (que aparece en algunos grupos de esfenofitas). De acuerdo a Savidge (2001) los mecanismos regulatorios que operaron en la formación del cámbium unifacial son diferentes que los que operan en el desarrollo del cámbium bifacial. Todas las demás variantes (diferencial, remanente, polixilia, inverso, sistema medular) tienen como condición ancestral el crecimiento secundario típico (bifacial, único, centrífugo y uniforme) y se originaron vía heterotopía.
Aunque cada una de dichas variantes cambiales se adquirió convergentemente en cada linaje, su evolución en todos los clados podría haber estado íntimamente relacionada con alteraciones en el desarrollo. En el pasado geológico, las variantes cambiales estaban muy generalizadas en gimnospermas. En la actualidad, su presencia en este grupo es reducida, en parte debido a la extinción de muchos linajes gimnospérmicos.
Las variantes del cámbium habrían tenido un valor adaptativo que otorgaba a las licofitas, esfenofitas y gimnospermas fósiles la posibilidad de dominar en condiciones ambientales particulares del Paleozoico y Mesozoico, como las que reinaban en los bosques pantanosos carboníferos y los bosques subtropicales estacionales triásicos. En el presente, ecosistemas análogos a aquellos son habitados principalmente por angiospermas, en las que se puede observar una gran variabilidad en el desarrollo secundario.
AGRADECIMIENTOS
Las autoras desean agradecer a la Dra. Analía Artabe por la lectura crítica del manuscrito, y a los revisores anónimos por sus valiosas sugerencias.
BIBLIOGRAFÍA
1. ALBERCH, P., S. J. GOULD, G. F. OSTER & D. B. WAKE. 1979. Size and shape in ontogeny and phylogeny. Paleobiology 5: 296-317. [ Links ]
2. ARCHANGELSKY, S. & D. W. BRETT. 1961. Studies on Triassic fossil plants from Argentina. 1. Rhexoxylon from the Ischigualasto Formation. Philos. T. R. S. Lon. B 706: 1-19. [ Links ]
3. ARCHANGELSKY, S. & E. R. DE LA SOTA. 1966. Estudio anatómico de una nueva Lycopsida del Pérmico de Bolivia. Rev. Mus. de La Plata (n. s.) 5: 17-26. [ Links ]
4. ARTABE, A. E. & M. BREA. 2003. A New Approach to Corystospermales based on petrified stems from the Triassic of Argentina. Alcheringa 27: 209-229. [ Links ]
5. ARTABE, A. E. & D. W. STEVENSON, 1999. Fossil Cycadales of Argentina. Bot. Rev. 65: 219-238. [ Links ]
6. ARTABE, A. E. & A.B. ZAMUNER. 1991. Una nueva Equisetal del Triásico de Cacheuta, Argentina, con estructura interna preservada. Ameghiniana 28: 287-294. [ Links ]
7. ARTABE, A. E. & A.B. ZAMUNER. 2007. Elchaxylon, a new corystosperm based on permineralized stems from the Late Triassic of Argentina. Alcheringa 31: 85-96. [ Links ]
8. ARTABE, A. E., M. BREA, & A. B. ZAMUNER. 1999. Rhexoxylon brunoi n. sp., a new Triassic Corystosperm from the Paramillo Uspallata, Mendoza, Argentina. Rev. Paleobot. Palyno. 105: 63-74. [ Links ]
9. ARTABE, A. E., A. B. ZAMUNER & D. W. STEVENSON. 2004. Two new petrified cycad stems, Brunoa gen. nov. and Worsdellia gen. nov., from the Cretaceous of patagonia , Argentina. Bot. Rev. 70: 121-133. [ Links ]
10. ARTABE, A. E., A. B. ZAMUNER & D. W. STEVENSON. 2005. A new genus of Late Cretaceous cycad stem from Argentina, with reappraisal of known forms. Alcheringa 29: 87-100. [ Links ]
11. ARTABE, A., A. B. ZAMUNER & D. W. STEVENSON. 2010. Neochamberlainia, a new name for Chamberlainia Artabe, Zamuner & D. W. Stev. (Zamiaceae) non Chamberlainia Grout (Brachytheciaceae). Brittonia 62: 95. [ Links ]
12. BALFOUR, E. 1965. Anomalous secondary thickening in Chenopodiaceae, Nyctaginaceae and Amaranthaceae. Phytomorphology 15:111-22. [ Links ]
13. BANCROFT, N. 1913. Rhexoxylon africanum, a new Medullosean stem. Trans. Linn. Soc. Lon. Ser. 2 (Bot.) 8: 87-103. [ Links ]
14. BATEMAN, R. M. 1994. Evolutionary-developmental change in the growth architecture of fossil rhizomorphic lycopsids: scenarios constructed on cladistic foundations. Biol. Rev. 69: 527-597. [ Links ]
15. BATEMAN, R. M. & W. A. DIMICHELE. 2002. Generating and filtering major phenotypic novelties: neoGoldschmidtian saltation revisited. En: CRONK, Q.C.B., R. M. BATEMAN & J. A. HAWKINS (eds.), Developmental genetics and plant evolution, pp. 109-159. Taylor & Francis, London. [ Links ]
16. BATESON, W. 1894. Materials for the study of variation: treated with especial regard to discontinuity in the origin of species. Macmillan, London. [ Links ]
17. BAUM, D. A. & M. J. DONOGHUE. 2002. Transference of function, heterotopy and the evolution of plant development. En: CRONK, Q.C.B., R.M. BATEMAN & J. A. HAWKINS (eds.) Developmental genetics and plant evolution, pp. 52-69. Taylor & Francis, London. [ Links ]
18. BODNAR, J. 2008. Rhexoxylon cortaderitaense (Menéndez) comb. nov., a species of permineralized stems newly assigned to the Corystospermaceae, from the Triassic of Argentina. Alcheringa 32: 171-190. [ Links ]
19. BODNAR, J. (en prensa). Estudios evolutivos-del desarrollo en tallos fósiles de Corystospermaceae (Corystospermales, Spermatopsida) Contrib. MACN 5. [ Links ]
20. BODNAR, J. & A. E. ARTABE. 2007. Estudio sistemático y paleodendrológico del leño de una Cupressaceae triásica de la Formación Ischigualasto, provincia de San Juan, Argentina. Ameghiniana 44: 303-319. [ Links ]
21. BONETTI, M. I. R. 1966. Protojuniperoxylon ischigualastensis sp. nov. del Triásico de Ischigualasto (San Juan). Ameghiniana 4: 211-218. [ Links ]
22. BRETT, D. W. 1968. Studies on Triassic fossil plants from Argentina. III. The trunk of Rhexoxylon. Palaeontology 11: 236-245. [ Links ]
23. BRONGNIART, A. T. 1822. Sur la classification et la distribution des végéteaux fossiles en général, et sur ceux des terrains de sédiments supérieur en particulier. Mem. Mus. Nat. Hist. Nat .Paris 8: 203-348. [ Links ]
24. CARLQUIST, S. 1988. Comparative Wood Anatomy. Systematic, Ecological, and Evolutionary Aspects of Dicotyledon Wood. Springer-Verlag, Berlin. [ Links ]
25. CARLQUIST, S. 1996a. Wood, bark, and stem anatomy of Gnetales: a summary. Int. J. Plant Sci. 157(6 suppl.): S58-S76. [ Links ]
26. CARLQUIST, S. 1996b. Wood and stem anatomy of Menispermaceae. Aliso 14: 155-170. [ Links ]
27. CARLQUIST, S. 2004. Lateral meristems, successive cambia and their products: a reinterpretation based on roots and stems of Nyctaginaceae. Bot. J. Linn. Soc. 146: 129-143. [ Links ]
28. CARLQUIST, S. 2007a. Successive cambia revisited: ontogeny, histology, diversity, and functional significance. J. Torrey Bot. Soc. 134:301-332. [ Links ]
29. CARLQUIST, S. 2007b. Successive cambia in Aizoaceae: products and process. Bot. J. Linn. Soc. 154: 141-155. [ Links ]
30. CARLQUIST S. & D.A. GOWANS. 1995. Secondary growth and wood histology of Welwitschia. Bot. J. Linn. Soc. 118: 107-121. [ Links ]
31. COPE, E. D. 1887. The Origin of the Fittest. Macmillan, New York. [ Links ]
32. DE BEER, G. R. 1930. Embryology and evolution. Clarendon Press, Oxford. [ Links ]
33. DE BEER, G. R. 1958. Embryos and ancestors, 3rd edition. Clarendon Press, Oxford. [ Links ]
34. DEN OUTER, R. W. & W. L. H. VAN VEENENDAAL, 1995. Development of included phloem in the stem of Combretum nigricans (Combretaceae). IAWA J. 16: 151-1 58 [ Links ]
35. DONOGHUE, M. J. 2005. Key innovations, convergence, and success: macroevolutionary lessons from plant phylogeny. Paleobiology 31: 77-93. [ Links ]
36. EGGERT, D. A. & N. Y. KANEMOTO. 1977. Stem phloem of a Middle Pennsylvanian Lepidodendron. Bot. Gaz. 138: 102-111. [ Links ]
37. FAHN, A. 1990. Plant anatomy. Pergamon Press, Oxford. [ Links ]
38. GARSTANG, W. 1928. The morphology of the Tunicata and its bearing on the phylogeny of the Chordata. Q. J. Microsc. Sci. 72: 51-54. [ Links ]
39. GIARD, A. 1887. La castration parasitaire et son influence sur les caractères extérieurs du sexe male chez les crustacés décapodes. Bull. Sci. Dep. Nord 18: 1-28. [ Links ]
40. GOLOBOFF, P.A., J.S. FARRIS & K. NIXON. 2008. TNT, a free program for phylogenetic analysis. Cladistics 24: 774-786. [ Links ]
41. GROOVER, A. T. 2005. What genes make a tree a tree? Trends Plant Sci. 10: 210-214. [ Links ]
42. GREGUSS, P. 1968. Xylotomy of the living cycads with a description of their leaves and epidermis. Akademiai Kiadó, Budapest. [ Links ]
43. GROSSO, M. A. 2006. Crecimiento secundario inusual en raíz principal de Pfaffa gnaphalioides (L. Fil.) Mart. (Amaranthaceae). Acta Bot. Bras. 21: 21-26 [ Links ]
44. HAECKEL, E. 1866. Generelle Morphologie der Organismen, Vols. 1-2. Georg Reimer Verlag, Berlin. [ Links ]
45. HAYDEN S. M. & W. J. HAYDEN. 1994 Stem development, medullary bundles, and wood anatomy of Croton glandulosus var. septentrionalis (Euphorbiaceae). IAWA J. 15: 51-63. [ Links ]
46. HEJNOWICZ, Z. & E. U. KURCZYNSKA. 1987. Occurrence of circular vessels above axillary buds in stems of woody plants. Act. Soc. Bot. Pol. 56: 415-419. [ Links ]
47. HERBST, R. & A. I. LUTZ. 1988. Rhexoxylon brasiliensis n. sp. (Corystospermaceae, Pteridospermales) from the Upper Triassic Caturrita Formation, Brazil, with comments on biology and environment. Med. Rijks Geol. Dienst 42: 21-28. [ Links ]
48. HERBST, R. & A. I. LUTZ. 1995. Tranquiloxylon petriellai nov. gen. et sp. (Pteridospermales) from the Upper Triassic Laguna Colorada Formation, Santa Cruz province, Argentina. Ameghiniana 32: 231-236. [ Links ]
49. HERMSEN, E. J., T. N. TAYLOR, E. L. TAYLOR & D. W. STEVENSON. 2006. Cataphylls of the Middle Triassic Cycad Antarcticycas schopfii and new insights into cycad evolution. Am. J. Bot. 93: 724-738. [ Links ]
50. HILTON, J. & R. M. BATEMAN. 2006. Pteridosperms are the backbone of seed-plant phylogeny. J. Torrey Bot. Soc. 133: 119-168. [ Links ]
51. JACQUES, F. M. B. & D. DE FRANCESCHI. 2007. Menispermaceae wood anatomy and cambial variants. IAWA J. 28: 139-172. [ Links ]
52. JAIN, K. P. 1962. Fascivarioxylon mehtae gen. et sp. nov., a new petrified cycadean wood from the Rajmahal Hills, Bihar, India. The Palaeobot. 11: 138-143. [ Links ]
53. KENRICK, P. & P. R. CRANE. 1997. The origin and early diversification of land plants. Smithsonian Institution Press, Washington D.C. [ Links ]
54. KO, J. H., J. YANG, S. OH, S. PARK & K. H. HAN. 2004. Genomics of wood formation. En: KUMAR, S. & M. FLADUNG (eds.) Molecular genetics and breeding of forest trees, pp. 113-140. Haworth's Food Products Press, New York. [ Links ]
55. KOLLMAN, J. 1885. Das Ueberwintern von europäischen Frosch- und Tritonlarven und die Umwandlung des mexikanischen Axolotl. Verhandlungen der Naturforschendeden Gesellschaft in Basel 7: 387-398. [ Links ]
56. KURCZYRISKA, E. U. & Z. HEJNOWICZ. 1991. Differentiation of circular vessels in isolated segments of Fraxinus excelsior. Physioi. Plant. 83: 275-280. [ Links ]
57. LARSON, P. 1994. The Vascular Cambium. Development and Structure. Springer Series in Wood Science, Berlin. [ Links ]
58. LEMOIGNE, Y. 1966. Les Tissus vasculaires et leur histogenese chez les Lepidophytales arborescentes du Paléozoique. Ann. Sci. Natur. Biol. 7: 445-474. [ Links ]
59. LEV-YADUN S. & R. ALONI. 1990. Vascular differentiation in branch junctions of trees: circular patterns and functional signifcance. Trees 4: 49-54. [ Links ]
60. LINNAEUS, C. 1753. Species plantarum, exhibentes plantas rite cognitas, ad genera relatas, cum differentiis specificis, nominibus trivialibus, synonymis selectis, locis natalibus, secundum systema sexuale digestas. Holmiae, Impensis Laurentii Salvii. L. Salvius, Stockholm. [ Links ]
61. METCALFE, C. R. & L. CHALK. 1950. Anatomy of the dicotyledons. I & II. 1rst edition. Clarendon Press, Oxford. [ Links ]
62. METCALFE, C. R. & L. CHALK. 1983. Anatomy of the dicotyledons. II. Wood structure and conclusion of the general introduction, 2nd edition, Clarendon Press, Oxford. [ Links ]
63. NISHIDA, H., M. NISHIDA & K. TANAKA. 1991. Petrified plants from the Cretaceous of the Kwanto mountains, central Japan. III. A polixylic Cycadean trunk, Sanchucycas gigantea gen. et sp. nov. Bot. Mag. Tokyo 104: 191-205. [ Links ]
64. NIXON K.C., W.L. CREPET, D. W. STEVENSON & E. M. FRIIS. 1994. A reevaluation of seed plant phylogeny. Ann. Mo. Bot. Gard. 81: 484-533. [ Links ]
65. OLSON, M. E. 2007. Wood ontogeny as a model for studying heterochrony, with an example of paedomorphosis in Moringa (Moringaceae). Syst. Biodivers. 5: 145-158. [ Links ]
66. RAJPUT, K. S. 2001. Secondary growth of the stem of Celosia argentea L. and Aerva sanguinolenta (L.) Blume (Amaranthaceae). Phyton-Horn 41: 169-177. [ Links ]
67. RAJPUT, K. S. 2002. Stem anatomy of Amaranthaceae: Rayless nature of xylem. Flora-Jena 197:224-232. [ Links ]
68. RAJPUT, K. S. & K. S. RAO. 2003. Cambial variant and xylem structure in the stem of Cocculus hirsutus (Menispermaceae). IAWA J. 24: 411- 420. [ Links ]
69. RAO, L. N. 1974. Cycas beddomei Dyer. Plant Sci. 79: 59-67 [ Links ]
70. RENAULT, B. 1876. Recherches sur quelques Calamodendrées et sur leurs afnités botaniques probables. C.R. Acad. Sci. Paris 83: 574-576. [ Links ]
71. ROTHWELL, G. W. & S. LEV-YADUN. 2005. Evidence of polar auxin fow in 375 million-year-old fossil wood. Am. J. Bot. 92: 903-906. [ Links ]
72. ROTHWELL, G. W. & K. C. NIXON. 2006. How does the inclusion of fossil data change our conclusions about the phylogenetic history of euphyllophytes? Int. J. Plant Sci. 167: 737-749. [ Links ]
73. SACHS, T. 1984. Axiality and polarity in vascular plants. En: BARLOW P. W. & D. J CARR (eds.), Positional Controls in Plant Development pp. 193-224. Cambridge University Press, Cambridge. [ Links ]
74. SACHS, T. & D. COHEN. 1982. Circular vessels and the control of vascular differentiation in plants. Differentiation 21: 22-26. [ Links ]
75. SAVIDGE, R. 2001. Intrinsic regulation of cambial growth. J. Plant Growth Regul. 20: 52-77. [ Links ]
76. SCHMITZ, N., E. M. R. ROBERT, A. VERHEYDEN, J. GITUNDU KAIRO, H. BEECKMAN & N. KOEDAM. 2008. A Patchy Growth via Successive and Simultaneous Cambia: Key to Success of the Most Widespread Mangrove Species Avicennia marina? Ann. Bot. 101: 49-58, [ Links ]
77. SCHWEINGRUBER, F. H. 1992. Annual growth rings and growth zones in woody plants in Southern Australia. IAWA Bull. n.s 13: 359-379 [ Links ]
78. SCHWEINGRUBER, F. H. 2007. Wood structure and environment. Springer Series in Wood Science, Berlin. [ Links ]
79. STEIDTMANN, W. E. 1937. A preliminary report on the anatomy and affinities of Medullosa noei sp. nov. from the Pennsylvanian of Illinois. Am. J. Bot. 24: 124-125. [ Links ]
80. STEVENSON, D. 1990. Morphology and systematics of the Cycadales. Mem. New York Bot. Gard. 57. 8-55 [ Links ]
81. STRASBURGER, E., F. NOLL, H. SCHENCK & A. F. W. SCHIMPER. 2004. Tratado de botánica 35a, ed. Omega, Barcelona. [ Links ]
82. TAYLOR, T. N., E. L. TAYLOR & M. KRINGS. 2009. Paleobotany. The Biology and Evolution of Fossil Plants. Elsevier/Academic Press Inc, Burlington. [ Links ]
83. TERRAZAS, T. 1991. Origin and activity of successive cambia in Cycas (Cycadales). Am. J. Bot. 78: 1335-1344. [ Links ]
84. TERRAZAS, T., S. AGUILAR-RODRÍGUEZ & C. TINOCO OJANGUREN. 2011. Development of successive cambia, cambial activity, and their relationship to physiological traits in Ipomoea arborescens (Convolvulaceae) seedlings. Am. J. Bot. 98:765-774. [ Links ]
85. VAN VEENENDAAL, W. L. H. & R. W. DEN OUTER. 1993. Development of included phloem and organisation of the phloem network in the stem of Strychnos rnillepunctata (Loganiaceae). IAWA J. 14: 253-265 [ Links ]
86. WALTON, J. 1923. On Rhexoxylon Bancroft, a Triassic genus of plants exhibiting a liana-type of vascular organization. Philos. T. R. Soc. Lond., Ser. B 212: 79-109. [ Links ]
87. WORSDELL, W. C. 1896. The anatomy of the stem of Macrozamia compared with that of other genera of Cycadaceae. Ann. Bot. 10: 601-620. [ Links ]
88. WORSDELL, W. C. 1906. The structure and origin of the Cycadaceae. Ann. Bot. 20: 129-155. [ Links ]
89. ZAMUNER, A.B. 1991. Estudio de una tafoflora de la localidad tipo de la Formación Ischigualasto (Neotrías), Provincia de San Juan. Tesis Doctoral Nº 583, Facultad de Ciencias Naturales y Museo, Universidad Nacional de La Plata, 97 pp., 25 pl. Inédito. [ Links ]
90. ZHANG, W., Y. WANG, K. SAIKI, N. LI & S. ZHENG. 2006. A structurally preserved cycad-like stem, Lioxylon liaoningense gen. et sp. nov., from the Middle Jurassic in Western Liaoning, China. Prog. Nat. Sci. 16 (Special Issue): 236-248. [ Links ]
Recibido el 14 de abril de 2011
Aceptado el 1 de septiembre de 2011.














