Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista industrial y agrícola de Tucumán
On-line version ISSN 1851-3018
Rev. ind. agric. Tucumán vol.89 no.2 Las Talitas July./Dec. 2012
ARTÍCULOS ORIGINALES
Análisis del proceso de sulfitación en la remoción de compuestos no azúcares en jugos de variedades de caña de Tucumán (R. Argentina)
B. Silvia Zossi*, Gerónimo J. Cárdenas**, Natalia Sorol* y Marcos Sastre*
*Sección Química de Productos Agroindustriales, EEAOC. silviazossi@eeaoc.org.ar
**Sección Ingeniería y Proyectos Agroindustriales, EEAOC.
Resumen
Se estudió la eficiencia de tres procesos de clarificación mediante sulfitación -sulfitación ácida en frío, sulfitación alcalina en frío y sulfitación en caliente-, en la remoción del color y de algunos compuestos responsables de este en jugos de caña de las cuatro variedades comerciales de caña de azúcar más difundidas en Tucumán, R. Argentina: LCP 85-384, TUCCP 77-42, RA 87-3 y CP 65-357. Mediante sulfitación, se eliminó entre un 40% y 61% de color y más del 40% de compuestos fenólicos, sin diferencias estadísticas entre los tres tratamientos. Los resultados indicaron que los jugos clarificados mediante sulfitación en caliente generalmente resultaron con mayor pureza, con colores comprendidos entre 5000 UI y 6800 UI, turbidez entre 2,67 UA y 8,87 UA, mayor eliminación de compuestos con nitrógeno amínico y una remoción superior al 87% del dióxido de sílice. La eliminación de compuestos protoantocininas fue mayor con la sulfitación ácida en frío. Se adaptó una metodología para el estudio cualitativo de los principales colorantes, tanto en los jugos mixtos como clarificados.
Palabras clave: Clarificación de jugo de caña de azúcar; Sulfitación; Compuestos azúcares y no azúcares.
Abstract
Efficiency of the sulphitation process in removing non-sugar compounds from juices of sugar cane varieties in Tucumán (Argentina)
The efficiency of three clarification processes by sulphitation -acid sulphitation, alkaline sulphitation and hot sulphitation- in removing color and some compounds responsible for it was assessed. The trials were conducted using cane juice from the four most widely planted commercial sugarcane varieties in Tucumán, Argentina: LCP 85-384, TUCCP 77-42, RA 87-3 and CP 65-357. By means of sulphitation, 40% to 61% of color was removed, together with more than 40% of fenolic compounds. The results indicated that regardless of variety, juice clarified by hot sulphitation had the highest purity levels, with its color ranging between 5000 UI and 6800 UI, turbidity between 2.67 UA and 8.87 UA, and the highest removal rate of non sugar compounds. This was especially so in the case of silicon dioxide, which was removed in more than 87%. A method for studying the principal colorants in mixed and clarified sugar cane juices was adapted.
Key words: Sugar cane juice clarification; Sulphitation; Sugar and non sugar compounds.
Introducción
Tucumán produce más del 60% del azúcar total elaborada en la Argentina, con 15 ingenios en actividad, y ocupa el 15º lugar en la producción mundial desde hace cinco años, con un promedio de 1.350.564 t (CART, 2011). De estas 15 fábricas, al menos 11 producen azúcar blanco directo empleando la sulfitación como medio de clarificación, a fin de eliminar partículas suspendidas y coloidales e impurezas no azúcares, solubles e insolubles, para obtener un azúcar de menor color, importante atributo para su comercialización.
En Tucumán, para la producción de azúcar blanco directo la mayoría de las fábricas emplean sulfitación en frío (T1), añadiendo dióxido de azufre en concentraciones comprendidas entre 750 ppm y 1000 ppm, encalan a pH próximo a 7, calientan el jugo a ebullición y luego decantan. En solo alguno de ellos, se pre encala el jugo a un pH comprendido entre 6,0 y 6,5, se calienta a 60ºC - 70ºC, se sulfita (a 800 ppm - 1000 ppm), se calienta a ebullición y se decanta (T3). También existen fábricas que emplean modificaciones de estas metodologías, variando la temperatura inicial del jugo y la concentración de SO2. En algunos ingenios de Brasil se aplica la sulfitación alcalina (T2), añadiendo lechada de cal al jugo mixto hasta un pH de 8,5 - 9,0, sulfitación a pH 7,0 - 7,2, con posterior calentamiento y decantación.
En la literatura, se pueden encontrar trabajos que hablan de los beneficios de la sulfitación en la clarificación de jugos de caña (Abd El-Kader, 1983; Abd El-Kader et al., 1983; Rein, 2007), como así también del comportamiento de algunas variedades de caña de azúcar frente a este proceso, especialmente en India, Egipto y China, pero no están actualizados ni son accesibles. Por este motivo, es importante analizar lo que ocurre con las variedades de caña más cultivadas en nuestra provincia frente al proceso de clarificación por sulfitación.
Es necesario destacar que la principal bibliografía disponible proviene de los Estados Unidos de América, Sudáfrica y Australia, países que no emplean la sulfitación como metodología de clarificación. Es ampliamente conocido el hecho de que el color del jugo de caña influye en gran medida en el color del azúcar y que depende especialmente de la cantidad de sustancias colorantes presentes en la caña, tales como clorofila, xantofilas y antocianinas, y de la concentración de polifenoles y aminoácidos. Estas sustancias, aunque son incoloras, desarrollan color durante el proceso (Godshall, 1996).
Se debe mencionar que las prácticas agrícolas afectan los niveles de aminoácidos en la caña, y dosis excesivas de fertilizantes resultan en concentraciones mayores de estos compuestos en los jugos (Paton, 1992). Aunque la autora no menciona los niveles de nitrógeno que pueden resultar perjudiciales para el proceso de elaboración de azúcar, en Tucumán es práctica común fertilizar la caña de azúcar con concentraciones promedio de 90 kg a 100 kg N/ ha por año(1). (1) Sanzano, G. A. 2012. Comunicación personal.
En un trabajo anterior (Zossi et al., 2010), se estudió la calidad industrial de las cuatro variedades de caña de azúcar más cultivadas en Tucumán: LCP 85-384, TUCCP 77-42, RA 87-3 y CP 65-57, que ocupan un 96% de la superficie sembrada (Cuenya et al., 2009). Se analizaron no solo los compuestos azúcares en los jugos de primera presión, sino también los principales no azúcares en los jugos mixtos que influyen en el color y en la calidad del azúcar.
El objetivo de este trabajo fue estudiar el comportamiento de esas cuatro variedades de caña frente a tres procesos de clarificación de jugo empleando sulfitación, de modo de establecer su efectividad en la remoción de color y de algunos compuestos responsables de este.
Materiales y métodos
Se utilizaron los jugos mixtos obtenidos en un trabajo anterior (Zossi et al., 2010) procedentes de caña limpia, despuntada y sin "trash", que inmediatamente fueron sometidos a tres procesos de clarificación empleando anhídrido sulfuroso y cal, semejantes a aquellos utilizados por la industria local y la de otros países, para la obtención de azúcar blanco directo, usándose dióxido de azufre gaseoso y lechada de cal de 10ºBe. Los tratamientos usados fueron:
. Tratamiento 1: sulfitación ácida en frío (T1). Se añadió dióxido de azufre al jugo de caña, hasta una concentración de 800 mg/l y luego se neutralizó con lechada de cal hasta alcanzar un pH de 7,2.
. Tratamiento 2: sulfitación alcalina en frío (T2). Se agregó al jugo lechada de cal hasta un pH de 9,0 y, posteriormente, dióxido de azufre hasta un pH de 7,0, con una concentración promedio de 800 mg/l de SO2.
. Tratamiento 3: sulfitación en caliente (T3). Se alcalinizó el jugo hasta pH 6,0 con lechada de cal, se calentó entre 65ºC y 70ºC, se sulfitó con 800 mg/l de SO2 y se añadió nuevamente cal hasta pH 7,2.
Posteriormente, se calentaron los jugos a ebullición durante tres minutos para eliminar el aire y se agregaron 3 mg/l de un polielectrolito floculante convencional (Separan AP), transfiriéndolos luego a probetas graduadas de vidrio de 500 ml, colocadas en un baño de agua termostatizado a una temperatura cercana a la ebullición. Se determinó la velocidad de sedimentación inicial (VSI) midiendo el volumen de lodos precipitados en el tiempo. Para determinar VSI (Copersucar, 2004), se graficaron estos volúmenes en función del tiempo, escogiéndose los puntos comprendidos en la fase inicial de la decantación donde la curva presenta mayor linealidad, siendo además la fase en que no interfieren los flóculos sedimentados (Rein, 2007).
De la gráfica se obtuvo una ecuación de la forma:
V = at + b (Ecuación 1)
Donde:
V = volumen de lodos en cm3;
a = pendiente de la recta en cm3/seg;
b= ordenada al origen, en cm3.
VSI se obtuvo derivando la Ecuación 1:
dV/dt = a [cm3/seg] (Ecuación 2)
Para expresar VSI en cm/min, se multiplicó la ecuación anterior por la altura de la probeta (24,2 cm) y por 60 seg/min y se dividió por el volumen de la probeta (500 cm3).
El volumen final de cachaza fue determinado una hora después de iniciado el ensayo.
También se llevó a cabo un estudio sobre los colorantes presentes en los jugos mixtos y clarificados, adaptando la metodología propuesta por Bento (1995a y b) para el proceso de refinación de azúcar. Para ello, se determinaron los espectros en la región UV entre 220 nm y 340 nm de soluciones de jugo a pH 9,0 ± 0,1, diluidas de manera tal que su absorbancia esté comprendida entre 0,300 y 0,800 a 273 nm. Los valores de L (del inglés "low wavelength fraction") y de H (del inglés "high wavelength fraction") fueron calculadas mediante la siguiente expresión (Bento, 1995a):
L ó H = (λ2 - λ1) x ∫ (Abs / Abs0) dλ) (Ecuación 3)
Esta integral fue evaluada entre los límites λ1 y λ2. Para el cálculo de L estos valores fueron 220 nm y 273 nm, respectivamente. Para el cálculo de H, se usaron λ1 y λ2 iguales a 273 nm y 340 nm, respectivamente. Abs representa las lecturas de absorbancia a diferentes longitudes de onda y Abs0, la absorbancia a 273 nm. En la Figura 1 se muestra un ejemplo de cálculo de L y H (Bento, 1995a).

Figura 1. Ejemplo de cálculo de L y H (Bento, 1995a), donde Lλf y Hλf corresponden a L y H, respectivamente.
Se prepararon en el laboratorio soluciones de algunos de los principales colorantes existentes en el jugo de caña y en el proceso de elaboración de azúcar (tales como melanoidina, productos de degradación ácida y alcalina, caramelo, melanina, ácido cafeico y ácido cromogénico), empleando la metodología propuesta por McGinnis and Muller (1984). Se determinaron sus espectros en el UV, obteniéndose sus correspondientes valores de L y H. Los valores de L y H de ácido cumárico, melanoidina y catecol fueron obtenidos de la literatura (Bento, 1995 a y b).
Para determinar L y H de acuerdo a la Ecuación 3, se empleó una hoja de cálculo Excel con un programa desarrollado por Will(2). (2) Dr. Will, A. (UNT). Comunicación personal, año 2006.
Para comparar el comportamiento de los jugos de las cuatro variedades estudiadas frente a los tres métodos de clarificación, se llevaron a cabo las siguientes determinaciones:
. Brix % jugo, empleando un refractómetro Leica AR 600; pol % jugo, mediante un polarímetro Optical Activity PolAAr20, y pureza.
. Concentración de dióxido de azufre de acuerdo a Copersucar (2004).
. Almidón, según el método propuesto por Godshall (2004) y validado por Zossi et al. (2008b).
. Fosfatos y cenizas sulfatadas, de acuerdo a la metodología ICUMSA (ICUMSA, 2005).
. Color con el método ICUMSA GS1/3-7 (ICUMSA, 2005).
. Turbidez, según ICUMSA (2005), solo en los jugos clarificados.
. Compuestos antocianos, según Godshall et al. (1996).
. Compuestos fenólicos, expresados como ácido cafeico, de acuerdo a la metodología propuesta por Clarke et al. (1985).
. Sílice soluble, basada en la metodología establecida por la South African Sugar Technologists' Association (SASTA, 2005).
. Sacarosa real, por cromatografía líquida de alta resolución, empleando una bomba Waters 590, un detector Waters 410 de índice de refracción y una columna Sugar Pak, de Waters.
. Ácidos cis y trans-aconítico, por cromatografía líquida de alta performance (HPLC), de acuerdo a Zossi et al. (2008a), en un cromatógrafo Waters compuesto de un detector de arreglo de diodos DAD 2996, bomba y autosampler 717 plus y columna Spherisorb ODS 1 de Waters.
. Nitrógeno amínico, según Smith and Gregory (1971) y Clarke et al. (1985).
. Sólidos remanentes en el jugo claro, mediante filtración de 50 ml de jugo a través de membrana de 8 µ, por diferencia de peso, luego de lavar y secar en estufa a 105ºC.
. Cationes calcio, magnesio y potasio por espectroscopia de absorción atómica (PerkinElmer, 2000).
En todas las técnicas colorimétricas, excepto para turbidez, se empleó un espectrofotómetro Hewlett Packard 8452A. La turbidez se determinó mediante un espectrofotómetro Agilent 8453.
Las determinaciones analíticas fueron realizadas en un laboratorio de la Estación Experimental Agroindustrial Obispo Colombres (EEAOC) certificado bajo Norma ISO 9001: 2000, cumpliendo con los lineamientos para asegurar la calidad del dato analítico.
El análisis estadístico de los datos se efectuó mediante análisis de la varianza, con un diseño totalmente al azar, usando el software Infostat. La comparación de medias se realizó con el test de Tuckey a un nivel de confianza del 5%.
Para llevar a cabo las comparaciones entre los jugos claros obtenidos mediante los tres tratamientos estudiados y los jugos mixtos originales, se tomaron los valores de los compuestos no azúcares para estos últimos, determinados en un trabajo anterior (Zossi et al., 2010), que se detallan en las Tablas 1 y 2. Se presentan, además, los valores de Brix, pol y pureza obtenidos para dichos jugos.
Tabla 1. Valores promedio de Brix%, pol%, pureza%, ácido cis-aconítico, ácido trans-aconítico y dióxido de silicio en los jugos mixtos de las cuatro variedades estudiadas.

Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Tabla 2. Valores promedio de fosfatos, color y compuestos fenólicos, antocianos y con nitrógeno amínico y almidón.

Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Resultados y discusión
Velocidad inicial de sedimentación (VSI)
Por la importancia de la VSI en el proceso de clarificación, se la determinó experimentalmente para cada una de las variedades estudiadas y para cada tratamiento de clarificación empleado. Se graficaron los volúmenes de lodos precipitados en función del tiempo (Tabla 3), lo cual se muestra en las Figuras 2, 3, 4 y 5. Las gráficas allí expuestas resultaron del promedio de los ensayos realizados durante los tres años estudiados.
En las figuras mencionadas se observa, para todas las variedades analizadas, que los tratamientos 1 y 2 dieron curvas del tipo a, en los que la sedimentación se mantiene continua y a una velocidad rápida y uniforme, hasta que la suspensión alcanza el volumen final de lodos. En tanto, el tratamiento 3 produjo una curva del tipo b, en la que inicialmente existe una velocidad de sedimentación constante, pero que pronto comienza a disminuir con el tiempo y entra en lo que muchos autores han descrito como la zona de compresión (Raha, 1977).
Tabla 3. Valores promedio de tiempos de sedimentación, desviación estándar y CV% para cada volumen leído.
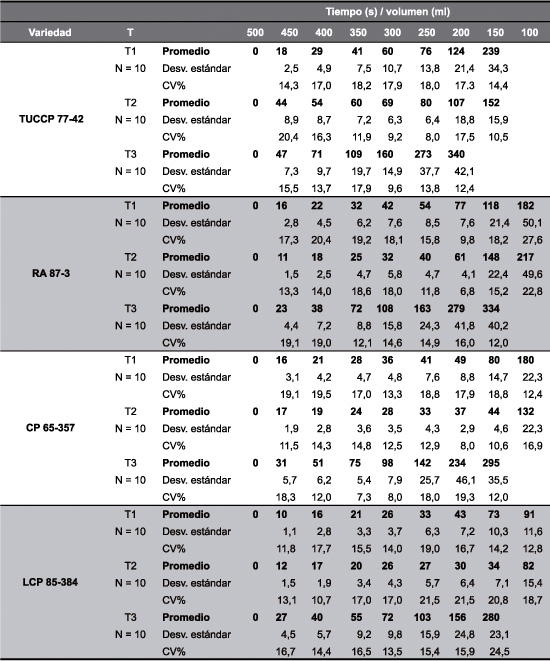
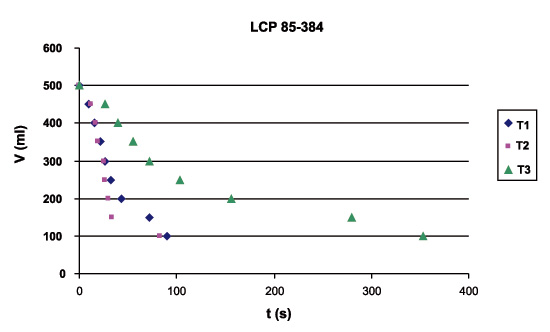
Figura 2. Volumen promedio decantado en función del tiempo para los tres tratamientos de clarificación de jugos de LCP 85-384.

Figura 3. Volumen promedio decantado en función del tiempo para los tres tratamientos de clarificación de jugos de TUCCP 77-42.

Figura 4. Volumen promedio decantado en función del tiempo para los tres tratamientos de clarificación de jugos de RA 87-3.

Figura 5. Volumen promedio decantado en función del tiempo para los tres tratamientos de clarificación de jugos de CP 65-357.
Los resultados de VSI obtenidos mediante la Ecuación 2 se presentan en la Tabla 4.
Tabla 4. Velocidades promedio en cm/min de sedimentación para los tres tratamientos de clarificación, en las cuatro variedades de caña.
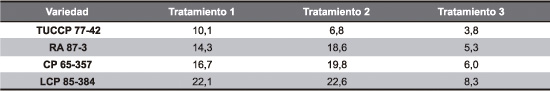
La variedad LCP 85-384, la de mayor velocidad de sedimentación, presentó velocidades semejantes para los tratamientos 1 y 2, resultando la velocidad del tratamiento 3 un 60% inferior. Para TUCCP 77-42, la variedad con menor velocidad de sedimentación, la velocidad del tratamiento 1 fue superior en más del 30% a la del tratamiento 2 y en más del 60% respecto a la del tratamiento 3. Para las dos variedades restantes, RA 87-3 y CP 65-357, la menor velocidad de decantación se obtuvo con el tratamiento 3 y la mayor con el tratamiento 2, siendo estas velocidades semejantes para ambas variedades. Los resultados obtenidos fueron menores a los determinados por Doherty et al. (2002) (VSI cercanas a 37 cm/min en jugos encalados a temperaturas de 36ºC y 76ºC) por tratarse de jugos limpios, sin tierra y sin "trash".
De acuerdo a Rein (2007), la velocidad de sedimentación y el volumen de lodos dependen de la reacción del medio en el cual se forma el precipitado, pero en la práctica, cuando se encala antes de sulfitar, la velocidad de decantación es menor y el volumen de lodos es mayor, con flóculos más hidratados. Esto se cumple solo para la variedad TUCCP 77-42, ya que para las otras tres siempre se obtuvieron mayores velocidades de sedimentación con el tratamiento 2. Bliss (1947) informó que es conveniente sulfitar antes de encalar, para asegurar la precipitación del sulfito de calcio en medio ácido y obtener una buena velocidad de decantación, lo que se cumple para TUC 77-42, pero no para las otras tres variedades.
Nuestro laboratorio determinó la viscosidad de los jugos clarificados, encontrándose valores comprendidos entre 1,70 cp y 1,85 cp a 25ºC, considerando la viscosidad del agua como igual a 1,00 cp, a la misma temperatura. Debido a la poca variabilidad de la viscosidad, podría decirse que la velocidad de sedimentación está influenciada principalmente por el diámetro de las partículas y la densidad del sólido.
En la Tabla 5, se presentan los valores de volumen de cachaza para cada variedad y tratamiento, luego de una hora de decantados, y el coeficiente de variabilidad porcentual (CV%) para el número de muestras analizadas (N), para los tratamientos en estudio (Ti).
Tabla 5. Valores promedio de volumen de cachaza al cabo de una hora y sólidos remanentes en el jugo claro.
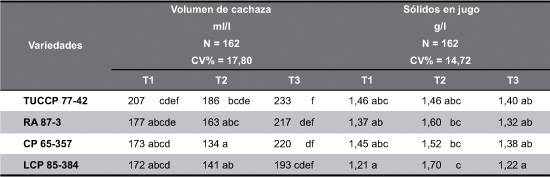
Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
En el volumen de cachaza solo se encontraron diferencias estadísticamente significativas entre los valores obtenidos mediante los tratamientos 2 y 3 para todas las variedades. No se determinaron diferencias estadísticas en la concentración de sólidos remanentes en el jugo claro, excepto para la variedad LCP 85-384, entre T1 y T3 con respecto a T2.
No se encontraron en la literatura concentraciones de sólidos remanentes en el jugo claro, pero es probable que los valores determinados en este trabajo sean mayores a los encontrados en la industria, especialmente por el tipo de equipo empleado, asimilable a un decantador de una sola bandeja.
Estas determinaciones fueron realizadas solamente para comparar variedades y tratamientos.
En la Tabla 6 se presentan los valores promedio de Brix, pol, pureza y sacarosa, obtenidos de las 176 muestras de jugos clarificados mediante los tres tratamientos estudiados.
No se encontraron diferencias significativas para ninguno de estos parámetros.
Tabla 6. Valores promedio de Brix, pol% jugo, pureza y sacarosa real en 176 muestras de las cuatro variedades estudiadas.
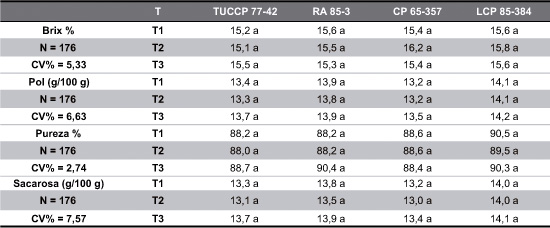
Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
La pureza aparente es la herramienta usada universalmente para determinar la calidad del jugo de caña y la eficiencia de la clarificación. Kulkarni (1996) dice que la pureza en los jugos clarificados puede variar entre -0,3 y 0,4 respecto al jugo mixto. La variación absoluta de la pureza para los tres tratamientos estudiados en las cuatro variedades, considerando los resultados presentados en las Tablas 1 y 4, se presentan en la Tabla 7.
Tabla 7. Variación absoluta en la pureza de los jugos clarificados respecto a los mixtos.

Esta variación absoluta de la pureza, mayor a la indicada en la literatura, podría deberse a que se trabajó con cañas limpias, sin tierra, despuntes ni hojas. Se obtuvieron mayores incrementos con T1 para CP 65-357, sin diferencias con T2, y LCP 85-384; para las dos variedades restantes las mayores diferencias de pureza se lograron con T3.
Abd El-Kader et al. (1983) determinaron incrementos de 0,76 de pureza en jugos de caña clarificados mediante el tratamiento 2. Los valores aquí determinados también son coincidentes con los hallados por Mehrotra et al. (2009) e iguales a 0,80.
En la Tabla 8 se presentan los resultados promedio para color, turbidez y compuestos fenólicos, antocianos y con nitrógeno amínico, encontrados en los jugos de las cuatro variedades clarificados mediante los tres tratamientos.
Para color no se determinaron diferencias estadísticas entre tratamientos, pero sí entre variedades.
Tabla 8. Valores promedio de color, turbidez, compuestos fenólicos (expresados como ácido cafeico), compuestos antocianos (expresados como unidades de absorbancia) y compuestos con nitrógeno amínico, para los jugos de las cuatro variedades clarificados con los tres tratamientos ensayados.
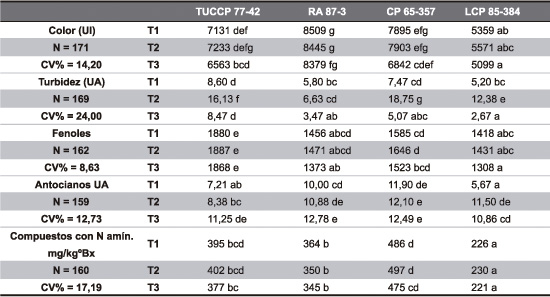
Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
La menor turbidez para todas las variedades se obtuvo con el tratamiento 3, con diferencias estadísticamente significativas con el tratamiento 2 en todos los casos y, solo para LCP 85-384, también con el tratamiento 1. Esto concuerda también con los resultados mostrados en la Tabla 5, ya que clarificando los jugos de caña con el tratamiento 3, se encontró siempre un mayor volumen de cachaza, estimándose una menor concentración de sólidos remanentes en el jugo clarificado.
Tampoco se determinaron diferencias significativas para compuestos fenólicos y con nitrógeno amínico entre tratamientos, pero sí entre variedades, y fueron semejantes a las determinadas para los jugos mixtos.
De acuerdo a Sharma (1977), la concentración de compuestos polifenólicos en el jugo de caña incide negativamente en la velocidad de sedimentación; esto se confirma comparando los valores de las Tablas 2 y 4: LCP 85-384, con menor contenido de estos compuestos, tiene la mayor velocidad de sedimentación para los tres tratamientos de clarificación, mientras que lo opuesto ocurre con TUCCP 77-42.
En la Tabla 9, se presenta la fracción promedio de estos compuestos removidos después de la clarificación respecto a su contenido en los jugos mixtos, expresados como eficiencia en su remoción: (contenido en JM - contenido JC)*100/ (contenido en JM). Los valores obtenidos para los jugos mixtos se informaron en la Tabla 2.
Tabla 9. Porcentajes promedio de remoción de color, fenoles, compuestos antocianos y con nitrógeno amínico en los jugos clarificados.

La eliminación del color de los jugos clarificados estuvo comprendida entre el 41% y el 61%, siendo siempre mayor con el tratamiento 3 para todas las variedades analizadas, especialmente TUCCP 77-42 y LCP 85-384, que mostraron valores superiores en más de un 15% a los determinados por Saska et al. (2010) mediante sulfitación para caña procesada con "trash". Estas diferencias se deberían no solo a las concentraciones mayores de SO2 empleadas en este trabajo, sino también a la calidad de la caña empleada (limpia, sin tierra y sin "trash") y a la influencia que tiene la variedad de caña sobre el color (Ivin and Doyle, 1989).
El tratamiento 3 es el que permitió eliminar mayor cantidad de color, tal como se muestra en la Tabla 9, a pesar de que presentó siempre la menor velocidad de decantación y el mayor volumen de lodos para las cuatro variedades estudiadas.
El contenido de compuestos fenólicos eliminados en los jugos clarificados fue mayor al 40% en todos los casos, lo que concuerda con lo expresado por Kulkarni (1996). Godshall and Legendre (1988) afirman que los compuestos fenólicos, especialmente fracciones de alto peso molecular, son eliminados en un 30% a 50% durante la clarificación, dependiendo de las condiciones de trabajo. Esta disminución es importante, ya que existe una correlación positiva entre la concentración de compuestos fenólicos y el color del azúcar, blanco o crudo (Simioni et al., 2006).
De acuerdo a la literatura (Paton, 1992, Kulkarni, 1996), los compuestos antocianos son inestables y, en general, son eliminados durante la clarificación. En este trabajo, se encontró que se remueven entre un 30% y un 66%, dependiendo de la variedad y tratamiento, pero en todas las variedades se eliminaron mayores concentraciones de estos compuestos con T1. El porcentaje remanente en el jugo podría deberse a que esta metodología solo determina los compuestos antocianos unidos a polisacáridos (proantocianidinas) (Godshall et al., 1996).
Rupa and Asokan (2008) expresaron que concentraciones mayores a 600 mg/kg de compuestos con nitrógeno amínico incrementarían la formación de color durante la etapa de evaporación. De acuerdo a esto y a los valores mostrados en la Tabla 8, ninguna de las variedades estudiadas presentaría este problema, independientemente del procedimiento de clarificación empleado. En la Tabla 9, se observa que el tratamiento 3 fue siempre el más efectivo para la eliminación del color en todas las variedades analizadas, lo que concuerda con lo expresado por Kulkarni (1996), quien afirma que el pre encalado del jugo reduce el contenido de aminoácidos.
Es importante destacar las desigualdades determinadas entre variedades en las concentraciones eliminadas de compuestos con nitrógeno amínico, lo que podría deberse a diferencias en su composición (Honig, 1969). Este tema debería ser estudiado con mayor profundidad.
Aunque en este trabajo no se hace mención a las concentraciones de azúcares reductores, es importante destacar que en las variedades analizadas los valores máximos determinados por HPLC para glucosa y fructosa fueron de 0,16 g y 0,15 g/100 ml de jugo respectivamente, tanto en los jugos mixtos como en los clarificados, en cañas frescas sin deterioro (Zossi et al., 2011)(3). (3)Zossi, B. S.; N. Sorol; R. Torres y S. Medina. 2011. Resultados de análisis de azúcares por HPLC en variedades de caña de azúcar. Informe interno, Sección Química, EEAOC.
En la Figura 6, se presenta un esquema con los principales colorantes presentes en el jugo mixto de caña para cada variedad, como así también aquellos remanentes luego de la clarificación, determinados mediante la Ecuación 3. Se graficaron los valores promedio de las funciones L y H obtenidas durante todo el período analizado, dados en las Tablas 10 y 11, respectivamente, junto con los valores de CV% determinados.
Como puede observarse en la Figura 6, existe una posición determinada en el plano L-H para algunos de los colorantes detectados en los jugos de caña de azúcar, tanto mixtos como clarificados.
Para todos los jugos analizados, tanto mixtos como clarificados, las posiciones determinadas fueron L > 1 y H < 1, siendo los principales colorantes pertenecientes a este grupo catequina, melanina, melanoidina y productos alcalinos de degradación (Bento, 1995a y b). La posición encontrada dependerá exclusivamente del tipo y concentración de los colorantes existentes, por lo que es posible obtener un mismo punto con concentraciones y colorantes diferentes.

Figura 6. Colorantes en jugos mixtos y clarificados.
Nota: ácida y alcalina corresponden a productos de la reacción de Maillard ácida y alcalina, respectivamente.
Tabla 10. Valores promedio y CV% de L para los jugos mixtos y clarificados de las cuatro variedades de caña estudiadas.
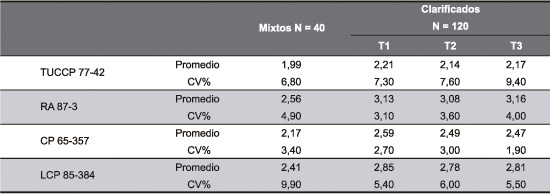
Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Tabla 11. Valores promedio y CV% de H para los jugos mixtos y clarificados de las cuatro variedades de caña estudiadas.

Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
En la Figura 6 es posible observar también los desplazamientos en el plano experimentados por los jugos clarificados, indicando estas posiciones relativas cambios en las concentraciones de los colorantes presentes.
La posición del jugo clarificado, con un desplazamiento hacia la derecha y abajo del plano L-H, muestra con diferente intensidad, según la variedad y tratamiento, la eficiencia de la eliminación de colorantes en el proceso de clarificación. Los resultados promedio de L mostrados en la Tabla 10 señalan que los valores de L en los jugos claros obtenidos por los tres tratamientos son mayores que sus correspondientes mixtos. Esto indicaría que durante la clarificación se eliminaron compuestos de bajo L, entre ellos, ácido cafeico y algunos compuestos fenólicos.
En la Tabla 11, se observa que los valores promedio de H de los jugos clarificados son inferiores a los obtenidos para los jugos mixtos, lo que significaría que mediante los tratamientos de clarificación empleados se eliminaron colorantes de H altos, principalmente polifenoles (Bento, 1995a y b).
Es importante destacar que esta metodología fue desarrollada por Bento (1995 a y b) para analizar el proceso de refinación de azúcar; el jugo de caña, de composición más compleja, podría tener otros componentes que también absorben en la región del UV, por lo que sería importante profundizar este estudio.
No azúcares orgánicos
Los valores de almidón en los jugos claros fueron siempre menores a 25 mg/kg, límite de cuantificación del método (Zossi et al., 2008b). Esto mostraría que el almidón fue eliminado en la etapa de clarificación por un proceso físico (precipitación) o químico, debido a su degradación por enzimas naturales presentes en el jugo durante el calentamiento (Eggleston et al., 2003).
Las concentraciones de ácidos cis- y trans-aconítico se presentan en la Tabla 12, mientras que en la Tabla 13 se indican los porcentajes de estos eliminados en cada tratamiento de clarificación, en relación a los jugos mixtos (Tabla 1).
Tabla 12. Contenidos promedio de las concentraciones de ácidos cis y trans-aconítico en los jugos clarificados de las cuatro variedades de caña de azúcar.

Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Tabla 13. Porcentajes de cada isómero eliminado en cada tratamiento de clarificación.
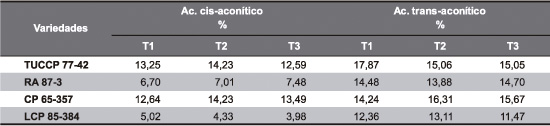
Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Los resultados obtenidos (Tabla 12) indican que no existen diferencias significativas entre los tratamientos de clarificación empleados, sino solo entre variedades, siendo estas diferencias las mismas que las determinadas en los jugos mixtos (Zossi et al., 2010).
Datos bibliográficos (Hanine et al., 1990) indican que, en la clarificación por sulfitación, se elimina un 16% del ácido aconítico y que la mayor parte de este que ingresa a la fábrica con la caña se concentra en el jarabe y, eventualmente, en la melaza (Mane et al., 2002). Como se observa en la Tabla 13, los porcentajes eliminados de ácido cis-aconítico varían entre el 4% y el 14% para las cuatro variedades estudiadas, eliminándose mayor porcentaje en los jugos con más alta concentración inicial. También es variable la cantidad de ácido trans-aconítico eliminado por los tres tratamientos (entre el 11% y el 18%) en las cuatro variedades de caña. Ninguno de los procedimientos de clarificación estudiados permitió disminuir un mayor porcentaje de las concentraciones de este compuesto en las variedades evaluadas. La eliminación de estos ácidos es importante ya que podrían estar asociados a un colorante de alto peso molecular en el azúcar crudo (van der Poel et al., 1998).
Cenizas y cationes
En la Tabla 14 se presentan los valores promedio de cenizas sulfatadas obtenidas para los jugos mixtos y clarificados de las cuatro variedades estudiadas.
Tabla 14. Valores promedio de cenizas sulfatadas en los jugos de caña.

Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Los resultados obtenidos, con un coeficiente de variabilidad porcentual cercano al 12%, son concordantes con los reportados en la bibliografía (Rein, 2007). Las diferencias estadísticas encontradas entre LCP 85-384 y las restantes variedades son acordes a aquellas determinadas años anteriores por Cárdenas et al. (2000) y Diez et al. (2000) empleando el mismo tipo de cosecha.
De acuerdo a Chen (1985), en numerosas investigaciones realizadas se encontraron diferencias en el contenido total de cenizas antes y después de la clarificación, aunque su composición cambia, lo que se explicaría porque a pesar de que se eliminan fosfato, sílice y otros constituyentes, esto se compensaría por el incremento de algunos compuestos con calcio. Las cenizas en los jugos claros resultaron entre 10% y 20% superiores a las determinadas en los jugos mixtos. Según Honig (1969), estas diferencias en las cenizas dependen también del pH de encalación: a mayor pH, menores diferencias.
En la Tabla 15 se presentan los valores promedio de cationes mayoritarios -calcio, magnesio y potasio- determinados en el jugo mixto, mientras que en la Tabla 16 se muestran los correspondientes a los jugos clarificados.
Tucumán posee suelos con alto contenido en potasio, lo que se refleja en las elevadas concentraciones obtenidas, superiores a los referidos por Chen (1985) para Estados Unidos. Los de calcio y magnesio concuerdan con los mencionados en la literatura. Estos valores son semejantes a los determinados en la EEAOC años atrás empleando metodologías diferentes: volumetría para calcio y magnesio y fotómetro de llama para potasio (Diez, 2012)(4), siendo notable la concentración de K en TUCCP 77-42 frente a las otras variedades. (4)Diez, O. (EEAOC). Comunicación personal, año 2012.
Tabla 15. Valores promedio de calcio, magnesio y potasio en 33 muestras de jugo mixto.

Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
Tabla 16. Valores promedio de calcio, magnesio y potasio en los jugos clarificados obtenidos.

Los valores promedio de los cationes analizados en los tres tratamientos de clarificación son muy próximos entre sí para cada variedad estudiada, con diferencias comprendidas entre ± 10%. Para el calcio, se determinaron valores superiores en un 10% a los obtenidos en el jugo mixto; Honig (1969) menciona incrementos de hasta un 35% en jugos clarificados mediante defecación en Louisiana (Estados Unidos). Para magnesio y potasio, los valores en los jugos claros fueron entre 1% y 11% menores.
Debido a los altos valores de CV% obtenidos (mayores al 35%), no se realizó análisis de la varianza. Por este motivo sería conveniente continuar con el estudio del comportamiento de cationes, especialmente del calcio, durante el proceso de clarificación por sulfitación.
Fósforo y silicio
En todas las muestras de jugos clarificados bajo los tres tratamientos ensayados, el contenido de fosfato fue siempre menor a 7 mg/l, límite de cuantificación del método para las condiciones de trabajo de nuestro laboratorio. Honig (1969) y Chen (1985) sugirieron que la concentración de fosfato inorgánico remanente en el jugo clarificado no debería ser menor a 10 mg/l. Si esto ocurriera, podría deberse a un sobreencalado del jugo, condición acompañada por un alto contenido de compuestos no azúcares en el jugo clarificado. A pesar de que las concentraciones de fosfato en los jugos claros fueron menores a 10 mg/l, no se determinaron altos incrementos en las concentraciones de calcio y se obtuvieron disminuciones aceptables de compuestos no azúcares en los jugos claros.
En la Tabla 17 se muestran los contenidos de dióxido de silicio en los jugos de las cuatro variedades de caña, clarificados mediante los tres tratamientos.
Se observan diferencias estadísticamente significativas entre variedades y tratamientos, siendo siempre menores las concentraciones de este compuesto en los jugos sulfitados mediante el tratamiento 3. El tratamiento 2 presentó siempre las mayores concentraciones, lo que podría deberse a la mayor cantidad de cal empleada durante la clarificación. De acuerdo a van der Poel et al. (1998), la lechada de cal podría añadir una cantidad apreciable de sílice soluble al jugo, porque su contenido en este compuesto podría superar al 1%.
Tabla 17. Valores promedio de dióxido de silicio en los jugos clarificados.
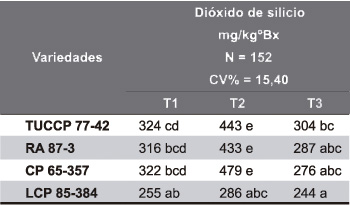
Valores promedio seguidos por la misma letra no difieren estadísticamente entre sí (Tuckey, P= 0,05).
En la Tabla 18 se presentan los porcentajes eliminados, expresados como eficiencia de remoción, para el dióxido de silicio en cada uno de los tratamientos, respecto a su contenido en jugo mixto (Tabla 1).
Los valores de sílice soluble eliminados durante la clarificación mediante sulfitación fueron siempre superiores con el tratamiento 3 (más del 87%) y en todos los casos resultaron mayores al porcentaje de 40%, mencionado por Lionnet and Walthew (2004) cuando emplearon defecación. Walthew et al. (1998) expresaron que este compuesto no se remueve apreciablemente durante la clarificación por defecación y que las concentraciones remanentes causan impactos de incrustaciones en los evaporadores. Además, las concentraciones de dióxido de silicio remanentes en el jugo claro podrían contribuir a la formación de flóculos ácidos en bebidas elaboradas con azúcares de este tipo (van der Poel et al., 1998).
Tabla 18. Valores promedio de dióxido de silicio en los jugos clarificados.

Conclusiones
De los resultados obtenidos en este trabajo, puede concluirse lo siguiente:
. De las cuatro variedades de caña comerciales, LCP 85-384 fue la que presentó jugos claros de mayor calidad, con mayor velocidad de sedimentación, mayor concentración de sacarosa y menor concentración de compuestos no azúcares, independientemente del tratamiento de clarificación empleado.
. Empleando sulfitación se eliminó entre el 40% y el 61% del color y más del 40% de compuestos fenólicos.
. El tratamiento 3, sulfitación en caliente, fue el de menor velocidad de sedimentación para todas las variedades estudiadas y el que produjo mayor volumen de cachaza y menor turbidez en los jugos claros.
. No se encontraron diferencias estadísticamente significativas para el color entre los tratamientos, pero sí entre variedades, concordando con lo que dice la literatura.
. Con el tratamiento 3 se obtuvieron jugos con valores de color comprendidos entre 5000 UI y 6800 UI y turbidez en un rango entre 2,67 UA y 8,87 UA, dependiendo de la variedad.
. No sobresalió ninguno de los tres tratamientos estudiados respecto a la eliminación de los ácidos cis y trans-aconítico.
. Con la sulfitación ácida en frío (T1) se eliminó mayor porcentaje de protoantocianinas.
. Con la sulfitación en caliente (T3) se eliminó más del 87% de la sílice soluble en los jugos de caña.
. Se estableció una metodología para estudiar la calidad industrial de variedades de caña de azúcar liberadas y a liberar frente al proceso de clarificación por sulfitación. Con este procedimiento, se pone especial énfasis en la eliminación de compuestos que contribuyen a la formación de color, lo que permitiría obtener un azúcar blanco directo de mejor calidad.
. Se adaptó una metodología para el estudio de los principales colorantes en el jugo de caña de azúcar.
Bibliografía citada
1. Abd El-Kader, A. 1983. Comparative study on various constituents of sugar cane juice affecting settling in the sulphitation and phosphatation processes. En: Proc. ISSCT Congress, 18, Cuba, 1983, pp. 1207-1221. [ Links ]
2. Abd El-Kader, A; M. Abd El-Kader and A. A. Yassin. 1983. Influence of clarification on sugar cane juices by the sulphitation and phosphatation processes. En: Proc. ISSCT Congress, 18, Cuba, 1983, pp. 507-530. [ Links ]
3. Bento, L. S. M. 1995a. UV spectrophotometric analysis of cane sugar colorants. Zuckerindustry 120 (1995): 19 - 22. [ Links ]
4. Bento, L. S. M. 1995b. Applications of UV spectrophotometry to study sugar colorants throughout the refining process. En: Proc. of SIT Conference, pp. 219 - 237. [ Links ]
5. Bliss, L. R. 1947. La cinética de la sedimentación del jugo de la caña. En: Memoria de la Conferencia Anual de Técnicos Azucareros de Cuba, 21, La Habana, Cuba, 1947, pp. 217-229. [ Links ]
6. Cárdenas, G.; O. Diez; S. Zossi y M. Coronel. 2000. Influencia de diferentes sectores del tallo en el comportamiento industrial de variedades de caña de azúcar de maduración temprana en Tucumán. Rev. Ind. y Agríc. de Tucumán 77 (2): 29-37 [ Links ]
7. Centro Azucarero Regional de Tucuman (CART). 2011. Estadísticas azucareras 2010 (compendio). CART, San Miguel de Tucumán, R. Argentina. [ Links ]
8. Chen, J. C. P. 1985. Cane sugar handbook. 11. ed. John Wiley, New York, USA. [ Links ]
9. Clarke, M. A.; R. S. Blanco; M. A. Godshall and T. B. T. To. 1985. Colour components in sugar refinery processes. Proc. Sugar Industry Technol. 44: 53-88. [ Links ]
10. Copersucar. 2004. Métodos de análisis em açúcar, álcool e processos. Versào 03. [CD ROM]. Centro de Tecnología Copersucar, Estado de São Paulo, Brazil. [ Links ]
11. Cuenya, M. I.; S. Ostengo; E. Chavanne; M. Espinosa; D. Costilla y M. Ahmed. 2009. Variedades comerciales de caña de azúcar: estimación de su área de cultivo en Tucumán en la campaña 2007/2008. Avance Agroind. 30 (4): 10-13. [ Links ]
12. Diez, O.; S. Zossi; E. R. Chavanne y G. Cárdenas. 2000. Calidad industrial de las variedades de caña de azúcar de maduración temprana LCP 85-384 y LCP 85-376 en Tucumán. Análisis de sus principales constituyentes físicos-químicos. Rev. Ind. y Agríc. de Tucumán 77 (2): 39-48. [ Links ]
13. Doherty, W. O. S.; J. Greenwood; D. Pilaski and P. G. Wright. 2002. The effect of liming conditions in juice clarification. Proc. Aust. Soc. Sugar Cane Technol. 24: 443-451. [ Links ]
14. Eggleston, G.; A. Monge and B. Ogier. 2003. Sugarcane factory performance of cold, intermediate and hot lime clarification processes. J. of Food Processing Preservation 26: 433-454. [ Links ]
15. Godshall, M. A. 1996. Recent progress in sugar colorants. En: Proc. Conf. on Sugar Processing Research, New Orleans, LA, USA, pp. 262 - 285. [ Links ]
16. Godshall, M. A. 2004. Collaborative study on starch in raw sugar using the SPRI rapid starch method. En: Proc. SPRI Conference, Atlanta, Georgia, USA, pp. 442-448. [ Links ]
17. Godshall, M. A. and B. Legendre. 1988. Phenolic content of maturing sugar cane. Int. Sugar J. 90 (1069): 16-19. [ Links ]
18. Godshall, M. A.; B. Legendre; M. Clarke; X. Miranda and R. Blanco. 1996. Starch, polysaccharide and proanthocyanidin in Louisiana sugarcane varieties. En: Sugar Proc. Res. Conf., New Orleans, LA, USA, 1996, pp. 423-436. [ Links ]
19. Hanine, H.; J. Mourgues and J. Molinier. 1990. Aconitic acid removal during cane juice clarification. Int. Sugar J. 92 (1103): 219-230. [ Links ]
20. Honig, P. 1969. Principios de tecnología azucarera. Tomo 1. Continental S. A., Méjico-R. Argentina. [ Links ]
21. International Commission for Uniform Methods of Sugar Analysis (ICUMSA). 2005. Method book. Bartens, Berlin, Germany. [ Links ]
22. Ivin, P. C. and C. D. Doyle. 1989. Some measurements of the effect of tops and trash on cane quality. En: Proc. of the Australian Society of Sugar Cane Technol. Tweed Heads, Australia, 1989: 1-7. [ Links ]
23. Kulkarni, D. P. 1996. Cane sugar manufacture in India. Ed. The Sugar Technologists´ Associaton of India, New Delhi, India. [ Links ]
24. Lionnet, G. R. E. and D. C. Walthew. 2004. Aspects of effects of silica during cane sugar processing. Proc. S. Af. Sug. Technol. Ass. 78: 55-63. [ Links ]
25. McGinnis, R. A. and E. G. Muller. 1984. Sugar Technology Reviews, vol. 12. Elsevier: Amsterdam-Oxford-New York-Tokyo. [ Links ]
26. Mane, J.; D. L. Kimbhar; S. C. Barge and S. P. Phadnis. 2002. Relationship between aconitic acid content in cane cultivars and molasses from various recovery zones of Maharashtra. Int. Sugar J. 104 (1240): 177-179. [ Links ]
27. Mehrotra, P.; A. Mehrotra and R. Suryawanshi. 2009. Effect of post harvest deterioration on efficiency of clarification and crystallization process of white sugar manufacture of CoS 91269 cane variety. En: International Conference on Emerging Trends in Engineering and Technology, ICETET-09, 2, IEEE Computer Society, Washington DC, USA, pp. 781-784. [ Links ]
28. Paton, N. H. 1992. The origin of colour in raw sugar. En: Proc. Australian Society of Sugar Cane Technol. Conference, 14, Mackay, Queensland, Australia, pp. 8-17. [ Links ]
29. PerkinElmer. 2000. Analytical methods for atomic absorption spectrometry. PerkinElmer Instruments LLC, Singapore. [ Links ]
30. Raha, A. 1977. Kinetics of the sedimentation process of cane juice. En: Proc. ISSCT Congress, 16, Brazil, 1977, pp. 2859 - 2872. [ Links ]
31. Rein, P. 2007. Cane sugar engineering. Bartens, Berlin, Germany. [ Links ]
32. Rupa, T. R. and S. Asokan. 2008. Effect of rind pigments and juice colorants on juice claribility, settling time and mud volume of sugarcane. Sugar Tech. 10 (2): 109-113. [ Links ]
33. Saska, M.; S. Zossi and H. Liu. 2010. Removal of colour in sugar cane juice clarification by defecation, sulphitation and carbonation. Int. Sugar J. 112 (1337): 258-268. [ Links ]
34. Sharma, S. C. 1977. Various constituents of sugarcane juice affecting settling in the sulphitation process under Indian conditions. En: Proc. ISSCT Congress, 16, Brazil, 1977, pp. 2951-2969. [ Links ]
35. Simioni, K. R.; L. F. Silva; V. Barbosa; F. E. Ré; C. D. Bernardino; M. L. Lopes e H. V. Amorim. 2006. Efeito da variedade e época de colheita no teor de fenóis totais em cana-de-açúcar. STAB 24 (3): 36-39. [ Links ]
36. Smith, P. and P. E. Gregory. 1971. Analytical techniques for colour studies. En: Proc. ISSCT Congress, 14, New Orleans, LA, USA, pp. 1415-1425. [ Links ]
37. South African Sugar Technologists' Association (SASTA). 2005. SASTA laboratory manual including the official methods. 4. ed. [CD ROM]. South African Sugar Technologists' Association, Durban, South Africa. [ Links ]
38. Van der Poel, P. W.; H. Schiweck and T. Schwartz. 1998. Sugar technology. Beet and cane sugar manufacture. Bartens, Berlin, Germany. [ Links ]
39. Walthew, D. C.; F. Khan and R. Whitelaw. 1998. Some factors affecting the concentration of silica in cane juice evaporators. Proc. S. Af. Sug. Technol. Ass. 72: 223-227. [ Links ]
40. Zossi, B. S.; G. J. Cárdenas; N. Sorol y M. Sastre. 2010. Influencia de compuestos azúcares y no azúcares en la calidad industrial de caña de azúcar en Tucumán (Argentina). Parte 1: Caña limpia y despuntada. Rev. Ind. y Agríc. de Tucumán 87 (1): 15-27. [ Links ]
41. Zossi, S.; M. E. Navarro y M. Alva. 2008a. Ácidos orgánicos en caña de azúcar. [CD ROM]. En: Resúmenes de trabajos del Congreso Nacional de Química, 27, S. M. de Tucumán, Argentina, 2008, pp. 3-26. [ Links ]
42. Zossi, B. S.; M. E. Navarro; N. Sorol; M. Sastre y R. M. Ruiz. 2008b. Validación de una metodología para determinar el contenido de almidón en azúcar. Rev. Ind. y Agríc. de Tucumán 85 (2): 1-7. [ Links ]














