Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista argentina de endocrinología y metabolismo
On-line version ISSN 1851-3034
Rev. argent. endocrinol. metab. vol.46 no.4 Ciudad Autónoma de Buenos Aires Oct./Dec. 2009
DIABETES
Mesa 2: Objetivo Glucémico en Diabetes Tipo 2: (Hba1c, Glucemia Plasmática en Ayunas, Glucemia Posprandial, Excursión Glucémica) *
Guillermo Alzueta, Gullermo Dieuzeide, Mabel Graffigna, Jorge Waitman (en representación del Panel de Expertos)
*Tercer Consenso Argentino sobre Patologías Endocrinológicas Federación Argentina de Sociedades de Endocrinología
Buenos Aires, 28 al 30 de agosto de 2009
Diabetes
Coordinadores Generales: Oscar A. Levalle - Eduardo Pusiol
Coordinador: Isaac Sinay
Panel de Expertos:
Guillermo Alzueta (Balcarce, Bs. As.)
José Costa Gil (La Plata)
Guillermo Dieuzeide (Chacabuco, Bs. As.)
Cristina Faingold (Bs. As.)
Mabel Graffigna (Bs. As.)
Silvia Lapertosa (Corrientes)
Astrid Libman (Rosario)
Guillermo Marcucci (Mendoza)
Ricardo Mileo Vaglio (San Luis)
Emilio Nader (Tucumán)
Silvia Saavedra (Salta)
Jorge Waitman (Córdoba)
Conflicto de interés: Jorge Waitman: ha dado clases para laboratorios: GlaxoSmithKline, Craveri y Servier
1) Si sólo disponemos de glucemia plasmática en ayunas, ¿cuál es la deseable para evitar complicaciones macro y microangiopáticas e hipoglucemias?
La glucemia plasmática en ayunas es aún una herramienta útil para el diagnóstico de diabetes y un predictor independiente de riesgo de enfermedad micro y macrovascular en población diabética y no diabética.
Se sugiere mantener el valor de glucemia plasmática en ayunas menor o igual a 100 mg/dl ya que ha partir de ese valor aumenta sustancialmente el riesgo de macro y microangiopatía.
Se recomienda mantener el valor de glucemia plasmática en ayunas mayor o igual a 70 mg/dl para evitar el riesgo de hipoglucemias.
Niveles elevados de glucemia en pacientes diabéticos se asocian con complicaciones microangiopáticas (retina, riñón y nervios periféricos) y aumento de riesgo de enfermedad cardiovascular.
La glucemia plasmática en ayunas (GPA) es uno de los criterios para efectuar el diagnóstico de DM. Ella es una medida de la habilidad de cada individuo para regular los niveles sanguíneos de glucosa en ausencia de ingesta dietaria de la misma. Es necesario determinar la GPA por lo menos en dos ocasiones antes de establecer el diagnóstico de diabetes.
Como resultado de importantes estudios observacionales epidemiológicos, la Asociación Americana de Diabetes (ADA) considera un valor de GPA ≥ 126 mg/dl para el diagnóstico de diabetes, asumiendo que este es el umbral glucémico que separa personas con alto y bajo riesgo de complicaciones microvasculares diabéticas (1).
La retinopatía es la complicación microvascular más específica de la diabetes. Tres estudios epidemiológicos determinaron cual era el valor de corte de glucemia por encima del cuál su prevalencia aumentaba drásticamente. Los estudios evaluados fueron: una población egipcia estudios de cohorte mostraron que no existe una clara evi(n=1018) con un valor de corte de glucemia de 129 mg/dl, dencia de un umbral glucémico para el desarrollo de la indios Pima (n=960) con 123 mg/dl y una población del misma sino que habría una relación continua entre la GPA NHANES III (n=2821) con 121 mg/dl. (Fig. 1) y prevalencia de retinopatía.
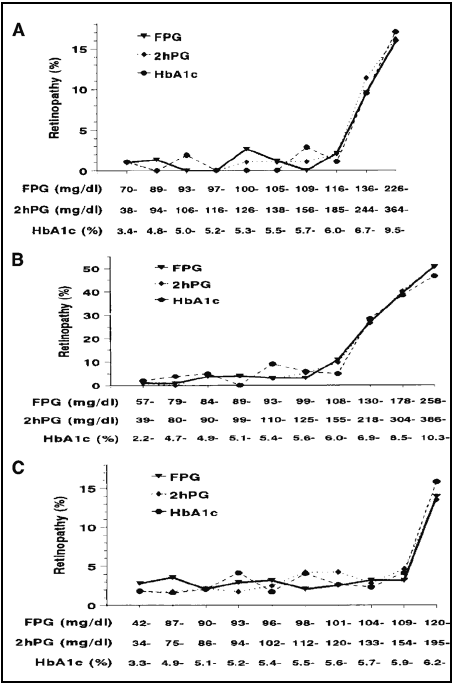
Figura 1- Prevalencia de retinopatía por decilos de distribución de GPA, GPP y HbA1C en indios Pima (A), egipcios (B) y participantes de 40 a 74 años en NHA- NES III (C) (1)
Si bien los estudios clásicos citados planteaban un umbral de riesgo para retinopatía de 126 mg/dl, nuevos estudios de cohorte mostraron que no existe una clara evidencia misma sino que habría una relación continua entre la GPA y prevalencia de retinopatía.
Estos estudios, utilizando fotografías retinales de múltiples campos encontraron una prevalencia de retinopatía del 7 a 13% en individuos diabéticos y no diabéticos con glucemias menores a 100 mg/dl, lo que sugiere que los estudios previos habrían subdiagnosticado retinopatía en una magnitud 2-5 veces menor con respecto a los actuales(2).
Los individuos con diabetes tipo 2 tienen un riesgo 2-4 veces mayor de desarrollar enfermedad cardiovascular que los individuos no diabéticos y ésto se relacionaría con el grado de hiperglucemia.
En individuos sanos generalmente los niveles de glucemia no sobrepasan los 100 mg/dl. Por lo tanto, es importante determinar el valor de la misma a partir del cual aumenta el riesgo de ECV en esta población.
Un metanálisis efectuado por Coutinho y col.(3) sobre 6 estudios que evaluaron 23604 individuos no diabéticos seguidos durante un promedio de 12,4 años, observó que aquellos con glucemias más altas tenían más riesgo de presentar enfermedad cardiovascular. Comparando el grupo con GPA de 75mg/dl vs. el de 110 mg/dl, éste último mostró un aumento del 33% del riesgo relativo de eventos cardiovasculares.
Otro metanálisis realizado por Levitan y col.(4), observó que en individuos no diabéticos, valores más elevados de glucemia producirían mayor riesgo de desarrollar enfermedad cardiovascular. Se evaluaron 9 estudios con un total de 13815 participantes que fueron divididos en 2 grupos de acuerdo a su glucemia de ayuno (66-90 mg/dl vs. 97-130 mg/dl), con un seguimiento entre 6 y 20 años y con el desarrollo de 643 eventos cardiovasculares. Comparando ambas categorías de glucemia, el RR de desarrollar enfermedad cardiovascular fue de 1,27 en aquellos individuos con glucemias más elevadas. Valores de GPA a partir de 100 mg/dl se asociaron con mayor riesgo cardiovascular. (Fig. 2)
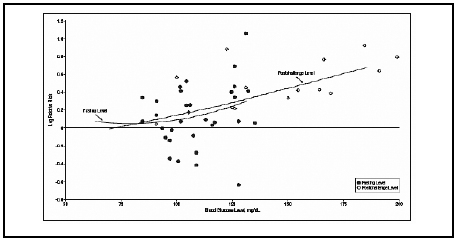
Figura 2- Relación dosis-respuesta de enfermedad cardiovascular con niveles de glucemia de ayuno y posprandial
Por lo tanto, el nivel de glucemia aún en el rango no diabético, sería un marcador de riesgo significativo para el desarrollo futuro de ECV.
La hipoglucemia inducida por el tratamiento es el factor limitante en el manejo de la glucemia en la diabetes. Ésta causa morbilidad recurrente en la mayoría de las personas con diabetes tipo I y en muchas con diabetes tipo II avanzada, siendo a veces fatal. También altera las defensas contra subsiguientes hipoglucemias y se opone al mantenimiento de la euglucemia.
En individuos con diabetes, la hipoglucemia es el resultado de la relación entre el exceso relativo o absoluto de insulina y la alteración de las defensas fisiológicas contra el descenso de las concentraciones plasmáticas de glucosa.
El ADA Workgroup on Hypoglycemia recomienda que los pacientes diabéticos tratados con drogas estén alertados sobre el desarrollo de hipoglucemias con concentraciones plasmáticas de glucosa de 70 mg/dl o menos(5).
Este valor es el límite inferior del rango de glucemia postabsortiva y el umbral para la activación de mecanismos contrarregulatorios fisiológicos de glucemia en no diabéticos. Además, es mayor que los niveles de glucemia requeridos para producir síntomas de hipoglucemia (aprox. 55 mg/dl) o para alterar la función cerebral en no diabéticos. Sin embargo, personas con diabetes mal controlada, a veces tienen síntomas con niveles de glucemia mayores. Por lo tanto, el valor de corte de 70 mg/dl de glucemia, generalmente le da tiempo al paciente para realizar alguna acción para prevenir un episodio de hipoglucemia sintomática.
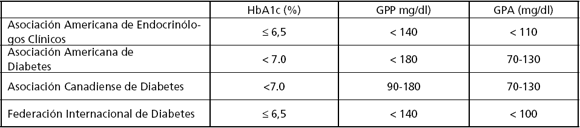
En la Tabla 1 pueden observarse los objetivos de tratamiento de acuerdo a diferentes Guías de manejo de Diabetes
Tabla 1: Objetivos de tratamiento de acuerdo a Guías de manejo de Diabetes
2) Glucemia posprandial y/o variabilidad glucémica cómo medirlas y cuáles son los objetivos Recomendaciones
La hiperglucemia posprandial aumenta el riesgo de enfermedades cardiovasculares. Deben instrumentarse estrategias para reducir las excursiones glucémicas posprandiales.
La glucemia posprandial no debe exceder los 140 mg/ dl evitando las hipoglucemias.
El automonitoreo glucémico es el método más práctico para evaluar la glucemia posprandial.
Faltan evidencias clínicas suficientes con eventos finales duros que permitan correlacionar la variabilidad glucémica y las complicaciones vasculares en el paciente diabético.
Glucemia posprandial
La importancia de la Hiperglucemia Posprandial (HPP) como factor de riesgo de eventos cardiovasculares (ECV) deviene de numerosos ensayos clínicos controlados y estudios epidemiológicos. El metanálisis de Coutinho y col. que totaliza 7 estudios con 33.813 individuos seguidos por 12.4 años, demuestra que el valor umbral de 140mg/dl para la glucemia 2 hs poscarga de glucosa aumenta significativamente el riesgo relativo de ECV en 1.58 (95% CI 1.192.10). No obstante, la mayoría de los estudios epidemiológicos señalan que la glucemia es una variable continua con respecto al riesgo de ECV y que el aumento de la glucemia posprandial en individuos no diabéticos conlleva un riesgo mayor que la hiperglucemia en ayunas (HAy). Dado que la HPP sucede más tempranamente que la hay es recomendable su detección y tratamiento temprano (6).
Las guías y consensos internacionales más importantes(3) concuerdan que en personas con tolerancia a la glucosa normal la glucemia no es mayor de 140mg/dl en respuestas a las comidas o a las 2 h poscarga de 75 gr. de glucosa al 20%, con retorno a los valores basales dentro de las 2 a 3 h. Si bien, la medición de la glucemia posprandial llevada a cabo a las 2 h después de comenzada la ingesta no es una cuestión que esté totalmente definida, es práctica y se aproxima al valor pico en pacientes con diabetes. En condiciones clínicas especiales como la diabetes gestacional puede ser recomendable la medición a la primera hora de comenzada la ingesta. El monitoreo de la glucemia posprandial debe ser recomendada en:
*Pacientes con glucemias preingesta normales pero cuyo control metabólico evaluado por HbA1c no es adecuado.
*Pacientes con HPP para monitorear el tratamiento de la misma.
*Hipoglucemias posprandiales en respuesta al ejercicio o a insulinoterapia preprandial.
*Mujeres con diabetes gestacional en las cuales la mejoría de la HPP se relaciona con el menor número de cesáreas, macrosomía fetal e hipoglucemia neonatal.
Variabilidad glucémica
Las excursiones de las glucemias posprandiales no pueden ser disociadas de la variabilidad glucémica que se expresa como las diferencias entre los picos hiperglucémicos y la subsecuente caída a los valores basales o aún más bajos. El estado posprandial sumado al período postabsortivo cubren gran parte del día quedando relegado el período neto de ayunas a 3 a 4 h. Sin embargo, esto no es totalmente aplicable a personas con diabetes en las cuales las excursiones de las glucemias posprandiales son mayores y de más duración y la variabilidad es también superior a la de los individuos sanos.
La hiperglucemia induce daño vascular a través de: 1) la activación de la Vía de los polioles causando acumulación de sorbitol y fructosa. 2) formación de Productos Finales de la Glicosilación. 3) activación de la Proteín Kinasa C y el Factor Nuclear NFkB. 4) aumento de la vía de la Hexosamina. Todas estas vías confluyen en la sobreproducción de superóxido por la cadena de transporte mitocondrial, en definitiva estrés oxidativo que juega un rol central en las complicaciones vasculares de la diabetes.
El problema es determinar si las oscilaciones glucémicas causan daño vascular y si éste es equiparable o aún mayor que el que produce la hiperglucemia sostenida.
Hay claros indicios de que las oscilaciones glucémicas o la variabilidad pueden tener efectos más deletéreos que la hiperglucemia sostenida como ha sido demostrado por Monnier y col(7).Dicho autor, al realizar un monitoreo continuo de la glucemia plasmática, encontró que las fluctuaciones glucémicas, calculadas por la amplitud media de las excursión glucémicas (índice MAGE) tenían una relación directa con la excreción urinaria de 8-iso PGF 2 alfa, un marcador de la producción de radicales libres derivado del ácido araquidónico de las membranas celulares. La amplitud media de las excursiones glucémicas (MAGE) fue significativamente más disparadora de estrés oxidativo que la hiperglucemia sostenida evaluada por la HbA1c. Esto explicaría porqué en el DCCT en subgrupos de pacientes diabéticos tipo 1 la reducción del riesgo de retinopatía sólo se obtuvo en aquellos con tratamiento intensivo con insulina vs. los tratados en regimen convencional a pesar de que ambos tuvieron iguales niveles de HbA1c final (9%).
Kilpatrick y col. no han podido confirmar la importancia de la variabilidad glucémica usando un análisis retrospectivo de los datos del DCCT.
El Monitoreo Continuo de la glucosa intersticial (CGMS)(8) puede ser muy útil para medir las fluctuaciones glucémicas, pero tiene limitaciones, pudiendo haber diferencias con la glucemia plasmática en tiempo real, especialmente en períodos de fluctuaciones rápidas como en el ejercicio y las hipoglucemias.
Aún no existen estándares de referencia publicados respecto a los valores de la glucemia intersticial.
Si bien es cierto que la variabilidad glucémica es más generador de estrés oxidativo que la hiperglucemia sostenida evaluada por la HbA1c, las limitaciones son básicamente dos:
1- No existe un índice objetivo y estándar publicado de la cuantificación de la variabilidad utilizando la glucemia intersticial.
2- Faltan estudios a largo plazo con eventos finales duros que permitan evaluar la correlación entre fluctuaciones glucémicas y complicaciones vasculares
3) ¿Es aún la HbA1c el mejor criterio de control metabólico en el diabético tipo 2?
Recomendaciones
La medición de HbA1c representa aceptablemente el promedio de las glucemias de 120 días atrás, por lo que sería el mejor método de laboratorio del que disponemos a la fecha para el control metabólico del paciente diabético, para considerar los cambios en el tratamiento y la valoración de riesgo de complicaciones vasculares de la Diabetes Mellitus.
Por ello se recomienda:
1º La medición de HbA1c debe realizarse como mínimo dos veces al año e idealmente tres veces y mantener la misma en un valor menor a 7%.
2º Que la determinación de HbA1c se realice en un laboratorio que esté debidamente acreditado, que cuente con un método internacionalmente estandarizado con la metodología de HPLC y preferiblemente automatizado.
La medición de HbA1c no reemplaza el valor clínico que tiene el automonitoreo glucémico diario.
Hace años que se describió la fracción A1c como una fracción glicada de la HbA y que era producto de la glicación no enzimático de la misma, en la vida circulante del glóbulo rojo. Más tarde se demostró la relación de la HbA1c inicialmente con los valores de glucemia en ayunas y posteriormente como representativo del promedio glucémico de las últimas 4 a 12 semanas.
A medida que la medición de HbA1c adquirió valor clínico para el control de los pacientes diabéticos, aparecieron múltiples métodos de medición de hemoglobina glicada, basados en diferentes metodologías tales como: cromatografía por intercambio iónico, cromatografía de afinidad, métodos de inmmunoensayo o electroforesis. Esto acarreó como problema la gran diversidad entre los valores que expresaban varios métodos para una misma muestra de sangre, lo que hacía difícil la correlación de los resultados y su aplicación en la práctica diaria. Los auto-res del DCCT (como más tarde también los investigadores del UKPDS) evaluaron las muestras en un solo laboratorio y con una sola metodología, que fue la medición por intercambio iónico por HPLC (High Performance Liquid Cromatogrophy) y de esa manera evitaron las diferencias entre métodos. Con esta experiencia el NGSP (National Glycohemoglobin Standarization Program) logró estandarizar los diferentes métodos y los laboratorios con la HbA1c medida por HPLC. Desde entonces las variaciones intermétodo se redujeron drásticamente y se pudo establecer en forma uniforme los criterios de control de los pacientes por HbA1c (9, 10).
La valoración de Hb A1c ha recibido cuestionamientos por diferentes razones. Algunas de las situaciones que pueden falsear los resultados son los defectos congénitos de HbA (hemoglobinopatías), condiciones que alteran el turnover eritrocitario (anemia hemolítica, malaria crónica, hemorragias, embarazo e IRC) y la interferencia de subfracciones defectuosas de HbA. Otras de las razones por la cual fue cuestionada es que la HBA1c, al resultar de una reacción de glicación potencialmente reversible, no es un cabal reflejo de todos los valores de glucemia y expresa más fielmente el valor de la glucemia en ayunas y precomidas y no tanto el de las excursiones posprandiales como se ha visto con monitoreos continuos de la glucemia.
El DCCT en diabéticos tipo 1 y el UKPDS en pacientes diabéticos tipo 2, así como muchos otros valiosos trabajos, fueron los que le dieron fuerza clínica al valor que tiene la HbA1c como predictor de la presencia futura de complicaciones microvasculares principalmente pero también macrovasculares. Desde ellos ya no se discute el valor que tiene la valoración de HbA1c en la toma de decisiones en el tratamiento de pacientes con diabetes, aunque se hayan considerado distintos niveles de recomendación a lo largo de los años y en diferentes territorios (en Europa el valor recomendado es ≤ 6.5% y en EEUU el mismo es ≤ 7%).
Hoy en día, la disponibilidad cada vez más frecuente de métodos internacionalmente estandarizados y automatizados, han hecho que a pesar de todas las críticas que se pueda hacer a la medición de Hb A1c, no haya otro método que la supere en practicidad, costo efectividad y disponibilidad casi universal, constituyéndose en un estándar para la valoración del control glucémico del paciente diabético.
4) ¿Reducir la HbA1c disminuye el riesgo de enfermedad cardiovascular en el diabético tipo 2?
Conclusión
Si bien es un tema aún sujeto a debate, la reducción de la HbA1c determina una reducción del riesgo de infarto de miocardio del 17% y de enfermedad coronaria en 15% en la población de diabéticos tipo 2, presentando un efecto neutro en la reducción del riesgo de mortalidad global y accidente cerebrovascular.
Esta es una pregunta clave pues sabemos que la principal causa de muerte en el paciente diabético tipo 2 es la enfermedad cardiovascular. Los pacientes diabéticos tipo 2 tienen el mismo riesgo de padecer un infarto de miocardio (IAM) o de morir por causa cardiovascular que aquellos no diabéticos que ya han padecido su primer infarto, lo que implica que se los debe considerar como una población de alto riesgo.
La primera observación que permitió inferir que reduciendo el nivel de HbA1c se lograba disminuir el riesgo de nuevos eventos cardiovasculares fue el estudio UKPDS. En una población de 3457 pacientes diabéticos tipo 2, divididos en un grupo de tratamiento con drogas antihiperglucemiantes o insulina y un grupo de tratamiento convencional tratado exclusivamente con dieta, se observó que por cada 1% de reducción de la HbA1c ser reducía en 14% el riesgo de infarto de miocardio. Al cabo de 10 años de seguimiento, y pese a que los niveles de HbA1c se habían homogeneizado entre ambos grupos, las diferencias en la tasa de eventos cardiovasculares se mantenían: el grupo inicialmente asignado a sulfonilureas e insulina presentaba un 15% de reducción del riesgo absoluto de la frecuencia de IAM con respecto al grupo control mientras que el grupo asignado a metformina presentaba una reducción del 33% del riesgo absoluto de IAM y del 30% de muerte atribuible a diabetes en referencia al grupo control. Esto fue denominado el "efecto legado" del UKPDS (11).
Sin embargo, otras investigaciones publicados ese mismo año y al comienzo del 2009 plantearon dudas con respecto a este hallazgo.
El estudio ACCORD, un estudio randomizado, doble ciego, que incluyó 10251 pacientes seguidos durante 3,5 años, comparó a un grupo de pacientes diabéticos tipo 2 asignados a un regimen de tratamiento intensivo con drogas y/o insulina con el fin de lograr una meta de HbA1c menor a 6%, con otro grupo asignado a un regimen menos intensivo con un objetivo de HbA1c de 7 a 7-9%. Al finalizar, no se apreciaron diferencias significativas en la tasa de eventos, aunque el grupo de tratamiento intensivo presentó una mayor frecuencia de muertes por causa cardiovascular y por cualquier causa que el grupo control. Pese a esto, la frecuencia de infartos de miocardio no fatales, fue inferior en este grupo que en el grupo control (12).
El siguiente estudio, el ADVANCE, también comparó la tasa de eventos macro y microvasculares en una población de 11.400 pacientes diabéticos tipo 2, seguidos durante 5 años, randomizados a un grupo tratado intensivamente con el fin de obtener una HbA1c media de 6,5% contra otro grupo control asignado a una meta de HbA1c media del 7,3% con el requisito de que en el grupo de tratamiento intensivo se debía utilizar la droga gliclazida. El grupo asignado a tratamiento intensivo tuvo una reducción significativa de la tasa de eventos microvasculares, especial-mente nefropatía diabética pero no obtuvo una reducción de los eventos cardiovasculares (13).
Otra investigación importante fue la realizada en los Hospitales de Veteranos de los EE.UU. durante 5,6 años en donde un grupo de diabéticos tipo 2 fueron asignados a un tratamiento intensivo con el fin de obtener una HbA1c de 6,5% vs. otro grupo en tratamiento estandar con la meta de una HbA1c de 8,4%,. Al concluir el estudio no hubo diferencias apreciables entre ambos grupos con respecto a la frecuencia de aparición del primer evento compuesto de IAM, accidente cerebrovascular, muerte de causa cardiovascular, falla cardíaca, cirugía por causa cardiovascular, enfermedad coronaria inoperable o amputación por gangrena (14).
Estos hallazgos plantearon dudas respecto de si descender la HbA1c podría tener algún efecto independiente del control de otros factores de riesgo, en la reducción de eventos cardiovasculares severos en pacientes con diabetes tipo 2. En un consenso conjunto de la American Diabetes Association, del American College of Cardiology y de la American Heart Association se estableció que "la utilidad y la eficacia de descender intensivamente la glucemia (en relación al descenso de lípidos y TA) está menos establecida por la evidencia o la opinión, configurando una recomendación clase IIb con un nivel de evidencia A. Debe considerarse que entre un 32 a 40% de los sujetos en estos tres últimos estudios (ACCORD, ADVANCE y VADT) habían presentado un evento cardiovascular previo, lo cual pudiera ser un factor de sesgo si quisiéramos determinar el efecto puro del descenso de la HbA1c en la reducción de eventos cardiovasculares en población de diabéticos 2 sin eventos previos.
No obstante, en un estudio sueco (DIGAMI 1) específicamente designado a una población de alto riesgo, diabéticos 2 que ingresaron al Hospital con infarto agudo de miocardio, divididos aleatoriamente a dos tipos de tratamiento: uno con insulina intensificada desde el comienzo y el otro con tratamiento convencional, concluyó al cabo de 12 meses de seguimiento que la reducción de la HbA1c en 0,9% en el grupo de tratamiento intensivo se asociaba a una reducción del riesgo absoluto de muerte por causa cardiovascular del 11%(15).
En otra visión del tema, un "modelo metabólico puro" puede ayudarnos a entender el valor independiente de la HbA1c en el pronóstico cardiovascular de los pacientes diabéticos tipo 2 y este es el que aporta el estudio DCCT/ EDIC sobre pacientes diabéticos tipo 1. Estos fueron seguidos durante 6,5 años y divididos aleatoriamente a un grupo tratado con insulinoterapia intensificada que obtuvo una HbA1c media de 7,4% versus un grupo en tratamiento convencional que consiguió una HbA1c media de 9.1%. Por exigencia de protocolo, la presencia de enfermedad cardiovascular previa, hipertensión arterial o dislipidemia era un criterio de exclusión para ingresar al protocolo. El grupo de tratamiento intensivo redujo el riesgo de cualquier enfermedad cardiovascular en 42% y el riesgo de infarto de miocardio no fatal, accidente cerebrovascular y muerte por causa cardiovascular en un 57% (16).
En un enfoque diferente, el estudio PROACTIVE se planteó si añadiendo al tratamiento ya preexistente de una población de diabéticos tipo 2 de alto riesgo vascular, la droga pioglitazona contra un grupo asignado a placebo se podía obtener una reducción de eventos finales de mortalidad por cualquier causa, infarto de miocardio no fatal y accidente cerebrovascular. Al final de un período de 2,8 años se había observado una reducción del 10% de la frecuencia de "end points" finales en el grupo asignado a TZD, pero con un incremento del 3% del riesgo de insuficiencia cardíaca. La meta terapéutica de HbA1c en ambos grupos había sido fijada en <6,5%, obteniéndose un descenso de 0.8% con referencia al basal en el grupo pioglitazona vs. 0,3% en el grupo control (17). Podemos realizar un análisis comparativo de estos estudios en la Tabla Nº 1.
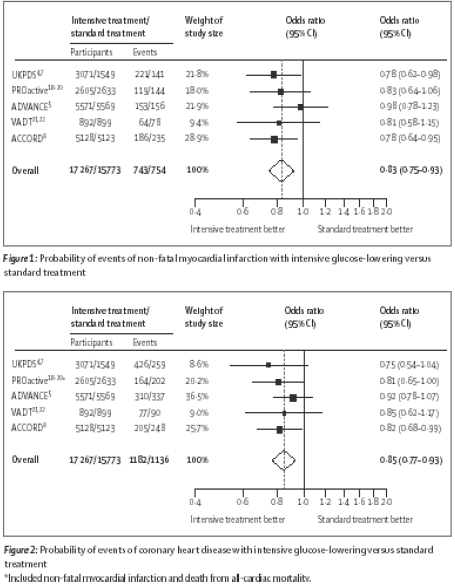
La respuesta posible a la pregunta del título ha sido publicada este año en un metanálisis realizado por el departamento de Salud Pública de la Universidad de Cambridge por Ray y col. que involucró 5 grandes trabajos prospectivos con un seguimiento de 33.040 pacientes (configurando una de las observaciones más grandes de la historia (163.000 personas/año). Se observó como resultado final que los pacientes con diabetes tipo 2 colocados en tratamiento intensivo, en quienes se había obtenido un descenso promedio de la HbA1c del 0,9% en comparación a controles, presentaban una reducción del 17% de la tasa de infartos de miocardio no fatales y un15% de reducción de eventos de enfermedad coronaria (Gráfico Nº 1). No se observaron efectos en la reducción de la frecuencia de eventos de ACV o en la reducción de la mortalidad global (18).
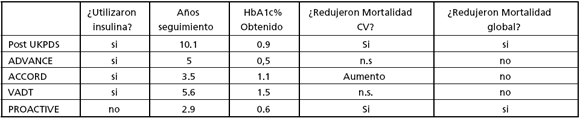
Gráfico 1
1) Expert Committee on the Diagnosis and Classification of Diabetes Mellitus: Report of the Expert Committee on the Diagnosis and Classification of Diabetes Mellitus. Diabetes Care 20:1183-1197, 1997 [ Links ]
2) Wong T, Liew G, Tapp R, y col. The relationship of fasting glucose to retinopathy: re-visiting a key criterion used to diagnose diabetes. Lancet 371:736-743, 2008 [ Links ]
3) Coutinho M, Gerstein H, Wang Y, y col. The relationship between glucose and incident cardiovascular events. A metaregression analysis of published data from 20 studies of 95,783 individuals followed for 12.4 years. Diabetes Care 22:233-240, 1999 [ Links ]
4) Levitan E, Song Y, Ford E, y col. Is nondiabetic hyperglycemia a risk factor for cardiovascul-ar disease? A meta-analysis of prospective studies. Arch Intern Med 164:2147-2155, 2004 [ Links ]
5) Defining and reporting hypoglycemia in diabetes. A report from the American Diabetes Association Workgroup on Hypoglycemia. Diabetes Care 28:1245-1249, 2005 [ Links ]
6) International Diabetes Federation guidelines for management of postmeal glucose: a review of recommendations. Ceriello A. and Colagiuri S. Diabet Med 25:1151-1156, 2008 [ Links ]
7) Monnier L, Mas E, Ginet C, y col. Activation of oxidative stress by acute glucose fluct-tuations compared with sustained chro-nic hyperglycemia in patients with type 2 diabetes. JAMA 295:1681-1687, 2006 [ Links ]
8) Continuos Glucose Monitoring and Intensive Treatment of Type 1 Diabetes. The juvenile Diabetes Foundation Continuos Glucose Monitoring Study Group. N Engl J Med 359:1464-1476, 2008 [ Links ]
9) Consensus Committee. Consensus Statement on the Worldwide Standarization of the Hemoglobin A1c Measurement. Diabetes Care 30:2399-2340, 2007 [ Links ]
10. Gorus F, Mathieu C, Gerlo E. How should HbA1c measurements be reported?. Diabetologia; 49:7-10, 2006 [ Links ]
11. Holman R, Paul S, Bethel A, Matthews D, Neil A. 10-year follow up of intensive glucose control in type 2 diabetes. NEJM 359:1577-89: 2008 [ Links ]
12) The ACCORD Group Effects of intensive glucose lowering in type 2 diabetes. NEJM 358:2545-59, 2008 [ Links ]
13) The Advance Collaborative Group Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N E J M 358:2560-72, 2008 [ Links ]
14) Duckworth W, Abraira C, Moritz T, Reda D, Emanuele N, Reaver P, Zieve F, Marks J, Davis S, et al. The VADT investigators Glucose control and vascular complications in veterans with type 2 diabetes. N E J M 360:129-39, 2009 [ Links ]
15) Malberg K and the DIGAMI group Prospective randomized study of intensive insulin treatment on long term survival after acute myocardial infarction in patients with diabetes mellitus. Br Med J 314:1512, 1997 [ Links ]
16) The DCCT/EDIC study research group. Intensive diabetes treatment and cardiovascular disease in patients with type 1 diabetes. NEJM 25:2643-2653, 2005 [ Links ]
17) Dormandy J, Charbonnel B, Eckland D and the PROactive investigators. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical Trial In macroVascular Events):a randomised controlled trial. Lancet:366:1279-89, 2005 [ Links ]
18) Ray K, Kondapally Seshasai Sr, Wijerusiya S, Sivakumaran R, Nethercott S, Preiss D, Erqou S, Sattar N. Effect of intensive control of glucose on cardiovascular outcomes and death in patients with diabetes mellitas a metanalisis of randomised controlled trials.. Lancet:373:1765-72, 2009 [ Links ]














