Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Phyton (Buenos Aires)
versión On-line ISSN 1851-5657
Phyton (B. Aires) v.77 Vicente López ene./dic. 2008
ARTÍCULOS ORIGINALES
Tasa de secado del suelo e intercambio de gases de tres variedades de Phaseolus vulgaris L. (Con 3 Tablas y 3 Figuras)
Soil drying rate and gas exchange of three Phaseolus vulgaris L. varieties (With 3 Tables & 3 Figures)
Aguirre-Medina1 JF, J Kohashi-Shibata2, J Cadena-Iñiguez2, C Avendaño-Arrazate2
1 INIFAP, Campo Experimental Rosario Izapa. Km 18,5 Carretera Tapachula-Cacaohatán, Chiapas, México. Address Correspondence to: JF Aguirre-Medina, e-mail: aguirre.juan@inifap.gob.mx
2 Especialidad de Botánica, Instituto de Recursos Naturales del Colegio de Postgraduados. Km 35,5 Carretera México-Texcoco, Estado de México, México.
Recibido/Received 26.09.2007. Aceptado/Accepted 28.01.2008.
Resumen. La sequía intermitente es la principal limitante para la producción del frijol en México. Se expuso el sistema radical de tres variedades de frijol de diferente origen y capacidad para tolerar el estrés hídrico a diferentes tasas de secado del suelo. Las variedades sintéticas fueron: Pinto Villa (PV, tolerante al estrés hídrico) y Bayo Madero (BM, susceptible al estrés hídrico) de origen mesoamericano y hábito de crecimiento tipo III (guía), e ICA Palmar (tolerante al estrés hídrico) de origen andino y hábito de crecimiento tipo I (mata o arbusto). Los tratamientos fueron tres tasas de secado del suelo, que se lograron al suspender el riego y mantener o retirar la cubierta de la maceta elaborada con tubos de PVC en un sistema de raíz dividida. Se estudió el intercambio de gases durante 32 hrs. La tasa de secado lenta del suelo (con cubierta) generó una declinación gradual en la conductancia estomática y la tasa de asimilación de CO2. En BM, los tres niveles de deshidratación afectaron significativamente la respuesta de las variables cuantificadas. Independientemente de la disponibilidad de agua en el suelo, las plantas permanecieron con los estomas cerrados. En PV e ICA Palmar, los efectos más contrastantes se lograron con las tasas intermedia y rápida de secado del suelo, aún con diferencias en la disponibilidad de agua en el mismo; en PV no se expresaron las diferencias entre tratamientos. En ICA Palmar, el potencial hídrico del suelo no expresó la respuesta en conductancia estomática. En ambas variedades, la respuesta fue de valores altos y bajos en conductancia estomática. La temperatura del folíolo se incrementó durante las primeras dos horas de muestreo. La variedad con menor cambio en la temperatura del folíolo, mayor control de la conductancia estomática y alta tasa de asimilación de CO2 fue ICA Palmar, posiblemente como consecuencia de su elevada presencia de tricomas en ambas caras del folíolo.
Palabras clave: Phaseolus vulgaris; Tasa de secado del suelo; Intercambio de gases; Potencial hídrico.
Abstract. Intermittent drought is the main limiting factor for bean production in Mexico. The root system of three bean varieties of different origin and tolerance to water stress was exposed to different drying soil rates. The synthetic varieties were: Pinto Villa (PV, water stress tolerant) and Bayo Madero (BM, water stress susceptible) both of mesoamerican origin and growth habit type III (climbing habit), and ICA Palmar (water stress tolerant) of Andean origin and growth habit type I (shrub). Treatments were three soil drying rates, which were achieved by stopping irrigation and either maintaining or removing the pot cover made with PVC tubes in a split root system. Gas exchange was studied during 32 h. Slow soil drying rate (with cover) generated a gradual decline in stomatal conductance and CO2 assimilation rate. In BM, the three dehydration levels significantly affected the response of the quantified variables. Despite water was available in the soil, plants remained with stomata closed. In PV and ICA Palmar, the most contrasting effects were achieved with intermediate and fast soil drying rates, even though there were differences in soil water availability; in PV, differences among treatments were not expressed. In ICA Palmar, soil water potential did not express the response in stomatal conductance. Both varieties showed high and low values in stomatal conductance. Leaflet temperature increased during the first two hours of sampling. ICA Palmar was the variety with less change in leaflet temperature, greater control of stomatal conductance, and high CO2 assimilation rate. This was possibly a result of its high presence of trichomes on both sides of the leaflet.
Key words: Phaseolus vulgaris; Rate of soil drying; Gas exchange; Soil water potential.
INTRODUCCIÓN
El contacto del sistema radical con el volumen del suelo es generalmente heterogéneo, y está influenciado por el tipo y tamaño de las partículas. Esta situación tiene una influencia determinante en la adquisición de recursos del suelo, y en particular en el balance entre la pérdida de agua por la parte aérea y su absorción por el sistema radical. La eficiencia del sistema radical en absorber y conducir el agua hasta la parte aérea es determinante, no solo para el óptimo crecimiento de las plantas, sino también por su influencia en la productividad de los cultivos (Blum et al., 1991).
Cuando se presenta un estrés hídrico en el suelo, la raíz es el primer órgano de la planta que lo percibe, y su presencia genera una serie de respuestas fisiológicas y metabólicas. El nivel de respuesta va a depender de la intensidad y duración del estrés hídrico, de la rapidez con que se alcance dicha intensidad, de la etapa fenológica en la que se presente, y/o del preacondicionamiento de la planta a la sequía (Begg y Turner, 1976; Hsiao et al., 1976). También dependerá de la capacidad genética de las especies para resistir dicho ambiente (Chaves, 1991; Tardieu y Simonneau, 1998; Subbarao y Johansen, 2002).
En los últimos años se ha podido demostrar que el crecimiento radical en condiciones de estrés, como el estrés hídrico, estrés de nutrientes y/o la compactación del suelo, causan una serie de respuestas fisiológicas en la parte aérea sin que se afecten las relaciones hídricas del vástago (Blackman y Davies, 1985; Schultze, 1986; Mulholland et al., 1999; Aguirre-Medina et al., 2005). Además, las raíces de las plantas son capaces de inducir una disminución de la conductancia estomática en ausencia de pérdida de turgencia bajo condiciones de estrés hídrico (Blackman y Davies, 1985; Trejo y Davies, 1991). Esto se ha observado aún cuando se suspende el riego en la mitad del sistema radical (Aguirre-Medina et al., 2005).
El efecto principal que resulta de la disminución del potencial hídrico en el suelo es una inhibición del crecimiento y la reducción en el intercambio gaseoso (Mansfield y Atkinson, 1990). En el presente estudio se investigó el efecto de tres tasas de secado del suelo en cámaras de crecimiento sobre el intercambio gaseoso de tres variedades de frijol con diferente capacidad de tolerancia a la sequía en un sistema de raíz dividida de plantas establecidas.
MATERIALES Y MÉTODOS
La investigación se desarrolló en cámaras de crecimiento en el Colegio de Postgraduados, Montecillo, Estado de México. Se utilizaron tres variedades sintéticas de Phaseolus vulgaris L.. Dos de ellas pertenecen al acervo Mesoamericano de la raza Durango: Pinto Villa (PV, tolerante al estrés hídrico) y Bayo Madero (BM, susceptible al estrés hídrico). La otra variedad, ICA Palmar, pertenece al acervo Andino y de la raza Nueva Granada (tolerante al estrés hídrico). PV, ICA Palmar y BM presentan 17, 24 y 57 estomas en la superficie adaxial, y 141, 127 y 104 estomas en la superficie abaxial, respectivamente. La densidad de tricomas (tricomas/células epidérmicas) tiene una relación de 1:67, 1:45 y 1:11 en PV, ICA Palmar y BM, respectivamente (Aguirre-Medina et al., 2002).
Las variedades se cultivan en la región templada y semiárida de México. Las semillas se hicieron germinar en cajas de Petri. Una vez emitida la radícula, se les dividió longitudinalmente y se transplantaron en macetas divididas, con una parte de la raíz a cada lado de la división. Las macetas se formaron con tubos de PVC de 9 cm de diámetro y 50 cm de altura divididos longitudinalmente. Las dos partes del tubo fueron unidas con cinta para conformar la maceta, y en el centro la división se logró con un plástico calibre 700. En el interior de las macetas se introdujeron bolsas hechas con malla de mosquitero para retener el sustrato de arena de río. Las plantas fueron regadas inicialmente con agua destilada durante 30 días en una cámara de crecimiento (Sherer CEL 11-38), a una temperatura de 20 a 22 °C y un fotoperíodo de 12 horas. La densidad de flujo de fotones fotosintéticos promedio fue de 670 μmol/m2/s, y la humedad relativa fue de 35%. Las plantas se regaron diariamente con agua destilada, y dos veces por semana se utilizó solución nutritiva de Hoagland (Epstein, 1972).
Los tratamientos en cada variedad fueron: 1) Tasa lenta de secado del suelo, que consistió en mantener toda la maceta unida (Testigo), 2) Tasa intermedia de secado del suelo, que consistió en retirar la mitad longitudinal del tubo de PVC, y 3) Tasa rápida de secado del suelo, que se obtuvo retirando de ambos lados los tubos de PVC, y el suelo quedó retenido en la bolsa de malla. En todos los casos las mediciones se iniciaron 31 días después de la siembra, cuando los tratamientos se dejaron de regar. Se determinaron el intercambio gaseoso y el potencial hídrico del suelo con intervalos de 2 h durante dos días a partir de las 9:30 y hasta las 17:30 horas. La conductancia estomática, asimilación de CO2 y temperatura se determinaron en el folíolo central de la primera hoja compuesta en cinco plantas por tratamiento. Se utilizó un sistema abierto y portátil de análisis gaseoso en el infrarrojo (IRGA) marca PPSystems modelo CIRAS-1.
Se tomó una muestra del substrato en el que crecieron las plantas a través de perforaciones laterales de la maceta para determinar el potencial hídrico (a 15 cm de profundidad). Las muestras se mantuvieron dos horas en cámaras psicrométricas C-52 (Wescor, Inc.) conectadas a un microvoltímetro (Wescor, HR 33T, Inc.), y se determinó el potencial hídrico por el método de punto de rocío. Los resultados obtenidos fueron analizados estadísticamente utilizando SAS para Windows. Las comparaciones entre medias de tratamientos se hicieron por Tukey (p<0,05).
RESULTADOS
Los tratamientos establecidos entre las variedades mediante la utilización de la malla mosquitera, y el recubrimiento o no de la misma con tubos de PVC, permitieron obtener tasas diferentes de deshidratación del suelo, con efectos subsiguientes en la conductancia estomática, la tasa de asimilación de CO2 y la temperatura del folíolo (Fig. 1, 2 y 3).
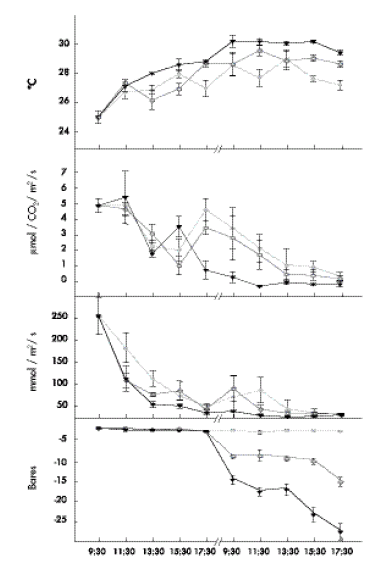
Fig. 1. Efecto de la tasa de secado del suelo, lenta, media y rápida en el intercambio de gases y la temperatura del foliolo central de la variedad Pinto Villa a través del tiempo. Cada valor representa el promedio de 5 observaciones ± 1 error estándar.
Fig.1. Effect of soil drying rate, slow , medium and fast on gas exchange and temperature of the central leaflet in the variety Pinto Villa through time. Each value represents the mean of 5 replicates ± 1 standard error.
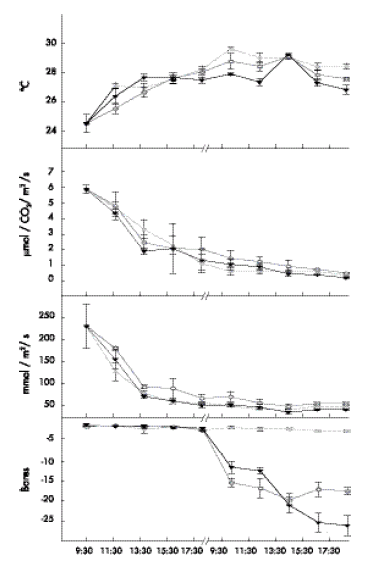
Fig. 2. Efecto de la tasa de secado del suelo, lenta, media y rápida en el intercambio de gases y la temperatura del foliolo central de la variedad Bayo Madero a través del tiempo. Cada valor representa el promedio de 5 observaciones± 1 error estándar.
Fig.2. Effect of soil drying rate, slow , medium and fast on gas exchange and temperature of the central leaflet in the variety Bayo Madero through time. Each value represents the mean of 5 replicates ± 1 standard error.
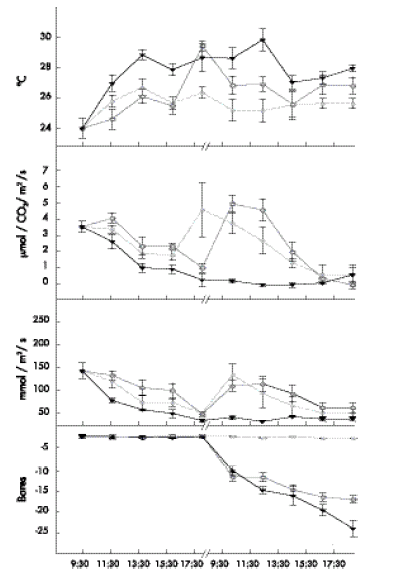
Fig. 3. Efecto de la tasa de secado del suelo, lenta, media y rápida en el intercambio de gases y la temperatura del foliolo central de la variedad ICA Palmar a través del tiempo. Cada valor representa el promedio de 5 observaciones ± 1 error estándar.
Fig.3. Effect of soil drying rate, slow , medium and fast on gas exchange and temperature of the central leaflet in the variety ICA Palmar through time. Each value represents the mean of 5 replicates ± 1 standard error.
La tasa lenta de secado del suelo originó una declinación gradual en la conductancia estomática (p<0,05) y la tasa de asimilación de CO2 (p<0,05) en los tres genotipos de frijol (Fig. 1, 2 y 3). En BM se presentó un descenso mayor en comparación con PV e ICA Palmar, y fue estadísticamente diferente al final del primer día de evaluación y al inicio del día siguiente (p<0,05). En la tasa intermedia de secado del suelo, los resultados más contrastantes se presentaron el segundo día de evaluación. ICA Palmar registró mayor conductancia estomática que los otros genotipos (p<0,05) (Tabla 1). La tasa rápida de secado de suelo afectó la conductancia estomática de manera semejante en las tres variedades. La tasa de asimilación de CO2 disminuyó en las tres variedades durante el primer día, y en PV e ICA Palmar se incrementó al final del mismo día y al inicio del siguiente. BM fue estadísticamente diferente (p<0,05) (Tabla 2) en las tasas lenta e intermedia de secado del suelo al final del primer día de evaluación y al inicio del día siguiente. En cambio, la diferencia estadística en PV e ICA Palmar se encontró al inicio de la evaluación del primer día en las tasas de secado lenta e intermedia del suelo. PV también presentó diferencias estadísticas al inicio del día dos de evaluación en la tasa intermedia de secado. En la tasa rápida de secado del suelo las diferencias estadísticas se presentaron en las primeras horas de iniciada la evaluación (Tabla 2). La temperatura del foliolo central en las tasas lenta e intermedia del suelo se incrementó más en BM y PV, y fueron estadísticamente diferentes respecto a ICA Palmar (p<0,05) (Fig. 1, 2 y 3). En la tasa rápida de secado del suelo durante el primer día, las tres variedades respondieron de manera semejante al tratamiento. Las diferencias se presentaron al día siguiente, con menor temperatura del folíolo en los genotipos BM e ICA Palmar (Tabla 3).
Tabla 1. Conductancia estomática (mmol/m2/s) del folíolo central en tres variedades de frijol bajo un sistema de raíz dividida. Cada valor representa el promedio de 5 observaciones ± 1 error estándar. Los valores con letras diferentes, dentro de cada columna, son estadísticamente distintos (p<0,05).
Table 1. Stomatal conductance (mmol/m2/s) of the central leaflet in three bean varieties under a split root system. Each value represents the mean of 5 observations ± 1 standard error. Values followed by different letters within the same column are statistically different (p<0.05).
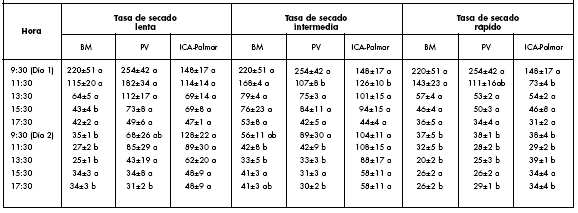
Tabla 2. Tasa de asimilación de CO2 (μmol CO2/m2/s) del folíolo central en tres variedades de frijol bajo un sistema de raíz dividida. Cada valor representa el promedio de 5 observaciones ± 1 error estándar. Los valores con letras diferentes, dentro de cada columna, son estadísticamente distintos (p<0,05).
Table 2. Rate of CO2 assimilation (μmol CO2/m2/s) of the central leaflet in three bean varieties under a split root system. Each value represents the mean of 5 observations ± 1 standard error. Values followed by different letters within the same column are statistically different (p<0.05).
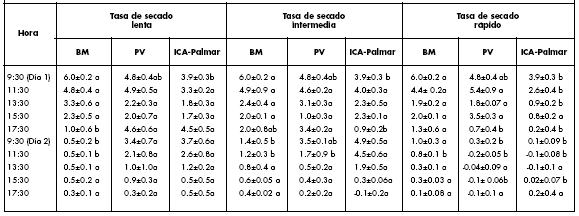
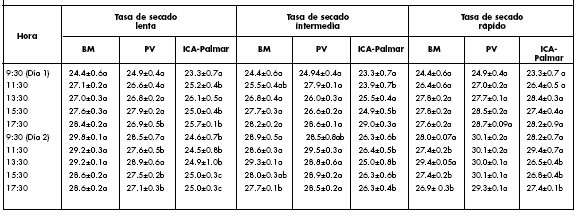
Tabla 3. Temperatura del folíolo central (°C) en tres variedades de frijol bajo un sistema de raíz dividida. Cada valor representa el promedio de 5 observaciones ± 1 error estándar. Los valores con letras diferentes, dentro de cada columna, son estadísticamente distintos (p<0,05).
Table 3. Temperature (°C) of the central leaflet in three bean varieties under a split root system. Each value represents the mean of 5 observations ± 1 standard error. Values followed by different letters within the same column are statistically different (p<0.05).
DISCUSIÓN
La sequía edáfica y sus efectos en la parte aérea de las plantas (vástago) se han estudiado en diversos contenedores con la finalidad de simular las condiciones de campo, y en este esquema se ha evaluado el sistema de raíz dividida en este estudio (Webb y Mansfield, 1992). Este sistema permite separar el mecanismo no hidráulico generado en respuesta a la sequía edáfica (Davies y Zhang, 1991), que se transporta al vástago e induce cierre estomático (Trejo y Davies, 1991) y en consecuencia disminuye la ganancia de carbono (Shulze et al., 1987). Bajo este sistema de raíz dividida, Aguirre-Medina et al. (2005) con las mismas variedades de Phaseolus vulgaris L., observaron una disminución de la conductancia estomática sin pérdida de turgencia. Las observaciones se hicieron en la misma hoja investigada en este estudio.
En las variedades tolerantes al estrés hídrico, PV e ICA Palmar, la conductancia estomática declinó gradualmente con las tasas lenta e intermedia de secado del suelo, y, con mayor fuerza en la tasa de secado rápida (Fig. 1 y 3). En PV, aún cuando se presentaron diferencias en el contenido de agua en el suelo entre los tratamientos, no se expresó esta diferencia en la planta. En cambio, en la variedad susceptible al estrés hídrico BM, los tres niveles de deshidratación redujeron significativamente la conductancia estomática a las cuatro horas de iniciados los tratamientos, a pesar de existir disponibilidad de agua en el suelo (Fig. 2). Muy probablemente, esta variedad tiene un mecanismo de control estomático menos eficiente en comparación con las otras variedades, que puede relacionarse con la baja presencia de tricomas en su superficie foliar y el mayor número de estomas en la superficie abaxial (Aguirre-Medina et al., 2002). Estos resultados son diferentes a los encontrados por Croker et al., (1998) cuando regó la mitad del sistema radical de diversas especies de árboles deciduos. Esto puede estar relacionado con el corto periodo de evaluación de nuestro estudio. El comportamiento anterior establece una respuesta diferencial entre las variedades para regular la pérdida de agua: (1) mediante el mejor control de la apertura estomática debido a la demanda evaporativa de la planta (Tardieu y Simonneau, 1998), o (2) a través de la emisión de algún mensaje químico generado en la raíz y transmitido al vástago (Blackman y Davies, 1985). En otros casos la conductancia estomática depende del desarrollo de adaptaciones morfológicas, como probablemente sucede en el incremento de la pubescencia en la lámina foliar de ICA Palmar (Aguirre-Medina et al., 2002). Esta pubescencia puede influir en la disminución de la difusión del agua en la superficie de la hoja (Johnson, 1975). Tardieu y Simonneau (1998) informaron que el potencial hídrico de la hoja durante el día es el resultado del nivel hídrico en el suelo y la demanda evaporativa de la planta.
Las diferencias en los niveles de fluctuación de la conductancia estomática durante el día entre las variedades de frijol explican alternativas diferentes ante condiciones de estrés hídrico. En el tratamiento testigo, con las variedades PV e ICA Palmar, la conductancia estomática tuvo un descenso gradual hasta el final del primer día y un incremento al día siguiente. Muy probablemente esto estuvo influenciado por la poca variación en el potencial hídrico del suelo (Fig. 1, y 3). Este comportamiento supone la limitación del flujo de agua desde el suelo hacia la planta durante el día conforme progresa la reducción de la humedad del suelo. Al reducirse la transpiración en la noche, la conductancia estomática se recupera en las primeras horas del día siguiente. Los cambios con el tiempo en la demanda evaporativa fueron diferentes entre variedades.
En la condición de tasa de secado intermedia del suelo, donde se retiró la mitad longitudinal de la maceta, la conductancia estomática fue similar en comparación con el tratamiento testigo. Este comportamiento sugiere que la declinación de la conductancia estomática probablemente no fue el resultado de una señal hidráulica. Resultados semejantes obtuvieron Croker et al. (1998). En la condición de tasa rápida de secado del suelo, donde se retiraron las dos partes de la maceta, no se registró uniformidad en la conductancia estomática entre muestreos en ambas variedades tolerantes al estrés hídrico PV e ICA Palmar. Es decir, a un tiempo se incrementó la conductancia estomática y en el siguiente muestreo disminuyó, y dos horas más tarde, se registró la conductancia estomática inicial.
El incremento y disminución de la conductancia estomática la presentaron ambas variedades durante 26 horas, y después de este tiempo la conductancia estomática disminuyó gradualmente en la última etapa. Esta respuesta se puede atribuir a cambios mecánicos y pasajeros del estoma en respuesta a la tasa rápida de secado del suelo. Sin embargo, también se puede atribuir a los cambios de presión entre las células epidérmicas y oclusivas cuando disminuye la absorción de agua (Raschke, 1970). Al día siguiente de evaluación, la recuperación de la conductancia estomática en ICA Palmar fue similar a la iniciada un día antes. Sin embargo, ésta disminuyó al 50%, y después de medio día llegó a su nivel más bajo en PV. En ICA Palmar, esta condición se alcanzó al final de la evaluación, en la tarde del día dos de estudio. Los cambios anteriores entre las variedades posiblemente se deban a una leve rehidratación del tejido durante la noche que indujo la apertura del estoma; esto fue seguido por la falta de humedad, como consecuencia de la absorción desigual de agua del suelo y la consecuente inducción del cierre de los estomas como resultado de la rápida tasa a la cual se secó el suelo. La mayor tolerancia a la deshidratación del suelo y su efecto en la reducción de la conductancia estomática en PV e ICA Palmar puede estar relacionada (1) a la presencia de tricomas y mayor densidad estomática en la superficie abaxial de la hoja (Aguirre-Medina et al., 2002) o (2) a la aptitud de cada planta para inducir el cierre de los estomas (Hartung et al., 1990; Dixon y Johnson, 1993). Otros autores consignan que el cierre estomático se origina por la emisión de un mensaje químico, como prolina (Aguirre-Medina et al., 2005), producido en la raíz al secarse el suelo que se transmite al vástago (Blackman y Davies, 1985; Masle y Passioura, 1987; Blum et al., 1991) y Bates y Hall (1981) sugieren que la conductancia estomática de las hojas depende más de la sequía edáfica que de las relaciones hídricas de la hoja. En el vástago, con la tasa rápida de secado del suelo, se observó mayor pérdida de turgencia en la hoja y bordes foliares de color café en la variedad susceptible al estrés hídrico BM en comparación con las otras dos variedades.
La tasa de asimilación de CO2 también fue afectada por los tratamientos en las tres variedades estudiadas. Esta presentó su pico más alto en la mañana, una declinación gradual durante el día en BM, y una recuperación al final del mismo día en PV e ICA Palmar. Esta respuesta se observó en el testigo y la tasa intermedia de secado del suelo. En la variedad susceptible al estrés hídrico BM, el efecto fue similar a lo observado para la conductancia estomática. Entre las variedades tolerantes, la tasa de secado rápido del suelo tuvo una declinación gradual durante el primer día y la más baja durante el segundo día. En ICA Palmar la reducción fue mayor que en PV. Al inicio del segundo día de evaluación, ambas variedades tolerantes registraron altas tasas de asimilación de CO2 en las tasas de secado lenta e intermedia del suelo.
Cuando las plantas se exponen a estrés hídrico severo disminuye la tasa de transpiración (McCree y Richardson, 1987; Chaves, 1991) y se induce el cierre parcial de los estomas que puede interferir con la adquisición de CO2 (Farquhar y Sharkey, 1982; Mansfield y Atkinson, 1990). Al aumentar la temperatura del foliolo se reduce la tasa de asimilación de CO2, y declina la conductancia estomática (Davies, 1987) en respuesta a un incremento en el déficit de presión de vapor (Turner et al., 1985).
La temperatura del folíolo central de la primera hoja compuesta se incrementó en las tres variedades durante las dos primeras horas de exposición al estrés hídrico. En las variedades de origen mesoamericano BM y PV, el incremento fue de alrededor de 2 °C, y en la variedad de origen andino ICA Palmar, de 3 °C. Después de este incremento, la temperatura en BM varió alrededor de medio grado durante el primer día, y en promedio entre muestreos se mantuvo en estos valores en los tres tratamientos hasta el final del estudio. La temperatura más alta se registró con las tasas intermedia y lenta de secado del suelo en toda la evaluación. La tasa rápida de secado del suelo indujo una deshidratación total de la hoja al final del primer día. En PV y el testigo reflejaron menores cambios de temperatura del foliolo entre muestreos en la tasa de secado intermedia del suelo. Una vez que se presentó el incremento inicial, los valores fueron alrededor de 1 ºC, en comparación con la tasa de secado rápida del suelo, en la cual los valores fueron ligeramente superiores. La temperatura del foliolo central de ICA Palmar se mantuvo con menor variación en el tratamiento testigo durante el estudio; se incrementó 1,8 °C en las primeras dos horas de inducido el estrés hídrico, y posteriormente se mantuvo ligeramente por encima (0,8 °C) hasta el final de la evaluación. En el tratamiento de tasa de secado intermedia del suelo, la temperatura del folíolo se incrementó 0,5 ºC en relación con la temperatura inicial, y 1,5 ºC con la temperatura de las primeras dos horas de evaluación. Al final del primer día se incrementó 4 ºC. Al día siguiente, se mantuvo en promedio a 26 °C. La tasa de secado rápida del suelo, también en esta variedad, indujo la temperatura más alta del foliolo. Las variaciones, después de iniciado el muestreo, fueron al principio de 3 ºC y posteriormente menores, alrededor de 1 ºC. En las tres variedades hubo una relación inversa entre la temperatura del foliolo central y su conductancia estomática, posiblemente por el aumento en la temperatura de la hoja (Hsiao, 1973) debido al cierre estomático (Gates, 1968; Hsiao, 1973; Jarvis, 1993). Asimismo, se redujo la tasa de asimilación de CO2 de manera diferencial entre variedades. Ya han sido documentadas diferencias entre especies (Hsiao, 1973; Jones, 1990; Aguirre-Medina et al., 2002), y en este caso entre variedades. El nivel de incremento en la temperatura parece estar relacionado con la presencia o ausencia de pubescencia en ambas caras del folíolo (Aguirre-Medina et al., 2002), que además de mantener la capa límite (Johnson, 1975), incrementa la reflectancia de luz desde la superficie de la hoja (Ehleringer et al., 1976).
En conclusión, la tasa de secado del suelo ejerció una respuesta diferencial entre las variedades de frijol en algunos de los parámetros determinados. La exposición de una parte longitudinal al secado del suelo en las variedades tolerantes PV e ICA Palmar, indujo el incremento y la disminución en la conductancia estomática y la asimilación de CO2 a través del tiempo. La exposición de ambos lados de la maceta al secado del suelo afectó ambas variables con mayor impacto al segundo día del estudio. La disponibilidad de agua en el suelo no influenció la apertura del estoma. El mayor incremento en la temperatura del folíolo se produjo al inicio de cualquier nivel de estrés hídrico en las tres variedades de frijol. Entre variedades, ICA Palmar mantuvo la menor temperatura del folíolo.
REFERENCIAS
1. Aguirre-Medina, J.F., J.A. Acosta-Gallegos, L.M. Ruiz-Posadas, J. Kohashi-Shibata y C. Trejo-López (2002). Diferencias morfológicas de la epidermis de la hoja en tres variedades de Frijol y su relación con la tolerancia a la sequía. Agricultura Técnica en México 28: 53-64. [ Links ]
2. Aguirre-Medina, J.F., J. Kohashi-Shibata, C. Trejo-López, J.A. Acosta-Gallegos y L.M. Ruiz-Posadas (2005). Respuesta fisiológica de dos variedades de Phaseolus vulgaris L. a la suspensión del riego en un sistema de raíz dividida. Phyton, International Journal of Experimental Botany 74: 143-149. [ Links ]
3. Bates, L.M. y A.E. Hall (1981). Stomatal closure with soil water depletion not associated with changes in bulk leaf water status. Oecología 50: 62-65. [ Links ]
4. Begg, J.E. y N.C. Turner (1976). Crop water deficits. Advances in Agronomy 28: 161-217. [ Links ]
5. Blackman, P.G. y W.J. Davies (1985). Root-to-shoot communication in maize plants of the effects of soil drying. Journal of Experimental Botany 42:1225-1231. [ Links ]
6. Blum, A., J.W. Johnson, E.L. Ramseur y E.W. Tollner (1991). The effect of drying a top soil and a possible non-hydraulic root signal on wheat growth and yield. Journal of Experimental Botany 42: 1-16. [ Links ]
7. Chaves, M.M. (1991). Effects of water deficits on carbon assimilation. Journal of Experimental Botany 42: 1-16. [ Links ]
8. Croker, L.J., W.T. Witte y R.M. Augé (1998). Stomatal sensitivity of six temperate, deciduous tree species to non-hydraulic root-to-shoot signalling of partial soil drying. Journal of Experimental Botany 49: 761-774. [ Links ]
9. Davies, T.D. (1987). Diurnal and seasonal patterns of net photosynthesis by irrigated Chrysothamnus nauseosus under field condition. Photosynthesis Research 11:201-209. [ Links ]
10. Davies, W.J. y J. Zhang (1991). Root signals and regulation of growth and development of plants in drying soil. Annual Review of Plant Physiology and Plant Molecular Biology 42: 55-76. [ Links ]
11. Dixon, M.A. y R.W. Johnson (1993). Interpretation of the dynamics of plant water potential. En: Borghetti, M., Grace, J. y Raschi, A. (eds), pp. 63-74. Water transport in plants under climatic stress. Cambridge University Press, Cambridge, UK. [ Links ]
12. Ehleringer, J., O. Bjorkman y H.A. Mooney (1976). Leaf pubescence: Effects on absorbance and photosynthesis in desert shrub. Science 192: 376-377. [ Links ]
13. Epstein, M. (1972). Mineral nutrition of plants: principles and perspectives. Wiley International Edition, USA. 412 p. [ Links ]
14. Farquhar, T.D. y T.D. Sharkey (1982). Stomatal conductance and photosynthesis. Annual Review of Plant Physiology 33: 317-345. [ Links ]
15. Gates, M.D. (1968). Transpiration and leaf temperature. Annual Review of Plant Physiology 19: 211-238. [ Links ]
16. Hartung, W., S. Slovik y M. Baier (1990). pH changes and redistribution of abscisic acid within the leaf under stress. En: Davies, W.J. y Jeffcoat, B. (eds), pp. 215-236. Importance of root to shoot communication in the response to environmental stress. British Society for Plant Growth Regulation, Monograph No. 21, Bristol, England. 398p. [ Links ]
17. Hsiao, T.C. (1973). Plant responses to water stress. Annual Review of Plant Physiology 24: 519-970. [ Links ]
18. Hsiao, T.C., E. Acevedo, E. Fereres y D.W. Henderson (1976). Water stress, growth and osmotic adjustment. Philosophical Transactions of the Royal Society of London 273: 479-500. [ Links ]
19. Jarvis, P.G. (1993). Global changes and plant water relations. En: Borghetti, M,, Grace, J. y Raschi, A. (eds), pp. 1-13. Water transport in plants under climatic stress. Cambridge University Press, Cambridge, UK. [ Links ]
20. Johnson, B.H. (1975). Plant pubescence: An ecological perspective. The Botanical Review 41: 233-258. [ Links ]
21. Jones H.G. (1990). Control of growth and stomatal behavior at the whole plant level: effect of soil drying. En: Davies, W.J. y Jeffcoat, B. (eds), pp.81-93. Importance of root to shoot communication in the response to environmental stress. British Society for Plant Growth Regulation, Monograph No. 21, Bristol, England. 398 p. [ Links ]
22. Mansfield, T. A. y C.J. Atkinson (1990). Stomatal behaviour in water stressed plants. En: pp.241-264. Stress Responses in Plants: Adaptation and Acclimation Mechanisms. Wiley-Liss, Inc. 407p. [ Links ]
23. Masle, J. y J.B. Passioura (1987). The effect of soil strength on the growth of young wheat plants. Australian Journal of Plant Physiology 14: 643-656. [ Links ]
24. McCree, K.J. y S.G. Richardson (1987). Salt increases the water use efficiency in water stressed plants. Crop Science 27: 543-547. [ Links ]
25. Mulholland, B. J., A. Hussain, C. R. Black, I. B. Taylor y J. A. Roberts (1999). Does root-source ABA have a role in mediating growth and stomatal responses to soil compactation in tomato (Lycopersicum esculentum)? Physiologia Plantarum 107: 267-276. [ Links ]
26. Raschke, K. (1970). Leaf hydraulic system: rapid epidermal and stomatal responses to changes in water supply. Science 167: 189-191. [ Links ]
27. Schultze, E.D. (1986). Carbon dioxide and water vapour exchange in response to drought in the atmosphere and in the soil. Annual Review of Plant Physiology 37: 247-274. [ Links ]
28. Schultze, E.D., N. C. Turner, T. Gollan y A. Shackel (1987). Stomatal response to air humidity and to soil drought. En: Zeiger, E., Farquhar, G.D. y Cowan, I.R. (eds), pp 311-321. Stomatal function. Stanford, California USA. [ Links ]
29. Subbarao, G.V. y C. Johansen (2002). Transpiration efficiency: Avenues for genetic improvement. En: Pessarakli, M. (ed), pp. 835-855. Handbook of Plant and Crop Physiology. 2nd Ed., Marcel Dekker, Inc., New York. [ Links ]
30. Trejo, C. y W.J. Davies (1991). Drought induces closure of Phaseolus vulgaris l. Stomata precedes leaf water deficit and any increase in xylem ABA concentration. Journal of Experimental Botany 42: 1507-1515. [ Links ]
31. Tardieu, F. y T. Simonneau (1998). Variability among species of stomatal control under fluctuating soil water status and evaporative demand: modeling isohydric and anisohydric behaviors. Journal of Experimental Botany 49: 419-432. [ Links ]
32. Turner, N.C., E.D. Schultze y T. Gollan (1985). The response of stomata and leaf gas exchange to vapour pressure deficits and soil water content. 2. In the mesophytic herbaceous species Helianthus annus. Oecología 65: 348-355. [ Links ]
33. Webb, A.A.R. y A. Mansfield (1992). How do stomata work? Journal of Biological Education 23: 19-26. [ Links ]














