Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Phyton (Buenos Aires)
versión On-line ISSN 1851-5657
Phyton (B. Aires) v.77 Vicente López ene./dic. 2008
ARTÍCULOS ORIGINALES
Micropropagación de plantas en líneas experimentales de maíces forrajeros derivadas de un cruzamiento entre Zea maysL. y Zea diploperennisIltis, Doebley y Guzmán (Con 1 Tabla y 1 Figura)
Plant micropropagation in experimental lines of forage maize coming from crossing Zea mays L. and Zea diploperennis Iltis, Doebley and Guzmán (With 1 Table & 1 Figure)
Torroba MC, HA Paccapelo, L Aguilera, J Mazzola
Facultad de Agronomía UNLPam. Dirección: CC 300. (6300) Santa Rosa, La Pampa, Argentina. Address Correspondence to: María del Carmen Torroba, e-mail: torroba@agro.unlpam.edu.ar; Telefax: 02954-433092.
Recibido/Received 13.11.2007. Aceptado/Accepted 18.04.2008.
Resumen. Se evaluó una metodología de cultivo in vitro tendiente a mejorar la regeneración de plantas de maíz por organogénesis directa, con el objetivo de lograr múltiples vástagos genéticamente homogéneos. La misma consiste en la utilización del meristema apical como explanto y el agregado de 2 mg/l de benziladenina (BA) al medio de cultivo Murashige y Skoog (MS). Se utilizaron dos líneas experimentales de maíces forrajeros. En éstos se evaluaron dos frecuencias de subcultivos (cada 15 ó 30 días) en la línea L.850 y 1 frecuencia (cada 30 días) para la línea L.769. La línea L.850 alcanzó su máxima tasa de regeneración en el segundo repique (1,8 plantas) con subcultivos cada 30 días, y en el quinto subcultivo (1,8 plantas) con sub-cultivos cada 15 días. La línea L.769 alcanzó la máxima tasa de regeneración en el cuarto subcultivo (1,7 plantas). Los valores mencionados son bajos comparados con embriogénesis somática, pero no se detectaron variaciones somaclonales en los fenotipos de las plantas a campo; se observó una acentuada uniformidad dentro de las líneas.
Palabras clave: Micropropagación; Tasa de regeneración; Cultivo in vitro; Benziladenina; Maíz forrajero; Zea mays L.; Zea diploperennis I; D&G.
Abstract. An optimized methodology for improving regeneration of maize plants by direct organogenesis was evaluated. Our objective was to obtain genetically homogeneous plants through in vitro methods to regenera-te clumps of multiple shoots from shoot tips at high frequency. Cultures were initiated from shoot tips of experimental lines of maize on a Murashige & Skoog (MS) medium supplemented with 2 mg/l benziladenine. Two experimental forage maize lines were used, in which two frequencies of subcultu-res were evaluated, namely line L. 850 (every 15 or 30 days) and line L.769 (every 30 days). It was observed that the highest rate of regeneration in line L.850 was reached in the second subculture (1.8 plants) with subculture every 30 days, and in the fifth subculture (1.8 plants) with subculture every 15 days. In line L.769, the highest frequency of regeneration was reached in the fourth subculture (1.7 plants). Regeneration rates were low compared with somatic embryogenesis, but no somaclonal variations were detected in field plant phe-notypes; a marked uniformity was detected within lines.
Key words: Micropropagation; Regeneration rate; In vitro culture; Benziladenine; Forage maize; Zea mays L.; Zea diploperennis I; D&G.
INTRODUCCIÓN
La introgresión de genes de la especie silvestre Zea diploperennis Iltis, Doebley y Guzmán en el genoma de Zea mays L. permitiría incorporar atributos morfológicos de interés para la utilización forrajera de la especie (Troiani et al., 1988; Paccapelo y Molas, 1996). El desarrollo de líneas endocriadas a partir de poblaciones recombinantes entre ambas especies se alarga respecto al método tradicional de cruzas intraespecíficas, debido a la incorporación de muchos genes indeseables de la especie silvestre (Bolaño et al., 2005).
La aplicación exitosa de las técnica de cultivo de tejidos es una herramienta muy poderosa para suplementar los métodos fitotécnicos convencionales para el mejoramiento de los cultivos (Rapela, 1986).
Hasta hace unos pocos años, era difícil obtener plántulas regeneradas mediante cultivos de callo embriogénico o por organogénesis directa en maíz (Zea mays L.), sorgo (Sorghum bicolor Moench.) y otras gramíneas (Vasil y Vasil, 1985; Rosatti et al., 1994, Boget et al., 1995, Santos et al., 1996 y Seetharama et al., 2000 citados por Iracheta-Donjuan et al., 2003). Sin embargo, son numerosos los antecedentes de obtención de plantas de maíz a partir de callos organogénicos y/o embriogénicos en la actualidad (Garcia et al., 1992; García y Molina, 1998; Huang y Wei, 2004; Guangyuan et al., 2006).
Actualmente, el uso de embriones inmaduros de 1-2 mm de longitud, obtenidos a los 10-15 días después de la fertilización (Green y Phillips, 1975; Springer et al., 1979; Duncan et al., 1985; Vasil et al., 1985) es el explanto más usado para obtener callos.
La utilización del medio de cultivo Murashige y Skoog (MS) (Murashige y Skoog, 1962) y Chu (Chu, 1978) (N6) con el agregado de ácido 2,4-diclorofenoxiacético (2,4-D) induce la formación de callos. Sin embargo, los mismos tienden a oxidarse, dependiendo del genotipo, impidiendo la proliferación y posterior regeneración (Millán y Cagnasso, 1997).
La organogénesis directa a partir de ápices produce escasos vástagos en maíz (Raman et al., 1980 citado por Iracheta-Donjuan et al., 2003). Sin embargo, recientes estudios mencionan un alto grado de desarrollo de tallos adventicios, yemas axilares y embriones somáticos (Zhong et al., 1992 a). Por otra parte, la respuesta del cultivo de tejido de maíz está muy influenciada por el genotipo, ya que con algunos se obtienen resultados exitosos, mientras que con otros la respuesta ha sido baja o nula (Tomes y Smith, 1985).
La regeneración de plantas utilizando como explanto meristemas apicales, es mucho menos dependiente del genotipo comparado con los embriones inmaduros. Otra de las ventajas de la utilización de meristemas apicales como explanto es que es más rápido y sencillo de obtener, comparado con los embriones inmaduros, que deben obtenerse de plantas enteras, requiriendo mayor tiempo, espacio y a veces costo (Wenbin Li et al., 2001).
El ápice de maíz puede ser utilizado como explanto para inducir la formación de múltiples vástagos o embriones somáticos in vitro, variando las concentraciones de benziladenina (BA) y ácido 2,4-diclorofenoxiacético (2,4- D) en el medio de cultivo (Zhong et al. ,1992b; García et al., 1996).
Los requerimientos de BA en genotipos de maíz, tanto para la formación de tallos como de embriones somáticos, indicarían que la misma podría ser la clave de la regulación de la morfogénesis en cultivos de meristemas de maíz. Por su parte, el cultivo de ápices de maíz con el agregado de 2,4-D solamente, no regenera plantas (Zhong et al., 1992a). Además, el uso de 2,4-D en concentraciones mayores de 4mg/l tiene altas posibilidades de mutaciones somáticas (Huang y Wei, 2004).
La organogénesis directa en especies como el maíz, permitiría evadir los problemas hormonales que se presentan al tratar de regenerar plántulas vía cultivo de células, callos y embriones somáticos. Sin embargo, la producción de brotes resulta escasa usando la misma (Iracheta-Donjuan et al., 2003).
La estabilidad genética en líneas endocriadas de un programa de mejoramiento tradicional demanda un largo periodo de tiempo, más aún cuando se logran líneas provenientes de cruzas amplias requiriéndose aumentar el número de generaciones de endocría para uniformarlas.
La multiplicación agámica (clonación) utilizando el cultivo in vitro ayudaría a lograr la uniformidad de las líneas experimentales permitiendo la obtención de dos generaciones de endocría al año.
La clonación a partir de múltiples vástagos, sin el uso de 2,4-D, evitaría las variaciones somaclonales que se generan como resultado de la utilización de este regulador de crecimiento.
Nuestro objetivo fue obtener una alta tasa de multiplicación asexual de individuos de líneas endocriadas (S8) originadas de la cruza entre Zea mays L. x Zea diploperennis Iltis, Doebley y Guzmán para acentuar la uniformidad genética en sus características forrajeras.
MATERIALES Y MÉTODOS
Se utilizaron semillas de las líneas endocriadas (S8) L.769 y L.850 provenientes de la población segregante derivada de la cruza entre Zea mays L. x Zea diploperennis Iltis, Doebley y Guzmán. Se lavaron con agua destilada y Triton en agitación durante 20 min y posteriormente se las sometió a un proceso de desinfección que consistió en: lavado con etanol al 70% durante 15 min, agua estéril 3 veces, hipoclorito de sodio 80 g/l al 30% durante 30 min y se enjuagaron 4 veces con agua estéril.
Las semillas permanecieron 24 h en agua estéril y se realizó en una segunda desinfección que consistió en un lavado con lavandina 802 g/l al 20% durante 15 min en agitación y 4 enjuagues con agua estéril.
Se extrajeron los embriones maduros tratando de eliminar todo el endosperma residual y se colocaron en tubos de 60 ml en el medio MS sólido en oscuridad durante 3 a 5 días para finalmente extraer el ápice. Estos ápices se sembraron en MS con el agregado de 500 mg/l de caseína hidrolizada, 3 % de sacarosa, y 2 mg/l de benziladenina.
A los treinta días de la siembra se iniciaron los subcultivos, y éstos se efectuaron cada treinta días en la línea 769 y cada quince o treinta días en la línea 850. Esta etapa de multiplicación se llevó a cabo en una cámara de crecimiento con 16 h de luz, una intensidad lumínica de 85 µmoles/m2/s a 26 ± 1 ºC.
La variable analizada fue el número de individuos obtenidos por explanto. Se evaluó la respuesta a partir del tercer subcultivo, y se establecieron tres categorías: sin respuesta (menos de cinco individuos), media (entre cinco y diez), y alta (mayor de diez).
Se determinó la tasa de regeneración entre subcultivos como el cociente entre número de individuos logrados en un determinado subcultivo respecto al número de individuos del subcultivo anterior.
El enraizamiento se efectuó en un medio MS libre de reguladores de crecimiento, permaneciendo en la cámara alrededor de 50 días en las mismas condiciones de intensidad lumínica y temperatura que las mencionadas en la etapa de multiplicación. La etapa de rustificación se llevó a cabo en invernáculo donde permanecieron durante 51 días y posteriormente fueron llevadas a campo. Se trasplantaron en surcos a campo 11 plantas de la línea L.850 con subcultivos cada 30 días ó 30 plantas con subcultivos cada 15 días, y 20 plantas de la línea L.769 con subcultivos cada 30 días. La separación entre plantas dentro del surco fue de 0,70 m y 0,30 m.
RESULTADOS Y DISCUSIÓN
La línea L.769 con subcultivos cada 30 días mostró un comportamiento diferencial de los individuos, tanto dentro como entre los subculti-vos (Tabla 1). La respuesta fue media para los individuos 1, 5, 7, 10, 12, 13, 15 y 19, y alta para el individuo 9 en el cuarto subcultivo.
Tabla 1. Número de individuos obtenidos por explanto en líneas autofecundadas de maíces forrajeros derivadas de una población recombinante, originada de la cruza entre Zea mays L x Zea diploperennis Iltis, Doebley y Guzmán. Los números inmediatamente debajo del subtítulo "Subcultivos cada 15 ó 30 días" representan el número de subcultivos.
Table 1. Number of individuals obtained per explant in self-pollinated lines of forage maize, derived from a recombinant population of the cross between Zea mays L x Zea diploperennis Iltis, Doebley and Guzmán. Numbers immediately below the subheading "Subcultivo cada 15ó 30 días" represent the number of subcrops.


La línea 850 con subcultivos cada 30 días mostró que los individuos 14 y 16 tuvieron una respuesta media para el cuarto subcultivo y sólo en el individuo 6 la respuesta fue alta (Tabla 1). El resto de los individuos no respondió al tratamiento.
En la línea L.850 también se efectuaron subcultivos cada 15 días hasta el séptimo subcultivo (Tabla 1). En éste último, los individuos 9, 10 y 11 tuvieron alta respuesta. La ventaja de este tratamiento en cuanto al número de individuos clonados se vería contrarestada por el aumento del riesgo de contaminación de los explantos, la posibilidad de inducir mutaciones en los individuos, y la floración anticipada al acumular horas de luz en cada subcultivo.
Zhong et al. (1992a) lograron la regeneración de plantas de distintos genotipos de maíz con el solo agregado de BA utilizando como explanto el ápice meristemático. Estos autores estudiaron la eficiencia relativa en la producción de vástagos luego de ocho semanas en las que se efectuó un cultivo y un subcultivo en el medio MS suplementado con caseína hidrolizada y 2mg/l de BA. El comportamiento de los genotipos fue diferente debido a que solo dos de ellos produjeron más de 20 vástagos por meristema cultivado mientras que el resto no superó los diez. Los tallos se presentaron bajo la forma de múltiples vástagos con dos orígenes diferentes: uno adventicio y otro a partir de yemas axilares.
El uso conjunto de 2,4- D y BA incrementó el número adventicios tanto por embriogénesis directa como a partir de callos que se originaron en el explanto; utilizando solo 2,4-D no se logró la regeneración de plantas (Zhong et al., 1992 a).
La inducción de callos, por la acción del 2,4-D, originó la aparición de variaciones somaclonales que resultan indeseables cuando se pretende obtener una multiplicación clonal de individuos (Garcia et al., 1992; Bai y Knott, 1993 cit. por Molina y García, 1998).
La L.850 con subcultivos cada 30 días alcanzó su máxima tasa de regeneración en el segundo subcultivo (1,8 plantas), descendiendo abruptamente en el tercero, y manteniéndose estable en el cuarto subcultivo (Fig. 1).
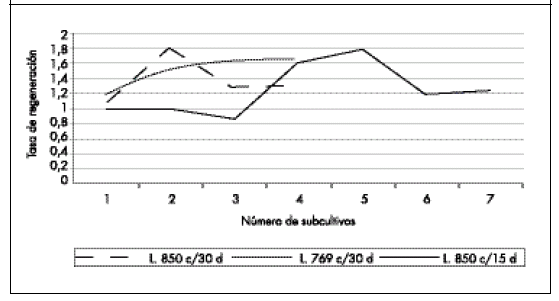
Fig 1. Tasa de regeneración de líneas experimentales de maíz forrajero en función del número de subcultivos.
Fig 1. Regeneration rate of experimental lines of forage maize versus the number of subcultures.
La L.850 con subcultivos cada 15 días mostró la mayor tasa de regeneración en el quinto subcultivo (1,8 plantas), o sea a los 75 días de iniciado el cultivo, y a partir de allí los valores de regeneración descendieron abruptamente (Fig. 1). Comparando ambos tratamientos se observa que el tratamiento cada 15 días fue ineficiente tanto desde el punto de vista temporal como operativo, reflejándose en un mayor consumo de drogas, mayor demanda de mano de obra, aumento del riesgo de contaminación y mayor probabilidad de mutaciones (García et al.,1992).
La línea L.769 presentó una respuesta relativamente uniforme a lo largo de los distintos subcultivos a partir del segundo subcultivo (Fig. 1). La máxima tasa de regeneración fue obtenida en el cuarto subcultivo (1,7 plantas). El aumento en la tasa de regeneración que se logró entre el segundo y el cuarto subcultivo, no resultó eficiente desde el punto de vista práctico. Esta respuesta diferencial entre genotipos está ampliamente corroborada en la bibliografía (Tomes y Smith, 1985 cit. por García et al., 1992; Vasil y Vasil, 1985; Shyamala y Smith, 1990).
El valor máximo de la tasa de regeneración fue prácticamente coincidente en los tres tratamientos (Fig. 1), y se considera bajo respecto a los valores obtenidos por tratamientos con numerosos subcultivos a través de embriogénesis somática (Green y Phillips, 1975; García et al., 1992) e indicativo de que el segundo subcultivo sería el óptimo. Nuestros resultados coinciden con la bibliografía respecto a que no resulta exitoso trabajar con numerosos subcultivos. Se debe resignar el número de plantas regeneradas para no aumentar la probabilidad de mutaciones o variaciones somaclonales (García y Molina, 1998).
La baja producción de brotes por organogénesis directa a partir de ápices fue mencionada en investigaciones previas en maíz (Raman et al., 1980 cit. por Iracheta-Donjuan, 2003).
Los porcentajes de enraizamiento de las líneas L.769 y L.850 con subcultivo a los 30 días para L.769 o a los 15 días para L.850 fueron de 68, 64 y 48%, respectivamente. Los subcultivos fueron posteriormente llevados al campo para que continuaran con sus etapas de crecimiento y desarrollo.
La observación fenotípica de las plantas llevadas a campo no permitió detectar variaciones morfológicas, lográndose un alto grado de uniformidad dentro de las líneas.
CONCLUSIONES
El uso de un único regulador de crecimiento (BA) y bajo número de subcultivos permite regenerar individuos con menores probabilidades de mutaciones. Si bien el número de individuos regenerados es menor comparado con la embriogénesis somática, el mismo resulta exitoso cuando el objetivo es multiplicar fielmente el genotipo de una línea selecta. Se debería ajustar el tipo y la dosis de reguladores a fin de optimizar el número de individuos regenerados.
REFERENCIAS
1. Bolaño, M.A.J., L M. Bosco, C. A. Fenoglio y H. A. Paccapelo (2005). Evaluación de híbridos simples de maíz forrajero originados de la cruza entre Zea mays x Zea diploperennis I. en Santa Rosa, La Pampa. Actas del VIII Congreso Nacional de Maíz. Rosario, 16-18 de Noviembre, p.327-330. [ Links ]
2. Chu, CC. (1978). The N6 medium and its application to another cultur of cereal crops. En: "Proceedings of Symposium on Plant Tissue Culture". Science Press. Peking. p 43-50. [ Links ]
3. Duncan, D.R., M.E. Williams, B.E. Zehr y J.M. Widholm (1985). The production of callus capable of plant regeneration from inmature embryos of numerous Zea mays genotypes. Planta 165: 322-332. [ Links ]
4. Garcia, M.D., M. del C. Molina y O.H. Caso (1992a). La regeneración de plantas de maíz (Zea mays ssp. mays) a partir del cultivo de tejidos y su aplicación en el mejoramiento genético. Revista de la Facultad de Agronomía, La Plata 68: 15-25. [ Links ]
5. García, M.D., J. Pesqueira y M.C. Molina (1996). Regeneración de plantas a partir de ápices caulinares de maíz (Zea mays ssp.mays). XXI Reunión Argentina de Fisiología Vegetal. Mendoza. p. 14-15. [ Links ]
6. García, M.D. y M.C.Molina (1998). Analysis of Genetic Variability in Longterm Callus Cultures and Regenerated Plants of Maize. Cytologia 63: 183-190. [ Links ]
7. Green, C.E. y R.L Phillips (1975). Plant regeneration from tissue culture of maize. Crop Science 15: 417-421. [ Links ]
8. Guangyuan, He., Z. Jinrui, K. Li , Z. Xiong, M. Chen, J. Chang, Y. Wang, G. Yang y B. Barnabás (2006). An improved system to establish highly embryogenic haploid cell and protoplast cultures from pollen calluses of maize ( Zea mays L.). Plant Cell, Tissue and Organ Culture 86: 15-26. [ Links ]
9. Huang, X.Q. y Z.M. We i (2004). High-frequency plant regeneration through callus initiaton from mature embryos of maize ( Zea Mays L.) Plant Cell Reports 22: 793-800. [ Links ]
10. Iracheta-Donjuan, L., M.C. López Peralta, V.A. González-Hernández, I Sanchez- Cabrera y E. Cárdenas-Soriano (2003). Variación genotípica en la capacidad organogénica in vitro del maíz. Agrociencia 37: 451-465. [ Links ]
11. Millán, R.H. y L. Cagnasso (1997). Inducción de callos a partir de embriones inmaduros en líneas S1 de maíz. Trabajo Final de Graduación. Facultad de Agronomía. UNLPam. [ Links ]
12. Molina, M.C. y M.D. García (1998). Analysis of genetic variability in long-term callus cultures and regenerated plants of maize. Cytologia 63: 183-190. [ Links ]
13. Murashige, T. y F. Skoog (1962). A revised medium for rapid growth and bioassay with tobacco tissue cultures. Physiologia Plantarum 15: 473-497. [ Links ]
14. Paccapelo, H.A. y M.L. Molas (1996). Caracterización de una población de maíz forrajero con introgresión de Zea diploperennis. Revista de Investigaciones Agropecuarias 27: 33-38. [ Links ]
15. Rapela, M.A. (1986). Mejoramiento del maíz. Un sistema experimental modelo para cultivo de tejidos in vitro. Revista de la Facultad de Agronomía 61 y 62: 1985-86. [ Links ]
16. Shyamala, B. y R.H. Smith (1990). Regeneration in cereal tissue culture. Crop Science 30: 1328-1337. [ Links ]
17. Springer, W.D, C.E. Green y K.A. Kohn (1979). An histological examination of tissue culture initia-tion from immature embryos of maize. Protoplasma 101: 269-281. [ Links ]
18. Tomes, D.T. y O.S. Smith (1985). The effect of parental genotype on initiation of embryonic callus from elite maize (Zea mays L) germplasm. Theoretical Applied Genetics 70: 505-509. [ Links ]
19. Troiani, H., H.A. Paccapelo y D.A. Golberg (1988). Descripción botánica del híbrido interespecífico entre Zea mays L. x Zea diploperennis. Revista de la Facultad de Agronomía de la UNLPam 3: 153-158. [ Links ]
20. Vasil, V. , C. Lu y I.K. Vasil (1985). Histology of somatic embryogenesis in cultured immature embryos of maize (Zea mays L). Protoplasma 127: 1-8. [ Links ]
21. Wenbin, Ll., P. Masilamany, K. Kasha y P. Pauls (2001). Developmental, tissue culture, and geno-typic factors affecting plant regeneration from shoot apical meristems of germinated ZEA MAYS L. seedlings. In Vitro Cell. Dev. Biol. Plant 38: 285-292. [ Links ]
22. Zhong, H., C. Srinivasan y M.B. Sticklen (1992a). In vitro morphogenesis of corn (Zea mays L) I. Differentiation of multiple shoot clumps and somatic embryos from shoot tip. Planta 187: 483-489. [ Links ]
23. Zhong, H., C. Srinivasan y M.B. Sticklen (1992b). In vitro morphogenesis of corn (Zea mays L) II. Differentiation of ear and tassel clusters from culture shoots apices and immature inflores-cences. Planta 187: 490-497. [ Links ]














