Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Insuficiencia cardíaca
versión On-line ISSN 1852-3862
Insuf. card. vol.1 no.4 Ciudad Autónoma de Buenos Aires dic. 2006
WORKSHOP DE BETA BLOQUEANTES EN INSUFICIENCIA CARDIACA
PARTE II
Estudio COMET
Estudio europeo: carvedilol vs metoprolol
Carvedilol or Metoprolol European Trial
Coordinador
Sergio V. Perrone*
Presentador COMET
Fabián Diez**
Panelistas invitados
Oscar Allal, Guillermo Allende, Marcos Amuchástegui, Roberto Colque, Carlos Poy, Alfredo D'Ortencio, Rodolfo Sarjanovich, Héctor Tacchi, Félix Zelaya
* Jefe de la División Trasplante Cardíaco. Instituto FLENI. Ciudad autónoma de Buenos Aires. República Argentina.
**Médico Cardiólogo. Jefe Unidad Coronaria Servicio de Cardiología Hospital Italiano "Garibaldi". Rosario. Santa Fe. República Argentina.
Correspondencia: Dr. Fabián Diez
Laprida 1564 3º A
2000 - Rosario, Santa Fe. República Argentina.
E-mail: fabiandiez@ciudad.com.ar
Estudio COMET
Dr. Fabián Diez (FD): Con el transcurso de los años se han modificado los modelos desarrollados de insuficiencia cardíaca (IC), y a partir del año 2000 se desarrolló el denominado modelo neurohormonal, básicamente dado por estas dos sustancias: la angiotensina y la norepinefrina (Fig. 1).
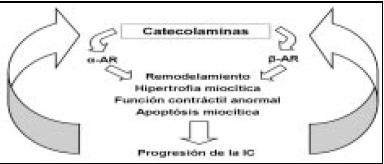
Figura 1. Papel del Sistema Adrenérgico en IC.
Hablando de beta bloqueantes, vamos a analizar el papel del sistema adrenérgico en la IC, donde constatamos que las catecolaminas estimulan los receptores beta y los receptores alfa, produciendo alteraciones tanto a nivel miocárdico como vascular: remodelamiento, hipertrofia, función contráctil anormal, apoptósis miocárdica. Todo eso conlleva a la progresión de la insuficiencia cardíaca. Y tal es así, que ya desde hace muchos años, conocemos que los pacientes con mayor nivel de norepinefrina en sangre, tienen mayor mortalidad (Fig. 2). También sabemos que a medida que los pacientes tienen más IC, disminuye la expresión de receptores beta 1, en los pacientes portadores de ella (Fig. 3).
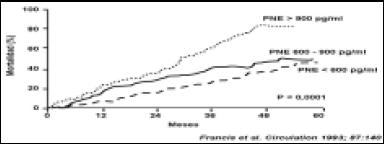
Figura 2. Relación entre niveles de norepinefrina plasmática y mortalidad.
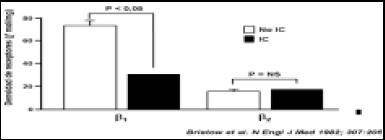
Figura 3. Densidad de receptores beta 1 y beta 2 en corazones con y sin IC.
En base a esto, se hizo una innumerable cantidad de estudios con diferentes beta bloqueantes (bisoprolol, metoprolol, carvedilol) que mostraban beneficios, tanto en la sobrevida, como en las re-hospitalizaciones (Fig. 4).
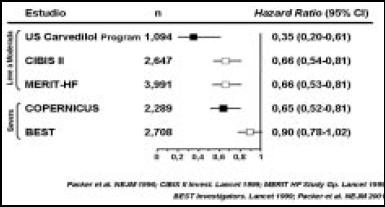
Figura 4. Estudios prospectivos de beta bloqueantes en ICC.
Pero, cada uno de los beta bloqueantes más conocidos, o autorizados para usar en IC tienen diferentes efectos (Fig. 5). El bisoprolol y el metoprolol, fundamentalmente actúan en el nivel del receptor beta 1; y el carvedilol actúa también sobre los receptores beta 2, y alfa 1.
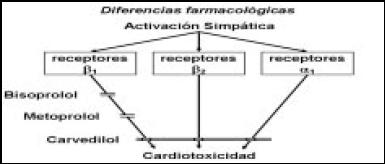
Figura 5. Efectos de diferentes agentes beta bloqueantes.
¿Qué hace el carvedilol a diferencia del metoprolol con la norepinefrina total, y la norepinefrina cardíaca específica-mente? La disminuye cuando la comparamos en estudios básicos (Fig. 6).
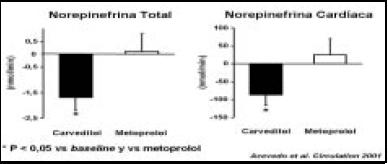
Figura 6. El carvedilol reduce la actividad simpática total y cardíaca; el metoprolol no.
Tiene, además, otros efectos adicionales, a diferencia de los otros beta bloqueantes, como el efecto antioxidante, antiendotelina, anti-proliferativo, y anti-inflamatorio (Fig. 7). La Figura 8 muestra como la sobreexpresión del receptor beta 2 es cardiotóxica.
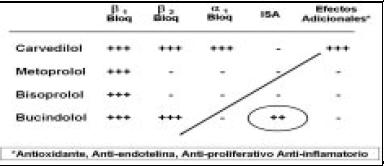
Figura 7. Diferencias farmacológicas entre los bloqueantes adrenérgicos.
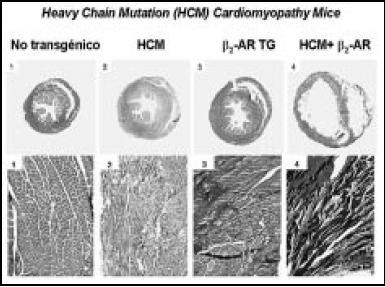
Figura 8. Cardiotoxicidad de la sobreexpresión beta 2-adrenoreceptor (AR).
¿Cuáles son los efectos de los receptores beta 2 a nivel miocárdico? Tienen un efecto directo cronotrópico, inotrópico y lusotrópico mediado por AMP cíclico (Fig. 9). Hay varios estudios básicos realizados. Estos efectos producen hiper-trofia, fibrosis y remodelamiento. Tienen también un efecto antiapoptótico, arritmogénico, y facilitan el lavado de la norepinefrina presináptica.

Figura 9. Efectos de los receptores beta 2.
¿Qué hace el receptor alfa 1? El receptor alfa 1 también promueve la hipertrofia y la fibrosis, es cardiotóxico, también arritmogénico, y produce vasoconstricción periférica con hipoperfusión renal y retención de sodio (Fig. 10).

Figura 10. Efectos de los receptores alfa 1.
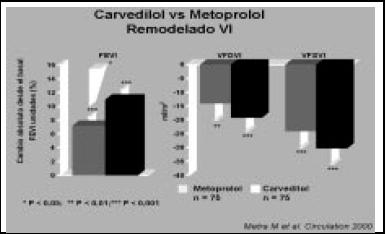
¿Antes del estudio COMET, existían estudios que comparaban metoprolol vs carvedilol? Sí, básicamente dos estudios (Fig. 11). El primero, del Dr. Metra en el año 2000, donde demostró en 150 pacientes que la fracción de eyección mejoraba más en los que recibían carvedilol, y esto estaba dado porque disminuían los volúmenes tanto de fin de diástole como de fin de sístole (Fig. 12). Y no solamente era mayor la función cardíaca, sino que clínicamente los pacientes estaban mejor, ya que mejoraba el consumo de oxígeno, el test de la caminata, el cuestionario de Minesota, y la clase funcional, todos estadísticamente significativos (Fig. 13).

Figura 11. Estudios randomizados comparando metoprolol vs carvedilol.
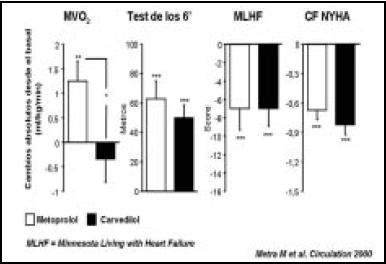
Figura 13. Cambios absolutos en la tolerancia al ejercicio y síntomas luego del tratamiento con metropolol o carvedilol.
En un meta análisis de todos estos estudios previos, realizado por el Dr. Packer, muestra la mejoría de la fracción de eyección en los pacientes que recibían carvedilol vs metoprolol (Fig. 14).
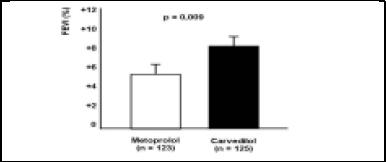
Figura 14. Meta-análisis de estudios comparativos entre metoprolol y carvedilol en ICC.
En base a estos antecedentes es que se pensó en realizar el estudio COMET, que es carvedilol vs metoprolol, un estudio eminentemente europeo.
¿Cuál fue la hipótesis de este estudio? Determinar si la acción antisimpática del carvedilol era más allá del bloqueo beta 1, para ver si tiene un efecto favorable en la sobrevida (Fig. 15).
El objetivo del estudio fue para observar las diferencias farmacológicas entre un beta bloqueante convencional y otro como el carvedilol, y si esto tenía traducción en la sobrevida de los pacientes con IC.
En este estudio europeo, el Comité Directivo estuvo formado por el Dr. Pool-Wilson y el mayor número de randomizados fue en Alemania (Fig. 16). El diseño del estudio incluyó a 3030 pacientes con IC, clase funcional II a IV, todos medicados con inhibidores de la enzima de conversión (IECA), y eran pacientes con IC leve, moderada o severa (Fig. 17). Se los randomizó, se les hizo un screening, y quedaron unos 1500 pacientes en cada grupo: metoprolol 50 mg, dos veces al día vs carvedilol 25 mg, dos veces al día, hasta llegar a un total de 1020 muertes, durante un períodode 4 a 6 años.
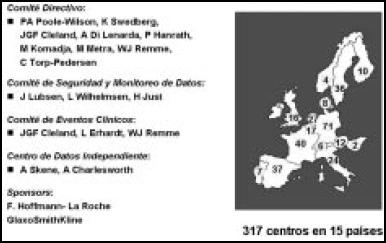
Figura 16. Organización del estudio.
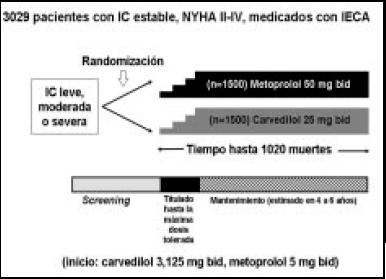
Figura 17. Diseño del estudio.
Los criterios de inclusión fueron: insuficiencia cardíaca sintomática con tratamiento estándar. Los pacientes debían estar recibiendo tratamiento diurético estable por al menos dos semanas, IECA por al menos 4 semanas, y el uso de digital y/o vasodilatador era opcional, la fracción de eyección debía ser menor o igual al 35%, y debían presentar una hospitalización cardiovascular en los dos años previos (Fig. 18).
¿Cuáles fueron los criterios de exclusión? Más o menos como todos los estudios: accidente cerebrovascular (ACV), infarto agudo de miocardio (IAM), angina inestable en los 2 meses previos; valvulopatía no corregida o arritmias; otras enfermedades que comprometan la vida; contraindicaciones absolutas con beta bloqueantes, como frecuencia cardíaca menor a 60 latidos por minuto, presión arterial sistólica menor a 85 mm Hg, bloqueo aurículo-ventricular, a menos que tenga un marcapasos, historia de asma o EPOC (enfermedad pulmonar obstructiva crónica), diabetes mellitus o insulino-dependiente inestable.
Los puntos finales primarios fueron: mortalidad, y el riesgo combinado de muerte u hospitalización por cualquier causa. El poder que se utilizó para este ensayo fue designar un 80% de poder para detectar una diferencia del 20% en la mortalidad y un 15% en el punto final combinado (Fig. 19).
Tenía otros puntos finales, los llamados secundarios, como en todos los estudios, que eran: todas las causas de mortalidad u hospitalización específicamente cardiovascular, muerte cardiovascular, infarto no fatal, trasplante cardíaco o progresión de la IC, muerte cardiovascular, clase funcional, progresión de la IC o discontinuación de la droga.
Se randomizaron 3030 pacientes, más o menos en dos grupos semejantes; no hubo diferencias, básicamente, ni en el retiro de consentimiento, ni en los perdidos en el seguimiento (Fig. 20).

Figura 20. Flujo de pacientes.
¿Cuáles eran las características basales de los pacientes? El promedio de edad fue de 62 años; la mayoría eran hombres; la mitad eran isquémicos; la IC en tiempo promedio era 42 meses; la frecuencia cardíaca de 80 latidos por minuto, con una tensión arterial bastante estable, 125-70 mm Hg; la mayoría era clase funcional II-III; y tenían fibrilación auricular, alrededor del 20%; y un cuarto de los pacientes presentaba diabetes (Fig. 21).
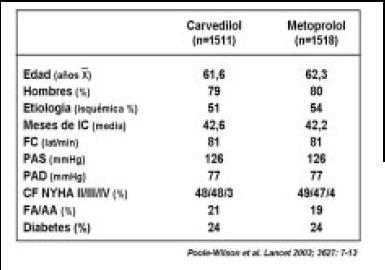
Figura 21. Características basales.
Comparado con otros estudios, el COMET mostró que la mayoría eran hombres (como casi todos); la edad promedio era similar a todos; la frecuencia cardíaca y la tensión arterial también eran similares; y el peso, con el MERIT que lo publicó, el resto no lo hizo, era bastante similar (Fig. 22).
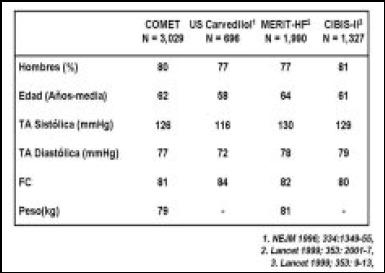
Figura 22. Características demográficas.
¿Cuáles eran las causas, o la etiología de la IC de los pacientes de este estudio? La mayoría era cardiopatía isquémica; un tercio de los pacientes tenía miocardiopatía no isquémica, un grupo importante de pacientes se le atribuyó a la hipertensión arterial, otros pacientes valvulares, diabéticos, o la misma arritmia (Fig. 23). ¿Cómo se dividían los grupos de la IC? La mayoría clase funcional II, III, muy poco porcentaje en clase IV, y la fracción de eyección similar a la que le había dado el MERIT, del 26% (Fig. 24).

Figura 23. Causas de insuficiencia cardíaca.

Figura 24. Severidad de la insuficiencia cardíaca
¿Qué medicación recibían los pacientes antes de ingresar alestudio? Como vemos, y a pesar de los malos datos que tenemos, la mayoría recibía diuréticos (99%); un alto porcentaje IECA (91%); un porcentaje bastante menor de bloqueantes de los receptores de la angiotensina (7%); un porcentaje menor de espironolactona (11%); un 59%, digoxina; el 49%, aspirina; y, un 46%, warfarina (Fig. 25).
La dosis planeada fue carvedilol: 25 mg c/12 hs y tartrato de metoprolol: 50 mg c/ 12 hs, titulados con intervalos cada 2 semanas: carvedilol: 6,25; 12,5; 25 a 50 mg/día y metoprolol: 10, 25, 50 a 100 mg/día (Fig. 26).
El punto final primario fue la mortalidad total de 17% a favor del carvedilol (Fig. 27).
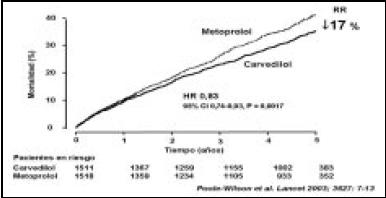
Figura 27. Punto final primario.
También hubo una reducción, especialmente de mortalidad cardiovascular del 20%, es decir, fue mayor que la diferencia en la mortalidad total (Fig. 28). Viéndolo por sub-grupo, vemos que no hubo diferencia, aunque muy pocas mujeres, pero no hubo diferencia en mayores o menores de 65 años, si hubo algunas diferencias, también eran muy pocos los pacientes en clase IV, que tenían etiología isquémica, o si tenían baja o alta fracción de eyección más allá del 25%, si tenían más o menos frecuencia cardíaca, o más o menos presión arterial sistólica, y si tenían o no diabetes (Fig. 29 y 30). Casi todos los grupos, salvo los que quedaron muy pequeños, dieron a favor de carvedilol.
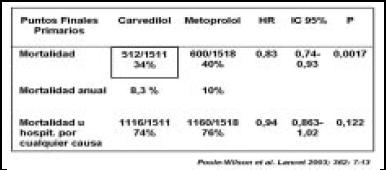
Figura 28. Puntos finales primarios.
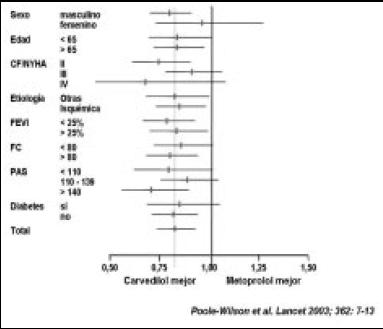
Figura 29. Mortalidad en sub-grupos.
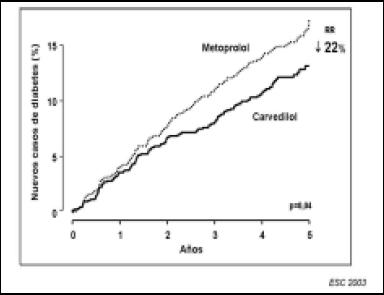
Figura 30. Nuevos casos de diabetes.
La reducción del riesgo en este grupo de pacientes fue del 22%, comparado con metoprolol. También hubo una fuerte reducción en las muertes por accidentes cerebrovasculares, de alrededor del 65%.
Volviendo a la frecuencia cardíaca, que fue una de las cosas que se cuestionó en este estudio, vemos que no hubo, prácticamente, ninguna diferencia (Fig. 31).
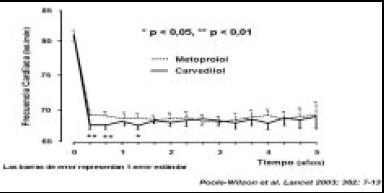
Figura 31. Cambios de frecuencia cardíaca.
Luego de los 16 meses, la frecuencia cardíaca fue similar en ambos grupos (Fig. 32). También fue criticado el tipo de metoprolol que se utilizó, entre el de liberación prolongada, o el de liberación convencional. Vemos la Figura 33 donde la media es básicamente igual, a diferentes dosis de cualquiera de los dos metoprolol.
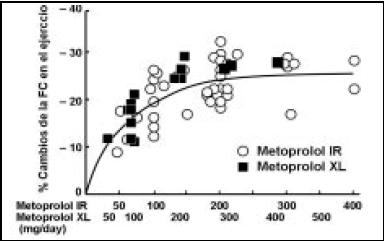
Figura 33. Efecto del metoprolol sobre la FC en la tasa de ejercicio en sujetos sin IC.
¿Qué pasó con la presión arterial? Tampoco hubo diferencias estadísticamente significativas, de la sistólica y de la diastólica comparando ambas drogas (Fig. 34). Y si hubo diferencias en el cambio de la calidad de vida referida por los pacientes, dando siempre a favor de carvedilol.
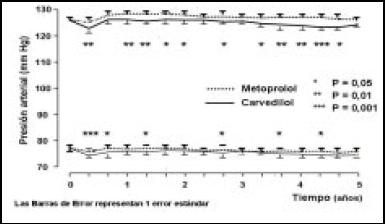
Figura 34. Cambios en la presión arterial.
Los eventos adversos que presentó este estudio, fueron similares en ambos grupos (Fig. 35). Y, a modo de resumen, los más importantes eran bradicardia e hipotensión. En la bradicardia prácticamente no hubo diferencia, y el número de eventos serios fue alrededor del 3%. En la hipotensión, igualmente no hubo diferencias, y en los eventos serios tampoco hubo diferencias estadísticamente significativas.
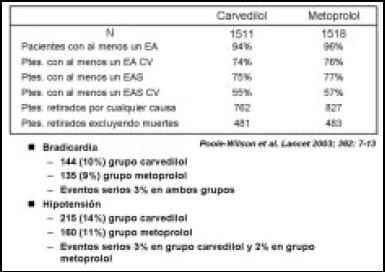
Figura 35. Eventos adversos y retiros del estudio.
Concluyendo, el estudio COMET, seguido año a año, es el de mayor magnitud en el seguimiento de insuficiencia cardíaca crónica (Fig. 36).
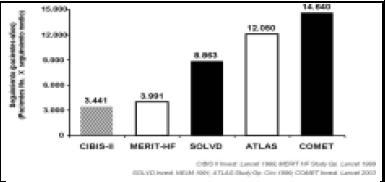
Figura 36. Estudio de mayor magnitud y duración en IC.
Entonces, es el primer estudio de mortalidad cabeza a cabeza que comparó a dos agentes beta bloqueantes en la IC crónica. Con más de 14.000 pacientes por año de seguimiento, el COMET es el estudio de ICC de mayor magnitud y duración. El carvedilol mejora la sobrevida un 17% vs metoprolol (p = 0,0017). Este estudio confirma que el bloqueocompleto beta 1, beta 2 y alfa 1 con carvedilol es superior al de un bloqueante beta 1 selectivo convencional (Fig. 37).

Figura 37. Resumen y conclusiones.
Bibliografía recomendada
1. Francis GS, Cohn JN, Johnson G, Rector TS, Goldman S, Simon A. Plasma norepinephrine, plasma rennin activity, and congestive heart failure: relations to survival and the effects of therapy in V-HeFT II: the VHeFT VA cooperative studies group. Circulation. 1993;87:140-8. [ Links ]
2. Bristow MR, Ginsburg R, Minobe W, et al. Decreased catecholamine sensitivity and ß-adrenergic-receptor density in failing human hearts. N Engl J Med. 1982;307:205-211. [ Links ]
3. Packer M, Bristow MR, Cohn JN, et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. N Engl J Med. 1996;334:1349-1355. [ Links ]
4. CIBIS II Investigators and Committees. The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II). A randomized trial. Lancet. 1999;353:9-13. [ Links ]
5. MERIT-HF Study Group. Effect of Metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomized Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet. 1999; 353: 2001-7. [ Links ]
6. The Beta-Blocker Evaluation of Survival Trial Investigators. A trial of the beta-blocker bucindolol in patients with advanced chronic heart failure. N Engl J Med. 2001; 344: 1659–1667 [ Links ]
7. Packer M, Coats AJS, Fowler MB, et al. Effect of carvedilol on survival in severe chronic heart failure. N Engl J Med. 2001;344:1651-1658. [ Links ]
8. Azevedo ER, Kubo T, Mak S, Al-Hesayen A, Schofield A, Allan R, Kelly S, Newton GE, Floras JS, Parker JD. Nonselective versus selective ßadrenergic receptor blockade in congestive heart failure: differential effects on sympathetic activity. Circulation. 2001; 104: 2194–2199. [ Links ]
9. Freeman K, et al. Alterations in cardiac adrenergic signaling and calcium cycling differentially affect the progression of cardiomyopathy. J Clin Invest. 2001;107:967–974. [ Links ]
10. Newton GE, Azevedo ER, Parker JD. Inotropic and Sympathetic Responses to the Intracoronary Infusion of a ß2 –Receptor Agonist. Circulation. 1999;99:2402-2407. [ Links ]
11. Kaumann A, Bartel S, Molenaar P, et al. Activation of ß2-Adrenergic Receptors Hastens Relaxation and Mediates Phosphorylation of Phospholamban, Troponin I, and C-Protein in Ventricular Myocardium From Patients With Terminal Heart Failure. Circulation. 1999;99:65-72. [ Links ]
12. Hall JA, Kaumann AJ, Brown MJ. Selective ß1-adrenoreceptor blockade enhances positive inotropic responses to endogenous catecholaminesmediated through ß2-adrenoreceptors in human atrial myocardium. Circ Res. 1990;66:1610–1623. [ Links ]
13. Du XJ, Autelitano DJ, Dilley RJ, Wang B, Dart AM, Woodcock EA. ß2- Adrenergic Receptor Overexpression Exacerbates Development of Heart Failure After Aortic Stenosis. Circulation. 2000;101:71. [ Links ]
14. Communal C, Singh K, Sawyer DB et al. Opposing effects of beta(1)- and beta(2)-adrenergic receptors on cardiac myocyte apoptosis : role of a pertussis toxin-sensitive G protein. Circulation. 1999; 100(22):2210- 2212. [ Links ]
15. Billman GE, Castillo LC, Hensley J, Hohl CM, Altschuld RA. ß2-Adrenergic Receptor Antagonists Protect Against Ventricular Fibrillation. In Vivo and In Vitro Evidence for Enhanced Sensitivity to ß2-Adrenergic Stimulation in Animals Susceptible to Sudden Death. Circulation. 1997;96:1914-1922 [ Links ]
16. Boudreau G, Peronnet F, De Champlain J, et al. Presynaptic effects of epinephrine on norepinephrine release from cardiac sympathetic nerves in dogs. Am J Physiol. 1993; 265: H205–H211 [ Links ]
17. Metra M et al. Heart Failure 2003. [ Links ]
18. Metra M, Giubbini R, Nodari S, et al.. Differential effects of ß-blockers in patients with heart failure a prospective, randomized, double-blind comparison of the long-term effects of metoprolol versus carvedilol. Circulation. 2000;102:546–551. [ Links ]
19. Di Lenarda A, Sabbadini G, Salvatore L, et al. Long-term effects of carvedilol in idiopathic dilated cardiomyopathy with persistent left ventricular dysfunction despite chronic metoprolol. The Heart-Muscle Disease Study Group. J Am Coll Cardiol. 1999;33:1926-1934. [ Links ]
20. Kukin ML, Kalman J, Charney RH, Levy DK, Buchholz-Varley C, Ocampo ON, Eng C. Prospective, Randomized Comparison of Effect of Long- Term Treatment With Metoprolol or Carvedilol on Symptoms, Exercise, Ejection Fraction, and Oxidative Stress in Heart Failure. Circulation. 1999;99:2645-2651. [ Links ]
21. Sanderson JE, Chan SKW, Yip G, et al. Beta-blockade in heart failure: a comparison of carvedilol with metoprolol. J Am Coll Cardiol. 1999;34:1522–1528. [ Links ]
22. Packer M, Antonopoulos GV, Berlin JA, et al.. Comparative effects of carvedilol and metoprolol on left ventricular ejection fraction in heart failure: results of a meta-analysis. Am Heart J. 2001;141:899. [ Links ]
23. Metra M, Nodari S, Parrinello G, Giubbini R, Manca C, Dei Cas L. Marked improvement in left ventricular ejection fraction during longterm beta-blockade in patients with chronic heart failure: clinical correlates and prognostic significance. Am Heart J. 2003; 145:292-9. [ Links ]
24. Poole-Wilson P, et al. Rationale and design of the Carvedilol or Metoprolol European trial in patients with chronic heart failure: COMET. E JHF. 2002; 4: 321-329. [ Links ]
25. Poole-Wilson PA, Swedberg K, Cleland JGF, et al. for the COMET investigators. Comparison of carvedilol and metoprolol on clinical outcomes in patients with chronic heart failure in the Carvedilol or Metoprolol European Trial (COMET): randomised controlled trial. Lancet. 2003;362:7–13. [ Links ]
26. Packer M, Bristow MR, Cohn JN, Colucci WS, Fowler MB, Gilbert EM, Shusterman NH, for the U.S. Carvedilol Heart Failure Study Group. The Effect of Carvedilol on Morbidity and Mortality in Patients with Chronic Heart Failure. NEJM. 1996; 334:1349-55. [ Links ]
27. Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet. 1999; 353: 2001-7. [ Links ]
28. SOLVD Invest. Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure. The SOLVD Investigators. N Engl J Med. 1991; 325:293-302 [ Links ]
29. Packer M, Poole-Wilson PA, Armstrong PW, Cleland JGF, Horowitz JD, Massie BM, Ryden L, for the ATLAS investigators. Comparative effects of low doses and high doses of angiotensin converting enzyme inhibitor, Lisinopril, on morbidity and mortality in chronic heart failure. Circulation. 1999; 100:2312-2318. [ Links ]