Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Insuficiencia cardíaca
versión On-line ISSN 1852-3862
Insuf. card. vol.2 no.2 Ciudad Autónoma de Buenos Aires abr./jun. 2007
GUÍA DE MONITOREO HEMODINÁMICO
Monitoreo de las presiones de la arteria pulmonar
Catéter de Swan-Ganz
Parte II
Aina Lauga* y Alfredo D'Ortencio**
*Jefa de Enfermería. Instituto Argentino de Diagnóstico y Tratamiento. Bs. As. Argentina.
** Médico Cardiólogo. Jefe de Cardiología y Director UDH del Instituto "Dr. Angel Roffo". Facultad de Medicina. UBA. Buenos Aires. Rep. Argentina.
Correspondencia: Lic. Aina Lauga
Jefatura de Enfermería. Instituto Argentino de Diagnóstico y Tratamiento.
Marcelo T de Alvear 2346. 1122 - Buenos Aires. Rep. Argentina.
E-mail: ainalau@yahoo.com.ar
Trabajo recibido: 20/10/2006
Trabajo aprobado: 07/03/2007
Métodos para la inserción del catéter de Swan-Ganz
Los catéteres para realizar el monitoreo de las presiones de la arteria pulmonar, como el catér de Swang Ganz (SG) (Fig. 6), se introducen en los grandes vasos venosos del tórax o en las cavidades cardíacas derechas, y no sólo se utilizan con fines diagnósticos (para determinar presiones y concentraciones de oxígeno en las cavidades cardíacas), sino también terapéuticos (su utilización más importante es el aporte de fluidos, o la colocación de un catéter marcapasos transitorio)58-64.
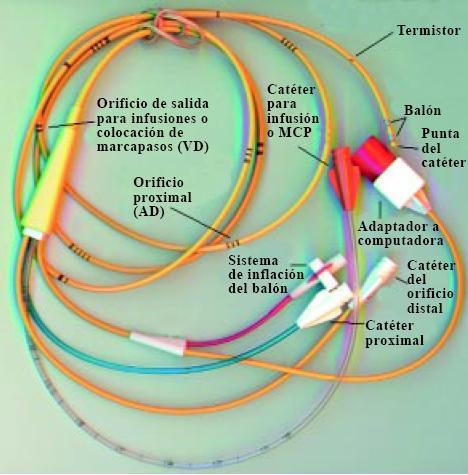
Figura 6. Catéter de Swan-Ganz. Descripción. MCP: Marcapasos
Los catéteres pueden colocarse por dos métodos65-68:
Disección de vena
Punción percutánea.
Sitios de acceso vascular
No existe un método o sitio ideal para la inserción de este tipo de catéteres. Estos están determinados por la experiencia del profesional y por las características del paciente69-71. Entre ellas nombraremos: edad, estructura corporal, existencia de zonas de trauma o quemaduras, tiempo estimado de permanencia del catéter, circunstancias clínicas como: anormalidades de perfusión y/o coagulación, anticoagulación, hipertensión pulmonar (HTP) severa, etc.66.
El acceso venoso a través de la disección de una vena, es poco usado actualmente, salvo que se trate de un niño.
El sistema más utilizado es el percutáneo, a través de la técnica de Seldinger. Después de la localización de la vena a utilizar, se coloca a través de esta punción inicial una guía (cuerda de piano), sobre ésta se ubica un introductor, se retira la guía y se coloca posteriormente el catéter de la arteria pulmonar (AP).
Esta técnica se utiliza para las venas centrales, ya sea yugular interna o subclavia.
Si la inserción es dificultosa, se aconseja utilizar otra vía de acceso para evitar las complicaciones por la excesiva manipulación de un solo vaso.
Acceso venoso central: subclavia (Fig. 7)
Ventajas
-Fácilmente accesible.
-Fácil mantención de una curación estéril.
-Movimientos libres del brazo y del cuello.
-Escasa posibilidad de desplazamiento del catéter.
-Escasa posibilidad de trombosis por el elevado flujo sanguíneo.
Desventajas
-Riesgo de embolia aérea.
-Riesgo de punción o laceración de la arteria subclavia.
-Riesgo de hemorragia importante, ya que no se puede aplicar compresión en la zona.
-Riesgo de neumotórax.
-Lesión del nervio frénico o braquial.
-Riesgo de perforación traqueal.
-Riesgo de perforación del manguito del tubo endotraqueal.
-Riesgo de complicaciones en aquellos pacientes con: cirugía previa en el área de la subclavia, enfisema, asistencia respiratoria mecánica (ARM), especialmente, con PEEP (Positive End Expiratory Pressure: presión positiva al final de la espiración).

Figura 7. Territorio para la punción de la vena subclavia.
Acceso venoso central: yugular interna (Fig. 8)
Ventajas
-Acceso directo a la vena cava superior y aurícula (AD).
-Sitio seguro para la ubicación del catéter.
-Menor posibilidad de desplazamiento del catéter,
-El flujo sanguíneo rápido disminuye la posibilidad de complicaciones trombóticas.
-Menor incidencia de punción o laceración arterial o neumotórax, si se compara con la vía subclavia.
Desventajas
-Riesgo de embolia aérea.
-Riesgo de punción o laceración de la arteria carótida.
-Riesgo de punción de la tráquea o del manguito del tubo endotraqueal.
-Riesgo de neumotórax, mayor en la vena yugular interna izquierda que en la derecha.

Figura 8. Territorio para la punción de la yugular interna.
Acceso venoso central: femoral (Fig. 9 y 10)
Ventajas
-Fácilmente accesible.
-Es uno de los sitios con el que los médicos están más familiarizados.
-Facilidad de inserción en pacientes añosos, con venas subclavias o yugulares tortuosas.
Desventajas
-Aumento en la posibilidad de infecciones por la proximidad de la zona inguinal, contraindicado en pacientes con sepsis abdominal.
-Dificultad para mantener una curación en condiciones óptimas.
-Dificultad de localización en pacientes obesos.
-La trombosis de la vena femoral es un factor de alto riesgo en el tromboembolismo de pulmón (especialmente en pacientes con estados de hipercoagulación).
-Necesidad de inmovilizar la pierna, aumento en la posibilidad de desplazamiento del catéter, especialmente, si el paciente está con excitación psicomotriz.

Figura 9. Territorio del triángulo femoral.

Figura 10. Territorio del triángulo femoral. Acceso percutáneo a la vena femoral a través de la identificación por el pulso de la arteria femoral y posterior inserción de la aguja.
Acceso venoso periférico: yugular externa (Fig. 8)
Ventajas
-Fácilmente accesible, especialmente en niños, por su localización superficial.
-Riesgo mínimo de punción de la arteria carótida o neumotórax.
Desventajas
-Puede haber cierta dificultad para el pasaje del catéter, en ocasiones puede ser necesario usar una guía "J" para atravesar la zona de unión a las venas centrales.
-Riesgo de punción o laceración de la arteria carótida (mínimo).
-Riesgo de ingresar a la vena axilar.
-El flujo sanguíneo es menor, por lo que aumenta el riesgo de trombosis.
-Riesgo de neumotórax (mínimo).
-Dificultad de mantener una curación estéril, especialmente si el paciente tiene una traqueostomía.
Accesos venosos periféricos: venas cefálica o basílica
Ventajas
-No hay riesgo de neumotórax o hemorragia importante.
-Control más fácil de la hemorragia en caso de coagulopatías o anticoagulación.
Desventajas
-Localización dificultosa en pacientes obesos o con edema importante.
-La mayoría de las veces el procedimiento debe hacerse por disección, ya que el acceso percutáneo puede ser dificultoso.
-La estasis sanguínea en la vena utilizada predispone a la trombosis.
-Mayor riesgo de sepsis.
-El avance del catéter puede ser dificultoso.
-El diámetro de la vena puede no ser suficiente para contener el catéter.
-El brazo debe ser inmovilizado para evitar el desplazamiento del catéter.
-El espasmo venoso puede dificultar el pasaje del catéter.
-El desplazamiento del catéter es más frecuente.
Preparación del equipo para la inserción del catéter
Bajo la situación de apuro y presión del medio ambiente de una unidad de cuidados intensivos, la atención se centra más en la enfermedad, la tecnología y el equipamiento, que en el paciente y su familia.
La premedicación con sedantes y/o analgésicos, puede ayudar a reducir la ansiedad y el dolor que acompaña a la colocación de este tipo de catéteres, mientras limita los movimientos del paciente durante el procedimiento, especialmente en los pacientes con excitación psicomotriz.
Ya que se trata de un procedimiento invasivo, se deben tomar todas las medidas necesarias para garantizar la máximas condiciones de asepsia en el procedimiento de la colocación del catéter.
Equipo para la colocación del catéter de Swan-Ganz
Cada institución tiene su propia sistemática de trabajo. Básicamente se requiere (Fig. 11a y 11b)69-71:
Monitor para registrar presiones.
Transductor de presiones preparado con llaves de tres vías y conector macho-macho.
Camisolín, barbijo, gorro, guantes estériles.
Sábanas estériles: 3 (dos para el campo quirúrgico y una para armado de la mesa).
Compresas estériles: 2.
Gasas estériles.
Xylocaína al 2% sin epinefrina.
Jeringas de 10 cm: 3.
Agujas 40/8 y 25/8 ó mosquito: 3.
Set de introductor (abbocath 18, cuerda de piano J 35 corta, dilatador, introductor con colateral).
Hoja de bisturí.
Sutura.
Set de catéter de SG.
Presurizador.
Sachet de lavado: 2 (dextrosa al 5% 250 + 5000 u de heparina).

Figura 11a. Monitor de presiones y ECG.

Figura 11b. Posición del paciente con el catéter en la arteria pulmonar (AP). El catéter está conectado a un transductor a través de una tubuladura. El transductor se conecta a un monitor de presiones que, visualmente, despliega una forma ondulada y valora las presiones de la AP: presiones sistólica, diastólica y presión media. El sistema está compuesto de una solución infundida bajo presión en un dispositivo de flujo contínuo y una serie de llaves de paso. La llave de paso se usa para extraer muestras de sangre de la AP.
El transductor de presiones recibe la presión de la columna de líquido y la transmite y digitaliza al monitor, se le coloca el lavado y se lo presuriza entre 150 y 200 mm Hg. Esto es necesario para asegurar un lavado continuo de la guía para evitar que se ocluya y para que no haya reflujo (por lo general, no existe con las presiones en la AD, pero sí en la AP) (Fig. 12).
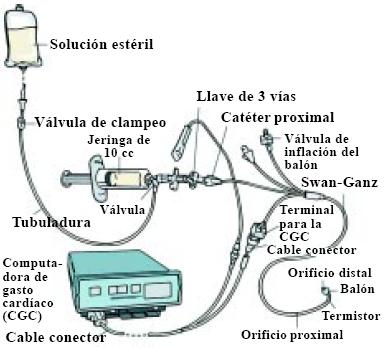
Figura 12. Sistema cerrado para la medición del gasto cardíaco.
Se colocan entonces 3 llaves de tres vías (Fig. 13):
Una para calibrar.
Una para conexión al extremo distal del catéter.
Una para conexión al prolongador macho-macho.
Una vez colocado el conector, se colocan en su extremo:
Una llave de tres vías para el lavado continuo.
Una llave de tres vías para infusión de solución para medición por termodilución.
Un termistor.

Figura 13. Sistema de conexión. Cápsula de presiones.
Técnica de cateterización dirigida por el flujo sanguíneo
Ya comentado en la parte I de la presente guía, la disponibilidad de catéteres de SG (Fig. 14) es muy amplia. Existen catéteres de 2, 4, 5 y 7 lúmenes, de acuerdo a las necesidades, como el catéter que informa continuamente sobre el gasto cardíaco (GC) por termodilución (Fig. 15 y 16).

Figura 14. Catéter de arteria pulmonar.
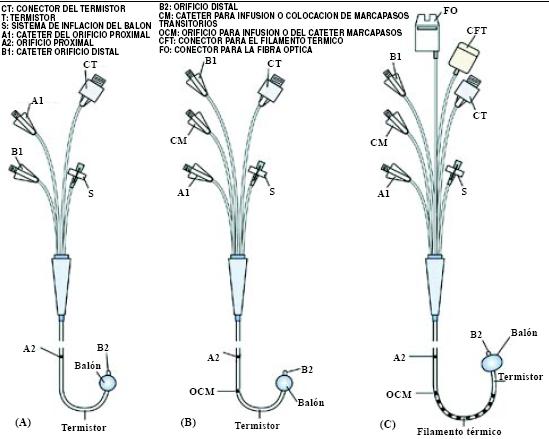
Figura 15. Tipos de catéteres de la arteria pulmonar (AP). (A) Catéter de 4 lúmenes. (B) Catéter de 5 lúmenes que incluye un puerto de infusión venoso adicional o para la introducción de un catéter marcapasos (CM). (C) Catéter de 7 lúmenes que incluye lúmenes adicionales para la medición del gasto cardíaco (CT), o la medición del gasto cardíaco en forma contínua (GCC) a través de la información brindada por un filamento térmico, y la saturación de oxígeno venoso mixto continuo (conector de la fibraóptica). Una opción adicional es combinar el uso del filamento del GCC y el monitoreo del tiempo de respuesta del termistor para calcular el volumen del fin de diástole.
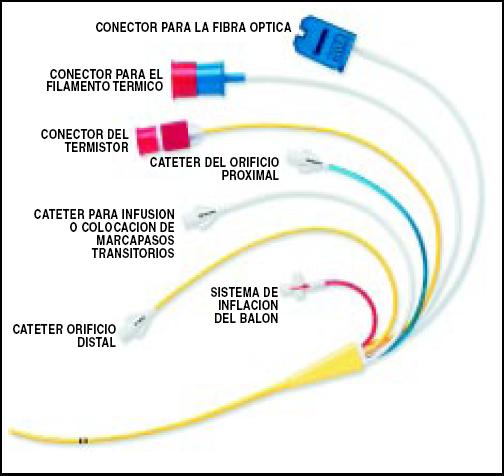
Figura 16. Catéter de 7 lúmenes.
Antes de comenzar con este procedimiento, es importante fijar el transductor de presiones, calibrándolo a cero antes del procedimiento y dejándolo listo para la conexión al catéter.
Antes de insertar el catéter, debe probarse la integridad del balón, inflándolo bajo solución salina. El balón del catéter debe ser probado sólo con aire (de 0,7 a 1,5 cc), la colocación de líquido en él hace que sus paredes sean más rígidas, pudiendo dañar la estructura de la vasculatura pulmonar. Una vez probado, se debe dejar salir el aire pasivamente, sin aspirar, ya que la presión negativa puede introducirlo dentro del catéter, dañándolo.
Se procede a la colocación del introductor, verificando que el balón del catéter de SG se encuentre indemne, y colocando la protección del mismo, se envuelve el catéter en una compresa estéril, dejando las conexiones (distal y proximal) al alcance del profesional que realizará las mediciones, éste las conecta y procede al lavado de ambas, observando su permeabilidad72-74.
Una vez colocado el catéter en el introductor, se avanzará el mismo observando las curvas de presión en el monitor; cuando se ha llegado a la AD, se inflará el balón con aire para poder atravesar la válvula tricúspidea (VT) y entrar en el ventrículo derecho (VD). Este avance del catéter es de aproximadamente 40 cm del área antecubital derecho y 50 cm si es del antebrazo izquierdo; si la vía utilizada es por Seldinger, puede necesitarse introducir al catéter de SG unos centímetros más, todo ello dependiendo de las características del paciente. Entonces, se infla el balón y se avanza bajo control permanente del electrocardiograma y de las presiones, a través de la AD, VD, y AP hasta que se obtiene presión capilar pulmonar (PCP) o de enclavamiento (Fig. 17). Se ha popularizado mucho la inserción percutánea de catéteres desde las venas yugular interna, subclavia y femoral75-78.

Fig. 17. Presiones registradas durante la colocación de un catéter guiado por el flujo. AD = presión de aurícula derecha, VD = presión de ventrículo derecho, AP = presión de arteria pulmonar, PC = presión capilar ("wedge"). La escala de la izquierda está calibrada de 0 a 50 mm de Hg. VI = Ventrículo izquierdo.
Habitualmente, el balón del catéter se infla con aire (Fig. 18); sin embargo, en situaciones en las que el catéter puede pasar a las cavidades izquierdas o a una arteria sistémica, o en presencia de corto circuito de derecha a izquierda, debe usarse anhídrido carbónico para inflar el mismo. Pues el anhídrido carbónico difunde a través del látex del balón, determinando que luego de varios minutos disminuya el diámetro de éste y que protruya la punta del catéter fuera de los márgenes del balón. Por ello, si la colocación del catéter no se completa dentro de dos minutos de haber sido inflado, el balón debe ser inflado nuevamente (con otros 0,8 ml de anhídrido carbónico).

Figura 18. Preparación de catéter de arteria pulmonar para su colocación. Prueba del inflado del balón.
A veces con el tiempo, la contracción del VD puede hacer avanzar la punta del catéter hacia una rama más pequeña de la AP; por ello, el volumen necesario para inflar al balón debe ser menor a 0,8 ml. En aquellos casos que el balón se encuentre inflado a su máxima capacidad, puede causar sobredistensión del vaso con potencial daño a la pared de la arteria y amortiguación y falsa elevación de las presiones. A fin de evitar estos inconvenientes, es imperativo que el balón sea inflado gradualmente bajo control permanente de la presión de la AP, cesando su inflado cuando la configuración de las presiones cambia de la AP al capilar pulmonar ("wedge")79.
Si hay una enfermedad valvular tricuspídea estenótica documentada, puede ser necesario inflar el balón con menos aire que el indicado en las especificaciones, para poder pasar a través de la estructura estenosada.
El balón debe continuar inflado mientras el catéter pasa por el VD y entra en la AP. Se puede ayudar al procedimiento, lateralizando al paciente ligeramente sobre su lado derecho o diciéndole que respire profundamente.
Si la inserción es dificultosa, puede ser necesario retirarlo parcialmente y reintentar la misma; durante esta maniobra se debe desinflar el balón, para recolocarlo nuevamente.
Una vez que se considera que el catéter está en posición, se lo protege en su longitud con la cobertura para tal fin y posteriormente se realizará una radiografía de tórax de control. También, se puede confirmar que el catéter se encuentra realmente en la posición "wedge" (enclavamiento), demostrando que la sangre aspirada desde la punta del catéter tiene una saturación de oxígeno del 95% ó mayor. Si la presión capilar se está midiendo desde una AP grande, será probablemente necesario retirar unos 5 a 15 ml de sangre de la AP, antes de tomar la muestra para medir la saturación de oxígeno equivalente a la sangre del capilar pulmonar. Esta sangre viene del "espacio muerto" situado en la AP80.
El pasaje del catéter hacia la AP, a través de la válvula pulmonar puede ser difícil en pacientes con cavidades derechas dilatadas, debido a la baja velocidad del flujo sanguíneo. En estos casos, inspiraciones profundas, el uso de la maniobra de Valsalva y haciendo más rígido el catéter inyectando en el lumen solución fría, pueden facilitar su pasaje81.
58. Falicov RE, Resenekov L. Relationship of the pulmonary artery enddiastolic pressure to the left ventricular end-diastolic and mean filling pressures in patients with and without left ventricular dysfunction. Circulation 42:65,1970. [ Links ]
59. Gardner RM, Scwartz R, Wong HC, Burk JP. Percutaneous indwelling radial artery catheters for monitoring cardiovascular function -prospective study of the risk of thrombus and infection. N Engl J Med 290:1227,1974. [ Links ]
60. Russel RO, et al. Effects of increasing left ventricular filling pressure in patients with acute myocardial infarction. J Clin Invest 49:1539,1970. [ Links ]
61. Alpert JS, Braunwald E. Pathological and Clinical Manifestations of Acute Myocardial Infarction. In E. Braunwald (Ed.), Heart Disease. Philadelphia: Saunders, 1984. [ Links ]
62. Rippe JM, Csete M. Manual of Intensive Care Medicine. Boston: Little, Brown, 1984. [ Links ]
63. Vander Salm TJ, Cutler BS, Wheeler HB. Atlas of Bedsides Procedures. Boston: Little. Brown, 1979. [ Links ]
64. Knopp R, Dailey RH. Central venous cannulation and pressure monitoring. J Am Coll Emerg Phys 6(8):3585,1977. [ Links ]
65. Bonilla JC, González A, Gómez E. Catéteres venosos centrales: evaluación de 310 catéteres colocados en el Hospital Universitario del Valle, Cali, Colombia. Colombia Méd 1988;19:68. [ Links ]
66. Triana F, Albornoz C. Inserción de catéteres venosos centrales de pediatría. Bol Epidemiol 1989;2:1. [ Links ]
67. Castro LA. Experiencia con catéteres venosos centrales en la Clínica Infantil Colsubsidio. Bol Epidemiol 1989, 2:1. [ Links ]
68. Benitez LM, Varón A, Roa J. Catéteres venosos centrales en medicina interna. Acta Méd Colomb 1992;17:273. [ Links ]
69. Gauntlett Beare P, Myers JL. Enfermería Medico-Quirúrgica. vol 2. Elsevier Science. España, 2002. [ Links ]
70. Grif Aspach JA. Cuidados intensivos de enfermería en el adulto. Mc Graw - Hill. México, 2001. [ Links ]
71. Urden LD, Lough ME, Stacy KM. Cuidados intensivos en enfermería. Harcourt Brace, España, 2003. [ Links ]
72. Cerra F, Milch R, Lajos TZ. Pulmonary catheterization in critically ill surgical patients. Ann Surg 1973;177:37. [ Links ]
73. Rosenbaum RW, Hayes MF Jr, Morello DC, Matcumoto T. The importance of pulmonary artery pressure monitoring. Surg Gynec Obstet 1973;136:261. [ Links ]
74. Civetta JM, Gabel JC. Flow-directed pulmonary artery catheterization in surgical patients. Indications and modifications of technic. Ann Surg 1972;176:753. [ Links ]
75. Scott ML, Webre DR, Arens JF, Ochsner JL. Clinical application of a flow-directed balloon-tipped cardiac catéter. Am Surg 1972;38(12):690-6. [ Links ]
76. Finfer A, Delaney B. Pulmonary artery catheters. British Med J 2006;333:930-931. [ Links ]
77. Blank W. A piece of my mind. Swan's way. JAMA 2006;296:1041-1042. [ Links ]
78. Lu, Mukkamala. Continuous cardiac output monitoring in humans by invasive and noninvasive peripheral blood pressure waveform analysis. J Appl Physiol 2006;101:598-608. [ Links ]
79. Heldt. Continuous blood pressure-derived cardiac output monitoring should we be thinking long term? J Appl Physiol 2006;101:373-374. [ Links ]
80. The National Heart, Lung, and Blood Institute Acut. Pulmonary-Artery versus central venous catheter to guide treatment of acute lung injury. N Engl J Med 2006;354:2213-2224. [ Links ]
81. Almeida Junior GL, Esporcatte R, Rangel FO, Rocha RM, Gouvea e Silva Gde M, Tura BR, Jorge JK, Drumond LE, Albanesi Filho FM. Advanced heart failure therapy adapted to hemodynamic objectives acquired from invasive hemodynamic monitoring. Arq Bras Cardiol 2005;85(4):247-53. [ Links ]














