Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Insuficiencia cardíaca
versão On-line ISSN 1852-3862
Insuf. card. vol.2 no.3 Ciudad Autónoma de Buenos Aires jul./set. 2007
GUÍA DE MONITOREO HEMODINÁMICO
Monitoreo de las presiones de la arteria pulmonar
Catéter de Swan-Ganz
Parte III
Aina Lauga* y Sergio V. Perrone**
* Jefa de Enfermería. Instituto Argentino de Diagnóstico y Tratamiento. Buenos Aires, República Argentina.
** Jefe de Servicio de Insuficiencia Cardíaca y Trasplante de Organos Intratorácicos, Instituto FLENI, Buenos Aires, República Argentina.
Correspondencia: Lic. Aina Lauga.
Jefatura de Enfermería.
Instituto Argentino de Diagnóstico y Tratamiento.
Marcelo T. de Alvear 2346.
1122 - Buenos Aires, República Argentina.
E-mail: ainalau@yahoo.com.ar
Trabajo recibido: 20/10/2006
Trabajo aprobado: 07/03/2007
Curvas de presiones
A medida que se va introduciendo el catéter de Swan-Ganz (SG), y éste pasa de la circulación venosa central a las cámaras cardíacas, se deben identificar las curvas específicas y de esta forma conocer la ubicación exacta del catéter (Figura 19).
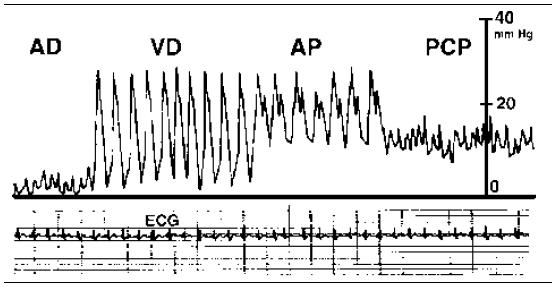
Figura 19. Presiones cavitarias derechas registradas durante la colocación de un catéter guiado por el flujo. AD = presión de aurícula derecha, VD = presión de ventrículo derecho, AP = presión de arteria pulmonar, PC = presión capilar ("wedge"). La escala de la derecha está calibrada de 0 a 50 mm de Hg. ECG = Electrocardiograma.
Aurícula derecha
Cuando el catéter se encuentra en la aurícula derecha (AD), la curva tiene tres ondas positivas: "a", "c" y "v", las cuales muestran oscilaciones continuas en su forma y dos valles"x" e "y". Si no existe enfermedad de la válvula tricúspide (VT), la presión media de la AD es igual a la presión de fin de diástole del ventrículo derecho (PFDVD), ya que ambos se encuentran comunicados en ese momento debido a que la VT está abierta (Figura 20).
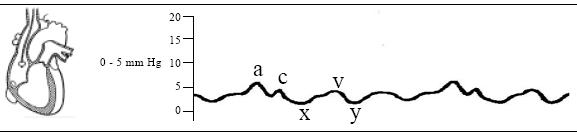
Figura 20. Presión de aurícula derecha.
La onda "a" se correlaciona con la contracción auricular que comienza alrededor del pico de la onda "P" del electrocardiograma.
El valle descendente "x" se produce ante la relajación de la aurícula (diástole auricular) y ocurre justo antes de la contracción ventricular.
La onda "c" está producida por el cierre brusco de la VT provocado ante la contracción del ventrículo derecho (VD) que induce una ligera elevación de la VT en la AD (período isovolumétrico sistólico), incrementando consecuentemente sus presiones ligeramente y provocando esta onda.
La onda "v" es provocada por el llenado de la aurícula por la sangre proveniente de las venas cavas. La presión media normal en la AD oscila entre 0 a 5 mm Hg.
Antes que pase la punta del catéter por la VT, se procede al inflado del balón lo cual reducirá el riesgo de arritmias ventriculares y permitirá que el catéter flote en el flujo sanguíneo, y avanzando desde el VD a la arteria pulmonar (AP).
Las curvas de presión se ven influenciadas por la respiración del paciente, especialmente si éste se encuentra conectado a un sistema de asistencia respiratoria mecánica (invasivo o no) con presión positiva y con presión positiva de fin de espiración (PEEP) superiores a la presión fisiológica.
Durante la ventilación, la PEEP provoca un aumento de la presión en la arteria pulmonar (AP), resultando en valores más elevados; mientras que en la respiración espontánea, la presión intratorácica negativa disminuye los valores de la curva, dando una medición más baja.
Por lo tanto, la presión de la AD deberá leerse al fin de la espiración, que constituye el punto más estable del ciclo respiratorio.
En algunos casos clínicos como el SDRA (síndrome de distress respiratorio del adulto), se requiere el uso de valores muy elevados de PEEP (más de 10 cm de H2O) y las presiones de la AP y de la presión capilar pulmonar de enclavamiento wedge (PCPW) pueden estar artificialmente elevadas.
Anteriormente, era considerado rutinario desconectar momentáneamente a los pacientes del respirador durante las mediciones, observándose que una reducción en la oxigenación del paciente y pudiendo provocar una hipoxemia grave.
Actualmente, la tendencia indica que si los pacientes necesitan recibir PEEP para su tratamiento, deben continuar conésta durante la medición de la presión del circuito derecho.
Ventrículo derecho
Cuando la punta del catéter ingresa en esta cámara, observaremos un cambio importante en la estructura de la onda de presión, ésta tendrá una forma ascendente, con una presión que es 3 a 4 veces mayor que la de la AD (Figura 21). El descenso de la misma también será abrupto, sin ninguna cisura en su forma.

Figura 21. Presión de ventrículo derecho. PS = presión sistólica. PD = presión diastólica.
Podemos decir que tiene forma de dientes de sierra, es pulsátil y sus valores normales se encuentran entre 0 y 5 mm Hg para la presión diastólica y 20 a 30 mm Hg para la sistólica.
Debemos tener en cuenta que, incluso al tener el balón inflado, la punta del catéter de SG puede rozar las paredes ventriculares y se pueden producir extrasístoles ventriculares.
Arteria pulmonar
A medida que el catéter entra en la AP, la morfología de la curva se modifica nuevamente. En ausencia de enfermedad de la válvula pulmonar (VP) de características estenóticas, la presión diastólica se eleva y en la morfología se observa la presencia de una cisura dícrota en el descenso de la curva, que indica el cierre de la VP (Figura 22).
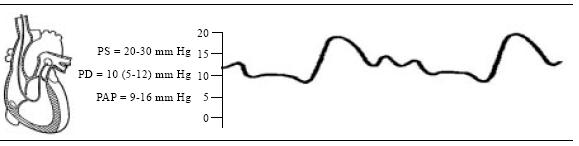
Figura 22. Presión de arteria pulmonar. PS = presión sistólica. PD = presión diastólica. PAP = presión arteria pulmonar media.
La presión diastólica de la AP es más alta que la del VD, y hemodinámicamente se correlaciona mejor con la presión de la aurícula izquierda (AI) debido a la resistencia que ofrece el pasaje de la sangre a través del lecho vascular pulmonar normal. La presión sistólica de la AP es, en cambio, igual a la sistólica del VD, ya que ambas estructuras se comunican al abrirse la válvula pulmonar, en ausencia de VP estenótica.
La presión diastólica normal de la AP es de aproximadamente 10 mm Hg y la sistólica entre 20 y 30 mm Hg.
En los casos en que existe hipertensión pulmonar, la punta del catéter puede ser empujada nuevamente hacia el VD, produciéndose un rulo en el catéter y en algunas ocasiones, el mal movimiento del mismo para redireccionarlo, ha dado como resultado el anudado del mismo.
Presión de enclavamiento (wedge) o presión capilar pulmonar (PCPW)
Mientras el balón continúa inflado, se continúa empujando hasta la posición de enclavado. Esta se alcanza cuando la curva se aplana, disminuyendo su tamaño, deja de ser pulsátil y aparecen nuevamente las ondas auriculares: "a", "c" y "v", pero ahora correspondientes a la curva de presiones de la AI (Figura 23).

Figura 23. Presión capilar pulmonar de enclavamiento o presión wedge.
Cuando la punta inflada del balón ha llegado a una AP de menor calibre o a una arteriola pulmonar que por su diámetro es ligeramente inferior, esto permite que el catéter se aloje en ella, ocluyéndola, con lo que el flujo sanguíneo queda interrumpido (enclavamiento).
Este enclavamiento crea una columna de sangre que recibe la presión en la punta del catéter (orificio distal del SG) en forma retrógrada, ya que, la circulación anterógrada en el vaso arterial está bloqueada al 100% (ocluida) por el balón inflado. Así, la medición en estas condiciones reflejaría la presión existente en la AI, que se transmite en forma retrógrada a través del lecho pulmonar, en ausencia de patología de estenosis de las venas pulmonares o fístulas AV pulmonares múltiples. Cuando el balón del catéter se desinfla, nuevamente se restablece el flujo sanguíneo en esa pequeña arteria.
Se debe tratar, en lo posible, de no medir en forma frecuente la presión wedge, para evitar complicaciones. Por ello, si la diferencia entre la PCPW y la presión diastólica (PD) de la AP no es superior a 6 mm Hg, no suele realizarse mediciones frecuentes de enclavamiento y se monitorea al paciente con la PD de la AP; salvo que ocurra algún cambio clínico o hemodinámico significativo en el paciente.
La presión wedge usualmente varía entre 5 y 12 mm Hg en sujetos normales.
Si a pesar de haber desinflado el balón del catéter, no reaparece la curva de la AP, se debe proceder a retirar el mismo hasta que ésta aparezca en el monitor, no es aconsejable avanzar el catéter desinflado y luego inflar el balón.
Correlación entre la presión de la aurícula izquierda (AI) y la presión de fin de diástole ventricular izquierda (PFDVI)
Cuando se abre la VM, en ausencia de valvulopatía mitral, la PD del VI se trasmite a la AI ya que ambas conforman una sola cavidad (en diástole). Imaginariamente, la punta del catéter de SG enclavado estaría en comunicación con una columna de sangre que llevaría la información en forma retrógrada desde el VI, atravesando la VM, la AI y las venas pulmonares hasta el capilar pulmonar, por lo que la curva estaría indicando la PFDVI ante la presencia de un circuito indemne.
La PCPW refleja en forma precisa la presión media de la AI; por ello, en ausencia de enfermedad de la VM, constituye un indicador útil y confiable de la dinámica y compliance del ventrículo izquierdo (VI). En ausencia de enfermedad vascular pulmonar, generalmente la PFD de la AP es solamente de 1 a 3 mm Hg más alta que la presión media capilar; por ello puede ser utilizada como un indicador de la presión media de la AI en pacientes sin HTP preexistente.
Diferencias mayores a 6 mm Hg entre la PFD de la AP y la PCP, sugieren un trastorno vascular pulmonar primario.
Debe destacarse que en presencia de severa insuficiencia mitral con grandes ondas "v", la presión media capilar puede exceder a la de PFD de la AP82.
Es relevante enfatizar que tan pronto hayan sido hechas las lecturas de la PCPW, el balón deberá desinflarse. Si se deja al balón inflado, especialmente si la punta del catéter está en una rama arterial pulmonar distal, puede provocar la erosión de la pared de la arteria con la consiguiente perforación y hemoptisis masiva o un infarto pulmonar.
Por lo tanto, podemos resumir diciendo que la presión wedge media se correlaciona con la presión media de la AI y ésta con la PFDVI.
Una vez que se ha posicionado el catéter, se deberá fijar la protección estéril del mismo, para evitar contaminaciones, evitando una manipulación innecesaria, colocando una curación estéril sobre la inserción del introductor. Posteriormente, se solicitará una radiografía (Rx) de tórax para verificar la posición del mismo.
Lo prioritario en la utilización de los catéteres de SG radican en la adecuada calibración del transductor de presiones a aire ambiente, cada vez que se deban realizar mediciones.
Medición del gasto cardíaco (GC)
El catéter de SG se utiliza para medir el GC, ya sea por (A) el método de termodilución, o por (B) el método de Fick83:
A. Termodilución
A mediados de 1900, se utilizó por primera vez el método de termodilución para la medición del GC, pero su aplicación clínica debió esperar el advenimiento del catéter de SG con su sensor de temperatura en el extremo distal. A partir de esta combinación "catéter-sensor térmico - método de termodilución", el método se ha convertido en la forma más común de calcular el volumen minuto cardíaco de nuestros pacientes.
El método de termodilución utiliza el cambio de temperatura que registra un líquido (solución fisiológica) inyectada por el extremo proximal del catéter de SG al llegar al sensor de temperatura ubicado en el extremo distal.
La técnica consiste en la rápida inyección (3 a 5 seg.) de una cantidad conocida de solución fisiológica (5 ó 10 cc) que se encuentra a una temperatura conocida (es necesario que ésta sea por lo menos 10º C menor que la del paciente, razón por la cual se puede utilizar indistintamente solución fisiológica a 4º C -en heladera- o a temperatura ambiente) por el extremo proximal del catéter de SG (situado en la aurícula derecha).
Esta solución, más fría que la sangre del paciente, se mezcla con la sangre que circula por las cavidades derechas y modifica su temperatura enfriándola. Este cambio de temperatura es detectado por el sensor de temperatura ubicado en el extremo distal del catéter quien remite la información a una computadora que procesa los datos de la "dilución del indicador".
La computadora de volumen minuto genera con estos datos una curva de tiempo y temperatura. El tiempo es representado en el eje horizontal y la temperatura en el vertical. La curva de GC normal presenta un aumento rápido hasta llegar a un pico y de allí un descenso suave hasta retornar a la línea de base.
El tope del pico, representa la temperatura más baja o el mayor gradiente de temperatura entre la temperatura central del paciente y la temperatura de la mezcla de sangre + solución inyectada, el descenso de la curva representa el tiempo en que esta solución sale de la AP y la temperatura registrada vuelve a ser la normal del paciente.
En pacientes con bajo GC, la temperatura tardará más tiempo en retornar a los valores basales, incrementando así el área bajo la curva y viceversa.
Habitualmente, la posición del paciente para este procedimiento es el decúbito dorsal, y es en la que se recomienda la calibración del transductor de presiones. Sin embargo, hay situaciones, como el edema agudo de pulmón o la presión intracraneal aumentada que requieren que la parte superior del cuerpo del paciente se encuentre más elevada.
El GC es calculado en base a la ecuación Stewart-Hamilton modificada, considerando el cambio de temperatura como indicador84-92:

GC= gasto cardíaco
V= Volumen del inyectado (ml)
A= área de la curva de termodilución en m2 dividida entre
la velocidad del papel (mm/s)
K= Constante de calibración en mm/ºC
TS, TI= Temperatura de la sangre (S) y del inyectado (I)
DS, DI= Densidad de la sangre y del inyectado
CS, CI= Calor específico de la sangre y del inyectado
60= 60 seg/min
CT= Factor de corrección para el calentamiento del inyectado
Siendo:

Con la intención de facilitar la medición del GC a la cabecera de los pacientes críticos, se desarrolló un catéter especial de triple lumen dirigido por flujo (Swan Ganz Flowdirected thermodilution catheter, Edwards Laboratories, Santa Ana, California). El diámetro externo de este catéter es de 2,2 mm (tamaño 7 F). El catéter tiene un pequeño lumen para inflar el balón, un lumen más grande que se abre a 30 cm de la punta del catéter y que permite inyectar el indicador frío, y, un segundo lumen grande, que se abre en la punta del catéter a fin de medir las presiones de la AP y de la PCPW.
Un pequeño termistor para medir la temperatura de la sangre en la arteria pulmonar está ubicado a 4 cm de la punta. La exactitud del método de la termodilución ha sido confirmada repetidamente93,94. Las ventajas de este método incluyen:
1. No se precisa reinfundir sangre.
2. No requiere punción arterial.
3. Se utiliza un indicador inerte y económico.
4. La calibración es simple y exacta.
5. La recirculación es mínima y la curva primaria es particularmente apta para el análisis computado.
B. Método de Fick95
El "patrón oro" para la determinación del GC se basa en los principios desarrollados por el alemán Adolph Fick, alrededor de 1870. Fick proponía que la captación y liberación de una sustancia por un órgano es igual al producto del flujo sanguíneo a través de dicho órgano por la diferencia entre los valores arterial y venoso de la misma sustancia.
La cantidad de eritrocitos que entra al pulmón es la misma al salir. Si se sabe cuantas moléculas de oxígeno adheridas a los eritrocitos entraron al pulmón y cuantas salieron y cuanto oxígeno se consumió en el trayecto, se podría determinar la tasa de flujo de estos eritrocitos a medida que pasaron a través de la circulación pulmonar.
En el método de Fick, la sustancia a utilizar es el oxígeno y el órgano en cuestión: los pulmones. Es así necesario medir el contenido arterial y venoso de oxígeno para obtener la diferencia arteriovenosa de oxígeno (A-v O2). El consumo de oxígeno se puede calcular a partir del contenido de oxígeno inspirado menos el espirado y de la velocidad de ventilación.
Para realizar la medición del GC mediante esta técnica, se toma una muestra de sangre arterial del paciente y una muestra de sangre del extremo distal del catéter de SG (sangre venosa mixta) en jeringas heparinizadas que deben ser enviadas inmediatamente al laboratorio.
Este método está basado en la suposición que la tasa a la cual se consume el oxígeno es una función de la tasa del flujo sanguíneo por la tasa de captación de oxígeno de los eritrocitos, en consecuencia, el GC es igual a:

Siendo, el contenido normal de oxígeno en sangre arterial de 20 volúmenes% (volumen%= 1 ml de oxígeno/100 cm3) y en la mezcla venosa de 15 volúmenes% (volumen%= 1 ml de oxígeno/100 cm3) para un consumo normal de oxígeno de 250 ml/min.
Estas mediciones no presentan cambios muy significativos si hay modificaciones en las presiones pulmonares secundarias a cambios en la cabecera de la cama (entre 0º ó a 30º); pero, si ésta debe estar aún más elevada, la medición del GC y de las presiones pulmonares será numéricamente menor, ya que la gravedad influye en las presiones pulmonares.
Uno de los inconvenientes que presenta esta técnica radica en que el paciente debe encontrarse en un estado fisiológico estable en el momento de su realización, algo bastante infrecuente en los pacientes que necesitan la colocación de un catéter de SG. Otro de los inconvenientes radica en que para la medición exacta por este método, deberán tomarse mediciones en forma simultánea de aire espirado y de sangre, el contenido controlado de oxígeno inspirado y la toma de muestras de sangre arterial, ya que, asumir valores "normales" puede llevar a una conclusión errónea.
El método de Fick es uno de los más exactos en los pacientes con GC, especialmente, bajo. Pero, debido a sus requisitos técnicos, es uno de los menos prácticos a nivel clínico.
Evaluación de la curva de GC
La curva normal presenta una elevación rápida, con un pico redondeado que luego inicia gradualmente un descenso (Figura 24). Una curva desigual puede indicar que ha habido una técnica de inyección defectuosa, aunque se debe tener en cuenta que el movimiento o la tos del paciente pueden alterar también la curva.

Figura 24. Curva de gasto cardíaco (termodilución).
Retiro del catéter de Swan-Ganz
Ante la necesidad de retirar el catéter de SG, es prioritario observar la última radiografía de tórax del paciente, para determinar la posición del catéter y que el mismo no se encuentre anudado. Se debe explicar al paciente, si éste está lúcido, que se le bajará la cama (cabecera en posición horizontal) y que deberá realizar una maniobra de Valsalva durante el procedimiento96. Esta maniobra, produce un aumento en la presión intratorácica, y tiene como finalidad evitar la entrada accidental de aire a la circulación; asimismo, hay que tomar la precaución de cerrar las llaves de tres vías de los accesos proximal y distal del catéter de SG.
Se debe verificar además que el balón se encuentre desinflado, y si al realizar la maniobra, se observa algún tipo de resistencia, se debe interrumpir inmediatamente el procedimiento, compensar al paciente y solicitar una nueva radiografía de tórax para verificar la condición del catéter.
Durante el retiro del catéter de SG, pueden producirse arritmias ventriculares a su paso por el VD.
En ocasiones, se deja colocado el introductor, y se retira solamente el catéter, en cuyo caso, se deberá ocluir la entrada del mismo en forma aséptica.
82. Carley JE, Wong BY, Pugh DM, Dunn M. Clinical significance of the V wave in the main pulmonary artery. Am J Cardiol 1977;39(7):982-85. [ Links ]
83. Brandi LS, Bertolini R, Pieri M, Giunta F, Calafa M. Comparison between cardiac output measured by thermodilution technique and calculated by O2 and modified CO2 Fick methods using a new metabolic monitor. Intensive Care Med 1997;23(8):908-15. [ Links ]
84. Arnould P, Lamarche M, Boulange M. Technique of taking arterial blood for measuring cardiac output by the method of Stewart-Hamilton. C R Seances Soc Biol Fil 1952;146(5-6):487-8. [ Links ]
85. Salonikides N. Measurement of cardiac output and central blood volume by the Stewart-Hamilton method (T-1824); principles, definitions, value, applications and technic. Acta Cardiol 1955;10(3):287-303. [ Links ]
86. Berti F, Zocche GP. Considerations on the Use of the Stewart-Hamilton Method in the Measurement of Cardiac Output in Rabbits. Boll Soc Ital Biol Sper 1963;39:1193-6. [ Links ]
87. Gerola A, Bassi G, Dringoli R, Bartorelli C. The cardiac output of the cat, Simultaneous measurement by the Stewart-Hamilton and Fick methods. Boll Soc Ital Biol Sper 1963;39:82-5. [ Links ]
88. Berti F, Laveneziana D, Marchi P, Zocche GP. Further considerations on the Stewart-Hamilton method in the measurement of cardiac output in the rabbit, in various types of anesthesia. Boll Soc Ital Biol Sper 1964;40(19):1143-5. [ Links ]
89. Innocenti P, Toso M, Buoncristiani U, Alicandri C, Todisco T, Marchesi N. Determination of the cardiac output by the dye dilution technic: comparison between the conventional Stewart-Hamilton method, the simplified initial triangle method and Fick's methods. Folia Cardiol 1968;27(6):354-62. [ Links ]
90. Valentinuzzi ME, Geddes LA, Baker LE. A simple mathematical derivation of the Stewart-Hamilton formula for the determination of cardiac output. Medical & biological engineering 1969;7(3):277-82. [ Links ]
91. Yoder RD, Swan EA. Cardiac output: comparison of Stewart-Hamilton and gamma-function techniques. J Appl Physiol 1971;31(2):318-21. [ Links ]
92. Karpman VL. The theoretical analysis of Fick's equation. On the centennial of the use of Fick's principle in physiology. Z Kardiol 1975;64(9):801-8. [ Links ]
93. Branthwaite MA, Bradley RD. Measurement of cardiac output by thermal dilution in man. J Appl Physiol 1968;24(3):434-8. [ Links ]
94. Ganz W, Donoso R, Marcus HS, Forrester JS, Swan HJ. A new technique for measurement of cardiac output by thermodilution in man. Am J Cardiol 1971;27(4):392-6. [ Links ]
95. Ehlers KC, Mylrea KC, Waterson CK, Calkins JM. Cardiac output measurements. A review of current techniques and research. Ann Biomed Eng 1986;14(3):219-39. [ Links ]
96. Garcia D, Garcia C. Valsalva: much more than a simple maneuver. Antonio Maria Valsalva (1666-1723). Rev Med Chil 2006;134(8):1065-8. [ Links ]














