Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Insuficiencia cardíaca
versión On-line ISSN 1852-3862
Insuf. card. vol.2 no.3 Ciudad Autónoma de Buenos Aires jul./set. 2007
HIPERTENSIÓN ARTERIAL E INSUFICIENCIA CARDÍACA
De la hipertensión arterial a la insuficiencia cardíaca
Daniel Piskorz*
* Médico de planta del Instituto de Cardiología del Sanatorio Británico. Rosario. Santa Fe. Rep. Argentina.
Correspondencia: Dr. Daniel Piskorz.
Salta 2942.
2000 Rosario. Santa Fe. Rep. Argentina.
Trabajo recibido: 15/06/2007
Trabajo aprobado: 18/07/2007
Definición y clasificación de hipertensión arterial
La presión arterial (PA) es una variable biológica que se relaciona en forma lineal, continua y directa con el riesgo de presentar un evento cardiovascular, y esta relación no se limita a valores aceptados de hipertensión arterial (HTA), sino que también se observa en rangos de valores considerados como de normotensión; por lo tanto, la definición de HTA está basada en criterios arbitrarios en función de la relación riesgo-beneficio de tratar o no tratar a un paciente.
Sin embargo, este concepto de todo o nada (hipertenso vs no hipertenso) se ha universalizado por su utilidad desde un punto de vista clínico en la toma de decisiones terapéuticas1.
El diagnóstico de HTA debe estar basado primariamente en una correcta técnica diagnóstica, para lo cual se sugieren los siguientes aspectos:
1.- Aspectos generales
- La medición de PA debe efectuarse luego de por lo menos 5 minutos en situación de reposo.
- El paciente debe abstenerse de fumar, tomar café, productos cafeinados y refrescos de cola al menos 30 minutos antes de las mediciones.
- El paciente no deberá tener necesidad de orinar ni defecar.
- El paciente debe estar tranquilo y en un ambiente apropiado.
2.- Posición del paciente
- El paciente sentado, con la espalda apoyada sobre el respaldar de la silla, el brazo completamente descubierto y a la altura del corazón.
- En las primeras visitas se deben efectuar mediciones en posición supina, sentado y de pie, con el objeto de identificar hipotensión postural, y se deben efectuar mediciones en ambos brazos, y eventualmente en el muslo.
3.- Equipo
- Es de elección un tensiómetro mercurial, en caso de no contar con este equipamiento lo recomendable es un esfigmomanómetro aneroide recientemente calibrado. Últimamente, equipos electrónicos han sido validados para medir PA, con la ventaja de evitar la potencial toxicidad por mercurio.
- El ancho del brazalete debe cubrir 2/3 de la circunferencia del brazo, y una longitud que abarque el 80% de la circunferencia del mismo. En la mayoría de los casos, esto se logra con un ancho de 13 cm a 15 cm y un largo de 24 cm.
4.- Técnica
- La vista del observador debe quedar a la altura del menisco de la columna de mercurio.
- El menisco de la escala debe estar en 0 mm Hg.
- El manguito del brazalete se deberá ubicar sobre la arteria humeral, con su borde inferior a 2 cm del pliegue del codo.
- Se debe inflar rápidamente el manguito mientras se palpa la arteria humeral a fin de determinar el momento de desaparición del pulso (presión sistólica).
- Se infla nuevamente el manguito hasta 20 mm Hg por encima de la presión sistólica determinada palpatoriamente, y se desinfla a una velocidad de 2 mm Hg/segundo.
- La auscultación del primer ruido de Korotkoff indica la presión arterial sistólica (PAS), y la desaparición de los mismos (5ta. fase) la presión arterial diastólica (PAD). En los niños se considera presión diastólica la atenuación de los ruidos (4ta. fase).
- Se deben efectuar al menos 2 mediciones separadas por 2 minutos, pero si las mismas difieren por más de 5 mm Hg, se deberá realizar al menos una tercera medición y promediar todas las efectuadas. Para el diagnóstico de HTA, se deben promediar las mediciones de 2 ó más visitas posteriores a la inicial2.
Luego de una buena técnica diagnóstica, se define HTA cuando la PAS es igual o mayor a 140 mm Hg y/o la PAD es igual o mayor a 90 mm Hg; y se define HTA sistólica aislada cuando la PAS es igual o mayor a 140 mm Hg y la PAD es menor a 90 mm Hg. La PA normal es menor a 120 mm Hg para la sistólica y 80 mm Hg para la diastólica. Se considera prehipertensión (según el reciente JNC 7) cuando la PAS se encuentra entre 120 y 139 mm Hg y la PAD entre 80 y 89 mm Hg. En el Cuadro 1, se presentan los criterios diagnósticos para los distintos estadios de HTA.
El estadio de HTA se define teniendo en cuenta el mayor valor de la presión sistólica o diastólica3,4.
En determinadas situaciones, como cuando se sospecha HTA de guardapolvo blanco, aparente resistencia al tratamiento instituido, síntomas compatibles con hipotensión arterial en pacientes con tratamiento antihipertensivo, HTA episódica o disfunción autonómica, se puede recomendar el monitoreo ambulatorio de la PA (MAPA) o las automediciones domiciliarias de PA; si bien no se han aceptado universalmente los valores de normalidad para estos procedimientos, en general se consideran como valores límites 135-85 mm Hg diurnos y 120-75 mm Hg nocturnos para la primera, y 135-85 mm Hg para la segunda.
Epidemiología de la hipertensión arterial
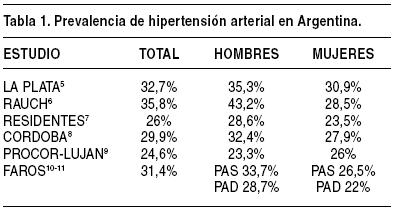
Diversos estudios epidemiológicos transversales han mostrado que la prevalencia de la HTA en nuestro país oscila entre el 25% y el 35%, cifras no muy diferentes de las que se publican en otras latitudes (Tabla 1).
Por otra parte, tanto la frecuencia de la HTA como las medias de PA son mayores en los hombres que en las mujeres (Tabla 1 y Gráfico 1) y la prevalencia de HTA, sistólica y diastólica se incrementa con la edad (Gráfico 2).
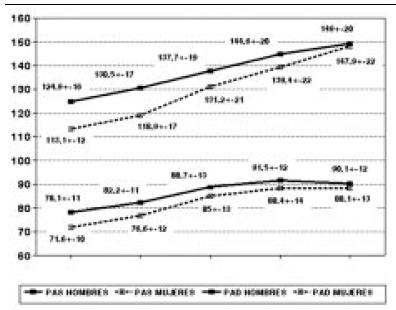
Gráfico 1. Estudio faros: medias de presión arterial según sexo y edad.
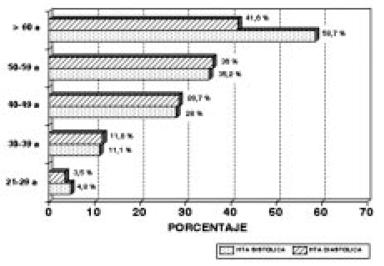
Gráfico 2. Estudio faros: prevalencia de hipertensión arterial en diferentes intervalos etarios.
Asimismo, mientras la PAD no continúa ascendiendo en individuos mayores de 50 años, esto sí ocurre con la PAS, por lo que en la población adulta mayor y geronte la prevalencia de hipertensión sistólica aislada se incrementa en forma significativa, del mismo modo que lo hace la presión de pulso (por pérdida de la distensibilidad arterial), dos situaciones que están fuertemente relacionadas con el mayor riesgo cardiovascular de este subgrupo de pacientes.
En nuestro país, se ha reportado una prevalencia de HTA que oscila entre el 40% y el 80% en individuos mayores de 65 años, mientras que la hipertensión sistólica aislada se ha comunicado entre el 9% y el 24% de los encuestados.
Pronóstico en la hipertensión arterial
Previamente, se ha planteado la controversia entre el modo en que se hace el diagnóstico de HTA y la relación continua y lineal que existe entre ésta y el riesgo cardiovascular. Por otra parte, el pronóstico del paciente hipertenso arterial no sólo depende de sus niveles de PA, sino del perfil de riesgo global, por lo tanto, es necesario efectuar una evaluación completa del paciente, con el objeto de detectar otros factores de riesgo cardiovascular y la presencia de daño en órgano blanco.
En este contexto, los pacientes hipertensos arteriales se pueden clasificar de acuerdo a su riesgo cardiovascular global en:
a) Riesgo bajo: presentan HTA estadio I y ausencia de factores de riesgo cardiovascular asociado y/o daño en órgano blanco, en ellos la incidencia de eventos cardiovasculares es menor de 0,5 por año.
b) Riesgo moderado: se caracterizan por HTA estadio II, con hasta 2 factores de riesgo cardiovascular asociados (excepto diabetes mellitus) y ausencia de daño en órgano blanco, en ellos se presentan entre 0,5 y 1,5 eventos cardiovasculares por año.
c) Riesgo alto: se definen por la presencia de 3 ó más factores de riesgo, o asociación con diabetes o presencia de daño en órgano blanco, o PA sistólica > 180 mm Hg ó diastólica > 110 mm Hg; presentan 1,5 a 2,5 eventos cardiovasculares por año.
d) Riesgo muy alto: caracterizados por falla de órgano blanco debida a cualquier nivel de PA o presión sistólica > 180 mm Hg y/o diastólica > 110 mm Hg con al menos 1 factor de riesgo asociado, en ellos se pueden observar más de 2,5 eventos cardiovasculares por año2,3.
Complicaciones de la hipertensión arterial
La HTA produce cambios funcionales y estructurales en los riñones, los primeros se deben a vasoconstricción de la arteriola eferente, cuyo objeto es aumentar la presión intraglomerular para mantener un filtrado glomerular estable e incrementar la reabsorción de sodio en el túbulo proximal, y a vasoconstricción en la arteriola aferente para proteger a los riñones del incremento excesivo de la presión intraglomerular; este mecanismo, denominado de autorregulación, permite que el flujo plasmático renal y la fracción de filtración glomerular se mantengan estables dentro de un amplio rango de presiones, y está regulado tanto por el sistema renina angiotensina aldosterona como por el sistema nervioso simpático. Sin embargo en el largo plazo, o frente a severas y sostenidas elevaciones de la PA no logra proteger a los riñones, y deviene el desarrollo de glomerulosclerosis, con incremento en la síntesis proteica, determinando cambios estructurales renales caracterizados fundamentalmente por proliferación de células mesangiales y expansión de la matriz mesangial, debida tanto a los cambios hemodinámicos como a la activación neurohumoral, la producción de citoquinas inflamatorias, o la estimulación de factores de crecimiento celular, entre otros. El daño renal en la HTA se manifiesta progresivamente por microproteinuria o microalbuminuria (excreción menor a 200 ó 300 mg/24 horas), que evidencia sólo daño funcional y reversible; proteinuria clínica (excreción mayor a 200 ó 300 mg/24 horas) expresión de daño orgánico; y finalmente insuficiencia renal crónica con creatininemias mayores a 1,4 ó 1,5 mg/dl o clearence de creatinina menores a 60 ml/min ó 45 ml/min/1,73 m2; por otra parte, la presencia de estas alteraciones bioquímicas no sólo indican lesión renal, sino que además son importantes marcadores pronóstico de alto riesgo cardiovascular12.
El fondo de ojo expresa la presencia y severidad de daño arterial en el paciente hipertenso arterial, y por otra parte es un marcador pronóstico independiente en sujetos que padecen esta afección; sin embargo, los grados menores de compromiso no son específicos de la patología, ya que también pueden ser observados en individuos normotensos con aterosclerosis sistémica. El fondo de ojo se puede estratificar de acuerdo a la clasificación de Keith-Wagener-Barker (Tabla 2), y la Organización Mundial de la Salud los ha dividido en dos grupos: 1) el hipertónico, que comprende los grados I y II de la clasificación, con una sobrevida de 80% a cinco años sin tratamiento; y 2) el hipertónico maligno, que incluye los grados III y IV de la clasificación, con una sobrevida de 5% a cinco años sin tratamiento13,14.
La reserva de flujo coronario se encuentra reducida en pacientes hipertensos arteriales, tanto en ausencia pero particularmente en presencia de hipertrofia ventricular izquierda (HVI), esto es debido a un incremento en la resistencia vascular por la elevada presión intracavitaria del ventrículo izquierdo y la compresión perivascular de los vasos de resistencia, como a una reducción marcada de la densidad de capilares y arteriolas por el incremento en la masa miocárdica y la disminución del área de sección vascular. En este último aspecto, es conveniente detenerse un instante, la elevación de la PA, así como la activación de mecanismos neurohumorales, disparan mecanismos de remodelado de la microcirculación, con excesivo crecimiento de la media arteriolar, debido fundamentalmente a hiperplasia del músculo liso, y no tanto a hipertrofia, determinando un incremento en la relación pared-lumen; la consecuencia neta de este proceso es el aumento de la resistencia periférica; simultáneamente, ocurre un proceso de angiogénesis reversa, también denominado de rarefacción, por el cual ocurre obliteración de los vasos de la microcirculación, con pérdida de hasta casi un 50% de la misma, lo que reduce la superficie capilar disponible para el intercambio de oxígeno y nutrientes y elevación de la resistencia tisular vascular, por lo que para similar diámetro arterial, los pacientes hipertensos generan mayores presiones endoluminales que los sujetos normotensos (Figuras 1 y 2). Por otra parte, en la HTA ocurre una sobreproducción de radicales libres de oxígeno, con destrucción de óxido nítrico e incremento del estrés oxidativo, por lo que la relajación vascular endotelio-dependiente se ve alterada. Esto se conoce como disfunción endotelial.

Figura 1. Remodelado de la microcirculación en hipertensión arterial.
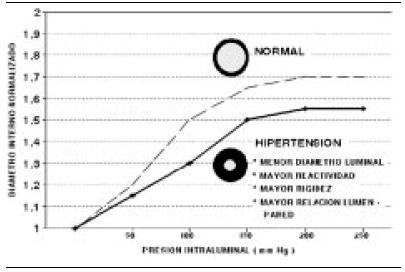
Figura 2. Relación lumen arterial - presión endoluminal en hipertensión arterial.
Finalmente, no se debe soslayar el impacto que la HTA tiene sobre el desarrollo de las placas ateroscleróticas, tanto en su formación, como en la progresión y ruptura de las mismas, con la consiguiente presentación de eventos arteriales agudos, de mayor jerarquía en el lecho vascular cerebral que en el coronario, sobre lo cual más adelante nos extenderemos15.
La masa ventricular izquierda se adapta geométricamente a las cargas de trabajo que someten al corazón a través del tiempo; la HTA es una forma típica de sobrecarga de presión del ventrículo izquierdo, con muy alta resistencia periférica y bajo volumen sistólico, y la forma característica de esta adaptación es la hipertrofia de tipo concéntrica, que no sólo se debe a factores hemodinámicos -estos sólo explican en un 50% su aparición-, sino también a factores genéticos y neurohumorales. La HVI del paciente hipertenso arterial se caracteriza tanto por cambios miocíticos como de la matriz extracelular; esta última también se ve afectada por alteraciones en la síntesis proteica, ya que los fibroblastos incrementan en forma excesiva la producción de tejido colágeno, alterando la relación entre tejido fibroso y miocitos, en los que se producen cambios fenotípicos de las proteínas contráctiles y de membrana. Este proceso de alteración en la estructura del músculo cardíaco tiene su correlato con la aparición de anomalías funcionales cardíacas, con disfunción diastólica primero, y disfunción sistólica luego, primero regional y más tardíamente global. Si bien durante años, el electrocardiograma ha sido el método tradicional de diagnóstico de HVI, su sensibilidad oscila sólo entre el 20% y el 50%; por lo tanto, el ecocardiograma, con una sensibilidad global superior al 90%, debe ser considerado el método de elección para la detección de compromiso cardíaco, permitiendo además definir las características de esta hipertrofia. Para ello se deben medir dos variables: la masa ventricular izquierda y el índice de excentricidad (IE). Para la primera, el método de Devereux es el más utilizado y se debe corregir por superficie corporal preferentemente en pacientes jóvenes y con peso normal, o por altura 2,7 en sujetos obesos, constituyendo entonces el índice de masa ventricular izquierda (IMVI), cuyos valores de normalidad oscilan según las diversas series entre 102 y 110 gramos/m2 en la mujer, y entre 111 y 141 gramos/m2 en el hombre, ó 47 gramos/m2,7 en la mujer y 50 gramos/m2,7 en el hombre.
El índice de excentricidad tiene un valor normal menor a 0,45 y deviene de la siguiente fórmula:
(2* pared posterior)/diámetro telediastólico ventricular izquierdo
Con estos criterios se pueden determinar cuatro tipos geométricos de remodelado ventricular izquierdo en el paciente hipertenso arterial:
1) Normal: IMVI normal e IE menor a 0,45.
2) Remodelado concéntrico: IMVI normal e IE mayor a 0,45.
3) Hipertrofia concéntrica: IMVI aumentado e IE mayor a 0,45.
4) Hipertrofia excéntrica: IMVI aumentado e IE menor a 0,45.
Este esquema de análisis tiene sus implicancias pronósticas, ya que aun con IMVI normal, no todos los pacientes tienen el mismo pronóstico, del mismo modo que no todas las formas de HVI confieren el mismo riesgo16-18 (Figura 3).
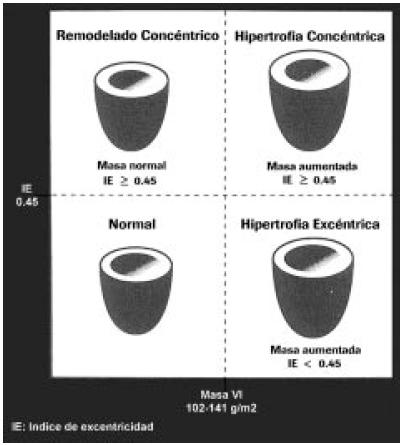
Figura 3. Esquema de la clasificación geométrica del ventrículo izquierdo en la hipertensión arterial.
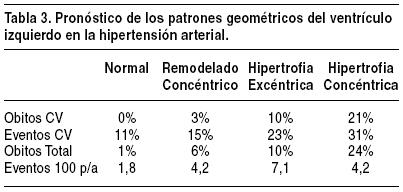
Los pacientes con HVI de tipo concéntrica presentan mayor mortalidad cardiovascular, fundamentalmente debida a un exceso de muerte súbita, mientras que los pacientes con hipertrofia de tipo excéntrica presentan mayor incidencia de insuficiencia cardíaca, y es por ello que desde el punto de vista de los eventos cardiovasculares, éstos son más frecuentes (Tabla 3).
Complicaciones neurológicas y psiquiátricas
La HTA contribuye tanto al desarrollo de enfermedad arterial cerebral de grandes vasos -aterosclerosis- como de pequeños vasos -arteriosclerosis-, y es el más potente factor de riesgo para la ocurrencia de un infarto cerebral. Múltiples infartos cerebrales aterotrombóticos derivan en la condición denominada demencia multiinfarto, mientras que la arteriosclerosis y la hipoperfusión subcortical consiguiente producen desmielinización de la sustancia blanca y demencia, condición denominada encefalopatía arteriosclerótica subcortical. En muchos individuos, ambas condiciones pueden coexistir; por lo que en conjunto se denominan demencia vascular. La aterosclerosis puede tornarse sintomática por múltiples mecanismos, por un lado a través de la producción de embolias arteriogénicas; por otro, determinando obstrucciones arteriales hemodinámicamente significativas que generan hipoperfusión distal a la estrechez; y finalmente, ocluyendo las pequeñas arterias penetrantes de menos de 1 mm de diámetro, lo que se conoce como lipohialinosis, dando origen a pequeñas cavidades denominadas infartos lacunares, que se pueden manifestar como ataques isquémicos transitorios. Por otra parte, puede desarrollarse hipertrofia y engrosamiento de la media de las pequeñas arterias intracerebrales, con estrechamiento difuso de las mismas, hipoperfusión y rarefacción isquémica de la sustancia blanca periventricular, que antes denominamos encefalopatía arteriosclerótica subcortical. La misma está presente en prácticamente la totalidad de los pacientes hipertensos arteriales de larga data y da origen a una forma de demencia conocida como enfermedad de Binswanger. También, pueden ocurrir hemorragias intracerebrales secundarias a microaneurismas de pequeñas arterias intracerebrales, y que contribuyen al proceso de lipohialinosis. Es de suma importancia clínica destacar que el 60% de los pacientes hipertensos arteriales con demencia vascular cursan clínicamente con un síndrome depresivo, y el 30% al 40% con labilidad emocional, debida a compromiso del lóbulo frontal. En pacientes hipertensos arteriales crónicos con elevaciones severas y súbitas de sus cifras tensionales, o en hipertensos arteriales de reciente comienzo, la capacidad de autorregulación del flujo cerebral puede ser sobrepasada, con vasodilatación primero de las vénulas -por su escasa estructura muscular- y luego de arteriolas y capilares, y disrupción de la barrera hematoencefálica, edema cerebral focal, cambios locales del intercambio iónico y de los neurotransmisores, que lleva finalmente al deterioro de la función neurológica normal, lo que se denomina encefalopatía hipertensiva, y cuya principal característica es la rápida resolución del cuadro clínico con el descenso de la PA19-21.
De la hipertensión arterial a la insuficiencia cardíaca
El incremento de la carga sistólica que ocurre en la HTA determina hipertrofia miocitaria, caracterizada por el aumento de las dimensiones laterales de los miocitos. Esta HVI se acompaña de alteraciones del estado contráctil, pero con mantenimiento inicial de la fuerza de contracción.
La síntesis de cadenas lentas de miosina se altera al igual que los sistemas de activación, lo que se manifiesta por una menor y más lenta velocidad de contracción y un retardo de la repolarización. Desde un punto de vista hemodinámico, esto se manifiesta por preservación de la capacidad de vaciamiento ventricular y volumen diastólico con fracción de eyección normales, pero tanto los tiempos sistólicos como diastólicos están prolongados a una determinada frecuencia cardíaca, y como los espesores parietales están aumentados, las presiones diastólicas tienden a elevarse. Por lo tanto, en esta etapa es posible observar signos de congestión venosa pulmonar, y aun edema agudo de pulmón con función sistólica normal. La taquicardia sinusal o las taquiarritmias supraventriculares al acortar la duración de la diástole pueden empeorar el cuadro clínico, y en el caso de la fibrilación auricular se debe considerar también la pérdida de la contracción auricular; la sobrecarga excesiva de sodio puede tener los mismos efectos. Este concepto es el que ha definido a la insuficiencia cardíaca (IC) por disfunción diastólica o IC con función sistólica conservada, y en el que nos detendremos a analizar unos instantes. La diástole es tanto un proceso pasivo como activo, en el que la extrusión de calcio celular es fundamental al favorecer la relajación diastólica ventricular. La diástole comienza cuando la presión intraventricular es menor que la auricular. El "período de lleno rápido" en la parte inicial de la diástole da cuenta de entre el 60% y el 70% del llenado ventricular, y es la fase diastólica mayormente comprometida por la HVI consecutiva a la HTA, ya que el ventrículo izquierdo se torna menos complaciente, lo que implica incremento en la presión telediastólica y eventual dilatación auricular izquierda. Como consecuencia de ello, el gradiente aurículo-ventricular se reduce, y por ende, la velocidad de flujo. En el ecocardiograma Doppler esto se manifiesta por una menor velocidad de onda E, que caracteriza al período de llenado rápido, con conservación de onda A, demostrativa de la sístole auricular, y con una relación E/A reducida; este patrón de lleno ventricular se denomina de alteración en la relajación diastólica, y es patognomónico de los estadios iniciales de la HTA con HVI sin incremento significativo en el tejido conectivo intersticial. Sin embargo, con el paso del tiempo y la falta de control de los niveles tensionales, comienza a observarse pérdida miocítica y su reemplazo por tejido conectivo; ya la alteración miocárdica es estructural y probablemente irreversible al menos en forma parcial; se puede objetivar en el ecocardiograma Doppler por el patrón restrictivo, con aumento de la velocidad de flujo E, y pobre sístole auricular, debido a que el ventrículo izquierdo ha alcanzado casi la totalidad de sus posibilidades de repleción en la etapa de lleno rápido, y no logra aceptar flujo durante la patada auricular; en consecuencia la relación E/A se encuentra aumentada (Figura 4).
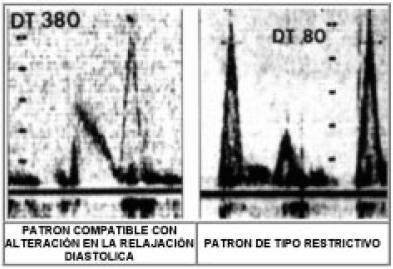
Figura 4. Análisis espectral del llenado ventricular izquierdo.
La HTA en forma aislada, pero más si está asociada a cardiopatía isquémica, junto al proceso de envejecimiento producen pérdida de miocitos. Los miocitos perdidos son reemplazados por tejido conectivo, lo que lleva a sobrecarga de trabajo de los miocitos remanentes y a mayor hipertrofia de los mismos, y finalmente se deteriora la función ventricular. Si la sobrecarga de presión se sostiene en el tiempo y la pérdida miocitaria se incrementa, la evolución hacia una fase de IC descompensada es inevitable. En este caso, el volumen diastólico del ventrículo izquierdo se incrementa con el objeto de mantener el volumen minuto, pero se desarrolla una progresiva caída de la fracción de eyección, agregándose a la disfunción diastólica, la disfunción sistólica. Con el progreso de la enfermedad se activan el sistema nervioso simpático y el sistema renina-angiotensinaaldosterona (SRA-A), que ya sea por mecanismos directos o indirectos generan mayor daño ventricular. Se ha observado un incremento progresivo en la liberación de norepinefrina miocárdica con el desarrollo de HVI, con una correlación directa con su severidad, y cuando la activación simpática se asocia a sobrecarga hemodinámica, como ocurre en la HTA, el remodelado miocárdico se hace evidente. La hiperactividad simpática se manifiesta por incremento de la frecuencia cardiaca, aumento de la demanda miocárdica de oxígeno y reducción de la perfusión miocárdica por acortamiento del tiempo de perfusión diastólica, lo que contribuye tanto a la disfunción diastólica como sistólica y a la caída de la reserva de flujo coronario. La hipoperfusión resultante de la caída del volumen minuto promueve disfunción endotelial e hipoperfusión tisular, y la isquemia focal activa SRA-A locales, factores de crecimiento y citoquinas, que junto con la activación sistémica son responsables de las alteraciones en la circulación coronaria y la circulación periférica, y del remodelado vascular que ocurre en estadios avanzados de la insuficiencia cardiaca22 (Figuras 5 y 6).
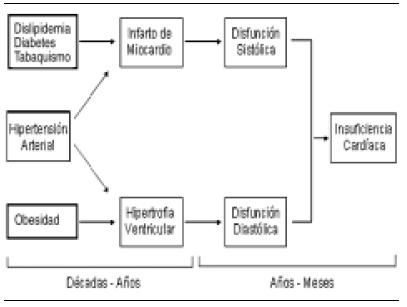
Figura 5. De la hipertensión arterial a la insuficiencia cardíaca.
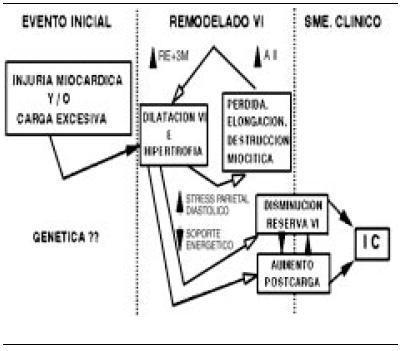
Figura 6. Estadios evolutivos a la insuficiencia cardíaca.
1. Anderson TW. Re-examination of some of the Framingham blood-pressure data. Lancet 1978;11:1139. [ Links ]
2. Expertos del Grupo de Trabajo del Comité de Epidemiología y Prevención de la Federación Argentina de Cardiología- 1999. Prevención de la enfermedad cardiovascular aterosclerótica. Recomendaciones prácticas. Resumen de las Normativas del Primer Grupo de Consenso en Prevención Cardiovascular. Rev Fed Arg Cardiol 1999;28:399-414. [ Links ]
3. The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. The JNC 7 Report. JAMA 2003;289:2560-2572. [ Links ]
4. Guidelines Subcommittee. 1999 WHO- International Society of Hypertension Guidelines for the Management of Hypertension. J Hypertens 1999;17:151-183. [ Links ]
5. Echevarria RF, Camacho RO, Carbajal HA, Salazar MR. Prevalencia de hipertensión arterial en La Plata. Medicina 1988;48:22-28. [ Links ]
6. Salazar M, Carbajal H, Aizpurua M y cols. Prevención primaria de la hipertensión arterial: ¿Qué es lo más importante? Rev Fed Arg Cardiol 1999;28(supl 1):59(Resumen). [ Links ]
7. Limansky R, Farias J, Camera MI. Prevalence of arterial hypertension in Argentina. J Hypertens 1992;10(Suppl 4):S94(Abstract). [ Links ]
8. Nigro D, Vergottini J, Kuschnir E y cols. Epidemiología de la hipertensión arterial en la ciudad de Córdoba, Argentina. Rev Fed Arg Cardiol 1999;28:69-75. [ Links ]
9. Fernández Contreras R, Terragno N, Gómez Llambi H y cols. Prevalencia, control y tratamiento de la Hipertensión Arterial. XVII Congreso Interamericano de Cardiología. Septiembre 1999. [ Links ]
10. Piskorz D, Locatelli H, Gidekel L y cols. Factores de riesgo en la ciudad de Rosario. Resultados del estudio FAROS. Rev Fed Arg Cardiol 1995;24:499-508. [ Links ]
11. Piskorz D, Locatelli H, Toni C y cols. Hipertensión arterial, colesterol plasmático total y tabaquismo. Un estudio epidemiológico de la ciudad de Rosario. Rev Arg Cardiol 1995;63:25-36. [ Links ]
12. Piskorz D. El cardiólogo, la hipertensión arterial y los riñones. Ref Fed Arg Cardiol 2002;31:26-30. [ Links ]
13. Piskorz D. PROCARDIO Programa de Actualización en Cardiología. Sistema de Educación Médica Continua a Distancia organizado por: Federación Argentina de Cardiología. Módulo 2 Primer Ciclo. Editorial Panamericana. Edición Año 2000. UD8: Fondo de ojo. Páginas 163 a 164. [ Links ]
14. Keith NM, Wagener HP, Barker NW. Some different types of essential hypertension: their course and prognosis. Am J Med Sci 1939;197:332-343. [ Links ]
15. Bendersky M, Piskorz D, Boccardo D. Cardiopatía Hipertensiva. Rev Fed Arg Cardiol 2002;31:321-334. [ Links ]
16. Devereux RB, Pini R, Aurigemma GP, Roman MJ. Measurement of left ventricular mass: methodology and expertise. J Hypertens 1997;15:801-809. [ Links ]
17. Piskorz D, Robiolo O, Citta N y cols. Fenotipos ventriculares en Hipertensión Arterial. Rev Fed Arg Cardiol 2000;29 (Supl 1):116(Resumen). [ Links ]
18. Koren MJ, Devereux RB, Casale PN, Savage DD, Laragh JH. Relation of left ventricular mass and geometry to morbidity and mortality in uncomplicated essential hypertension. Ann Intern Med 1991;114:345-352. [ Links ]
19. Caplan LR, Schoene WC. Clinical features of subcortical arteriosclerotic encephalopathy (Binswanger disease). Neurology 1978;28:1206-1215. [ Links ]
20. Yao H, Sadoshima S, Ibayashi S et al. Leukoaraiosis and dementia in hypertensive patients. Stroke 1992;23:1673-1677. [ Links ]
21. Healton EB, Brust JC, Feinfeld DA et al. Hypertensive encephalopathy and the neurologic manifestations of malignant hypertension. Neurology 1982;32:127-132. [ Links ]
22. Sonnenblick EH, LeJemtel TH. Pathogenesis of congestive heart failure. En: Izzo JL, Black HR. Hypertension Primer. Second Edition. Año 1999. Páginas 180-182. [ Links ]