Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Insuficiencia cardíaca
versión On-line ISSN 1852-3862
Insuf. card. v.3 n.1 Ciudad Autónoma de Buenos Aires ene./mar. 2008
ARTÍCULO ORIGINAL
Asistencia y regeneración del miocardio combinando terapia celular e ingeniería de tejidos
Resultados del estudio clínico MAGNUM
Juan C. Chachques, MD, PhD*; Jorge C. Trainini, MD**; Noemí Lago, MD**; Alejandra Christen, MD**; Osvaldo H. Masoli, MD***; José L. Barisani, MD**; Miguel Cortés-Morichetti, MD*; Olivier Schussler, MD*; Alain Carpentier, MD, PhD*
* Departamento de Cirugía Cardiovascular, Hospital Pompidou, París, Francia.
** Departamentos de Cirugía Cardiovascular. Hospital "Tte. Gral. Juan Domingo Perón". Avellaneda. Buenos Aires. República Argentina.
*** División Cardiología. Hospital Gral. De Agudos "Dr. Cosme Argerich". GCBA. Ciudad de Buenos Aires. Rep. Argentina.
Correspondencia: Juan C. Chachques, MD, PhD.
Department of Cardiovascular Surgery.
Pompidou Hospital.
20 rue Leblanc.
75015 Paris, France.
Phone: ++33613144398
Fax ++33140728608
E-mail: j.chachques@brs.aphp.fr
Trabajo recibido: 08/02/2008
Trabajo aceptado:10/03/2008
Objetivos. El trasplante celular para la regeneración del miocardio está limitado por la escasa viabilidad del injerto y la baja retención celular. En la miocardiopatía isquémica la matriz extracelular está profundamente alterada, por consiguiente, sería importante asociar un procedimiento para regenerar las células miocárdicas y restaurar la función de la matriz extracelular. En este estudio clínico, fue evaluada la terapia celular intrainfarto asociada a una matriz de colágeno sembrada con células e implantada sobre ventrículos infartados.
Métodos. En 15 pacientes (54,2±3,8 años de edad) que presentaban cicatrices miocárdicas postisquémicas en el ventrículo izquierdo (VI) y con indicación de cirugía de revascularización miocárdica, se implantaron, durante la operación, células de la médula ósea mononucleares autólogas (CMO) en la cicatriz. Se agregó sobre esa zona infartada una matriz de colágeno tipo I con el mismo número de CMO.
Resultados. No hubo mortalidad ni eventos adversos relacionados (seguimiento 15±4,2 meses). La clase funcional según la New York Heart Association (NYHA) mejoró de 2,3±0,5 a 1,4±0,3 (p=0,005). El volumen de fin de diástole del VI evolucionó de 142±24 a 117±21 mL (p=0,03), el tiempo de desaceleración del llenado del VI mejoró aumentando de 162±7 mseg a 196±8 mseg (p=0,01). El espesor del área cicatrizada progresó de 6±1,4 a 9±1,5 mm (p=0,005). La fracción de eyección (FE) mejoró de 25±7 a 33±5% (p=0,04).
Conclusiones. La inyección intramiocárdica de células de médula ósea y la fijación simultánea de una matriz sembrada con progenitores celulares (stem cells) sobre el epicardio fue simple y sin complicaciones. La matriz de colágeno aumento el espesor de la zona del infarto con nuevos tejidos viables, limitando la dilatación ventricular y mejorando la función diastólica. Estos resultados positivos no pueden ser absolutamente relacionados a las células y la matriz, pues se asociaron puentes de revascularización coronaria. En conclusión, la ingeniería de tejidos puede extender las indicaciones y beneficios de la terapia con células madre en cardiología, convirtiéndose en un camino prometedor para la creación de un "miocardio bioartificial".
Palabras clave: Terapia celular; Regeneración miocárdica; Ingeniería de tejidos; Insuficiencia cardíaca; Enfermedad cardíaca isquémica; Miocardio bioartificial; Cardiomioplastia celular
Summary
Myocardial regeneration and asistance combined cardiac tissue engineering and stem cell therapy
Outcome of trial MAGNUM
Objectives. Stem cell therapy for myocardial regeneration is limited by poor graft viability and low cell retention. In ischemic cardiomyopathy the extracellular matrix is pathologically modified, therefore it could be important to associate a procedure aiming at regenerating both, myocardial cells and the extracellular matrix. We evaluated intrainfarct cell therapy associated with a cell-seeded collagen scaffold grafted onto infarcted hearts.
Methods. In 15 patients (aged 54.2±3.8 years) presenting LV postischemic myocardial scars and with indication for a single off-pump-CABG, autologous mononuclear bone marrow cells (BMC) were implanted during surgery in the scar. A 3D collagen type I matrix seeded with the same number of BMC was grafted onto the infarction zone.
Results. There was no mortality and any related adverse events (follow-up 15±4.2 months). NYHA FC improved from 2.3±0.5 to 1.4±0.3 (p=0.005). LV end-diastolic volume evolved from 142±24 to 117±21 mL (p=0.03), LV filling deceleration time improved from 162±7 ms to 196±8 ms (p=0.01). Scar area thickness progress from 6±1.4 to 9±1.5mm (p=0.005). EF improved from 25±7 to 33±5% (p=0.04).
Conclusions. Simultaneous intramyocardial injection of mononuclear bone marrow cells and fixation of a BMC-seeded matrix onto the epicardium is feasible and safe. The cell seeded collagen matrix seems to increase the thickness of the infarct scar with viable tissues and help to normalize cardiac wall stress in injured regions, thus limiting ventricular remodelling and improving diastolic function. Patients' improvements can not be conclusively related to the cells and matrix due to the association of CABG. Cardiac tissue engineering should extend the indications and benefits of stem cell therapy in cardiology, becoming a promising way for the creation of a "bioartificial myocardium".
Key words: Stem cell therapy; Myocardial regeneration; Tissue engineering; Heart failure; Ischemic heart disease; Bioartificial myocardium; Cellular cardiomyoplasty
Resumo
Assistência e regeneração do miocárdio combinando terapia celular e engenharia de tecidos
Resultados do estudo clínico MAGNUM
Objetivos. O transplante celular para a regeneração do miocárdio está limitado pela escassa viabilidade do enxerto e a baixa retenção celular. Na Cardiomiopatia isquêmica a matriz extracelular está profundamente alterada, por conseguinte, seria importante associar um procedimento para regenerar as células miocárdicas e restaurar a função da matriz extracelular. Neste estudo clínico, foi avaliada a terapia celular intra-enfarto associada a uma matriz de colágeno semeada com células e implantada sobre ventrículos enfartados.
Métodos. Em 15 pacientes (54,2±3,8 anos de idade) que apresentavam cicatrizes miocárdicas post isquêmicas no ventrículo esquerdo (VE) e com indicação de cirurgia de revascularização miocárdica, implantaram-se, durante a operação, células da medula ósseas mononucleares autológamas (CMO) na cicatriz. Agregou-se sobre essa zona enfartada uma matriz de colágeno tipo I com o mesmo número de CMO.
Resultados. Não houve mortalidade nem eventos adversos relacionados (seguimento 15±4,2 meses). A classe funcional segundo a New York Heart Association (NYHA) melhorou de 2,3±0,5 a 1,4±0,3 (p=0,005). O volume de fim de diástole do VE evolucionou de 142±24 a 117±21 mL (p=0,03), o tempo de desaceleração do enchido do VE melhorou aumentando de 162±7 mseg a 196±8 mseg (p=0,01). A espessura da área cicatrizada progrediu de 6±1,4 a 9±1,5 mm (p=0,005). A fração de ejeção (FE) melhorou de 25±7 a 33±5% (p=0,04).
Conclusões. A injeção intramiocárdica de células de medula óssea e a fixação simultânea de uma matriz semeada com progenitores celulares (stem cells) sobre o epicárdio foi simples e sem complicações. A matriz de colágeno aumentou a espessura da zona do enfarto com novos tecidos viáveis, limitando a dilatação ventricular e melhorando a função diastólica. Estes resultados positivos não podem ser absolutamente relacionados às células e à matriz, pois se associaram pontes de revascularização coronária. Em conclusão, a engenharia de tecidos pode estender as indicações e benefícios da terapia com stem cells em cardiologia, convertendo-se em um caminho prometedor para a criação de um "miocárdio bioartificial".
Palavras clave: Terapia celular; Regeneração miocárdica; Engenharia de tecidos; Insuficiência cardíaca; Doença cardíaca isquêmica; Miocárdio bioartificial; Cardiomioplastia celular
Introducción
La medicina regenerativa es ya aceptada como una nueva y promisoria disciplina, su desarrollo ha sido posible gracias a los avances en la "biología celular" y más recientemente a la creación de una nueva disciplina denominada "ingeniería de tejidos". El objetivo de los tratamientos de regeneración de células y tejidos es reparar la estructura y función de órganos patológicos, de esa manera se podría postergar o evitar el trasplante de órganos.
En el dominio de la cardiología, la terapia celular se ha integrado dentro de la sub-especialidad "Bioasistencia Cardíaca"1-3. Los procedimientos de bioasistencia cardíaca fueron creados para tratar la insuficiencia cardíaca (IC) refractaria, que persiste cuando los tratamientos médicos y quirúrgicos clásicos han agotado sus efectos.
El objetivo del trasplante de células progenitoras indiferenciadas en el miocardio patológico es el de regenerar las células cardíacas y su matriz extracelular, a través de mecanismos de "angiogénesis" y "miogénesis"4,5.
Diversas vías de inyección han sido propuestas y evaluadas, utilizando técnicas de cardiología intervencionista y procedimientos quirúrgicos. Las técnicas transcutáneas mediante catéteres utilizan la vía intracoronaria (transvascular) o la vía endoventricular (transendocárdica)3. Ambas vías pueden ser complementarias para un mismo paciente en distintos estadios de su enfermedad. En casos agudos, se puede comenzar utilizando la vía intracoronaria para inyectar células progenitoras después de una angioplastia. En casos crónicos, puede utilizarse la vía endoventricular, principalmente, si la arteria que irriga la zona infartada está ocluida. Debe recordarse que los sistemas de mapping disponibles para detectar la zona infartada son costosos y necesitan un buen entrenamiento y tiempo6.
Además una inyección única suele no ser suficiente, las inyecciones sucesivas pueden ser necesarias, repetidas a los 6 ó 12 meses del tratamiento inicial. La necesidad de realizar nuevas inyecciones celulares estará determinada por los resultados funcionales y los estudios de viabilidad miocárdica.
Si el paciente necesita cirugía de revascularización coronaria, en esos casos, hay que aprovechar la oportunidad para inyectar directamente las células en el centro y sobre todo en la periferia de la zona infartada (borderzone). En cardiomiopatías no isquémicas (idiopáticas, chagásicas), se puede realizar terapia celular por vía intracoronaria, el 60% de las células se inyectarán en la coronaria izquierda y el 40% en la coronaria derecha.
Después de 8 años de experiencia clínica, utilizando células madre en cardiología1,7,8, en muchos estudios clínicos, la cardiomioplastia celular sola no ha demostrado categóricamente mejorías de la función ventricular9-12. El trasplante de células madre parece estar limitado por una escasa viabilidad de los injertos y por una baja retención celular13. Además, en la enfermedad isquémica, tanto las células contráctiles como la matriz extracelular se encuentran enfermas. Por consiguiente, será importante asociar un procedimiento que apunte a la regeneración de células miocárdicas y la restauración de la función de la matriz extracelular1. El uso de matrices bioartificiales permitiría reestablecer una atmósfera beneficiosa para la supervivencia, multiplicación, diferenciación y función celular. Investigaciones preclínicas con tecnologías de ingeniería de tejidos14,15, mostraron que esta asociación de células madre y matrices puede contribuir a mejorar la eficacia de la terapia celular para la regeneración de órganos. El objetivo de este estudio clínico es evaluar el potencial de una matriz biodegradable de colágeno tipo I sembrada con células de médula ósea (CMO) para ser injertada en ventrículos infartados.
Material y métodos
Pacientes
En un estudio clínico que incluyó 15 pacientes (90% hombres) de edad media 54,2±3,8 años, se asoció trasplante de células madre antólogas con el implante de una matriz de colágeno sembrada con CMO. El estudio MAGNUM es auspiciado por la International Cardiac Bioassist Association, los pacientes fueron tratados en Argentina dentro de un protocolo de Cooperación Científica Franco-Argentina (Hospitales Perón de Avellaneda y Georges Pompidou de Paris), contando con la participación de profesionales de ambas instituciones. Los pacientes presentaban cardiomiopatías isquémicas crónicas, el tiempo de evolución de los infartos era de 8,4±3,2 meses, las arterias afectadas eran descendente anterior (70%) y territorio marginal (30%). La clase funcional (CF) media según la New York Heart Association (NYHA) a la que pertenecían los pacientes era de 2,3±0,5; presentando una disfunción del ventrículo izquierdo (VI): fracción de eyección radioisotópica media del 25±7%, cicatrices postisquémicas en la pared ventricular (acinética y metabólicamente no viable) e indicación quirúrgica de revascularización coronaria.
Los criterios de exclusión fueron: shock cardiogénico o IC congestiva (CF IV - NYHA); historia de leucopenia o trombocitopenia; evidencia de enfermedad maligna o terminal; paciente bajo tratamiento con esteroides, drogas oncológicas o inmunosupresión; insuficiencia renal o insuficiencia hepática conocida y cirugía mayor durante el último mes.
Aislamiento y preparación de las CMO
Cuatro horas antes de la cirugía cardíaca y bajo anestesia local, se aspiró médula ósea (330±28 ml) del hueso ilíaco para obtener células madre mononucleares. La suspensión celular fue tratada mediante gradiente de densidad (método de Ficoll) y centrifugada por 20 minutos a 2000 g. Las CMO fueron aisladas de la capa entre el reactivo Ficoll-Paque y el plasma sanguíneo, y lavadas dos veces en buffer-fosfato salino (PBS). Se obtuvo una suspensión de CMO (CD34+8%, AC133+3%) y se diluyó en suero autólogo del paciente. Se prepararon dos muestras con 250±28 millones de células cada una para la inyección intramiocárdica y el sembrado de la matriz.
Preparación de la matriz de colágeno
La matriz de colágeno fue preparada a partir de un kit de colágeno comercialmente disponible (Pangen 2, CE Mark, Laboratoire Urgo, Chenove, France). Esta matriz 3D biodegradable (tamaño: 5 x 7 x 0,6 cm) es fabricada utilizando colágeno de origen bovino, no desnaturalizado, liofilizado. Los poros de la matriz miden 50-100 µm. En la sala de operaciones, se colocaron las matrices en una placa de Petri, luego 250±28 millones de CMO suspendidas en el medio de cultivo fueron sembradas en cada matriz. Para promover una distribución regular en los poros de las matrices, la placa de Petri conteniendo la matriz de colágeno fue agitada durante 10 minutos a 120 RPM, utilizando un Orbital Shaker (Stuart Scientific, UK). Este procedimiento se puede realizar también utilizando centrifugación (10 minutos a 900 g) de la matriz y de las células.
Procedimiento quirúrgico
Luego de la esternotomía, se realizó el puente de revascularización coronario utilizando arteria mamaria interna izquierda (LIMA: left internal mammary artery). Los puentes fueron realizados sobre arterias con posibilidades de irrigar zonas remotas a la cicatriz de los infartos. Al final de la cirugía realizada sin circulación extracorpórea, el implante de las CMO en la zona infartada (volumen de inyección: 6 ml, conteniendo 250±28 millones de células) se realizó mediante 20±8 puntos de inyección en el centro y principalmente alrededor del infarto (borderzone), utilizando una aguja oftálmica de 25 G x 40 mm.
Luego, una matriz de colágeno tipo I (tamaño: 7 x 5 x 0,6 cm) sembrada con el mismo número de CMO (250±28 millones de células en 12 ml de volumen líquido) fue colocada sobre la zona infartada. Fue fijada sobre el epicardio utilizando 6 suturas de PDS (6-0) y se cubrió con una segunda matriz no-celu larizada (Figura 1).

Figura 1. Procedimiento quirúrgico asociando la inyección de células madre en el miocardio seguida de la fijación de una matriz sembrada con células en la superficie ventricular.
Manejo postoperatorio y seguimiento clínico
Todos los pacientes recibieron amiodarona oral (200 mg/día) como droga antiarrítmica, comenzando una semana antes de la cirugía y hasta el 3er mes postoperatorio. Durante el período postoperatorio, el ritmo cardíaco fue monitoreado en el hospital a través de telemetría continua. Luego del alta, se realizaron estudios ECG-Holter a los 1, 2 y 3 meses. La función ventricular y la viabilidad miocárdica fueron evaluadas por ecocardiografía, ventriculografía radioisotópica (MIBI Gated Spect) y resonancia magnética nuclear (RMN).
Estadísticas
Los resultados fueron analizados y reportados como porcentaje o media ± desviación estándar (SD). Se utilizó el test T de Student para comparar los grupos. Fue considerado como estadísticamente significativo un valor de p<0,05.
Resultados
Todos los pacientes tuvieron una recuperación sin complicaciones y permanecieron en terapia intensiva 3,6±1,8 días. Luego fueron dados de alta, permaneciendo 10±3 días internados. No se reportaron arritmias cardíacas malignas en una media de seguimiento de 15±4,2 meses, sin mortalidad ni eventos adversos relacionados.
La CF según la NYHA mejoró de 2,3±0,5 a 1,4±0,3 (p=0,005) (Figura 2). Los estudios de medicina nuclear y de RMN mostraron que el 58±9,3% de los segmentos ventriculares tratados con células madre y matrices mejoraron su cinética y viabilidad (Figuras 3 y 4). La fracción de eyección (FE) mejoró de 25±7 a 33±5% (p=0,04) (Figura 5). Con respecto al remodelamiento post isquémico y a la función diastólica, los estudios ecocardiográficos mostraron que el volumen de fin de diástole del VI se redujo de 142±24 a 117±21 mL (p=0,03) (Figura 6), y que el tiempo de desaceleración del llenado del VI mejoró aumentando de 162±7 mseg a 196±8 mseg (p=0,01) (Figura 7). El espesor de la pared ventricular medido en la zona infartada progresó de 6±1,4 a 9±1,5 mm (p=0,005) después del tratamiento con matrices y células madre (Figura 8).

Figura 2. Evaluación funcional de los pacientes (clase funcional de la New York Heart Association), seguimiento de 15±4,2 meses.

Figura 3. Evaluación preoperatoria de la perfusión miocárdica utilizando radioisótopos (SPECT Tc99m sestamibi). El área antero-latero-apical del ventrículo izquierdo infartada está coloreada en azul (representación 3D).

Figura 4. A los 6 meses el paciente tratado con células madre (stem cells) asociado a la matriz de colágeno muestra una reducción del área infartada de 62 % (en azul).
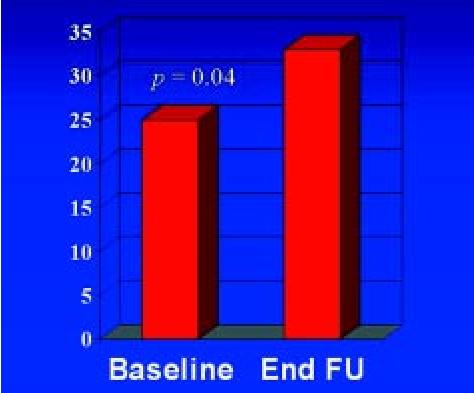
Figura 5. Fracción de eyección ventricular izquierda preoperatoria (dentro de los 10 días previos a la intervención) versus final de la evaluación (a 15±4,2 meses).

Figura 6. Volúmenes de fin de diástole del ventrículo izquierdo.

Figura 7. Estudio ecocardiográfico de función diastólica. Tiempos de desaceleración medidos a nivel del flujo diastólico transmitral.

Figura 8. Estudio del espesor de la pared ventricular en el sitio de la cicatriz del infarto, tratada con trasplante de células madre y una matriz de colágeno "celularizada" (miocardio bioartificial).
Discusión
Existen, principalmente, dos tipos de fibras de colágeno en el corazón adulto normal, el tipo I y el tipo III, producidas por fibroblastos y miofibroblastos. Las fibras de tipo I representan el 80% de la proteína colágeno en el corazón y la fibra de tipo II cerca del 10%. Las fibras de colágeno tipo I proveen un soporte estructural y otorgan al corazón propiedades que incluyen firmeza y resistencia a la deformación. Las fibras de colágeno tipo III desempeñan un importante rol como eslabón entre los elementos contráctiles adyacentes (cardiomiocitos), llevando información útil para la función celular.
En la zona infartada, la matriz extracelular es modificada, el colágeno tipo I disminuye del 80 al 40% y el colágeno tipo III aumenta del 10 al 35%, creando una fibrosis patológica. El resultado es un remodelado ventricular adverso, dilatación y disfunción diastólica y sistólica16-18.
Diversos estudios experimentales mostraron que las matrices de colágeno influyen positivamente sobre la sobrevida de las células trasplantadas y contribuyen a la mejoría de la función ventricular y a la limitación de la dilatación postisquémica14,15.
El presente estudio clínico realizado en pacientes isquémicos, mostró que la terapia con células de médula ósea asociada con el implante quirúrgico de una matriz de colágeno tipo I sembrada con células evita el adelgazamiento de la pared miocárdica, limita el remodelado postisquémico adverso y mejora la función diastólica. El uso de este biomaterial parece crear una micro-atmósfera donde las células exógenas y endógenas encuentran el micro-ambiente óptimo para reparar con baja producción de fibrosis cicatrizal.
En el procedimiento utilizado, las células progenitoras fueron sembradas en la matriz conjuntamente con su medio de cultivo celular, momentos antes de la fijación quirúrgica de la matriz sobre la superficie del corazón. Esas células encuentran durante los primeros días un ambiente nutritivo favorable (colágeno + medio de cultivo proteico), a una temperatura similar al cultivo en estufas de incubación (37° C). Es bien conocido por todos los cardiocirujanos por reoperar pacientes, que después de la cirugía cardíaca se desarrollan rápidamente adherencias muy vascularizadas en la cavidad pericárdica. Estas adherencias son muy importantes a partir del 5° día de postoperatorio y favorecerían la irrigación de la matriz de colágeno y del contenido celular. También, un alto porcentaje de células monucleadas de médula ósea son progenitores vasculares, que producirán una angiogénesis local. La matriz de colágeno utilizada tiene un periodo de "biodegradabilidad" de 2 meses, en ese lapso un nuevo tejido viable se habrá constituido que contribuirá a la irrigación del miocardio isquémico a partir del pericardio. Algunas células mesenquimales de médula ósea podrán diferenciase en "cardiomiocitos". Hemos observado que ese tejido se incorpora a la pared isquémica (sin desaparecer completamente) y contribuye a su regeneración. Varios estudios experimentales contribuyen a demostrar estos hechos14,15,19,20.
Los efectos favorables de una matriz sembrada con células pueden ser atribuidos a varios mecanismos. Primero, la matriz de colágeno contribuye a la retención y la sobrevida celular, estimulando efectos paracrinos. Las CMO sembradas en la matriz de colágeno son, probablemente incorporadas en el miocardio huésped a través de los canales del epicardio creados al nivel de los sitios de la inyección de la aguja, donde los infartos han sido tratados directamente por células. Segundo, la matriz sembrada con células ayuda a prevenir la apoptosis en el miocardio isquémico. Este efecto antiapoptótico puede ser mediado por una mejoría en la perfusión del miocardio a través de la angiogénesis inducida por células progenitoras endoteliales.
El efecto antiapoptótico puede también ser mediado por un efecto mecánico, debido a una disminución de la tensión parietal relacionada con el engrosamiento de la pared ventricular y la reducción en las dimensiones del VI21.
La evolución exacta de las células implantadas en el miocardio patológico no ha sido completamente dilucidada. Este proceso puede potencialmente incluir:
1) Transdiferenciación de las células madre trasplantadas (plasticidad celular).
2) Fusión de las células implantadas con células residentes (quimerismo).
3) Angiogénesis reactiva, consecuencia probable de la secreción parácrina de factores de crecimiento angiogénicos.
4) Modulación de la inflamación a nivel de la matriz extracelular22,23.
La ingeniería de tejidos es un campo emergente, comenzó en 1970 y está basado en el uso de una combinación de células, materiales de ingeniería y factores bioquímicos aptos para mejorar o reemplazar las funciones biológicas. Probablemente, la primera definición de ingeniería de tejidos fue la de Langer y Vacanti24, quiénes indicaron que es "un campo interdisciplinario que aplica los principios de las ciencias de la ingeniería y de la vida en pos de un desarrollo de sustitutos biológicos que restauren, mantengan o mejoren las funciones tisulares o un órgano completo".
Los materiales de ingeniería pueden ser implantados o "sembrados" en una estructura natural o sintética capaz de soportar una formación de tejido tridimensional. Estos soportes (scaffolds) son generalmente críticos, tanto ex vivo como in vivo, deben simular el medio ambiente in vivo y permitir a las células influenciar su propio micro-ambiente. Tales soportes sirven al menos a uno de los siguientes propósitos: permitir acoplamiento y migración celular, entregar y retener células y factores bioquímicos, permitir la difusión de nutrientes celulares vitales y productos expresados y ejercer ciertas influencias mecánicas y biológicas para modificar el comportamiento de la fase celular18,25,26. Dispositivos específicos denominados "birreactores" han sido diseñados y son utilizados para manufacturar tejidos in vitro que reemplazarán luego los tejidos enfermos in vivo27,28.
Para alcanzar el objetivo de reconstrucción tisular, los soportes (en la mayoría de los casos son matrices tridimensionales) deben tener algunos requerimientos específicos. Son necesarios una alta porosidad y un adecuado tamaño de los poros para facilitar el sembrado y difusión de las células a través de toda la estructura de ambos, células y nutrientes. La biodegradabilidad es esencial ya que los soportes necesitan ser absorbidos por los tejidos que los rodean sin necesidad de ser removidos quirúrgicamente.
El grado en que ocurre la degradación debe coincidir, lo mejor posible, con el grado de formación de tejido: esto significa que mientras hay células fabricando su propia estructura natural de matriz alrededor de ellas mismas, el soporte puede proveer integridad estructural dentro del cuerpo, y eventualmente se romperá, dejando el neotejido (el tejido recientemente formado) que se encargará de soportar la carga mecánica.
Las actuales aplicaciones clínicas de la ingeniería de tejidos incluyen especialidades como neurocirugía, ortopedia, urología, dermatología, cirugía plástica, odontología, reemplazo traqueal, cirugía vascular y cirugía cardíaca valvular20,29.
Los resultados presentados en este articulo sugieren que la acumulación de colágeno causada por la colocación sobre el corazón de un parche de colágeno sembrado con células evita el adelgazamiento de la pared cardíaca y limita el remodelamiento adverso postisquémico. El colágeno es una de las nuevas familias de soportes biomiméticos que es comercializado para uso clínico y está impactando la ingeniería de tejidos. La integración funcional de las fibras de colágeno provistas por el parche dentro del área infartada, sumado al proceso fisiológico reparativo de fibrosis refuerza la pared ventricular infartada aumentando la tolerancia al estrés y limitando la expansión ventricular.
Otra opción en la ingeniería de tejidos cardíacos es inyectar un gel de colágeno tipo IV laminado (por ejemplo: matrigel) para tratar el infarto . Los gels de colágenos disponibles para investigación (ejemplo: matrigel) están contraindicados para el uso clínico, debido a su origen (sarcoma de ratón EHS) y la toxicidad de los componentes en solución. Un riesgo adicional es la creación de un área disecada en el tejido miocárdico, debido a la inyección del gel, que puede dejar como secuela un espacio muerto después de la absorción del material. Esta situación podría ser comparada con la patología del "miocardio no compactado"30.
Entre los límites de este estudio debe considerarse la asociación de la cirugía de revascularización coronaria a la terapia celular y las matrices. Por ese motivo la mejoría clínica y funcional no puede atribuirse exclusivamente al nuevo tratamiento biológico. Estudios aleatorios prospectivos podrán dilucidar esa incógnita. Además, se utilizó una matriz de colágeno de primera generación, biodegradable entre 2 y 3 meses. Actualmente, estamos desarrollando matrices de segunda generación, con periodos más prolongados de absorción, que llevan incorporados mediante "cross-linking" factores de crecimiento angiogénicos y antiapoptóticos para favorecer la multiplicación y diferenciación celular31.
En conclusión, el uso de matrices permite reestablecer una atmósfera beneficiosa para la multiplicación, sobrevida, diferenciación y función celular14,32,33. La ingeniería de tejidos cardíacos emerge como un nuevo útil terapéutico y extiende, aún más, las posibilidades de la terapia celular en cardiología34,37, convirtiéndose en un camino prometedor para la creación de un "miocardio bioartificial".
1. Chachques JC, Acar C, Herreros J, Trainini, JC, Prosper F, D'Attellis N, Fabiani JN, Carpentier A. Cellular cardiomyoplasty: clinical application. Ann Thorac Surg 2004;77:1121-1130. [ Links ]
2. Chachques JC. Cardiomioplastía celular y miocardio bioartificial. Insuf Cardíaca 2006;1:34-37. [ Links ]
3. Carpentier A, Chachques JC, Grandjean P (Eds): Cardiac Bioassist. Futura Publishing, New York 1997: 1-632. [ Links ]
4. Trainini JC, Chachques JC, Lago N. Asistencia miocardica con matrices bioartificiales. Rev Argent Cardiol 2006; 74: 401-405. [ Links ]
5. Chachques JC, Herreros J, Trainini JC. Cardiomioplastia celular. Rev Argent Cardiol 2003; 71: 138-145. [ Links ]
6. Chachques JC, Azarine A, Mousseaux E, El Serafi M, Cortes-Morichetti M, Carpentier A: MRI evaluation of local myocardial treatments: epicardial versus endocardial (Cell-Fix catheter) injections. J Interv Cardiol 2007;20:188-196. [ Links ]
7. Wollert KC, Drexler H. Clinical applications of stem cells for the heart. Circ Res 2005;96:151-163. [ Links ]
8. Chachques JC, Herreros J, Trainini J, Juffe A, Rendal E, Prosper F, Genovese J. Autologous human serum for cell culture avoids the implantation of cardioverter-defibrillators in cellular cardiomyoplasty. Int J Cardiol 2004;95(Suppl 1):S29-S33. [ Links ]
9. Janssens S, Dubois C, Bogaert J, Theunissen K, Deroose C, Desmet W, et al. Autologous bone marrow-derived stem-cell transfer in patients with ST-segment elevation myocardial infarction: double-blind, randomised controlled trial. Lancet 2006;367:113-121. [ Links ]
10. Lunde K, Solheim S, Aakhus S, Arnesen H, Abdelnoor M, Egeland T, et al. Intracoronary injection of mononuclear bone marrow cells in acute myocardial infarction. N Engl J Med 2006;355:1199-1209. [ Links ]
11. Meyer GP, Wollert KC, Lotz J, Steffens J, Lippolt P, Fichtner S, et al. Intracoronary bone marrow cell transfer after myocardial infarction: eighteen months' follow-up data from the randomized, controlled BOOST (BOne marrOw transfer to enhance ST-elevation infarct regeneration) trial. Circulation 2006;113:1287-1294. [ Links ]
12. Stamm C, Kleine HD, Choi YH, Dunkelmann S, Lauffs JA, Lorenzen B, et al. Intramyocardial delivery of CD133+ bone marrow cells and coronary artery bypass grafting for chronic ischemic heart disease: safety and efficacy studies. J Thorac Cardiovasc Surg 2007;133:717-725. [ Links ]
13. Teng CJ, Luo J, Chiu RC, Shum-Tim D. Massive mechanical loss of microspheres with direct intramyocardial injection in the beating heart: implications for cellular cardiomyoplasty. J Thorac Cardiovasc Surg 2006;132:628-632. [ Links ]
14. Cortes-Morichetti M, Frati G, Schussler O, Van Huyen JPD, Lauret E, Genovese J, Carpentier AF, Chachques JC. Association between a cell-seeded collagen matrix and cellular cardiomyoplasty for myocardial support and regeneration. Tissue Eng 2007;13:2681-87. [ Links ]
15. Kutschka I, Chen IY, Kofidis T, Arai T, von Degenfeld G, Sheikh A, et al. Collagen matrices enhance survival of transplanted cardiomyoblasts and contribute to functional improvement of ischemic rat hearts. Circulation 2006;114(1 Suppl):I167-173. [ Links ]
16. Brown L. Cardiac extracellular matrix: a dynamic entity. Am J Physiol Heart Circ Physiol 2005;289:973-974. [ Links ]
17. Jugdutt BI, Joljart MJ, Khan MI. Rate of collagen deposition during healing and ventricular remodelling after myocardial infarction in rat and dog models. Circulation 1996;94:94-101. [ Links ]
18. Eschenhagen T, Zimmermann WH. Engineering myocardial tissue. Circ Res 2005;97:1220-1231. [ Links ]
19. Eschenhagen T, Zimmermann WH, Kleber AG. Electrical coupling of cardiac myocyte cell sheets to the heart. Circ Res 2006;98:573-575. [ Links ]
20. Leor J, Landa N, Cohem S. Renovation of the injured heart with myocardial tissue engineering. Expert Rev Cardiovasc Ther 2006;4:239-252. [ Links ]
21. Jessup M, Brozena S. Heart failure. N Engl J Med 2003;348:2007-2018. [ Links ]
22. Fedak PW, Szmitko PE, Weisel RD, Altamentova SM, Nili N, Ohno N, et al. Cell transplantation preserves matrix homeostasis: a novel paracrine mechanism. J Thorac Cardiovasc Surg 2005;130:1430-1439. [ Links ]
23. Lunkenheimer PP, Redmann K, Westermann P, Rothaus K, Cryer CW, Niederer P, et al. The myocardium and its fibrous matrix working in concert as a spatially netted mesh: a critical review of the purported tertiary structure of the ventricular mass. Eur J Cardiothorac Surg 2006;29(Suppl 1):S41-49. [ Links ]
24. Langer R, Vacanti JP. Tissue engineering. Science 1993;206:920-926. [ Links ]
25. Kofidis T, de Bruin JL, Hoyt G, Ho Y, Tanaka M, Yamane T, et al. Myocardial restoration with embryonic stem cell bioartificial tissue transplantation. J Heart Lung Transplant 2005;24:737-744. [ Links ]
26. Kofidis T, Lebl DR, Martinez EC, Hoyt G, Tanaka M, Robbins RC. Injectable bioartificial tissue facilitates targeted, less invasive, large-scale tissue restoration on the beating heart following myocardial injury. Circulation 2005;112(9 Suppl):I173-177. [ Links ]
27. Barron V, Lyons E, Stenson-Cox C, McHugh PE, Pandit A. Bioreactors for cardiovascular cell and tissue growth: a review. Ann Biomed Eng 2003;31:1017-30. [ Links ]
28. Mironov V, Kasyanov VA, Yost MJ, Visconti R, Twal W, Trusk T, Wen X, Ozolanta I, Kadishs A, Prestwich GD, Terracio L, Markwald RR. Cardiovascular tissue engineering I. Perfusion bioreactors: a review. J Long Term Eff Med Implants 2006;16:111-30. [ Links ]
29. Vacanti C. A. History of tissue engineering and a glimpse into its future. Tissue Eng 2006;12:1137-1142. [ Links ]
30. Ganame J, Ayres NA, Pignatelli RH. Left ventricular noncompaction, a recently recognized form of cardiomyopathy. Insuf Cardíaca 2006;1:119-124. [ Links ]
31. Schussler O, Coirault C, Louis-Tisserand M, El-Chare W, Oliviero P, Menard C, Michelot R, Salomon DR, Chachques JC, Carpentier A, Lecarpentier Y. RGD-coupling to collagen scaffold improves cardiomyocyte viability and contractility: new possibilities for cardiac tissue engineering. Circulation 2007;116(Suppl II):II-70. [ Links ]
32. Zimmermann WH, Melnychenko I, Wasmeier G, Didié M, Naito H, Nixdorff U, et al. Engineered heart tissue grafts improve systolic and diastolic function in infarcted rat hearts. Nat Med 2006;12:452-458. [ Links ]
33. Kresh JY. Cell replacement therapy: the functional importance of myocardial architecture and intercellular gap-junction distribution. J Thorac Cardiovasc Surg 2006;131:1310-1313. [ Links ]
34. Rajnoch C, Chachques JC, Berrebi A, Bruneval P, Benoit MO, Carpentier A. Cellular therapy reverses myocardial dysfunction. J Thorac Cardiovasc Surg 2001;121:871-878. [ Links ]
35. Chachques JC, Duarte F, Cattadori B, Shafy A, Lila N, Chatellier G, Fabiani JN, Carpentier A. Angiogenic growth factors and/or cellular therapy for myocardial regeneration: a comparative study. J Thorac Cardiovasc Surg 2004,128:245-253. [ Links ]
36. Chachques JC, Herreros J, Trainini JC (eds): Regeneración Cardíaca. Editorial Magister Eos, Buenos Aires 2005: 1-205. [ Links ]
37. Chachques JC, Trainini MD, Lago N et al Myocardial assistance by grafting a new bioartificial upgraded myocardium (MAGNUM trial): clinical feasibility study. Ann Thorac Surg 2008;85:901-8. [ Links ]














