Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Insuficiencia cardíaca
versión On-line ISSN 1852-3862
Insuf. card. v.3 n.4 Ciudad Autónoma de Buenos Aires oct./dic. 2008
ARTÍCULO DE ACTUALIZACIÓN
Balón de contrapulsación intraaórtico
Aina Lauga*, Cecilia Perel** y Alfredo O. D'Ortencio***
* Jefa de Enfermería. Instituto Argentino de Diagnóstico y Tratamiento (IADT). Ciudad de Buenos Aires. Buenos Aires. República Argentina.
** Cardióloga universitaria. Especialista en hipertensión arterial. Instituto Médico de Alta Complejidad (IMAC). Ciudad de Buenos Aires. República Argentina.
*** Jefe de Cardiología y Director de la Unidad Docente Hospitalaria (UDH) del Instituto «Dr. Angel H. Roffo». Facultad de Medicina. Universidad de Buenos Aires (UBA). Coordinador del Dpto. de Insuficiencia Cardíaca y Trasplante Cardíaco del Sanatorio Güemes. Ciudad de Buenos Aires. República Argentina
Correspondencia: Lic. Aina Lauga.
Jefatura de Enfermería.
Instituto Argentino de Diagnóstico y Tratamiento.
Marcelo T. de Alvear 2346.
1122 - Buenos Aires, República Argentina.
E-mail: ainalau@yahoo.com.ar
Recibido: 03/09/2007
Aceptado:29/09/2008
Palabras clave: Shock cardiogénico; Infarto agudo de miocardio; Hemodinamia de la Insuficiencia Cardíaca
Introducción
La primera aplicación clínica del balón de contrapulsación intraaórtico (BCPIAO) fue hacia finales de 1960 y se ha convertido en el dispositivo de asistencia circulatoria más ampliamente utilizado hoy en día. Actualmente, esta modalidad de tratamiento es rutinaria en un amplio rango de pacientes que padecen enfermedades cardiovasculares graves, que van desde la estabilización hemodinámica en pacientes que sufren las complicaciones del infarto agudo de miocardio (IAM) o del shock cardiogénico, a pacientes de alto riesgo que serán sometidos a cirugía cardíaca o angioplastia, incluyendo aquellos que requieren su uso como puente al trasplante cardíaco1-3.
Si bien se han diseñado y puesto en funcionamiento otro tipo de dispositivos de asistencia mecánica cardíacos, el balón de contrapulsación sigue siendo el menos traumático, especialmente desde la evolución satisfactoria de los diseños de los catéteres-balón.
Ante la decisión de colocarlo, se deben conocer los principios fisiológicos básicos del sistema circulatorio, la hemodinamia de la insuficiencia cardíaca (IC) y el efecto de los medicamentos específicos cardiovasculares4,5.
De la misma manera, el personal de enfermería que, dentro del equipo de salud cumple uno de los roles más importantes en la atención del paciente, debe tener los conocimientos necesarios para el manejo de los valores hemodinámicos y poder relacionarlos con los signos y síntomas, que pasados por alto o mal interpretados, pueden provocar graves consecuencias para el enfermo.
Objetivo
Aunque, en esencia, la filosofía de los cuidados de enfermería en una Unidad de Cuidados Intensivos es idéntica a otras áreas de la disciplina, los cuidados a pacientes de alta dependencia presentan diferencias:
• Conocimientos específicos para dar respuesta rápida a situaciones de emergencia.
• Observación permanente de eventos que complican la evolución de los pacientes.
•Vigilancia continua y cuidadosa del funcionamiento cardíaco mediante monitorización.
• Aspectos tecnológicos del cuidado.
El objetivo de este artículo de revisión es actualizar y asegurar el conocimiento necesario para dar respuesta a los requerimientos que presentan los pacientes con balón de contrapulsación intraaórtico.
Fundamentos fisiológicos
Es esencial entender los beneficios fisiológicos que se producen con el uso del balón de contrapulsación, a partir de la comprensión de la anatomía y fisiología cardíaca normal.
El corazón se puede definir como un conjunto de dos bombas que trabajan en serie y que proveen la fuerza necesaria para impeler sangre venosa (carboxigenada) dentro del circuito pulmonar y sangre oxigenada hacia la circulación sistémica. El balón de contrapulsación es, generalmente, utilizado cuando el ventrículo izquierdo (VI) no puede cumplir satisfactoriamente su función de bombeo.
El trabajo del ventrículo derecho (VD) es mucho menor que el del VI, y la pared del primero tiene un grosor tres veces menor que la del segundo (el VD maneja volúmenes y el VI presiones).
Flujo sanguíneo
La aorta proximal y las grandes arterias, por su condición elástica, se adaptan al flujo sanguíneo que reciben durante la sístole. Esto permite que la mayor parte de la fuerza que recibe la sangre por la contracción ventricular, se conserve en forma de energía en la pared arterial elástica (momento de fuerza). Cuando el miocardio se relaja y la presión intravascular en los grandes vasos cae, estas paredes elásticas vuelven a su forma primaria manteniendo una línea de presión que permite que el flujo sanguíneo continúe llegando a los tejidos periféricos durante la diástole, alimentado por la energía almacenada anteriormente, que denominamos energía kinética.
Este efecto que se produce se conoce como el efecto Windkessel, y sirve para que el flujo sanguíneo dentro de la circulación se mantenga constante6-11.
Determinantes del gasto cardíaco
El gasto cardíaco (GC) resulta de multiplicar el volumen de sangre eyectado en cada latido por la frecuencia cardíaca (FC).
El volumen-latido (volumen sistólico) representa un promedio de 70 ml de sangre en el adulto. Por lo tanto, a una FC de 70 latidos por minuto (lpm), el corazón bombea o mantiene un GC de 4900 ml por minuto.
Este volumen-latido representa el funcionamiento cardíaco y depende de cuatro variables diferentes pero interdependientes: precarga, postcarga, contractilidad o capacidad inotrópica del corazón y frecuencia cardíaca.
Precarga
En el año 1884, Howell y Donaldson, enunciaron que el miocardio poseía un mecanismo intrínseco por el cual el volumen de sangre que eyectaba dependía del retorno venoso. Este concepto, conocido como precarga, sugería que la longitud de las fibras ventriculares antes de la contracción, causada por el volumen de fin de diástole, determinaba la fuerza de dicha contracción.
La capacidad del ventrículo intacto para variar su fuerza de contracción con cada latido, basado en la longitud inicial de la fibra miocárdica al fin de la diástole, constituye la ley de Frank-Starling (regulación heterométrica).
Cuando las fibras del miocardio están más dilatadas (al final de la diástole ventricular) porque hay un mayor volumen diastólico, producirán una mayor fuerza contráctil.
Pero este efecto disminuye cuando las fibras miocárdicas se estiran más allá de lo que se denomina "límite fisiológico", perdiéndose entonces esta regulación positiva sobre la fuerza de la contracción ventricular.
Como la presión intraventricular y la longitud la fibra miocárdica al fin de la diástole están normalmente relacionadas, en la práctica clínica se considera que la presión de fin de diástole del ventrículo izquierdo, la presión wedge (o de enclavamiento o capilar pulmonar) de la arteria pulmonar son representativas de la longitud de las fibras ventriculares al final de la diástole.
Postcarga
La resistencia a la eyección del VI se denomina postcarga.
Los mayores contribuyentes a la postcarga ventricular izquierda son: las resistencias vasculares periféricas y la impedancia de la aorta.
La presión de fin de diástole de la aorta representa la presión que el ventrículo debe vencer para abrir la válvula aórtica durante la contracción isovolumétrica. La presión de fin de diástole de la aorta es un punto importante en la contrapulsación intraaórtica, el objetivo es bajar esta presión de fin de diástole.
Aproximadamente el 90% del consumo miocárdico de oxígeno se produce en esta fase isovolumétrica sistólica, mientras el corazón trabaja contra la postcarga.
Contractilidad
La contractilidad es una propiedad intrínseca de la fibra miocárdica, refiriéndose a los cambios en la fuerza de la contracción del miocardio y es una función de la interacción entre los elementos contráctiles: los puentes de actina y miosina a nivel celular.
Por definición, la contractilidad se refiere a las variaciones que se producen en la fuerza de contracción independientemente de la longitud de la fibra miocárdica.
La contractilidad puede estar disminuida por hipoxemia o por drogas como el propranolol, quinidina, lidocaína o barbitúricos.
Frecuencia cardíaca
El aumento de la frecuencia produce escalonadamente un aumento en fuerza de contracción miocárdica, aumentando el volumen-latido hasta cierto punto. Este fenómeno se llama "efecto de la escalera o efecto Bowditch". Sin embargo, cuanto más elevada es la FC, menor es la duración de la diástole, disminuyendo por lo tanto el tiempo de llenado ventricular, consiguiéndose por lo tanto un menor volumen de fin de diástole, y disminuyendo la fuerza de contracción ventricular por presentar una regulación heterométrica negativa.
Uso miocárdico del oxígeno: aporte y demanda
Si el corazón es privado de oxígeno, aunque sea por pocos minutos, cesa su actividad mecánica. Los procesos metabólicos de la contracción son totalmente aeróbicos, el miocardio extrae entre el 75 y el 80% del oxígeno arterial que le proporciona el flujo coronario. Está comprobado que el balance entre la demanda y el aporte de oxígeno es muy importante, cuando el trabajo miocárdico aumenta, debe aumentar también el flujo coronario para poder mantenerlo.
Circulación coronaria
Los orificios de las arterias coronarias derecha e izquierda se ubican en los senos de Valsalva en la aorta, inmediatamente por encima de la válvula aórtica. Durante la diástole, la sangre entra en los senos, los distiende e ingresa así a las arterias coronarias derecha e izquierda.
La arteria coronaria derecha, que nace en la superficie anterior de la aorta, atraviesa en forma diagonal el lado derecho del corazón y desciende por el surco existente entre el ventrículo derecho y el izquierdo.
En el 80% de la población, la coronaria derecha da origen a la arteria descendente posterior y se dice en este caso que la coronaria derecha es dominante. En el restante 20% de la población la arteria descendente posterior se origina en la arteria circunfleja, rama de la arteria coronaria izquierda, esto se llama dominancia izquierda.
La arteria coronaria izquierda nace en la superficie posterior de la aorta y en el seno izquierdo de Valsalva y después de un corto trayecto se subdivide en dos ramas: la arteria descendente anterior y la arteria circunfleja.
Flujo sanguíneo coronario
La sangre fluye de las arterias coronarias principales y sus ramas por la superficie del corazón y entra al miocardio por ramas mucho más pequeñas.
El epicardio recibe sangre de las ramas que se abren en forma de ángulos rectos de las arterias coronarias principales. Otros vasos más pequeños, que también se originan en forma angular de las arterias coronarias derecha e izquierda, penetran en el miocardio y en el endocardio (arterias intramurales). El músculo cardíaco está recorrido por una red muy grande de capilares, pero la sangre se distribuye por éstos, no en forma continua, sino fásica con los ciclos de diástole y sístole de la contracción cardíaca.
Contrastando con los otros órganos, la perfusión a través de la arteria coronaria izquierda es mayor durante la diástole que durante la sístole. Esto se debe a que, al producirse la contracción cardíaca, produce un marcado aumento en la resistencia vascular coronaria, por aumento de la presión transmural del ventrículo izquierdo, produciendo una reducción importante del flujo sanguíneo a través de estos vasos. Durante la diástole, el miocardio se relaja, y ya no hay resistencia al flujo sanguíneo coronario.
Auto-regulación del flujo coronario
El flujo sanguíneo coronario se controla por medio de un proceso de auto-regulación que se regula por el balance entre la demanda y el aporte de oxígeno.
La hipoxia del miocardio es el estímulo más potente para aumentar el flujo sanguíneo coronario y el aporte de oxígeno por medio de la vasodilatación. De la misma manera cuando cae la demanda de oxígeno, se produce una reducción en el flujo coronario a través de la vasoconstricción.
Principios básicos del balón de contrapulsación intraaórtico
El uso del balón de contrapulsación permite un soporte hemodinámico y/o el control de la isquemia miocárdica antes y después de la cirugía de revascularización miocárdica.
A diferencia de la mayoría de los medicamentos inotrópicos, el balón da una asistencia fisiológica al miocardio claudicante, disminuyendo la demanda de oxígeno y mejorando la perfusión coronaria, fundamentalmente la de la coronaria izquierda.
Indicaciones para la colocación del balón de contrapulsación
Las principales indicaciones clínicas de la asistencia ventricular izquierda con balón de contrapulsación son12-20:
• Control de la angina inestable refractaria al tratamiento médico (betabloqueantes, nitritos, bloqueantes cálcicos, antiagregantes plaquetarios y heparina.), generalmente como puente hacia la angioplastia o la cirugía de revascularización miocárdica.
• Insuficiencia cardíaca isquémica, necrótica o postoperatoria (tensión arterial pulmonar mayor de 15 mm Hg y/o resistencias sistémicas altas) que no responde al tratamiento farmacológico convencional a dosis máximas.
• Taquicardia ventricular refractaria al tratamiento médico, en especial si se sospecha etiología isquémica.
• Miocarditis aguda con insuficiencia cardíaca.
• Como método de apoyo durante la angioplástia coronaria transluminal percutánea (ACTP) de alto riesgo (lesión del tronco, lesión "símil tronco", lesión de tres vasos, deterioro ventricular severo).
• Reperfusión del infarto agudo de miocardio cuando se administran trombolíticos. El efecto de la contrapulsación en estos casos es el de aumentar la permeabilidad de la lesión causal.
• Método de apoyo ventricular en valvuloplástias en ausencia de insuficiencia aórtica.
• Fallo del bombeo ventricular de etiología variada:
- Shock cardiogénico.
- Shock séptico.
- Síndrome de bajo gasto cardíaco.
- Traumatismo torácico.
- Infarto de miocardio intraoperatorio.
• Soporte cardíaco en pacientes quirúrgicos de alto riesgo, como en la intervención con circulación extracorpórea y en la retirada del by-pass cardiopulmonar.
• Mantenimiento de pacientes durante su transporte para que lleguen al centro de destino en las mejores condiciones hemodinámicas posibles.
Recientemente, se ha demostrado que el BCPIAO puede ser eficaz en pacientes que no cumplen estrictamente con los criterios anteriormente mencionados, ejemplo de ello es un síndrome coronario agudo, angina inestable o isquemia relacionada con arritmias ventriculares. La mejoría del cuadro isquémico, seguida del BCPIAO, relacionado con un aumento en el flujo sanguíneo coronario y una disminución en la demanda de oxígeno miocárdico. En general, los pacientes con angina inestable reciben apoyo del BCPIAO en la fase de deterioro hemodinámico y también los que cursan con angina previa a la revascularización14,21.
Contraindicaciones absolutas
- Insuficiencia valvular aórtica moderada o severa.
- Disección aórtica.
- Arterioesclerosis periférica y aórtica severa.
- Daño cerebral irreversible.
- Insuficiencia hepática grave (coagulopatías).
- Infecciones graves no controladas.
- Problemas quirúrgicos no resueltos.
- Endoprótesis colocada previamente.
- By-pass aorto-bifemoral (se debe optar por la colocación transtorácica).
- Obesidad extrema en la que la distancia entre la piel y la femoral excede los 5 cm.
El síndrome de bajo volumen minuto por IC izquierda perioperatoria se presenta en el destete de la circulación extracorpórea o en las primeras horas del postoperatorio del paciente y no puede ser resuelta luego de haberlo tratado con, por lo menos, dos inotrópicos combinados hasta la dosis considerada máxima y con los siguientes parámetros hemodinámicos:
-Tensión arterial media (TAM) < 80 mm Hg.
- Indice cardíaco < 1,8 L/m2.
- Presión capilar pulmonar (PCP) > 18 mm Hg.
- Resistencias sistémicas > 2100 dinas/seg/cm-5.
- Oliguria (< 1 ml/Kg peso/hora).
Dispositivo e inserción
El balón de contrapulsación intraaórtico es un balón distensible de látex o silicona no trombogénico, se presenta comercialmente en varios volúmenes para colocación en pacientes adultos (Figura 1 y 2):
7,5 Fr. volumen de 30 cc y diámetro de 13,9 mm.
7,5 Fr. volumen de 40 cc y diámetro de 15 mm.
9 Fr. volumen de 50 cc y diámetro de 16 mm.

Figura 2. Balón de contrapulsación intraaórtico desinflado e inflado.
Se coloca habitualmente en forma retrógrada en la aorta descendente, 3 centímetros por debajo de la arteria subclavia y por encima de las arterias renales.
El balón está montado sobre un catéter vascular que tiene múltiples aberturas. El gas inerte que se usa actualmente para insuflar el balón es el helio, el que es enviado desde la consola de control hacia el balón, saliendo por estos orificios y permitiendo el inflado (Figura 3, 4 y 5).
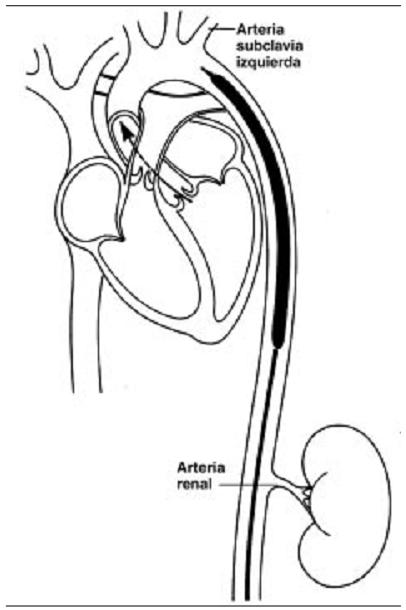
Figura 3. Ilustración esquemática del balón de contrapulsación intraaórtico posicionado en la aorta torácica descendente, justo debajo de la arteria subclavia izquierda, y sobre las arterias renales.

Figura 4. Ilustración que muestra al balón de contrapulsación intraaórtico inflado en diástole (A) y desinflado durante la sístole (B).

Figura 5. Ilustración que muestra al balón de contrapulsación intraaórtico al estar inflado compartamentaliza a la aorta. El compartimiento proximal incluye la raíz aórtica y los ostium coronarios.
El helio es un gas inerte, muy liviano, lo que minimiza el tiempo de transferencia y por lo tanto, aumenta la eficiencia del dispositivo.
Además, si el balón se rompe y el helio llega a la corriente sanguínea, tiene la propiedad de difundirse a través de los tejidos formando una cantidad mínima de burbujas, reduciendo el riesgo de embolia gaseosa.
La punta del catéter-balón es radio-opaca para visualizarse como un rectángulo opaco de 3 x 4 mm, paralelo a las paredes de la aorta descendente en la radiografía de tórax (Figura 6).
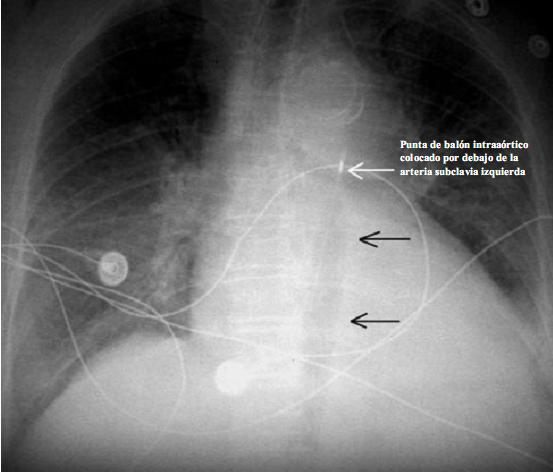
Figura 6. Radiografía de tórax frente donde se visualiza el balón de contrapulsación intraaórtico inflado.
El catéter se conecta a la consola de contrapulsación por medio de un prolongador, y por un sistema neumático, infla y desinfla el balón, llenándolo y vaciándolo de helio sincronizado con el ciclo cardíaco (Figura 7).

Figura 7. Miembro inferior con balón de contrapulsación.
El inflado del balón ocurre inmediatamente después del inicio de la diástole y el desinflado durante la contracción isométrica de la sístole. Por lo tanto la pulsación del balón es contraria fásicamente con el ciclo cardíaco del paciente.
El catéter-balón está conectado a una consola externa desde donde se maneja por medio de controles (Figura 8).

Figura 8. Equipo de monitoreo con balón de contrapulsación.
Esta consola externa desempeña tres funciones importantes:
- Tiene un circuito de detección de electrocardiograma y de curva de tensión arterial incorporado que permite la sincronización entre el balón y la actividad del corazón. Asimismo dentro de las opciones del electrocardiograma, está la detección de marcapasos, en caso que el paciente requiera de este dispositivo.
- Tiene controles neumáticos que activan el inflado y desinflado del balón, éste tiene que ser usado con la menor cantidad de gas que logre los efectos hemodinámicos deseados.
- Cuenta con alarmas y dispositivos de seguridad automáticos.
Actualmente, las consolas son pequeñas y cuentan con batería interna que permite el traslado del paciente con una autonomía de 4 a 6 horas.
La consola debe mantenerse en estado operativo, con su batería cargada, conectada a una fuente de energía, con el tanque de gas lleno y con el cable paciente y el cable transductor de presiones disponibles.
Se utilizan los transductores de presión descartables en la actualidad, que irán conectados directamente a la salida arterial del balón de contrapulsación.
La inserción del catéter-balón puede ser realizada por un cirujano o por un médico con experiencia en el procedimiento, ya que es invasivo y de alto riesgo. La asistencia la realiza un instrumentador y/o una enfermera que esté a cargo del paciente, si el procedimiento debe llevarse a cabo en la cabecera de la cama.
Si el paciente está consciente, se le debe explicar el procedimiento, el motivo del mismo, la necesidad de mantener la pierna sobre la que se trabajará extendida para evitar que el catéter se doble, también de mantener los miembros superiores inmóviles para no contaminar en caso de movimiento el campo quirúrgico y la sensación que tendrá, de una pulsación alternativa dentro de su tórax, lo que por lo general inquieta o asusta a los pacientes.
Si el paciente no está intubado y en asistencia respiratoria mecánica, es necesario que tenga una máscara de oxígeno, ya que posiblemente parte de los campos cubrirá su rostro, por lo que la enfermera periódicamente debe preguntarle como se siente e informarle sobre el desarrollo del procedimiento.
El chequeo del balón pre-inserción lo realiza el cirujano, mientras la enfermera coloca los 5 electrodos que tiene el cable paciente en los cuatro miembros del paciente y uno en posición indiferente.
Debe posicionar a la altura de la aurícula derecha el transductor de presiones con su lavado y realizar la calibración a "cero".
Es de suma importancia que la enfermera interviniente observe y registre cuáles son las características de miembros inferiores y superiores del lado de la inserción, antes del procedimiento.
En cuanto a temperatura, color y pulsos presentes, y características para obtener datos basales y detectar precozmente los cambios y complicaciones posteriores.
Es importante pedir un examen completo de coagulación para ser usado como control basal, especialmente, en cuanto al recuento plaquetario, ya que la acción mecánica del balón de contrapulsación tiende a producir plaquetopenia.
El catéter se inserta generalmente por la arteria femoral (es el acceso de elección en los pacientes sin vasculopatía periférica) y con menor frecuencia por la arteria axilar o en forma transtorácica (Figura 9).

Figura 9. Balón de contrapulsación colocado vía Seldinger.
La colocación del balón por vía axilar demanda la disección del surco deltopectoral con mayor incidencia de isquemia del miembro afectado y extracción por medio de la redisección axilar.
Durante la cirugía cardiovascular, y con la esternotomía realizada se puede colocar el balón en la aorta descendente por aortotomía. Este método puede ser usado cuando hay imposibilidad de usar el acceso femoral, pero requerirá una nueva cirugía torácica para su extracción.
La inserción arterial se puede realizar percutáneamente, usando la técnica de Seldinger o por medio de una arteriotomía22.
El lavado para la línea arterial se prepara con una solución de Ringer lactato o solución fisiológica de 500 cc con el agregado de 1250 unidades de heparina sódica y se lo mantiene presurizado a 300 mm Hg para mantener un flujo continuo de lavado de aproximadamente 4 ml/hora.
Una vez fijado el balón en posición por medio de suturas e iniciada la contrapulsación, se debe realizar una radiografía de tórax para determinar la posición del mismo, en caso que no sea el adecuado se debe reposicionar repitiendo el control radiográfico.
El uso del balón de contrapulsación como apoyo ventricular derecho es controvertido, poco común, en estos casos se lo coloca en el tronco de la arteria pulmonar y se lo opera con los mismos principios que rigen la contrapulsación aórtica.
Efectos hemodinámicos del balón de contrapulsación intraaórtico
El balón de contrapulsación actúa como una bomba auxiliar del corazón, pero para ello necesita que el ventrículo izquierdo del paciente mantenga una actividad significativa. Cuando el balón se infla, aumenta la presión diastólica y esto contribuye a mejorar el flujo sanguíneo coronario cerebral y sistémico. El desinflado pre-sistólico disminuye la resistencia a la eyección sistólica del VI con lo que el trabajo miocárdico y la demanda de oxígeno del mismo se reducen.
El aumento en el GC es de aproximadamente 1 litro por minuto, lo que beneficia al paciente.
¿Cómo se contrapulsa un paciente?
El dispositivo debe funcionar según el ciclo cardíaco. Kantrowitz expresó que "la eficacia hemodinámica de la contrapulsación depende totalmente de la sincronización del inflado y desinflado del mismo en relación con los diferentes eventos del ciclo cardíaco".
Por lo general se utiliza la señal del electrocardiograma del paciente para disparar el inflado o desinflado, caso contrario se puede utilizar la curva de presión arterial, o un ritmo de marcapasos. Básicamente hay que entender que el inflado se realiza durante la diástole y el desinflado durante la sístole, (inflándose en la cúspide de la onda T y desinflándose al comienzo del complejo QRS).
La contrapulsación se inicia disparada por el complejo QRS, el balón inmediatamente se desinfla en el momento de la sístole, con lo que se produce una remoción física de 30 a 40 cc de volumen en el interior de la aorta.
Esta rápida disminución en el volumen aórtico hace que la presión aórtica caiga justo antes del inicio de la eyección del ventrículo izquierdo, o sea que éste al expeler la sangre lo hará contra una carga o presión menor, con lo que su trabajo disminuye.
Tan pronto como la válvula aórtica se cierra, el volumen que se había retirado durante la sístole por desinflado del balón, se repone por inflado en la diástole. Este volumen aórtico ahora expandido en 30 o 40 cc, aumenta la presión aórtica y por lo tanto mejorará el flujo y la perfusión coronaria.
La presión diastólica aumentada en la aorta no afecta al ventrículo izquierdo porque la válvula aórtica está cerrada durante la diástole y eso protege al ventrículo de lo que sucede retrógradamente a dicha válvula.
Otra de las ventajas es que también se incrementa el flujo sanguíneo y la perfusión de otros órganos.
Básicamente al desinflar el balón dentro de la aorta se produce un efecto similar al vacío reduciendo la resistencia vascular y mejorando la propulsión de la sangre a través de la aorta.
Es como si se produjera un espacio virtual en el lugar que ocupa el balón dentro de la aorta, generando casi una presión negativa en ese sector.
Como en todo sistema hemodinámico con diferencia de presiones a lo largo de su trayecto, las pérdidas de presión en algún punto del circuito tienden a ser compensadas rápidamente a partir de los lugares de más presión.
Por lo tanto, el momento inicial del desinflado debe coincidir con el final de la fase de contracción isovolumétrica ventricular y antes de la contracción isotónica, ya que se aprovecha este efecto de vacío para convertir al ventrículo izquierdo en el sector de mayor presión, modificando en consecuencia sus condiciones de trabajo.
El trabajo mecánico que realiza el balón de contrapulsación se traduce en un efecto metabólico importante.
La disminución en el consumo de oxígeno, se debe a la disminución de la tensión parietal y de la frecuencia cardíaca por el exceso de catecolaminas circulantes que hay en los casos de bajo volumen minuto.
La disminución de la frecuencia cardíaca se debe a que al mejorar el estado hemodinámico se reduce la cantidad de catecolaminas y esto afecta favorablemente al inotropismo cardíaco.
La segunda etapa de la contrapulsación ocurre después del cierre de la válvula aórtica y es el inflado del balón, esto produce una onda de presión durante la diástole que genera un aumento de la presión diastólica media y un desplazamiento de sangre de 30 a 40 ml del lugar que ocupará el balón al inflarse.
Al comienzo de la asistencia con el balón de contrapulsación se nota un aumento del volumen minuto y del índice cardíaco en un rango que varía entre un 20% y un 40%, y que está en relación directa a la patología a tratar.
Esto se observa mientras el miocardio está insuficiente y se nota que desaparece con la mejoría del mismo, al caso que se llega a tener un mejor índice cardíaco cuando se suspende la asistencia.
La contrapulsación por aumento de la presión diastólica, redistribuye el flujo coronario a favor de las áreas isquémicas y aumenta el flujo coronario por las colaterales existentes, pero no funcionales.
Si las colaterales son pequeñas o no se han desarrollado, el balón no tiene efecto sobre el flujo coronario distal a una obstrucción severa, pero que en presencia de obstrucciones menores o con colaterales bien desarrolladas se puede observar un aumento de la presión diastólica post-obstrucción.
Los efectos del balón de contrapulsación se pueden observar en la onda de presión arterial del paciente con una inversión en la curva de las presiones23.
Definición de sincronización de un balón de contrapulsación
La sincronización consiste en la regulación automática o manual de los puntos de inflado y desinflado referidos a la sístole y a la diástole.
La consola de controles está diseñada para que un operador programe manualmente los puntos de inflado y desinflado en forma específica.
Tanto el médico como la enfermera a cargo, deben entender perfectamente la morfología de la onda de presión arterial y sus puntos clave para determinar si el balón está sincronizado con el latido cardíaco y, por lo tanto, está cumpliendo su función.
La consola del BCPIAO requiere de una señal de disparo o "trigger" que le indique cual es la sístole y cuál es la diástole.
La señal de disparo más frecuentemente usada es la onda R del electrocardiograma del paciente.
La señal del electrocardiograma se puede obtener directamente a través de un cable paciente o desde un monitor. Es importante que esta señal de electrocardiograma sea una señal monofásica y limpia sin artefactos que pueda ser reconocida fácilmente por dispositivo.
Si la señal del electrocardiograma no es clara o como en el caso del quirófano en el que es interferida por el electrocauterio, se puede reemplazar por la señal de la onda arterial del paciente.
Pero para poder sincronizar correctamente al balón de contrapulsación, debemos hacerlo en relación a la onda de presión arterial.
Esto sería que, el inflado del balón de contrapulsación se realice al inicio de la diástole o sea inmediatamente después del cierre de la válvula aórtica, que se manifiesta en la onda de presión arterial en la cisura dícrota.
El desinflado del balón se debería producir durante la contracción isovolumétrica, es decir, inmediatamente antes de la aparición de la sístole arterial.
Inflado del balón durante la diástole
El inflado rápido del balón de contrapulsación con helio (unos 40 cc aproximadamente en adultos) se debe producir justo en el momento del cierre de la válvula aórtica; esto eleva la presión diastólica en lo que se llama "presión diastólica aumentada".
Esto debería ocurrir en un momento muy preciso y por lo tanto se sincroniza el balón de contrapulsación con la cisura dícrota.
Idealmente la onda de presión debería tomarse en la raíz aórtica donde esta cisura indica el cierre exacto de la válvula aórtica.
Pero como en las unidades de cuidados intensivos la presión en esta parte de la aorta no puede monitorearse, debemos considerar que hay un pequeño retraso por la distancia a recorrer entre la raíz aórtica y las arterias periféricas donde por lo general se insertan los catéteres arteriales24 (Figura 10).

Figura 10. Curvas de presión con la inserción del balón de contrapulsación intraaórtico.
Complicaciones en el uso del balón de contrapulsación
Las complicaciones se pueden producir durante la colocación del catéter-balón, la contrapulsación o el retiro del mismo25.
Debemos también nombrar las complicaciones mecánicas más frecuentes y que afectan directamente la funcionalidad del equipo.
1) Marcapasos auricular: cuando el paciente tiene un marcapasos auricular, la espiga de éste es interpretada por el equipo como un complejo QRS y activa el mecanismo en un momento que no es el indicado. La solución es colocar un marcapasos bipolar o ajustar el disparo de la consola a la modalidad marcapasos.
2) Taquicardia: por lo general la efectividad del balón cesa con frecuencias cardíacas por encima de 120 latidos por minuto, ya que el dispositivo no puede inflarse y desinflarse tan rápidamente. La solución es: tratar de disminuir la frecuencia cardíaca del paciente o programar la modalidad del balón en 2:1 en vez de 1:1.
En la modalidad 1:1 el balón contrapulsa cada latido cardíaco, en la modalidad 2:1 contrapulsa ciclo por medio.
3) Disminución del volumen del gas del balón detectado por la consola y sus monitores de alarma. Puede haber una fuga de gas ya sea por desajuste de las conexiones o por rotura del balón.
Inicialmente verificamos la presencia de sangre en las tubuladuras de polivinilo del balón que es la señal inequívoca y cierta de la rotura del balón dentro de la aorta, esto implica detener el mismo y llamar con suma urgencia a cirugía para su retiro, ya que su presencia inerte no sólo no aporta ningún beneficio, sino que es altamente trombogénica.
Si la alarma proviene de una desconexión accidental, se reconecta y se pulsa autofilling para el nuevo llenado del balón con gas y se reiniciará el ciclo.
Complicaciones vasculares
Las complicaciones más severas como disección aórtica, o ruptura de la arteria femoral o aorta, son afortunadamente poco comunes. El pronóstico generalmente es fatal, más en el segundo caso que en el primero.
Algunas de las alteraciones vasculares no se verán directamente durante la internación del paciente sino después de su alta; se han documentado tres categorías de insuficiencia vascular: presencia de calambres, entumecimiento y sensación de hormigueo y claudicación intermitente.
Todos estos síntomas son descriptos por los pacientes que además refieren presencia de edemas en la pantorrilla, dolor difuso pero continuo en los miembros inferiores, calambres nocturnos, temperatura disminuida en los miembros inferiores, e inclusive celulitis en la pierna donde estuvo emplazado el balón de contrapulsación. Funk ha descrito también gangrena yúlceras isquémicas que pueden aparecer dos o tres semanas después de la colocación del dispositivo.
Dentro de las alteraciones vasculares que se ven a muy corto plazo:
Pérdida de pulsos
Este signo aparece entre el 20% y el 25% de los pacientes.
Debemos considerar que el pulso promedio está normalmente ausente al tacto en más del 40% de los pacientes, pero si el pulso estaba presente antes del procedimiento y desaparece después de él es una señal a considerar.
Hay que realizar una evaluación exhaustiva de la temperatura y el color de los miembros inferiores, si bien pueden estar fríos e hipoperfundidos inmediatamente después de la cirugía por la hipotermia, por la medicación vasoactiva y por el bajo gasto cardíaco, con la colocación del balón de contrapulsación estas condiciones deberán mejorar.
En ocasiones después de la inserción del balón de contrapulsación, el pulso y la temperatura del miembro afectado, disminuyen al principio, para luego mejorar, esto se debe al espasmo de la arteria como consecuencia del trauma y manipulación durante la inserción.
Se puede evaluar mediante Doppler (en algunos balones de contrapulsación, se dispone del mismo), la existencia de flujo. Es muy posible que estos síntomas se presenten con mayor frecuencia en aquellos pacientes en los que la inserción del balón de contrapulsación ha sido dificultosa.
Si estas medidas no mejoran la perfusión del miembro, el balón deberá ser retirado y si es necesario, reinsertado desde otra posición.
Isquemia
Como se deduce del tema anterior, la isquemia de los miembros inferiores es la complicación más frecuente, pero no podemos descartar otros tipos de isquemia que se pueden producir.
El paciente puede indicar, si está consciente, dolor en el miembro afectado, parestesias y disminución de la función motora, mientras podemos constatar que la temperatura disminuye y la perfusión del miembro empeora con la aparición de cianosis.
Obviamente, el tratamiento es el retiro del balón de contrapulsación en forma urgente.
Pero en ocasiones, por desplazamiento del BCPIAO la isquemia se puede detectar por otros signos y síntomas:
Si el balón se desplaza cefálicamente puede obstruir el nacimiento de las arterias carótidas con compromiso cerebral (disminución del nivel de conciencia con evolución hacia el coma, convulsiones, signos neurológicos focales).
Si el balón se desplaza obstruyendo la arteria subclavia, especialmente la izquierda, veremos los signos antes descriptos en los miembros inferiores, en el brazo afectado.
Si el balón se desplaza caudalmente puede ocluir el nacimiento de las arterias renales, lo que se manifestará con una oligoanuria e hiperkalemia, urea y creatinina sérica. Obviamente la primera señal de peligro es la disminución de la excreción urinaria que usualmente había mejorado después de la inserción del balón de contrapulsación.
La posición descendida del balón de contrapulsación puede ocluir las arterias mesentéricas, provocando una isquemia e infarto mesentérico de muy mal pronóstico o inclusive unos días después, puede aparecer una colecistitis no litiásica que requiere una intervención quirúrgica abdominal.
Los signos y síntomas que se pueden observar son: disminución de los ruidos hidroaéreos, abdomen distendido, leucocitosis y con defensa al tacto, diarrea.
Es de rutina, el control de la radiografía de tórax, para determinar si hay un desplazamiento del balón especialmente si se detectan los cambios antes mencionados en el estado del paciente.
Tromboembolismo
La inserción del balón de contrapulsación, especialmente la percutánea, representa una injuria vascular importante. Las placas ateroscleróticas pueden ser fisuradas e incluso desalojadas durante una inserción dificultosa.
El tromboembolismo puede ser localizado o múltiple. Puede producir accidentes cerebrovasculares, oclusión de las arterias renales, tromboembolismo pulmonar, infarto mesentérico, infarto esplénico, hemianopsia, émbolos periféricos y en contadas ocasiones isquemia medular y paraplejía por oclusión del flujo por las arterias vertebrales.
La anticoagulación terapéutica con heparina para mantener un tiempo de protrombina en 1,5 a 2 veces su valor normal puede prevenir este tipo de fenómenos embólicos, sin embargo puede predisponer al paciente a incrementar sus posibilidades de sangrado.
Síndrome compartimental
El denominado síndrome compartimental es un tipo de isquemia periférica. En los miembros inferiores, los huesos, músculos, tejido nervioso y vasos sanguíneos están rodeados por una membrana fibrosa denominada fascia. Esto hace que las estructuras anatómicas, antes mencionadas, parecieran estar en compartimientos.
El síndrome compartimental se define como la condición en la que el incremento de presión reduce el flujo capilar comprometiendo los tejidos que se encuentran dentro de la fascia que recubre los tejidos, pues se produce en un espacio no distensible o cerrado.
Los pacientes que necesitan un balón de contrapulsación tienen un riesgo muy alto de padecer este tipo de patología, por la inmovilización prolongada, la pérdida del flujo sanguíneo capilar, enfermedad vascular periférica pre-existente, uso de drogas vasoactivas y trombosis.
En el paciente consciente, el síndrome compartimental se diagnostica a través de signos y síntomas como el dolor en la pantorrilla (especialmente en la dorsiflexión del pie) y pérdida de la función sensitiva o motora del miembro. El paciente puede referir dolor en el miembro afectado, incluso hasta anestesia de dicha región.
En el síndrome compartimental, la presión que se produce, puede causar lesiones a los nervios y músculos, pero no la oclusión arterial o la pérdida de los pulsos periféricos. Esto diferencia al síndrome compartimental de la isquemia.
Pero como muchos pacientes que requieren el uso de balón de contrapulsación están ventilados mecánicamente y son sedados, el diagnóstico de síndrome compartimental es dificultoso. El nivel de la creatinin-fosfoquinasa (CPK) es usado a menudo como un índice de la isquemia muscular, y en el síndrome compartimental los niveles de CPK pueden oscilar entre 1000 a 5000 unidades internacionales.
La isquemia muscular de 4 horas de duración produce una mioglobinuria importante, alcanzando su máximo en las tres horas subsiguientes a la restauración del flujo sanguíneo. La mioglobinuria se produce por la filtración y excreción de la mioglobina procedente de las células musculares dañadas y puede persistir hasta 12 horas después.
Una vez que se ha diagnosticado el síndrome compartimental, se debe realizar una fasciotomía para disminuir la presión. Las complicaciones del síndrome compartimental, por sí solo, incluyen hiperestesia permanente, debilidad motora, infección ósea y de tejidos blandos, insuficiencia renal y amputación.
Es importante entonces que la enfermera valore los miembros inferiores del paciente para detectar cualquier alteración, especialmente cuando no hay cambios en los pulsos del paciente.
Disección aórtica
La disección de la aorta, a consecuencia de la inserción del catéter-balón, es una de las complicaciones más serias, y puede causar la muerte del paciente. En ocasiones este proceso se reconoce solamente en el momento en que el balón intraaórtico se retira, ya que se produce la progresión del daño de la íntima con aparición del falso lumen, inestabilidad hemodinámica y muy mal pronóstico en la mayoría de los casos.
Los síntomas incluyen dolor dorsal y/o abdominal, caída abrupta del hematocrito y/o ensanchamiento mediastinal. En muchos casos, esto se produce durante la remoción del catéter-balón, por lo que la enfermera debe estar muy atenta a la situación clínica del paciente después de este procedimiento.
Daño vascular local
Otra de las complicaciones posibles es la formación de un falso aneurisma en la zona de inserción, aparición de hematoma, linfedema, formación de una fístula linfática, laceración de la arteria femoral, ilíaca o aorta.
Esto requerirá la reparación de la arteriotomía, un by-pass fémoro-femoral, evacuación del hematoma, endarterectomía del vaso, angioplastia u otros procedimientos quirúrgicos para la reparación de este tipo de secuelas.
Se puede identificar un falso aneurisma de la arteria femoral por la presencia de un hematoma acompañado de una masa pulsátil en la zona femoral. Si se sospecha que hay una fístula arteriovenosa infectada, es necesario obtener un cultivo de la zona antes de la cirugía reconstructiva vascular.
Alteraciones hematológicas
La heparina y los antiagregantes plaquetarios están indicados en todos los pacientes que reciben asistencia con BCPIAO para evitar los accidentes tromboembólicos. Los trombos se pueden desarrollar en los pliegues del balón desinflado, motivo por el cual nunca debe dejarse instalado un balón sin funcionar.
Trombocitopenia. Es raro que la trombocitopenia alcance valores clínicamente significativos. Cerca de la mitad de los pacientes presenta una disminución del recuento plaquetario del 50%, en un periodo de cinco a siete días de asistencia con BCPIAO.
Posiblemente, el paciente requiera transfusiones de glóbulos rojos sedimentados y concentrados plaquetarios, especialmente si hay que realizar algún tipo de procedimiento invasivo.
Ruptura y/o atrapamiento intraaórtico del balón de contrapulsación
Se ha documentado el uso del balón de contrapulsación en un paciente durante 327 días, mientras éste esperaba un trasplante cardíaco. Evidentemente, ha sido un caso aislado, pero es muy poco frecuente que el dispositivo sufra una ruptura. Cuando esto ocurre se detecta inmediatamente ya que aparece sangre en la tubuladura que une el balón interno con el externo, y implicando el inmediato retiro del dispositivo, y si es necesario, su reemplazo por otro.
La causa que se supone produce este fenómeno es la perforación, debida al roce continuo del dispositivo con una placa ateromatosa calcificada.
Los riesgos de la ruptura es la embolia gaseosa causada por el helio. Si bien en la mayoría de los casos, la pérdida de pequeñas cantidades de helio en la corriente sanguínea del paciente es bien tolerada, puede tener consecuencias fatales y la única manera de contrarrestarla es colocar al paciente en una cámara hiperbárica, que desafortunadamente no existe en la mayoría de las instituciones.
El atrapamiento del balón de contrapulsación dentro de la aorta se produce generalmente cuando la fisura que se produce en el mismo es muy pequeña, pero permite la entrada de sangre que se coagula en su interior, lo que hace sumamente riesgoso su retiro por la vía de inserción por lo que requiere un procedimiento quirúrgico de muy alto riesgo.
Infección
El proceso infeccioso se puede producir en el sitio de la inserción, lo que requerirá drenaje, debridamiento y limpieza del foco y en el caso de haberse realizado una arteriotomía, remoción del injerto. Si esto no se realiza o el tratamiento no es el adecuado puede llevar a la ruptura de la arteria, formación de un falso aneurisma y bacteriemia.
Conclusión
El BCPIAO ha sido ampliamente establecido como un soporte mecánico26,27 de gran valor para la asistencia ventricular transitoria en el tratamiento de la falla cardíaca, la reducción significativa de la postcarga, y la mejoría en el aporte del flujo coronario a través del aumento en la presión diastólica. El BCPIAO también permite una redistribución del flujo coronario hacia los territorio de isquemia miocárdica.
Diversos estudios han demostrado que el BCPIAO reduce la isquemia miocárdica perioperatoria y que mejora el resultado de la cirugía cardíaca en los pacientes de alto riesgo. El EuroSCORE, además de determinar el riesgo pre-operatorio en pacientes que serán sometidos a cirugía cardíaca, también permite predecir la mortalidad28.
Los pacientes de alto riesgo y sin BCPIAO preoperatorio requerirán, en un 19% de los casos, la colocación del mismo intra o post-operatorio por presentar bajo volumen minuto. Los pacientes que más se beneficiarían del balón preoperatorio son aquellos de alto riesgo, pero que no sean sometidos a cirugías de urgencia, debido a que en ellos la mortalidad intrahospitalaria no puede ser reducida29-35.
1. Ryan TJ, Antman EM, Gibbons RJ. 1999 update: ACC/AHA Guidelines for the management of patients with acute myocardial infarction. Circulation 1999;100:1016-1030. [ Links ]
2. Holman WL, Li Q, Kiefe CI, McGiffin DC, Peterson ED, Allman RM, Nielsen VG, Pacifico AD. Prophylactic value of preincision intra-aortic balloon pump: analysis of a statewide experience. J Thorac Cardiovasc Surg 2000;120:1112-1119. [ Links ]
3. Gutfinger DE, Ott RA, Miller M, et al. Aggressive preoperative use of intraaortic balloon pump in elderly patients undergoing coronary artery bypass grafting. Ann Thorac Surg 1999;67:610-3. [ Links ]
4. Trost JC, Hillis LD. Intra-aortic balloon counterpulsation. Am J Cardiol 2006;97:1391-398. [ Links ]
5. Boehmer JP, Popjes E. Cardiac failure: mechanical support strategies. Crit Care Med 2006;34:S268-S277. [ Links ]
6. Hales S. Statistical Essays. II. Haemostatics, 1733. London: Innays and Manby; 1733, reprinted by Haffner, New York. [ Links ]
7. Frank O. Die grundform des arteriellen pulses. Erste Abhandlung. Mathematische Analyse Z Biol 1899;37:483-526. [ Links ]
8. Young T. Hydraulic investigations, subservient to an intended Croonian lecture on the motion of the blood. Phil Trans Roy Soc. London 1808;98:164-86. [ Links ]
9. Moens AI. Die Pulkswive. The Netherlands: Brill, Leiden; 1878. [ Links ]
10. Korteweg DJ. Ueber die fortpflanzunggesgeschwingdigkeit des schalles in elastischen rohren. Ann Physik Chemie 1878;5:525-42. [ Links ]
11. Boltzmann L. Zur theorie der elastischen Nachwickung. Ann Phys 1876; Suppl 7:624-54. [ Links ]
12. Maccioli GA, Lucas WJ, Norfleet EA. The intra-aortic balloon pump: a review. J Cardiothorac Anesth 1988;2:365-373. [ Links ]
13. Christenson JT, Schmuziger M, Simonet F. Effective surgical management of high-risk coronary patients using preoperative intra-aortic balloon counterpulsation therapy. Cardiovasc Surg 2001;9:383-390. [ Links ]
14. Arafa OE, Pedersen TH, Svennevig JL. Intraaortic balloon pump in open heart operations:10 year follow-up with risk analysis. Ann Thorac Surg 1998;65:741-747. [ Links ]
15. Dietl CA, Berkheimer MD, Woods EL. Efficacy and cost- effectiveness of preoperative IABP in patients with ejection fraction of 0.25 or less. Ann Thorac Surg 1996;62:401-409. [ Links ]
16. Torchiana DF, Hirsch G, Buckley MJ. Intraaortic balloon pumping for cardiac support; trends in practice and outcome 1968 to 1995. J Thorac Cardiovasc Surg 1997;113:758-769. [ Links ]
17. Rosenbaum AM, Murali S, Uretsky BF. Intraaortic balloon counterpulsation as a bridge to cardiac transplantation. Chest 1994;106:1683-1688. [ Links ]
18. Brodie BR, Stuckey TD, Hansen C, Muncy D. Intra-aortic balloon counterpulsation before primary percutaneous transluminal coronary angioplasty reduces catheterization laboratory events in high-risk patients with acute myocardial infarction. Am J Cardiol 1999;84:18-23. [ Links ]
19. Aguirre FU, Kern MJ, Bach R. Intraaortic balloon pump support during high-risk coronary angioplasty. Cardiology 1994;84:175-186. [ Links ]
20. Barry WL, Sarembock IJ. Cardiogenic shock: Therapy and prevention. Clin Cardiol 1998;21:72-80. [ Links ]
21. Schmid C, Wilhelm M, Reimann A, Rotker J, Deiwick M, Loick M, Kerber S, Hammel D, Weyand M, Scheld HH. Use of an intraaortic balloon pump in patients with impaired left ventricular function. Scand Cardiovasc J 1999;33:194-198. [ Links ]
22. Gutfinger DE, Ott RA, Miller M, et al. Aggressive preoperative use of intraaortic balloon pump in elderly patients undergoing coronary artery bypass grafting. Ann Thorac Surg 1999;67:610-3. [ Links ]
23. Bolooki H, Williams W, Thurer RJ, et al. Clinical and hemodynamic criteria for use of the intra aortic balloon pump in patients requiring cardiac surgery. J Thorac Cardiovasc Surg 1976;72:756-68. [ Links ]
24. Barnet MG, Swartz MT, Peterson GJ. Vascular complications from intraaortic balloons. Risk analysis. J Vasc Surg 1994;19:81-89. [ Links ]
25. Richenbacher WE. Mechanical circulatory support. Austin, Texas. Ed. Landes Bioscience.1999. [ Links ]
26. Kaplan JA, Reich DL, Konstadt SN. Cardiac Anesthesia, Fourth Edition. Philadelphia, Pennsylvania. W.B. Saunders Company 1999:1193-1212. [ Links ]
27. Claudius Diez, Rolf-Edgar Silber, Michael Wächner, Markus Stiller, Hans-Stefan Hofmann. EuroSCORE directed intraaortic balloon pump placement in high-risk patients undergoing cardiac surgery - retrospective analysis of 267 patients. Interactive CardioVascular and Thoracic Surgery 2008;7:389-397. [ Links ]
28. Michel P, Roques F, Nashef SA. Logistic or additive EuroSCORE for high risk patients? Eur J Cardiothorac Surg 2003;23:684-687; discussion 687. [ Links ]
29. Nashef SA, Roques F, Hammill BG, Peterson ED, Michel P, Grover FL, Wyse RK, Ferguson TB. Validation of European System for Cardiac Operative Risk Evaluation (EuroSCORE) in North American cardiac surgery. Eur J Cardiothorac Surg 2002;22:101-105. [ Links ]
30. Gogbashian A, Sedrakyan A, Treasure T. EuroSCORE: a systematic review of international performance. Eur J Cardiothorac Surg 2004;25:695-700. [ Links ]
31. Bolooki H, Williams W, Thurer RJ, et al. Clinical and hemodynamic criteria for use of the intra aortic balloon pump in patients requiring cardiac surgery. J Thorac Cardiovasc Surg 1976;72:756-68. [ Links ]
32. Mundth ED. Preoperative intra aortic balloon pump assistance. Ann Thorac Surg 1976;22:603-4. [ Links ]
33. Christenson JT, Badel P, Simonet F, et al. Preoperative intraaortic balloon pump enhances cardiac performance and improves the outcome of redo CABG. Ann Thorac Surg 1997;64:1237-44. [ Links ]
34. Christenson JT, Licker M, Kalangos A. The role of intraaórtica counterpulsation in high risk OPCAB surgery: a prospective randomized study. J Card Surg 2003;18:286-94. [ Links ]
35. Stone GW, Ohman M, Miller MF, Joseph DL, Christenson JT, Cohen M, Urban PM, et al. Contemporary Utilization and Outcomes of Intra-Aortic Balloon Counterpulsation in Acute Myocardial Infarction. The Benchmark RegistryJ Am Coll Cardiol 2003;41:1940-5. [ Links ]















