Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Insuficiencia cardíaca
versión On-line ISSN 1852-3862
Insuf. card. v.4 n.4 Ciudad Autónoma de Buenos Aires oct./dic. 2009
ARTÍCULO DE OPINIÓN
Insuficiencia cardíaca y respuesta inflamatoria sistémica
Alfredo Navigante* y Alfredo D’Ortencio**
* Médico clínico oncólogo. Unidad de Investigación de Transferencia. Instituto de Oncología "Angel H. Roffo". Facultad de Medicina. Universidad de Buenos Aires. UBA. Ciudad de Buenos Aires. República Argentina.
** Médico cardiólogo. Jefe de Cardiología. Instituto de Oncología "Angel H. Roffo". Ciudad de Buenos Aires. República Argentina. Director de la Unidad Docente Hospitalaria. Facultad de Medicina. Universidad de Buenos Aires. UBA. Ciudad de Buenos Aires. República Argentina.
Correspondencia: Dr. Alfredo D’Ortencio
Servicio de Cardiología. Instituto de Oncología "Angel H. Roffo".
Av. San Martín 5481. CP: 1417. Ciudad de Buenos Aires. República Argentina.
E-mail: adortencio@intramed.net
Recibido: 10/08/2009
Aceptado: 20/10/2009
Palabras clave: Insuficiencia cardíaca; Respuesta inflamatoria sistémica; Síndrome inmuno-metabólico sistémico
Introducción
La insuficiencia cardíaca (IC), verdadero y creciente problema en la Salud Pública, no sólo es el resultante de sobrecarga y/o injuria cardíaca; sino también, de una compleja interrelación de cambios genéticos, neurohormonales, inflamatorios y bioquímicos que actúan sobre el miocito y el intersticio1.
Los biomarcadores que se encuentran en creciente estudio y evaluación, son expresión de estos procesos.
Un biomarcador para tener interés de uso clínico debe reunir tres criterios a saber:
a- Tener costo y tiempo de realización razonables.
b- Aportar información aún no disponible para la evaluación clínica.
c- Debe servir para tomar decisión médica.
Los biomarcadores de inflamación en IC son:
a- Proteína C reactiva (PCR).
b- Factor de necrosis tumoral alfa (FNT alfa).
c- Fas (APO-1).
d- Interleukinas (IL 1,6 y 18).
Los efectos deletéreos de los biomarcadores de inflamación en la IC son:
a- Conocidos: disfunción del ventrículo izquierdo (VI), edema pulmonar, cardiomiopatía, isquemia del músculo esquelético, disfunción endotelial, anorexia y caquexia.
b- Potenciales: desacople del receptor de la adenil-ciclasa, activación del programa de genes fetales y apoptosis de cardiomiocitos.
Al ser la inflamación un factor patogénico importante en la progresión de muchas formas de IC, el interés del estudio de sus mediadores comienza en 1954 con el dosaje de PCR, en 19562 se encuentra presente en 30 de 40 pacientes con IC, siendo mayores sus niveles en los casos severos.
La PCR es un reactante de fase aguda producida por el hepatocito en respuesta a una citoquina proinflamatoria la IL 6.
En 1990, Levine3 describió además niveles elevados de factor de necrosis tisular alfa en pacientes con IC.
El FNT alfa y por lo menos 3 interleukinas (IL1,6 y 18) son consideradas citoquinas proinflamatorias y son producidas por las células nucleadas del corazón.
En esa misma década, se comienza a hablar de síndrome de respuesta inflamatoria sistémica (SRIS).
Síndrome de respuesta inflamatoria sistémica
La respuesta inflamatoria sistémica (RIS) es considerada en la actualidad como una de las piezas fundamentales en los mecanismos fisiopatológicos de mantenimiento de una serie de condiciones mórbidas. En la década del noventa, comenzó a hablarse de síndrome de RIS cuando este cuadro se presenta en pacientes críticos con disfunción hepática, politraumatismo o nutrición parenteral total.
En el nuevo milenio, merced a la adquisición de nuevos conocimientos sobre mecanismos a nivel molecular, algunos autores lo denominan síndrome inmuno-metabólico sistémico (SIMS)4-6.
Importa reconocer el rol central de las citoquinas proinflamatorias en esta entidad, ya que en base a ello y no al cuadro o a la entidad clínica "per se" podemos considerar SIMS agudo cuando existe la denominada "tormenta de citokinas" como en el caso de la sepsis, entidad paradigmática, así como en las leucemias agudas, en el 12% del subgrupo de pacientes con pancreatitis aguda, en la mayoría de los pacientes con síndrome de distress respiratorio del adulto (SDRA) y en la púrpura trombocitopénica trombótica, también conocida como síndrome urémico-hemolítico del adulto o enfermedad inflamatoria sistémica. Y SIMS subagudo y crónico cuando implica enfermedades que tienen como denominador común un estado hipercatabólico, a saber: enfermedad pulmonar obstructiva crónica (EPOC), diabetes, síndrome de caquexia por cáncer (la anorexia en la actualidad no tiene implicancia), cirrosis hepática, artritis reumatoidea e insuficiencia cardíaca7,8.
Si debemos adjudicarle un puntaje en cuanto a intensidad (factor de mayor peso en el primer grupo) y persistencia (factor de mayor implicancia en el segundo grupo), podemos graficarlo en una escala como se muestra en la Figura 1.

Figura 1. Escala de mayor a menor (100-0) respecto a intensidad y persistencia de RIS (respuesta inflamatoria sistémica). SIDA: síndrome de inmunodeficiencia humana adquirida. EPOC: enfermedad pulmonar obstructiva crónica. HTA: hipertensión arterial.
Fisiopatología
La insuficiencia cardíaca que en primera instancia comienza por la incapacidad, merced a una alteración estructural o funcional, de eyectar la sangre del corazón con el consiguiente aumento de la presión y volumen de fin de diástole y limitación funcional del mismo (alteración de la ley de Frank-Starling)9,10.
A poco de instaurarse el mecanismo de falla cardíaca, sobreviene un estado hipercatabólico el cual en la actualidad se considera que está producido por RIS.
El disparador de éste sería un fenómeno de estrés oxidativo tanto a nivel de las membranas biológicas de los miocitos como del endotelio, determinando la activación de cascadas intracelulares mediadas por diacilglicerol y fosfolipasa A2, fundamentalmente, generando activación del factor NFK beta, que es un factor de transcripción genética, promoviendo la transcripción y síntesis de citoquinas proinflamatorias.
A su vez existe activación de sistemas enzimáticos como la ciclooxigenasa 2 (cox 2) y lipooxigenasa 5-12 y 15 que a partir del ácido araquidónico de las membranas plasmáticas generan prostaglandina E2 (PgE2) y leucotrienos, respectivamente.
Las citoquinas proinflamatorias, el factor de necrosis tumoral alfa 55 Sv (Svedverg), las interleuquinas 1 beta y 6 que estimulan el factor inductor de proteólisis (FIP) llevan a un estado de sarcopenia y disfunción mitocondrial en donde se afecta la sarcómera de las células estriadas cardíacas, motivando disfunción ventricular; a su vez, la ciclooxigenasa 2 produce estimulación de los factores inductores de hipoxia 1-2 (FIH 1-2) que producen estimulación de mecanismos pro-apoptóticos por inhibición de caspasa 3-chaperonas, sumando radicales libres del estrés oxidativo que dañan el miocardio por la ausencia fisiológica de catalasas de éste11-15 (Figuras 2 y 3).
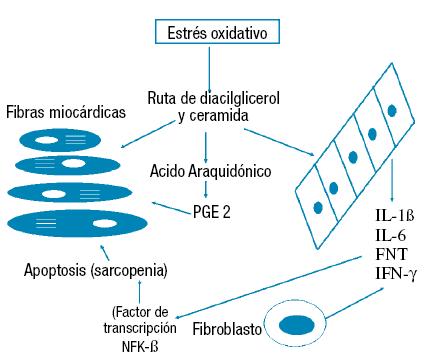
Figura 2. Estrés oxidativo y respuesta inflamatoria sistémica.
PGE 2: prostaglandina E2. IL1ß: interleukina-1ß. IL6: interleukina-6. FNT: factor de necrosis tumoral. IFNγ: interferón γ.
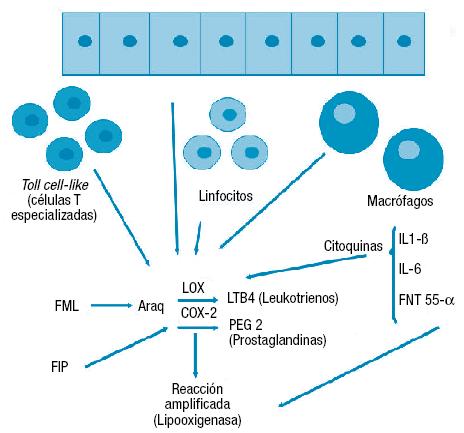
Figura 3. Mediadores biológicos de respuesta inflamatoria sistémica.
FML: factor movilizante de lípidos. FIP: factor inductor de proteólisis. PGE 2: prostaglandina E2. Araq: ácido araquidónico. IL1ß: interleukina-1ß. IL6: interleukina-6. FNT 55α: factor de necrosis tumoral 55α.
En este paso hay un fenómeno inflamatorio donde al cardiomiocito, al endotelio y a la matriz extracelular se suman linfocitos de tipo toll like-cells (expresan receptores T) y macrófagos que (de no existir intervención terapéutica) perpetúan el fenómeno, ya que sintetizan y liberan los mediadores mencionados y el factor movilizante de lípidos16-18.
Hay ciertos fenómenos que pueden ocurrir y deberían ser mencionados:
A- Los corticoides son estimuladores de la enzima 2 (E2) del sistema ubiquina-proteosomal, que normalmente se encarga de extruir de las células las proteínas no integrales de membrana; al estimularse la E2 existe un aumento de tal sistema y determina que extruya proteínas útiles para la célula como las implicadas en el proceso de contracción: actina-miosina, troponina; ello podría explicar en parte la posibilidad de la descompensación de la insuficiencia cardíaca al dar corticoides, no sería tanto por la retención de sodio y agua como por sumarse a otros factores que producen disfunción ventricular.
B- La interleuquina 6, si bien tiene gran capacidad proinflamatoria, es ubicua (está presente en todas partes, en el mismo momento), ya que puede movilizarse en estados como la fase proliferativa del ciclo menstrual o la radioterapia en el pulmón; no obstante a los fines del SIMS, resulta relevante en cuanto es la principal inductora a nivel hepático de la síntesis y liberación de PCR19, hoy en día considerado el principal representante de los reactantes de fase aguda.
Nutrición
En la IC, en la forma crónica en particular, existe una disminución en la función del páncreas exócrino que conlleva a una alteración en la digestión de alimentos con la consiguiente disminución de los aminoácidos (AA) en plasma.
Frente a esto, se ha ensayado en modelos animales y en el hombre, la infusión endovenosa (EV) aguda de AA mixtos que estimulan la síntesis de proteínas en músculo esquelético, pero no en el hígado. El flujo de AA a través de la vena porta es el estímulo para la síntesis y liberación del factor de crecimiento de la insulina (sigla en inglés: IGF 1), también denominado somatomedina, que a su vez es responsable de la modulación de la hormona de crecimiento (GF) a través de las serina proteasas.
Se ha visto que la sobreexpresión de IGF 1 protege a los cardiomocitos del infarto, disminuye la dilatación ventricular, la carga miocárdica y la hipertrofia.
La IGF 1 también parece disminuir la degradación de proteínas del músculo estriado esquelético en situaciones de estrés oxidativo.
Las propiedades de los AA, que son destacables y pueden jugar un rol de defensa del organismo ante la IC, disminuyendo la RIS, son: por un lado que atraviesan la membrana celular sin consumo de energía (ATP), por el contrario son utilizados para la producción y utilización de fuentes energéticas para la neoglucogénesis a través de la transaminación catalizadas por las enzimas GOAT y GPT para formar intermediarios del ciclo de Krebs. Este fenómeno tiene lugar principalmente a nivel de la formación de alfa ceto-glutarato, fumarato, succinato y oxaloacetato (la chispa encendedora del ciclo de Krebs), canalizando hacia la formación de glucosa y ésta puede entrar en la vía de glucólisis aeróbica para aportar energía (por cada molécula se forman 36 ATP), o bien acumularse como glucógeno, siguiendo la glucogenogénesis. No obstante, en condiciones de RIS persistente como es nuestro caso, la diabetes mellitus tipo II o más aún en el síndrome plurimetabólico o síndrome X (obesidad central - hipertensión arterial - diabetes mellitus tipo II) o en la esteatosis hepática no alcohólica20 y algunos autores agregan en la actualidad: linfoma Hodking; que la glucosa se canaliza hacia la vía de Embden-Meyeroff más que a la acumulación de glucógeno.
Por otra parte, los AA específicos en el corazón regulan la producción de ATP como los que se encuentran en el esqueleto de la creatina, y por otro lado facilita que la glucosa, vía la producción de NADH, genere glutation que se utiliza como recolector de radicales libres, siendo importante ya que como se aclaró el miocardio carece de catalasas. El músculo estriado esquelético y el cardíaco en su conjunto poseen el 45% de los AA del organismo.
El funcionamiento descripto predispone a la puesta en marcha de un estado hipercatabólico con disfunción mitocondrial por alteración de subsistemas de la cadena respiratoria, en particular la I y la III. Los AA son también convertidos en piruvato que se transforma en acetato en condiciones aeróbicas para unirse al oxalacetato y generar el ciclo de los ácidos tricarboxílicos, o en lactato por medio de la enzima láctico dehidrogenasa (LDH) en condiciones de anaerobiosis.
Se está investigando el aporte de suplemento oral con AA mixtos por lo referido en la IC y en el síndrome plurimetabólico21,22.
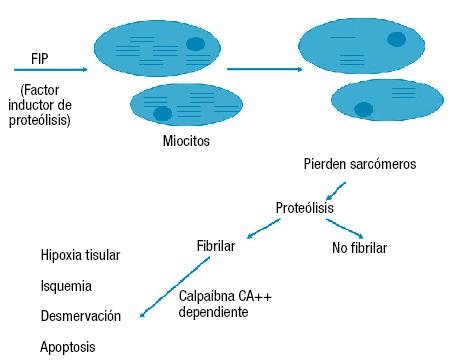
Figura 4. Mediadores biológicos de respuesta inflamatoria sistémica.
FIP: factor inductor de proteólisis.
Conclusión
La RIS es considerada, actualmente, relevante en la mayoría de las enfermedades crónicas. En un extremo estaría el cáncer, en el otro la artritis reumatoidea y en la mitad se podrían considerar la diabetes tipo II y la insuficiencia cardíaca. Si bien en esta última, la relevancia clínica puede ser limitada, por existir tratamientos específicos para el control de la misma; existen subgrupos que podrían beneficiarse, disminuyendo el hipercatablismo emergente de la RIS a través de implementación nutricional de aminoácidos mixtos y drogas que están actualmente en ensayo.
1. Braunwald E. Biomarkers in Heart Failure. N Engl J Med 2008;358;20:2148-2159. [ Links ]
2. Elster SK, Braunwald E, Wood HF. A study of C-reactive protein in the serum of patients with congestive heart failure. Am Heart J 1956;51:533-41. [ Links ]
3. Levine B, Kalman J, Mayer L, Fillit HM, Packer M. Elevated circulating levels of tumor necrosis factor in severe chronic heart failure. N Engl J Med 1990;323:236-41. [ Links ]
4. Perman M. Soporte nutricional. En: Terapia Intensiva. Sociedad Argentina de Terapia Imtemsiva. Ed. Panamericana, 2a edición, 1995; XI: 517-44. [ Links ]
5. Cerchietti L, Nte A, Peluffo G, et al. Effects of celecoxib, medroxyprogesterone, and dietary intervention on systemic syndromes in patients with advanced lung adenocarcinoma. J Pain Symptom Manage 2004;27:85-95. [ Links ]
6. González C. Caquexia, inflamación y cáncer: las piezas comienzan a encajar. Actualización en Nutrición 2004;5;3:8-10. [ Links ]
7. Wessley S, Hotopf M, Sharpe M. Chronic fatigue and its syndromes. Oxford University Press 1999;3:45-79. [ Links ]
8. Aird W. The hematologic system as a marker of organ dysfunction in sepsis. Mayo Clinic Proc 2003;78:869-81. [ Links ]
9. Echazarreta D. Abordaje diagnóstico de la insuficiencia cardíaca. Rev Insuf Cardíaca 2008;3;4:191-204. [ Links ]
10. Cingolani H. Hemodinamia: presión arterial y volumen minuto. En: H. Cingolani, A. Houssay. Fisiología Humana, Ed. El Ateneo, 7a edición, 2005;25:296-305. [ Links ]
11. Agostino C, Labinsky V, Lionetti V, et al. Altered cardiac metabolic phenotype after prolonged inhibition of NO synthesis in chronically instrumented dogs. Am J Physiol Heart Circ 2006;290:H1721-26. [ Links ]
12. Hare J. Nitroso-redox balance in the cardiovascular system. N Engl J Med 2004;351;20:2112-14. [ Links ]
13. Pfeiffer T, Schuster S, Bonhieffer S. Cooperation and competition in the evolution of ATP-producing pathways. Science 2001;292:504-7. [ Links ]
14. Landmesser U, Spiekerman S, Didakov S, et al. Vascular oxidative stress and endothelial dysfunction in patients with chronic heart failure: role of xanthine-oxidaes and extracellular superoxide dismutase. Circulation 2002;106:3073-8. [ Links ]
15. Rogers S, Macheda M, Docherty S, et al. Identification of a novel glucose transporter-like protein-GLUT-12. Am J Physiol Endocrinol Metab 2002;283:E733-8. [ Links ]
16. Jarvinen H. Thiazolidinediones. N Engl J Med 2004; 351: 1106-18. [ Links ]
17. Matthys P, Billau A. Cytokines and cahexia. Nutrition 1997; 13:763-70. [ Links ]
18. Cosio M, Saetta M, Agusti A. Inmunologic aspects of chronic obstructive pulmonary disease. N Engl J Med 2009;360:2445-54. [ Links ]
19. Epstein F. Mechanisms of wascle wasting. The role of the ubiquitinproteoseme pathway. N Engl J Med 1996;335:1897-1905. [ Links ]
20. Santoro S, Stolarza S, Milici L, y col. Esteatosis hepática no alcohólica: un enfoque sobre la relación con la obesidad y sus comorbilidades. Actualizaciones en Nutrición 2004;5;2:19-24. [ Links ]
21. Pasini E, Aquilani R, Dioguardi F. Aminoacids= chemistry and metabolism in normal and hypercatabolic states. Am J Cardiol 2004;93(Suppl):3A-5A. [ Links ]
22. Dioguardi F. Wasting and the substrate-to-energy controlled pathway: a role for insulin resistance and amino acids. Am J Cardiol 2004;93(Suppl):6A-12A. [ Links ]














