Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Insuficiencia cardíaca
On-line version ISSN 1852-3862
Insuf. card. vol.14 no.2 Ciudad Autónoma de Buenos Aires June 2019
ARTICULO DE ACTUALIZACIÓN
Puente miocárdico sintomático
¿El paciente debe resignarse a los síntomas?
Braian A. Cardinali Ré1, Federico J. Olgiati1, Lucía M. Ortiz2, Diego Echazarreta3, Marcelo Portis4
1 Médico residente. Servicio de Cardiología. Hospital Interzonal Especializado de Agudos y Crónicos San Juan de Dios. La Plata. Buenos Aires. República Argentina.
2Médica cardióloga. Servicio de Cardiología. Hospital Interzonal Especializado de Agudos y Crónicos San Juan de Dios. La Plata. Buenos Aires. República Argentina.
3 Médico cardiólogo. Jefe de Sala de Cardiología. Hospital Interzonal Especializado de Agudos y Crónicos San Juan de Dios. La Plata. Buenos Aires. República Argentina.
4 Médico cardiólogo. Jefe del Servicio de Cardiología. Hospital Interzonal Especializado de Agudos y Crónicos San Juan de Dios. La Plata. Buenos Aires. República Argentina.
Institución: Servicio de Cardiología. Hospital Interzonal Especializado de Agudos y Crónicos San Juan de Dios. La Plata. Buenos Aires. República Argentina.
Correspondencia: Dr. Braian A. Cardinali Ré.
Servicio de Cardiología. Hospital Interzonal Especializado de Agudos y Crónicos (HIEA y C) San Juan de Dios. La Plata. CP: 1900. Buenos Aires.
República Argentina.
Email: cardinali_re@hotmail.com Tel.: 2317 557646
Recibido: 01/02/2019
Aceptado: 06/05/2019
Resumen
El puente miocárdico (PM) es una anomalía congénita en la que un segmento de una arteria coronaria toma un curso intramuscular tunelizado bajo un puente de miocardio suprayacente, pudiendo tener diferentes longitudes, las cuales van desde 4 mm hasta 80 mm. El PM puede darse en cualquier arteria coronaria, pero el 67-98% de los casos ocurren en la arteria coronaria descendente anterior. Habitualmente, el PM es un hallazgo angiográfico o puede encontrarse en autopsias. Sin embargo, algunos pacientes pueden presentar isquemia miocárdica, sintomática o silente, inducida por el ejercicio; así como también, presentar un síndrome coronario agudo, atontamiento miocárdico, disfunción ventricular, síndrome de Tako-tsubo, arritmia ventricular o incluso debutar con muerte súbita. La gran mayoría de los paciente portadores de un PM son asintomáticos, y el diagnóstico en muchos casos se hace en forma incidental ante la realización de una cinecoronariografía solicitada por otros motivos. Actualmente, contamos con distintos métodos complementarios, invasivos y no invasivos para realizar el diagnóstico. Con respecto al tratamiento, es de elección el tratamiento médico, pero de no ser útil contamos con la opción de resolución endovascular o quirúrgica. Esta patología es una entidad olvidada con pocos ensayos clínicos controlados que prueben la eficacia de los tratamientos propuestos, hecho que conlleva a que nuestros pacientes deban resignarse a los síntomas.
Palabras clave: Puente miocárdico; Síntomas; Tratamiento médico; Miotomía; Resolución endovascular
Summary
Symptomatic myocardial bridge
Should the patient be resigned to the symptoms?
Myocardial bridging (MB) is a congenital anomaly in which a segment of a coronary artery takes a tunneled intramuscular course under a bridge of overlying myocardium, and it can have different lengths, ranging from 4 mm to 80 mm.
MB can occur in any coronary artery, but 67-98% of cases occur in the anterior descending coronary artery. Usually, the MB is an angiographic finding or it can be found in autopsies. However, some patients may present myocardial ischemia, symptomatic or silent, induced by exercise; as well as presenting an acute coronary syndrome, myocardial stunning, ventricular dysfunction, Tako-tsubo syndrome, ventricular arrhythmia or even debut with sudden death. The vast majority of patients with a MB are asymptomatic, and in many cases the diagnosis is made incidentally when performing a coronary angiography requested for other reasons. Currently, we have different complementary methods, invasive and non-invasive to make the diagnosis. With regard to treatment, medical treatment is the choice, but if it is not useful, we have the option of endovascular or surgical resolution. This pathology is a forgotten entity with few controlled clinical trials that prove the efficacy of the proposed treatments, which leads to our patients being resigned to the symptoms.
Keywords: Myocardial bridge; Symptoms; Medical treatment; Myotomy; Endovascular resolution
Resumo
Ponte miocárdica sintomática
O paciente deve ser resignado aos sintomas?
A ponte miocárdica (PM) é uma anomalia congênita na qual um segmento de uma artéria coronária toma um curso intramuscular tunelado sob uma ponte de miocárdio sobrejacente, e pode ter diferentes comprimentos que variam de 4 mm a 80 mm. A PM pode ocorrer em qualquer artéria coronária, mas 67-98% dos casos ocorrem na artéria coronária descendente anterior. Normalmente, a PM é um achado angiográfico ou pode ser encontrada em autópsias. Entretanto, alguns pacientes podem apresentar isquemia miocárdica, sintomática ou silenciosa, induzida pelo exercício; além de apresentar síndrome coronariana aguda, atordoamento miocárdico, disfunção ventricular, síndrome de Tako-tsubo, arritmia ventricular ou até mesmo debutar com morte súbita. A grande maioria dos pacientes com PM é assintomática e, em muitos casos, o diagnóstico é feito incidentalmente quando se faz uma angiografia coronariana solicitada por outros motivos. Atualmente, temos diferentes métodos complementares, invasivos e não invasivos para fazer o diagnóstico. Com relação ao tratamento, o tratamento médico é a escolha, mas se não for útil, temos a opção de resolução endovascular ou cirúrgica. Essa patologia é uma entidade esquecida, com poucos ensaios clínicos controlados que comprovam a eficácia dos tratamentos propostos, o que leva nossos pacientes a se resignarem aos sintomas.
Palavras-chave: Ponte miocárdica; Sintomas; Tratamento médico; Miotomia; Resolução endovascular
Introducción
El puente miocárdico (PM) es una anomalía congénita en la que un segmento de una arteria coronaria toma un curso intramuscular tunelizado bajo un puente de miocardio suprayacente, pudiendo tener diferentes longitudes, las cuales van desde 4 mm hasta 80 mm1,2.
El PM puede darse en cualquier arteria coronaria, pero el 67-98% de los casos ocurren en la arteria coronaria descendente anterior3,4.
Los pacientes con PM a menudo son asintomáticos, pero esta anomalía puede estar asociada con angina de esfuerzo, síndromes coronarios agudos, arritmias cardíacas, síncope o incluso muerte cardíaca súbita. Esta revisión pone de manifiesto nuestra comprensión actual de la fisiopatología del PM, describe las modalidades diagnósticas de elección y las opciones terapéuticas para esta entidad clínica desafiante.
Objetivo
Realizar una actualización sobre la epidemiología, la fisiopatología, la clínica, los métodos diagnósticos disponibles y el tratamiento del PM.
Objetivo secundario
Generar un punto de partida para la realización de ensayos clínicos randomizados que comparen el tratamiento médico y quirúrgico en este tipo de pacientes.
Materiales y métodos
Se realizaron búsquedas en MEDLINE desde el año 1980 hasta diciembre de 2018, utilizando una estrategia de búsqueda jerárquica con los siguientes términos de búsqueda: puente miocárdico coronario, puente miocárdico y síndrome coronario agudo, síndrome coronario agudo con coronarias normales, miotomía, tensión cortante de la pared coronaria.
Se realizaron búsquedas en el registro Cochrane y también en Internet, resúmenes de las principales conferencias de cardiología de América del Norte, América del Sur y Europa. Utilizamos referencias relevantes de publicaciones recuperadas y la función de artículos relacionados de PubMed para identificar estudios no captados por nuestra estrategia de búsqueda principal.
Criterios de inclusión
Estudios de revisión que detallen la epidemiología, fisiopatología, clínica y el tratamiento.
- Estudios prospectivos o retrospectivos con una muestra superior a cien pacientes.
- Estudios prospectivos de autopsias forenses.
Todos los estudios fueron evaluados por dos de los autores del presente trabajo y se calificaron según representatividad de la muestra del estudio, resultados finales obtenidos, fiabilidad y validez de los criterios de inclusión. Los desacuerdos fueron resueltos por consenso.
Se extrajeron datos generales, conclusiones, extractos de texto y se formuló una conclusión formada por el contenido extraído de cada texto en particular y se completo con la experiencia y vivencias personales de los autores.
Desarrollo
Esta anomalía congénita se ve hasta en un 40% a 80% de las autopsia; sin embargo, el PM funcional se observa con menos frecuencia en la angiografía (0,5% a 16,0%)1,2.
Pueden darse en cualquier arteria coronaria, pero del 67% al 98% de los casos ocurren en la arteria coronaria descendente anterior (DA)3,4, rama de la coronaria izquierda.
El impacto hemodinámico del PM depende del grosor y la longitud del puente, la orientación del puente en relación con las fibras miocárdicas y la presencia de tejido conectivo o adiposo alrededor del segmento involucrado5.
Fisiopatología
El mayor flujo de la perfusión miocárdica en la DA (irrigando al ventrículo izquierdo) ocurre en diástole, fundamentalmente, debido al aumento de presión transmural originado por la contracción sistólica del ventrículo izquierdo, impidiendo el flujo coronario. Debido a que sólo el 15% del flujo coronario izquierdo ocurre durante la sístole ventricular en condiciones normales, y que el efecto del puente muscular es mayor en sístole, visualizado en las angiografías, su relevancia clínica ha sido cuestionada. Sin embargo, más recientemente, se ha reconocido que la isquemia miocárdica no está puramente relacionada con la compresión vascular sistólica. De hecho, se ha demostrado que la compresión sistólica del vaso persiste en la diástole media-tardía.
Los estudios de autopsias y de ultrasonido intravascular han demostrado que los segmentos intramurales y distales de los vasos con puentes permanecen libres de enfermedad aterosclerótica, mientras que el segmento proximal del vaso es propenso a desarrollar aterosclerosis5.
En la entrada de un PM, la mecánica de fluidos desempeña un papel importante en la formación de placa, ya que aquí el flujo es netamente turbulento, además la tensión de cizallamiento de la pared se asocia con una mayor expresión y adhesión de células vasculares y la producción de especies reactivas de oxígeno, así como el desarrollo de un fenotipo de células endoteliales pro-aterogénicas. De hecho, los estudios de autopsia han demostrado que los segmentos coronarios, inmediatamente proximales a los puentes miocárdicos, tienen células endoteliales planas y poligonales disfuncionales; mientras que las células endoteliales, que recubren los segmentos puenteados, son estructuralmente normales6.
Ciertos cambios fisiopatológicos adicionales pueden inducir síntomas de isquemia miocárdica en pacientes previamente asintomáticos, estos aspectos fisiopatológicos son:
- El aumento de la disfunción diastólica del ventrículo izquierdo, asociada con el envejecimiento, la hipertensión y la aterosclerosis coronaria, puede exacerbar el desajuste entre la oferta y la demanda impuesta por el puente.
- El desarrollo de hipertrofia ventricular izquierda puede aumentar la compresión y reducir la reserva microvascular coronaria.
- El vasoespasmo coronario, la disfunción microvascular o disfunción endotelial relacionada con factores de riesgo cardiovascular.
- El desarrollo de placa proximal al puente puede aumentar la obstrucción coronaria por el puente.
- La remodelación negativa dentro del puente puede reducir el flujo miocárdico.
Cada uno de estos factores puede contribuir en un grado variable al desarrollo de síntomas en pacientes con PM.
Presentación clínica
Habitualmente el puente muscular es un hallazgo angiográfico o en autopsias. Sin embargo, algunos pacientes pueden presentar isquemia miocárdica sintomática o silente, inducida por el ejercicio, así como también presentar síndrome coronario agudo, atontamiento miocárdico, disfunción ventricular silente, síndrome de Tako-tsubo, arritmias ventriculares o muerte súbita7.
Diagnóstico
En la actualidad existen varias formas de hacer el diagnóstico y ninguna de ellas es considerada hoy en día como la prueba de oro (gold standard).
Para referirnos a la pruebas diagnósticas vamos a clasificarlas en invasivas y no invasivas.
Pruebas no invasivas
- Tomografía multicorte
Es una prueba que gracias a la reconstrucción tridimensional nos aporta una gran caracterización anatómica, resultando superior a la angiografía. Como desventaja expone al paciente a una dosis no despreciable de radiación.
Pruebas invasivas
- Ecografía intracoronaria
Una técnica diagnóstica novedosa, poco disponible en nuestro medio; pero con ventajas diagnósticas sobre otros métodos.
El hallazgo característico es el signo de media luna, un área ecolúcido presente sólo entre el segmento coronario puenteado y el tejido epicárdico que persiste durante todo el ciclo cardíaco. Además, la ecografía intravascular puede caracterizar la aterosclerosis subangiográfica proximal (Figura 1).

Figura 1. Ecografía intracoronaria: signo de "media luna", área ecolúcida que está presente sólo entre el segmento coronario con puente miocárdico y el tejido epicárdico. Imágen tomada de Michel T Corban el al. JACC 2014; 63(22):2346-235521.
-Angiografía
Es una de las técnicas diagnósticas más usuales en nuestro medio, donde muchas veces se hace el diagnóstico de manera incidental o por sospecha de otras causas de dolor precordial.
El diagnóstico depende del cambio de diámetro entre la sístole y la diástole dentro del segmento coronario con PM. Un efecto de ordeñe significativo está presente cuando hay una reducción â¥70% en el diámetro luminal mínimo durante la sístole y una reducción â¥35% persistente en el diámetro luminal mínimo durante la diástole media-tardía (Figura 2).
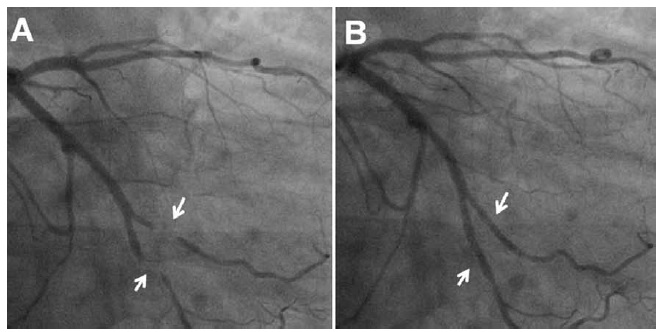
Figura 2. Cinecoronariografía: A. Compresión sistólica de puentes miocárdicos: efecto de ordeñe. B. Aumento posterior del diámetro de la luz del vaso durante la diástole. Las flechas blancas indican áreas de puente miocárdico. Imágen tomada de Michel T Corban el al. JACC 2014; 63(22):2346-235521.
El estrechamiento sistólico en el PM puede acentuarse mediante la inyección intracoronaria de nitroglicerina, debido a la vasodilatación de segmentos coronarios adyacentes sin puentes.
Tratamiento
Terapia no farmacológica
Se recomienda la modificación agresiva de los factores de riesgo. Descenso de peso, actividad física aeróbica moderada, dieta hiposódica e hipograsa.
Terapia farmacológica
Se debe considerar la terapia antiplaquetaria en pacientes con PM, porque tienen un mayor riesgo de desarrollar aterosclerosis y complicaciones de placa.
Para los pacientes sintomáticos, los beta bloqueantes siguen siendo el pilar del tratamiento, modificando la alteración hemodinámica causada por el PM al disminuir la frecuencia cardíaca, aumentar el período de llenado coronario diastólico y disminuir la contractilidad y compresión de las arterias coronarias8.
Los bloqueantes de los canales de calcio también se usan con frecuencia, ya que tienen efectos vasodilatadores que pueden ser beneficiosos en pacientes con vasoespasmo concomitante.
No se dispone de comparaciones directas de beta bloqueantes y bloqueantes de los canales de calcio o ensayos clínicos aleatorizados sobre los resultados de los beneficios de ambos8.
En contraste, los agentes vasodilatadores puros, como la nitroglicerina, deben usarse con precaución en pacientes con PM. Aunque los nitratos tienen propiedades anti vasoespasmos coronarios y pueden disminuir la precarga, también pueden empeorar los síntomas al intensificar la compresión sistólica del segmento con PM y los segmentos vasodilatadores proximales al puente, exacerbando el flujo retrógrado en el segmento proximal y aumentando la isquemia miocárdica18.
Los vasodilatadores deben evitarse a menos que exista un vasoespasmo coronario coexistente significativo.
Intervención coronaria percutánea
La implantación de stent en pacientes sintomáticos con PM puede mejorar la presión sistólica intracoronaria máxima y la compresión vascular, normalizar el flujo y eliminar los síntomas; sin embargo, las complicaciones como: la perforación durante el despliegue del stent, la fractura del stent, la reestenosis y la trombosis del stent, han limitado su uso en esta condición. Los stent liberadores de drogas (DES) tienen menos tasas de trombosis y reestenosis, por ende, deben ser los elegidos para este tipo de pacientes10.
Un pequeño estudio que comparó la implantación de DES (n=8) con stents metálicos -BMS- (n=4) en pacientes sintomáticos refractarios a la terapia médica máxima, reportó tasas más bajas de trombosis en el grupo DES que en el grupo BMS, pero ambos grupos tuvieron tasas más altas que los pacientes revascularizados con angioplastia por lesiones ateroscleróticas12.
En resumen, aunque no hay ensayos controlados aleatorizados de terapia médica óptima versus terapia médica óptima y angioplastia con DES, la terapia médica parece ser superior a la angioplastia. La revascularización guiada por isquemia, utilizando DES, puede considerarse para pacientes sintomáticos refractarios a la terapia médica máxima y que no son candidatos quirúrgicos óptimos11,12.
Tratamiento quirúrgico
La intervención quirúrgica implica una miotomía supraarterial o cirugía de by pass aorto-coronario. Aunque tanto la miotomía como el by pass son elecciones iniciales razonables, no está claro qué procedimiento es superior. Por un lado, debido a que la miotomía intenta corregir la patología subyacente, puede ser el tratamiento de elección para los pacientes que tienen puentes miocárdicos sintomáticos refractarios al tratamiento médico, â¥75% de compresión coronaria sistólica en la angiografía, o evidencia de isquemia o infarto de miocardio. Por otra parte, el by pass es superior sobre la miotomía en casos de puentes miocárdicos extensos (> 25 mm) o profundos (> 5 mm) (el riesgo de miotomía puede ser considerable) o cuando el segmento coronario con PM no se descomprime completamente en diástole (es poco probable que la miotomía corrija la compresión diastólica persistente)14.
Es importante destacar que no hay ensayos clínicos aleatorios que comparen la intensificación de la terapia médica con la intervención quirúrgica y la endovascular. Estos datos limitados sugieren que la terapia quirúrgica, ya sea miotomía o by pass parece segura y eficaz en pacientes sintomáticos con puentes miocárdicos refractarios a la terapia médica15-19.
Conclusión
El PM es una patología frecuente con la que el médico cardiólogo debe enfrentarse a menudo. Es una patología olvidada, poco estudiada, con evidencia poco sólida a la hora de elegir un tratamiento, lo cual muchas veces el paciente resulta afectado por nuestro desconocimiento20-22.
Se espera que a partir de esta revisión el cardiólogo tengas mayores herramientas para brindarle una adecuada respuesta a su paciente en consulta y que sirva como llave para mayores ensayos clínicos controlados que den respuesta a nuestras dudas y mejore la calidad de vida de los pacientes con esta alteración cardíaca y no se resignen a los síntomas.
Recursos financieros
Los autores no recibieron ningún apoyo económico para la investigación.
Conflicto de intereses
Los autores declararon no tener conflicto de intereses.
1. Mohlenkamp S, Hort W, Ge J, Erbel R. Update on myocardial bridging. Circulation 2002;106:2616-2622. [ Links ]
2. Bourassa MG, Butnaru A, Lesperance J, Tardif JC. Symptomatic myocardial bridges: overview of ischemic mechanisms and current diagnostic and treatment strategies. J Am Coll Cardiol 2003; 41 :351-359. [ Links ]
3. Loukas M, B Curry, Bowers M, et al. The relationship of myocardial bridges to coronary artery dominance in the adult human heart. J Anat 2006; 209:43-50. [ Links ]
4. Qian JY, Zhang F, Dong M, et al. Prevalence and characteristics of myocardial bridging in coronary angiogram-data from consecutive 5525 patients. Chin Med J Engl 2009;122:632-635. [ Links ]
5. Ge J, Jeremias A, Rupp A, et al. New signs characteristic of myocardial bridging demonstrated by intracoronary ultrasound and Doppler. Eur Heart J 1999; 20:1707-1716. [ Links ]
6. Uusitalo V, Saraste A, Pietilͤ M, Kajander S, Bax JJ, Knuuti J. The Functional Effects of Intramural Course of Coronary Arteries and its Relation to Coronary Atherosclerosis. J Am Coll Cardiol Img 2015;8:697-704. [ Links ]
7. Gowda RM, Khan IA, Ansari AW, Cohen RA. Acute ST segment elevation myocardial infarction from myocardial bridging of left anterior descending coronary artery. Int J Cardiol 2003; 90:117-118. [ Links ]
8. Klein DI, Krebs W, Hanrath P. Functional, angiographic and intracoronary Doppler flow characteristics in symptomatic patients with myocardial bridging: effect of short-term intravenous beta-blocker medication. J Am Coll Cardiol 1996; 27:1637-1645. [ Links ]
9. Klues HG, Schwarz ER, vom Dahl J, et al. Disturbed intracoronary hemodynamics in myocardial bridging: early normalization by intracoronary stent placement. Circulation 1997; 96:2905-2913. [ Links ]
10. Ernst A, Bulum J, Separovic Hanzevacki J, Lovric Bencic M, Strozzi M. Five-year angiographic and clinical follow-up of patients with drug-eluting stent implantation for symptomatic myocardial bridging in absence of coronary atherosclerotic disease. J Invasive Cardiol 2013; 25:586-592. [ Links ]
11. Kunamneni PB, Rajdev S, Krishnan P, et al. Outcome of intracoronary stenting after failed maximal medical therapy in patients with symptomatic myocardial bridge. Catheter Cardiovasc Interv 2008;71: 185-190. [ Links ]
12. Nardi F, Verna E, Secco GG, et al. Variant angina associated with coronary artery endothelial dysfunction and myocardial bridge: a case report and review of the literature. Intern Med 2011; 50:2601-2606. [ Links ]
13. Duygu H, Zoghi M, Nalbantgil S, Kirilmaz B, Türk U, Ozerkan F, et al. Myocardial bridge: a bridge to atherosclerosis. Anadolu Kardiyol Derg 2007;7(1):12-6. [ Links ]
14. Noble J, Grondin P, Bourassa MG. Succesful periarterial muscle resection for myocardial bridging and milking effect on the left anterior descending artery. Am J Cardiol 1977;39:267. [ Links ]
15. Grondin P, Bourassa MG, Noble J, Petitclerc R, Dydra I. Successful course after supraarterial myotomy for myocardial bridging and milking effect of the left anterior descending artery. Ann Thorac Surg 1977; 24 (5): 422-9. [ Links ]
16. Katznelson Y, Petchenko P, Knobel B, Cohen AJ, Kishon Y, Schachner A. Myocardial bridging: surgical technique and operative results. Mil Med 1996; 161: 248-50. [ Links ]
17. Bayes A, Marti V, Auge JM. Coronary stenting for symptomatic myocardial bridging. Heart 1998; 80: 102-3. [ Links ]
18. Ishimori T, Raizner AE, Chahine RA, Awdeh M, Luchi RJ. Myocardial bridges in man: clinical correlations and angiographic accentuation with nitroglycerin. Cathet Cardiovasc Diagn 1977; 3: 59-65. [ Links ]
19. Xiao-hong H, Shui-yun W, Jian-ping X, et al. Surgical outcome and clinical follow-up in patients with symptomatic myocardial bridging. Chin Med J (Engl) 2007;120:1563-6. [ Links ]
20. Lozano I, Baz JA, López Palop R, y col. Pronóstico a largo plazo de los pacientes con trayecto intramiocárdico de la arteria descendente anterior con compresión sistólica. Rev Esp Cardiol 2002;55:359-64. [ Links ]
21. Corban MT, Hung OY, Eshtehardi P, Rasoul-Arzrumly E, McDaniel M, Mekonnen G et al. Myocardial bridging: contemporary understanding of pathophysiology with implications for diagnostic and therapeutic strategies. J Am Coll Cardiol 2014; 63(22): 2346-2355. [ Links ]
22. Lee MS, Chen CH. Myocardial bridging: an up-to-date review. J Invasive Cardiol 2015; 27(11): 521-528. [ Links ]














