Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO  uBio
uBio
Compartilhar
Cuadernos de herpetología
versão On-line ISSN 1852-5768
Cuad. herpetol. vol.25 no.1 San Salvador de Jujuy jul. 2011
TRABAJOS
Ampliación del conocimiento sobre uso de hábitat en Liolaemus multimaculatus, sitios de fuga
Federico P. Kacoliris1,2, Jorge D. Williams1,2, Sofia Quiroga1, Alejandro Molinari1, Natalin Vicente1
1 Sección Herpetología, Facultad de Ciencias Naturales y Museo, Universidad Nacional de La Plata. Paseo del Bosque s/n (1900). La Plata, Buenos Aires, Argentina.
2 Consejo Nacional de Investigaciones Científicas y Técnicas
Recibido: 30/12/10
Revisado: 05/04/11
Aceptado: 09/05/11
RESUMEN
El conocimiento acerca de las preferencias espaciales representa una primera etapa para la comprensión de las interacciones entre los organismos y su ambiente. La lagartija de las dunas (Liolaemus multimaculatus) es una especie altamente adaptada a la vida en la arena. El objetivo del presente trabajo fue estudiar el uso del hábitat en diferentes situaciones/momentos durante su período de actividad, con el fin de obtener un mayor entendimiento acerca de las preferencias espaciales en esta especie. Se aplicaron modelos basados en el criterio de uso vs disponibilidad para evaluar las preferencias por sitios de fuga y para comparar estos con los sitios en donde los individuos se hallaban posados originalmente. Los modelos mostraron diferencias entre uso y disponibilidad y también se observaron diferencias entre sitios originarios y de fuga. La especie utilizó una gran diversidad de microhábitats, rechazando microhábitats con ausencia de vegetación. La conservación de hábitats óptimos para la especie deberá partir de un enfoque integral que incluya tanto microhábitats de termorregulación/alimentación como microhábitats de fuga.
PALABRAS CLAVE: Selección de hábitat; Autoecología; Lagartijas arenícolas; Patrones espaciales.
ABSTRACT
The knowledge about spatial preferences in animals represents the first stage to understand the interactions between the organisms and its environment. The sand dune lizard (Liolaemus multimaculatus) is a species highly adapted to live in the sand. The goal of this work was to study the habitat use in different moments/situation during its period of activity, in order to obtain a more understanding about spatial preferences in this species. Models based on the use vs availability criterion were applied in order to assess the preferences for sites used as refuge and to compare those sites with perch sites. The models shows differences between use and availability and also differences between perch sites and refuge sites were observed. Results shows that this species used a great diversity of microhábitats with a high reject for microhabitats without vegetation cover. The conservation of good habitats for this species must consider both kinds of microhábitats, those used for thermoregulation and feed and those others used for refuge.
KEYWORDS: Habitat selection; Autoecology; Sand lizards; Spatial patterns.
INTRODUCCIÓN
La necesidad de determinar las preferencias espaciales en el uso del hábitat ha sido reconocida como una primera etapa para entender y explicar las interacciones ecológicas entre los organismos y su ambiente (Neu et al., 1974). Tal conocimiento provee información acerca de la historia natural y las presiones selectivas (Stark et al., 2005) a la vez que permite evaluar el estado de conservación y la disponibilidad de hábitats de importancia para la supervivencia de las especies estudiadas (Manly et al., 1993; Johnson, 2000).
Algunas de las principales causas que condicionan las preferencias de hábitats en reptiles se hallan relacionadas con la estructura de la vegetación (Huey et al., 1983; Dias y Rocha, 2004; Attum y Eason, 2006) y con las posibilidades de termorregular (Grover, 1996; Clóvis & Verrastro, 2008). Los patrones espaciales pueden también estar afectados por variables individuales como la edad y el sexo (Butler et al., 2007) y simultáneamente pueden existir variaciones en un mismo individuo producto del contacto con predadores, competidores, presas, etc. (Rocha, 1991; Converse y Savidge, 2003).
La lagartija de las dunas, Liolaemus multimaculatus (Duméril & Bibron, 1837) es una especie vulnerable y endémica de las dunas costeras de las provincias de Buenos Aires y norte de Río Negro (Cei, 1993; Avila et al., 2000). Estudios previos han propuesto que el uso de hábitat en esta especie estaría relacionado con el gradiente estructural de la vegetación, siendo más abundante en hábitats con cobertura vegetal baja a media (Vega, 2001; Kacoliris et al., 2009a). No obstante, tales estudios estuvieron basados sobre información de lagartijas que en la mayoría de los casos se hallaban posadas sobre el terreno, sin evaluar las preferencias de los individuos por sitios de huida/fuga. En este contexto el presente estudio propone evaluar: 1) patrones de selección de sitios durante eventos de fuga y 2) diferencias entre estos y los patrones de selección relacionados a sitios donde los individuos se hallaban posados originalmente (previamente publicado en Kacoliris et al., 2009a).
MATERIALES Y METODOS
El área de estudio comprendió un sector de 140 ha de dunas costeras localizadas dentro de la Reserva Provincial Mar Chiquita. Para un conocimiento más detallado sobre la vegetación que puede encontrarse en el área de estudio ver Kacoliris et al. (2009a). Los muestreos se efectuaron durante los meses de enero y febrero de 2007, considerando que las lagartijas de esta especie permanecen inactivas o subactivas durante otoño e invierno (Vega, 2001).
Los diferentes microhábitats se caracterizaron en base a la cobertura de la vegetación (CV). Para cuantificar la disponibilidad de cada microhábitat se muestrearon 156 cuadrantes de 1 m2 cada uno, ubicados en forma sistemática sobre el área de estudio. Sobre cada cuadrante se tomó una fotografía con una cámara digital de alta resolución y sobre la base de la misma se registró la CV. Para determinar las categorías de CV a las cuales fueron asignadas las fotografías, se utilizó una escala modificada a partir del método propuesto por Domin- Krajina (Mueller-Dombois & Ellenberg, 1974). Esta escala permite una mayor discriminación entre valores medios y bajos de cobertura, los cuales son los más difíciles para separar. Se reconocieron las siguientes categorías: 1) 0%; 2) 0,5%; 3) 1-5%; 4) 6- 10%; 5) 11-20%; 6) 21-30%; 7) 31-40%; 8) 41-50%; 9) 51-70%; 10) 71-100%. El número de categorías fue determinado teniendo en cuenta las sugerencias de Garshelis (2000), estableciendo un número que fuera suficiente para evitar que se solapasen categorías importantes y, al mismo tiempo, evitando tomar un número demasiado alto que pudiera disminuir el poder de discernimiento estadístico del método utilizado.
La búsqueda de individuos se realizó aplicando un muestreo por reconocimiento visual (Crump y Scott, 1994) utilizando un diseño de transectas de 1000 m de largo y 80 m de ancho (n = 13), dispuestas en forma sistemática. Las transectas fueron recorridas por cuatro observadores a velocidad constante y dispuestos equidistantemente a fin de abarcar el ancho total de cada una de ellas. Todos los muestreos fueron desarrollados bajo condiciones climáticas similares: días soleados, vientos bajos a moderados y substrato seco, totalizando un total de 340 días/hombre de esfuerzo. Para cada lagartija se registraron dos microhábitats (cada uno dentro de un cuadrante de 1 m2), aquel en el cual el individuo fue detectado inicialmente, y aquel al cual se dirigió ante la presencia de los observadores, quienes permanecieron inmóviles durante el proceso de huida. La caracterización de los microhábitats utilizados por los individuos se desarrolló aplicando la misma metodología utilizada para definir la disponibilidad (descripta anteriormente). Los sitios en los cuales los individuos se hallaban inicialmente fueron nombrados como sitios originarios; mientras que los sitios a los cuales huyeron fueron nombrados como sitios de fuga.
Los modelos aplicados se basaron en el criterio de uso vs disponibilidad. En estos se considera preferencia por determinado microhábitat a una frecuencia de uso mayor a la esperada, mientras que se considera rechazo a la situación inversa. En este contexto el valor esperado por azar sería aquel que distribuye las frecuencias de uso en relación a la disponibilidad de cada microhábitat. Como índice de uso se utilizó el valor alfa de Manly, mientras que para testear la existencia de preferencias se utilizaron modelos nulos. Los valores observados y esperados fueron comparados utilizando el índice de disimilitud de Bray-Curtis. Para el test general se utilizó un algoritmo incorporando una distribución al azar con 10.000 permutaciones. Debido a que en varios casos se hallaron diferencias por medio del índice de Bray-Curtis, se realizó un test a posteriori a fin de determinar cuáles de los microhábitats tuvieron un valor de selección mayor o menor de lo esperado por azar. El test a posteriori se basó en el cálculo del índice D que mide la desviación del valor del índice de Manly con respecto al uso esperado por azar. La dirección de la preferencia se deduce del signo, en donde valores de D > 0 indican preferencia, mientras que valores de D < 0 indican rechazo. Debido a que se realizaron 10 tests consecutivos, se aplicó un ajuste secuencial de Bonferroni para evaluar de manera múltiple los valores de P (Holm, 1979). Los tests analizados incluyeron un modelo general de uso vs disponibilidad basado en la información de los sitios originarios, un modelo general de uso vs disponibilidad basado en la información de los sitios de fuga, y un modelo comparativo para medir las diferencias entre ambos. El nivel de significancia considerado en todos los caso fue de P < 0,05. Para una lectura más profunda referente al método aplicado remitirse a Pledger et al. (2007).
RESULTADOS
Los modelos generales muestran diferencias significativas entre uso y disponibilidad, pero también se observan algunas diferencias al comparar entre sitios originarios y de fuga (Fig. 1). En el caso de los sitios originarios, previamente se hallaron diferencias significativas entre uso y disponibilidad (ver Kacoliris et al., 2009a). El test a posteriori mostró que los microhábitats con cobertura escaza (categorías 1 y 2) y elevada (categorías 9 y 10) fueron rechazados, mientras que los microhábitats con cobertura baja a intermedia (categorías 3, 4, 5, 6 y 7) fueron preferidos (Tabla 1).
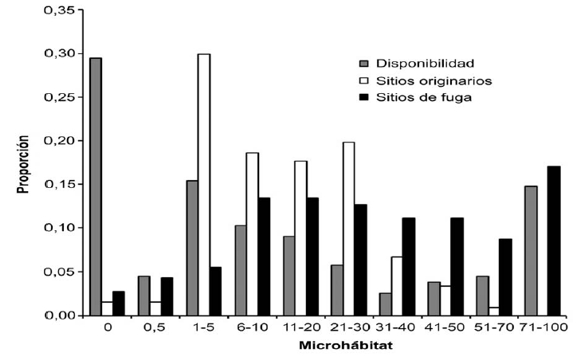
Figura 1. Proporciones de frecuencias de disponibilidad, sitios originarios y sitios de fuga por categoría de microhábitat. En el eje horizontal se representan las categorías de porcentaje de cobertura de la vegetación (CV).
Tabla 1. Resultados de los modelos de uso vs disponibilidad: CM = categoría de microhábitat; Disp = disponibilidad (proporción) de cada categoría de microhábitat; Dif. sitios = diferencias entre sitios originarios y de fuga, P = valor de significancia (* = valores significativos); D = test a posteriori específico por microhábitat, valores positivos indican preferencia y valores negativos indican rechazo.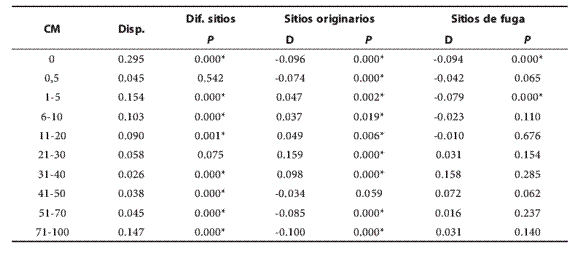
Para el caso del modelo general de sitios de fuga también se observaron diferencias significativas entre uso y disponibilidad. El test a posteriori mostró que microhábitats de baja cobertura (categorías 1 y 3) fueron rechazados, mientras que para el resto de los microhábitats no se observan valores significativos, es decir que fueron utilizados en función de su disponibilidad (Tabla 1).
Al comparar ambos modelos se puede observar la existencia de diferencias en los patrones generales de uso entre sitios originarios y de fuga. Un test a posteriori dio como resultado la ausencia de diferencias para las categorías de microhábitats 2 y 6, mientras que para el resto de los microhábitats se observaron diferencias significativas (Tabla 1). Un análisis de las frecuencias de individuos, en relación a la disponibilidad de cada microhábitat, muestra que las proporciones de uso de categorías con coberturas bajas a medias son mayores para los sitios originarios, mientras que proporciones de uso de categorías con coberturas medias a altas son mayores para los sitios de fuga (Fig. 1).
CONCLUSIONES Y DISCUSION
Los resultados muestran que las lagartijas utilizan un gran espectro de los microhábitats disponibles, rechazando solamente aquellos microhábitats de escaza CV, al menos en las situaciones comportamentales evaluadas. Para el caso particular de los sitios originarios, y como se observara previamente en Kacoliris et al. (2009a), existen preferencias por aquellos microhábitats de baja a mediana cobertura, mientras que microhábitats sin cobertura o con coberturas muy elevadas son rechazados.
Estudios realizados en las cogenéricas Liolaemus occipitalis y Liolaemus lutzae (Rocha, 1991; Clóvis & Verrastro, 2008), así como también en otras especies (Grover, 1996), han concluido que las principales causas asociadas al uso diferencial de hábitats/microhábitats tendría relación con la termorregulación, la alimentación y la detección de predadores. Considerando que L. multimaculatus habita en ambientes similares a los que utilizan estas dos especies, los sitios originarios podrían hallarse relacionados a causas similares, aunque esta hipótesis debería testearse experimentalmente en futuros estudios.
Igualmente a lo que ocurre en otros saurios de pequeña talla (Galdino et al., 2006), L. multimaculatus presenta una variedad de estrategias de escape, entre las cuales las más importantes son la de refugiarse y la de enterrarse bajo la arena (Halloy et al., 1998; Kacoliris et al., 2010). Durante los eventos de fuga solo se observaron rechazos significativos por aquellos microhábitats con ausencia de cobertura. Sin embargo, el patrón general para sitios de fuga mostró que las frecuencias de uso en relación a la disponibilidad aumentaron considerablemente en microhábitats con coberturas medias a altas. Debido a que a mayor densidad de vegetación, mayor dificultad para enterrarse (Kacoliris et al., 2009a), es probable que las lagartijas, en las condiciones planteadas, estuvieran favoreciendo la estrategia de refugiarse por sobre la de enterrarse. Esto se condice con los resultados de Kacoliris et al. (2009b) en donde se observó que una mayor frecuencia de lagartijas prefiere refugiarse por sobre enterrarse ante una persecución por parte de los observadores. Sin embargo, y a diferencia de aquel trabajo, en el presente estudio no se persiguió a los individuos simulando a un predador. Por lo tanto, es probable que frente a una amenaza (al menos cuando se trata de predadores terrestres), las lagartijas prefieran correr a ocultarse en sitios con mayor densidad de vegetación, independientemente del grado de presión ejercida sobre las mismas.
De la comparación entre sitios originarios y sitios de fuga solo se observan similitudes para aquellos microhábitats de escaza cobertura (los cuales son rechazados), mientras que para el resto de los microhábitats se observan diferencias importantes. Originariamente las lagartijas prefieren posarse en microhábitats de menor cobertura, mientras que huyen hacia sitios con mayor cobertura al contacto con los observadores.
Los resultados de este trabajo reflejan la necesidad de extender los estudios sobre uso de hábitat, incluyendo diferentes variables individuales y externas, además de considerar situaciones que reflejen diferentes comportamientos de los individuos. Sin embargo, el empleo de modelos de uso vs disponibilidad se vería altamente beneficiado si se complementaran con estudios de telemetría, a fin de evaluar el tiempo relativo que disponen los individuos en cada microhábitat.
En términos de conservación, ambos sitios (originarios y fuga) resultan de vital importancia para la supervivencia de los individuos. En tal caso la protección de las poblaciones debería fundamentarse en la conservación de microhábitats vegetados. Otra recomendación sería regular la circulación de vehículos sobre las dunas. El tránsito continuo de los mismos remueve y reduce la densidad de vegetación nativa, aumentando la proporción de sectores sin cobertura, los cuales son rechazados por esta especie.
AGRADECIMIENTOS
A A. Rafael; E. Guerrero; G. Guaitoli; R. Cañete; F. Tuñon; M. Buzato y J. Mangiarotti por su ayuda durante el trabajo de campo. El trabajo de campo fue realizado con fondos de Rufford Small Grants (Rufford Foundation) e International Reptile Conservation Foundation. El salario de FK y JW es cubierto por el Consejo Nacional de Investigaciones Científicas y Técnicas. El Organismo Provincial de Desarrollo Sostenible otorgó los permisos necesarios para trabajar en el área.
LITERATURA CITADA
1. Attum, O.A. & Eason, P.K. 2006. Effects of vegetation loss on a sand dune lizard. Journal of Wildlife Management 70: 27-30. [ Links ]
2. Avila, J.L.; Montero, R. & Morando, M. 2000. Categorización de las lagartijas y anfisbénidos de Argentina: 51-74. En: Lavilla, E.O.; Richard, E. & Scrocchi, G.J. (eds.), Categorización de los anfibios y reptiles de la República Argentina. Asociación Herpetológica Argentina. San Miguel de Tucumán. [ Links ]
3. Butler, M.A.; Sawyer, S.A. & Losos, J.B. 2007. Sexual dimorphism and adaptive radiation in Anolis lizards. Nature 447: 202-205. [ Links ]
4. Cei, J.M. 1993. Reptiles del Noroeste, Nordeste y Este de la Argentina. Herpetofauna de las selvas subtropicales, puna y pampas. Museo Regionali di Scienze Naturali (Monografie 14). Torino. Italia. [ Links ]
5. Converse, S.J. & Savidge, J.A.. 2003. Ambient temperature, activity, and microhabitat use by Ornate Box Turtles (Terrapene ornata ornata). Journal of Herpetology 37: 665- 670. [ Links ]
6. Clóvis, S.B. & Verrastro, L. 2008. Annual activity of the lizard Liolaemus occipitalis (Squamata, Liolaemidae) in the coastal sand dunes of southern Brazil. Iheringia 98: 156- 160. [ Links ]
7. Crump, M.L. & Scott Jr., N.J.. 1994. Standard techniques for inventory and monitoring. Visual Encounter Surveys: 84- 92. En: Heyer, W. R.; M. A. Donnelly; M. W. Mc Diarmid; L. C. Hayek & M. S. Foster (eds.), Measuring and monitoring biological diversity. Standard methods for amphibians. Shmitsonian Institution Press. Washington and London. [ Links ]
8. Dias, E.J.R. & Rocha, C.F.D.. 2004. Thermal ecology, activity patterns, and microhabitat use by two sympatric Whiptail Lizards (Cnemidophorus abaetensis and Cnemidophorus ocellifer) from Northeastern Brazil. Journal of Herpetology 38: 586-588. [ Links ]
9. Galdino, C.A.B.; Pereira, E.G.; Fontes, A. & Van Sluys, M. 2006. Defense behavior and tail loss in the endemic lizard Eurolophosaurus nanuzae (Squamata, Tropiduridae) from southeastern Brazil. Phyllomedusa 5: 25-30. [ Links ]
10. Garshelis, D.L. 2000. Delusions in habitat evaluation: measuring use, selection, and importance: 111-164. En: Boitani, L.I. & Fuller, K. (eds), Research Techniques in Animal Ecology: Controversies and Consequences. Columbia University Press. New York. [ Links ]
11. Grover, M.C. 1996. Microhabitat use and thermal ecology of two narrowly sympatric Sceloporus (Phrynosomatidae) lizards. Journal of Herpetology 30: 152-160. [ Links ]
12. Halloy, M.; Etheridge, R. & Burghardt, G.M. 1998. To bury in sand: phylogenetic relationships among lizard species of the boulengeri group, Liolaemus (Reptilia: Squamata: Tropiduridae), based on behavioural characters. Herpetological Monographs 12: 1-37. [ Links ]
13. Holm, S.A. 1979. A simple sequential rejective multiple test procedure. Scandinavian Journal of Statistics 6: 65-70. [ Links ]
14. Huey, R.B.; Pianka, E.R. & Schoener, T.W. 1983. Lizard Ecology. Studies of a Model Organism. Harvard University Press, Massachusetts. [ Links ]
15. Johnson, G. 2000. Spatial ecology of the eastern massasauga (Sistrurus c. catenatus) in a New York peatland. Journal of Herpetology 64: 186-192. [ Links ]
16. Kacoliris, F.P.; Celsi, C.E. & Monserrat, A.L. 2009a. Microhabitat use by the sand dune lizard Liolaemus multimaculatus in a pampean coastal area in Argentina. Herpetological Journal 19: 61-67. [ Links ]
17. Kacoliris, F.P.; Guerrero, E.; Molinari, A.; Moyano, B. & Rafael, A. 2009b. Run to shelter or bury into the sand? Factors affecting escape behaviour decisions in Argentinian sand dune lizards (Liolaemus multimaculatus). Herpetological Journal 19: 213-216. [ Links ]
18. Kacoliris, F.P.; Williams, J.D. & Molinari, A. 2010. Selection of key features of vegetation and escape behavior in the Sand Dune Lizard (Liolaemus multimaculatus). Animal Biology 60: 157-167. [ Links ]
19. Manly, B.L.; McDonald, L. & Thomas, D. 1993. Resource Selection by Animals. Statistical design and analysis for field studies. Chapman and Hall. London. [ Links ]
20. Mueller-Dombois, D. & Ellenberg, H. 1974. Aims and Methods of Vegetation Ecology. Wiley. New York. [ Links ]
21. Neu, C.W., Byers, C.R. & Peec, J.M. 1974. A technique for analysis of utilization availability data. Journal of Wildlife Management 38: 541-545. [ Links ]
22. Pledger, S.; Geange, J., Hoare, J. & Pérez-Matus, A. 2007. Resource Selection: Tests and Estimation using Null Models. disponible en: www.mcs.vuw.ac.nz/research/ publications/reports/mscs/mscs07-04.pdf [ Links ]
23. Rocha, C.F. 1991. Composicão do habitat e uso do espaco por Liolaemus lutzae (Sauria: Iguanidae) em uma área de Restinga. Revista Brasileira de Biologia 51: 839-845. [ Links ]
24. Stark, R.C.; Fox S.F. & Leslie Jr., D.M. 2005. Male Texas lizards increase daily movements and area covered in spring: A mate searching strategy? Journal of Herpetology 39: 169- 173. [ Links ]
25. Vega, L.E. 2001. Herpetofauna: diversidad, ecología e historia natural: 213-226. En: Iribarne, E. O. (ed.), Reserva de Biosfera Mar Chiquita: características físicas, biológicas y ecológicas. Editorial Martin. Mar del Plata. [ Links ]














