Introducción
La obesidad es una enfermedad crónica no transmisible que presenta una alta prevalencia a nivel mundial. La Organización Mundial de la Salud (OMS) ha informado que más de 1.900 millones de adultos en todo el mundo tienen sobrepeso y casi un tercio de esas personas padecen obesidad (1). En Argentina los datos publicados en la 4ta Encuesta Nacional de Factores de Riesgo (ENFR 2018) (2) describieron que la prevalencia de sobrepeso del 36,3%, se mantuvo constante con respecto a las tres ediciones previas y en cuanto a la obesidad se observó una prevalencia del 25,3%, resultando un incremento del 21,6% respecto del 2013 (3) y del 73,3% respecto del 2005 (4).
La obesidad es una enfermedad de origen multifactorial caracterizada por un aumento anormal del tejido graso, secundario a un dese-quilibrio entre el consumo y gasto energético, que conlleva riesgos para la salud (5). El aumento en la ingesta de alimentos calóricos de pobre calidad nutricional en detrimento del consumo de alimentos saludables, combinado con el creciente estilo de vida sedentario, enmarcado en un ambiente obesogénico, determinan la necesidad de un abordaje complejo e interdisciplinario de la patología (1). El exceso de peso constituye un factor de riesgo para el desarrollo de enfermedades no transmisibles (ENT) tales como enfermedades cardiovasculares, accidentes cerebrovasculares, diabetes tipo 2, osteoartritis, algunos tipos de cáncer, entre otras (6).
En relación al tratamiento para la obesidad, las Guías de Práctica Clínica nacionales (7) establecen un abordaje multidisciplinario, que contempla los aspectos psicológicos y la actividad física junto con el tratamiento nutricional. En relación con el tratamiento dietoterápico, la restricción energética continua (REC) es la estrategia nutricional más elegida, consistiendo en una disminución de aproximadamente 600 kcal diarias, sostenida por al menos 12 meses (7). Hay evidencia suficiente que demuestra que es posible un descenso de peso con esta metodología, y que produce una mejora del riesgo cardiometabólico (8,9). Uno de los aspectos más cuestionados de este tratamiento es la reganancia de peso luego de la intervención (10,11). Asimismo, las dietas muy restrictivas generan más abandono y menor adherencia, influyendo negativamente en los resultados (7). Por esta razón y ante el creciente aumento de la obesidad y la baja adherencia al tratamiento a largo plazo, se plantean continuamente nuevas estrategias terapéuticas, alternativas al tratamiento convencional, como es el ayuno intermitente (AI), aunque los resultados han sido controvertidos (12-14).
Existen diversos protocolos de ayuno intermitente. La gran mayoría consisten en restringir la ingesta de energía en diversos grados durante un período de tiempo predefinido, alternado con períodos de alimentación ad libitum (para satisfacer el apetito) o siguiendo un plan alimentario preestablecido (12,15-18). La diferencia principal entre ellos, es la duración y frecuencia de los ciclos de ayuno (19). Los protocolos existentes son:
alimentación restringida en el tiempo (ART),
ayuno de días alternos (ADA),
ayuno 5:2,
ayuno periódico y dieta que imita el ayuno (DIA)
Si bien estos son los patrones generales, existe una diversidad de adaptaciones a los mismos donde varían los tiempos y las características cuali-cuantitativas de la alimentación (14).
La alimentación restringida en el tiempo o alimentación restringida es un término que se utiliza para referirse a la alimentación en ventanas específicas de tiempo. Frecuentemente el fin último es sincronizar la ingesta de alimentos con el reloj circadiano (20). Se pueden distinguir dos variantes: alimentación temprana (early-TRF, por sus siglas en inglés) y alimentación tardía (mid-day TRF). La alimentación temprana es una forma de ayuno intermitente que implica comer temprano en el día para estar en alineación con los ritmos biológicos del metabolismo (21). En esta última, la ventana de ingesta suele ser de 8 horas, mientras que en la tardía abarca 12 horas, admitiendo posibles variaciones (21). Este enfoque pretende restringir completamente la ingesta de alimentos a una ventana temporal dentro de la fase de vigilia, extendiendo el ayuno nocturno (22), siendo práctica común omitir el desayuno o la cena (23). Este protocolo de ayuno permite a los individuos consumir una ingesta de energía ad libitum, no necesariamente implicando restricción calórica (10).
La restricción energética de días alternos, comúnmente llamada ayuno de días alternos consiste en un día de ayuno alternado con un día de alimentación (24). En los días de ayuno no se consumen calorías y los días de realimentación pueden ser ad libitum (25,26) o con ingesta controlada (27). La dificultad de completar un día total de ayuno exigió su adaptación, surgiendo así el ayuno modificado de días alternos (23). En esta modalidad, el término ayuno se utiliza para describir períodos de severa restricción de ingesta en lugar de ninguna ingesta energética (25). En general se limita al 20-25% de las necesidades energéticas en los días de ayuno regularmente programados (8,18,24,25,28-31). El aporte energético suele provenir de una comida diaria, frecuentemente el almuerzo (18).
Otra alternativa de esta práctica es la dieta denominada 5:2, caracterizada por dos días consecutivos o no consecutivos de ayuno (24). Estos últimos días involucran una restricción energética severa, generalmente del 75%, seguidos de 5 días de alimentación ad libitum (16,22,25,32-34).
Por otra parte, el ayuno periódico dura 2 o más días con una realimentación calórica habitual (19). A diferencia del protocolo 5:2, esta práctica se lleva a cabo cada dos o más semanas (35).
La dieta que imita el ayuno (DIA) sugiere seguir ciclos de ayuno de 5 días continuos separados por 25 días de dieta habitual (19). Se caracteriza por ser bajo en calorías, azúcares y proteínas, pero alto en grasas insaturadas (36). Este protocolo demanda una restricción de entre 25-50% del gasto energético total (GET) durante 5 días. La duración de su práctica es muy diversa, pudiendo prolongarse de dos semanas a seis meses (23).
Por lo expuesto anteriormente, consideramos de importancia evaluar la efectividad del ayuno intermitente en cualquiera de sus formas, sobre el descenso de peso y la mejora de variables cardiometabólicas en comparación con la restricción energética continua, como una alternativa terapéutica en el descenso de peso.
Materiales y método
Estrategia de búsqueda
Se siguieron los lineamientos metodológicos para realizar revisiones sistemáticas de PRISMA. La estrategia de búsqueda se ha llevado a cabo en las bases electrónicas de datos PubMed y Cochrane Library con la siguiente combinación de términos MeSH y palabras clave: “‘alternate day fast*’’’, ‘’intermittent fast*’’, ‘’time restricted fast*’’, ‘’modified fast*’’, ‘’mimicking fast*’’, ‘’alternate day diet”,‘’alternate day modified fast*’’, ‘’weight loss’’, ‘’obes*’’, ‘’body composition’’, ‘’lipid profile’’, ‘’glycemic’’, ‘’blood pressure’’. La búsqueda se realizó en el período comprendido entre 2015 y 2020.
Selección de estudios y extracción de datos
Se incluyeron estudios con las siguientes características: ensayos clínicos aleatorizados (ECA), realizados en hombres y/o mujeres, mayores de 18 años de edad, que incluyeran al menos 10 sujetos, con una duración mínima de 4 semanas y publicados a partir de 2015, que compararan ayuno intermitente con restricción energética continua, que evaluaran como variables de resultado el cambio en el peso o índice de masa corporal (IMC); alguna de las siguientes variables antropométricas: masa grasa (MG), masa libre de grasa (MLG), circunferencia de cintura (CC); y alguna de las variables cardiometabólicas bioquímicas: glucemia, insulinemia, índice del modelo homeostático de evaluación de resistencia a la insulina (HOMA-IR, por sus siglas en inglés), colesterol total (COL-T), lipoproteína de baja densidad (LDL), lipoproteína de alta densidad (HDL), triglicéridos (TAG); y clínicas: presión arterial sistólica (PAS) y presión arterial diastólica (PAD).
Se excluyeron aquellos estudios realizados en deportistas, mujeres embarazadas, pacientes con diabetes o con otras patologías de base que pudieran sesgar las variables en estudio. También se excluyeron aquellos que contemplaron la variable actividad física como estrategia de intervención. No se incluyeron estudios piloto.
La búsqueda fue realizada por dos de los autores de manera independiente. De cada estudio se extrajo: autor, año, características de la población, número de individuos, duración de la intervención, tipo de intervención y comparador, las variables antropométricas y cardiometabólicas antes mencionadas.
Resultados
Estudios incluidos
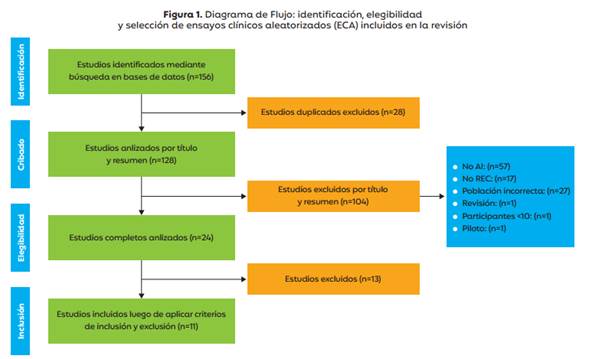
En la búsqueda inicial fueron incluidos un total de 156 artículos publicados en los últimos 5 años. Luego de descartar los duplicados, se revisaron 128 por título y resumen. Se eliminaron 104 por diferentes causas nombradas en la Figura 1. Posteriormente se analizaron los textos completos de 24 estudios según los criterios de inclusión y exclusión, dando como resultado 11 ensayos clínicos aleatorizados. De los ECA que se incluyeron, seis utilizaron como protocolo de ayuno intermitente ADA (28,37-40) y cinco el denominado 5:2 (16,17,34,41,42).
Características de los estudios
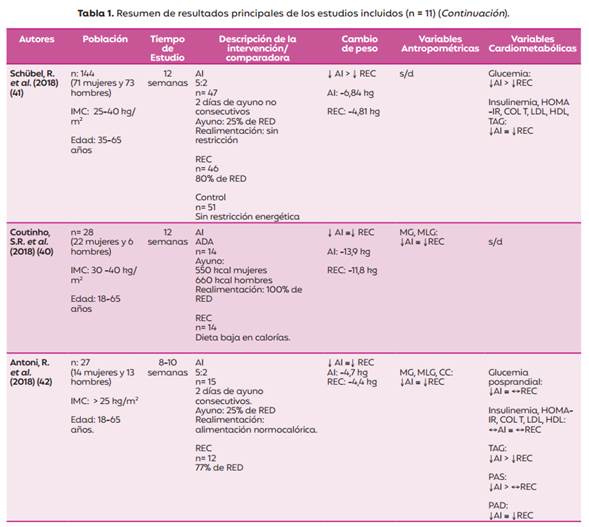
El tamaño muestral de los estudios que fueron incluidos varió de 27 a 146 participantes, con una mediana de 69 individuos (RIQ: 37; 112). De los once artículos incluidos, tres de ellos fueron realizados únicamente en mujeres, mientras que el resto abarcó ambos sexos. La edad mínima de los participantes fue de 18 años y la edad máxima de 75 años. El IMC más bajo contemplado fue 25 kg/m2 teniendo todos los individuos sobrepeso u obesidad. El tiempo de duración de las intervenciones dietéticas presentó una mediana de 12 semanas con un mínimo de 4 semanas y un máximo de 48 semanas (Tabla 1).
Intervenciones dietéticas
De los cinco estudios que realizaron el protocolo 5:2, dos hicieron ayuno en días consecutivos (34,42), otros dos en días no consecutivos (17,41) y en uno (16) los participantes podían elegir hacerlo indistintamente. La restricción energética fue del 75% en dos de ellos (41,42), mientras que en el resto se definió un aporte calórico de entre 400 y 600 kcal (16,17,34). En cuatro artículos, la ingesta en los días de realimentación fue la habitual de cada sujeto (16,17,41,42) y en la restante, se prescribió un déficit de 500 kcal (34). La restricción energética continua con la que se comparó este protocolo de ayuno, fue de un déficit de 500 kcal en un artículo (34), una restricción del 20% al 23% en otros dos (41,42), y asignándole una ingesta de 1000 kcal a mujeres y de 1200 kcal a hombres en otro caso (16). Mientras que, en el estudio restante, la restricción fue proporcionalmente similar al grupo de ayuno (17).
Seis artículos llevaron adelante el protocolo de ADA (28,29,37-40). Para los días de ayuno, en cinco estudios se prescribió una restricción de entre el 63% y 75% (28,29,37-39), en el restante se estableció una ingesta de 550 kcal para mujeres y 660 kcal para hombres (40). La ingesta en los días de realimentación fue heterogénea: en tres de ellos se determinó el consumo del 100% de los requerimientos energéticos para todos los días de realimentación (28,38,40), admitiendo Parvaresh A. et al. un día de alimentación ad libitum. En el estudio de Trepanowski J.F. et al. (29) la misma fue del 125%. Por último, en los artículos de Liu B et al. y Hutchison A.T. et al. (37,39) se realizaron dos intervenciones de realimentación simultáneamente, una cubriendo el 100% de los requerimientos y la otra, el 145%. Con respecto al comparador, la restricción energética continua, se llevó a cabo cubriendo entre el 70% y 75% de los requerimientos (28,29,37-39) en todos los estudios, excepto Coutinho S.R. et al. (40) que refiere haber prescrito una dieta baja en calorías, sin especificar el rango calórico.
Cambios en el peso corporal
En cuanto a la variable principal estudiada, cambio de peso corporal, los resultados de siete (16,17,29,34,38,40,42) de los once ECA concluyeron que, si bien ambas ramas alcanzaron un descenso de peso significativo, no presentaron diferencias estadísticamente significativas entre ellas y en uno de los estudios el valor de significación estadística fue borderline (p=0,053) (41). Por el contrario, los tres ECA restantes (28,37,39) determinaron que el protocolo de AI logró un mayor descenso de peso comparado con la REC.
La intervención de AI mostró un valor mínimo de descenso de peso de 1,8 kg en 4 semanas, y un máximo de 13,9 kg en 12 semanas, con una mediana de 5,5 kg (RIQ: 4,7; 6,8 kg). Mientras que, en los sujetos que realizaron REC, el descenso de peso mínimo fue de 1,7 kg en 8 semanas, el máximo de 11,8 kg en 12 semanas, con una mediana de 4,8 kg (RIQ: 3,8; 6,6 kg). En la Figura 2 se describen los promedios de descenso de peso comparando AI con REC de cada uno de los estudios incluidos.
Otras variables antropométricas
En diez de los once estudios se analizaron diferentes variables antropométricas. En cuatro estudios (17,28,34,38) se evaluó el IMC dando como resultado un descenso significativo en ambas ramas, sin presentar diferencias estadísticamente significativas entre ellas.
La circunferencia de cintura (CC) disminuyó en la intervención y en el grupo comparador en los seis ECA donde se analizó la variable (17,28,34,38,39,42). En cinco de ellos, las diferencias entre los grupos no fueron estadísticamente significativas (17,34,38,39,42) y en uno (28), la intervención de AI logró mejores resultados.
En cuanto a la composición corporal, se evaluaron la masa grasa y la masa libre de grasa en siete (16,29,37-40,42) y cinco (16,29,38,40,42) estudios respectivamente. Ambas variables disminuyeron en todos los casos, sin presentar diferencias estadísticamente significativas entre AI y REC; excepto en dos estudios (37,39) donde el protocolo de AI resultó en una mayor reducción de masa grasa.
Variables cardiometabólicas
En siete estudios (16,17,28,29,34,39,41) se contemplaron variables cardiometabólicas, aunque no se evaluaron las mismas en todos los casos.
Se analizaron los cambios en la glucemia basal luego del tiempo de intervención. Considerando exclusivamente los resultados intragrupo de AI, tres de siete ECA reportaron un descenso estadísticamente significativo de glucemia basal (28,39,41). En dos de los siete ECA (28,41), los participantes de la rama AI presentaron valores estadísticamente significativos más bajos de glucemia basal que los de la rama REC. Asimismo, en cuatro estudios los valores se mantuvieron constantes, sin manifestar diferencias estadísticamente significativas entre grupos (16,17,29,39). En el caso restante, fue el protocolo de REC el que logró un descenso estadísticamente significativo con respecto al AI (34).
En cuatro ECA de los seis que evaluaron insulinemia, se reportó un descenso estadísticamente significativo de la variable en el grupo AI (28,29,39,41) mientras que dos mantuvieron constantes los valores (34,42). La misma tendencia se observó en la rama REC, aunque en ningún caso se encontraron diferencias estadísticamente significativas entre la intervención y el comparador.
El índice HOMA-IR fue evaluado en siete ECA (28,29,34,37,39,41,42). En la rama AI, se evidenció una mejora estadísticamente significativa respecto de los valores basales en seis de siete estudios (28,29,34,37,39,41). Mientras que en el grupo REC, fueron cuatro los estudios que mostraron mejoras estadísticamente significativas (29,34,39,41), y en los restantes estudios la variable no se modificó (28,37,42). No se encontraron diferencias estadísticamente significativas entre AI y REC.
Al considerar el perfil lipídico, se evaluaron COL-T, LDL, HDL y TAG. Tres de siete ECA reportaron un descenso estadísticamente significativo de colesterol total (28,39,41) al implementar la intervención de AI. En seis ECA (16,28,29,34,41,42), no hubo diferencias estadísticamente significativas entre AI y REC en los niveles de COL-T, exceptuando una publicación donde AI obtuvo mejores resultados (39). Mientras que de los siete estudios (16,17,28,29,39,41,42) donde se analizaron los niveles de LDL y HDL, solamente uno (39) presentó diferencias estadísticamente significativas en la primera variable y otro en la segunda (29), obteniendo mayores beneficios los sujetos que realizaron el AI. Siete de ocho estudios presentaron una disminución estadísticamente significativa respecto de los valores basales de TAG en la intervención de AI (16,28,29,34,39,41,42). Solamente exhibieron diferencias estadísticamente significativas dos ECA (39,42), donde el AI presentó un descenso mayor que el comparador.
Variables clínicas
Las únicas variables clínicas incluidas en la presente revisión fueron la PAS y la PAD. Cinco ECA (17,28,29,34,42) reportaron que no se encontraron diferencias estadísticamente significativas entre grupos, manteniéndose sin cambios los valores de PAD. Mientras que, respecto a la PAS, únicamente dos estudios reportaron un descenso superior al llevar a cabo el AI (28,42).
Comparación indirecta de protocolos de AI en el descenso peso
La presente comparación indirecta sobre la efectividad en el descenso de peso se corresponde sólo a los protocolos ADA vs. 5:2, dado que son los que se utilizaron en los ECA incluidos en la presente revisión. Fueron cinco (16,17,34,41,42) los ECA que utilizaron el protocolo 5:2 y seis el ADA (28,29,37-40).
En el protocolo de ADA, el descenso de peso mínimo fue de 4,1 kg en ocho semanas, el máximo fue de 13,9 kg en doce semanas, con una mediana de 6 kg (RIC: 5,3; 6,8 kg). En el protocolo de 5:2, el peso mínimo perdido fue de 1,8 kg en cuatro semanas, el máximo de 9,1 kg en 24 semanas, con una mediana de 5 kg (RIC: 4,1; 7,9 kg).
Discusión
Cambios de peso corporal
Los resultados hallados en la presente revisión concluyen que el AI es una estrategia dietoterápica eficiente para la pérdida de peso. Sin embargo, en la mayoría de los estudios no demostró superioridad con respecto a la REC. Los resultados de este trabajo concuerdan con revisiones sistemáticas y metaanálisis previos, donde se reportó una pérdida de peso similar para la intervención AI en comparación con la REC (12,14,15,24,43).
Las Guías de Práctica Clínica (GPC) establecen que una pérdida de peso inicial del 5 al 10% se asocia a una mejora de los factores de riesgo para ENT (7). Según el presente estudio, el descenso de peso se logra en todos los casos independientemente de la rama intervención o del comparador, siendo la mediana de descenso de peso del 6,6% para AI y 5,2% para REC. En la presente revisión, ocho (17,29,37-42) y siete (16,17,29,38,40-42) de los once ECA que utilizaron el protocolo de AI y REC respectivamente, se encontraron dentro del rango recomendado. La mediana del descenso de peso fue similar a la descripta en estudios anteriores (14,15), aunque se reportaron valores extremos alejados de la misma. Esto podría deberse a aspectos internos de cada ECA como por ejemplo la duración de la intervención, forma de implementación y control de las intervenciones dietéticas.
Debido a que en todos los ECA las intervenciones de AI se realizaron con un balance energético negativo, no se puede diferenciar si la pérdida de peso alcanzada es exclusivamente debida a la modalidad del protocolo o a la restricción calórica que este implica (8). Estudios analizados en esta revisión (16,29,39), reportan que los sujetos que realizaron AI redujeron su ingesta en los días de realimentación, logrando un balance energético neto negativo aún menor que el prescripto. Esto coincide con lo reportado previamente en otras revisiones (24,33).
Analizando la composición corporal, en investigaciones anteriores (12,15,24) se han reportado resultados similares a los del presente estudio. Se reportó una disminución de masa grasa al implementar el AI en comparación con la REC, aunque sin diferencias estadísticamente significativas entre grupos. Estos resultados podrían deberse al descenso de peso logrado independientemente del protocolo implementado. Con respecto a la MLG, se demostró una disminución estadísticamente significativa de la variable tanto para la intervención como para el comparador en todos los casos. Estos resultados no coincidieron con lo reportado en revisiones previas donde se reportó una mayor conservación de la misma al implementar AI en comparación con REC (8,10,44).
Variables cardiometabólicas
Tanto el AI como la REC demostraron un impacto similar en las variables cardiometabólicas contempladas. En la presente revisión, no existe una tendencia que demuestre un beneficio superior en cuanto a la mejora de estas variables en comparación con la REC. En consonancia con este estudio, investigaciones anteriores concuerdan en líneas generales en esta falta de superioridad de AI sobre REC (15,18,24,43).
En cuanto a la glucemia, estudios anteriores (8) reportaron resultados favorables para la intervención de AI. En este trabajo se ha descripto que algunos estudios demostraron mayores beneficios al implementar el AI mientras que otros no manifestaron cambios. Solo un ECA demostró superioridad de la REC (34). Estudios incluidos en la presente revisión que analizaron los valores de insulinemia, demostraron un descenso de la misma en la mayoría de los casos. Sin embargo, no fue posible demostrar mayor efectividad por parte del AI en comparación con la REC. En contraposición, en revisiones anteriores (8,14), se evidenció una mejora significativa de insulinemia al implementar AI en comparación con REC. Los mismos autores adjudicarían este efecto a los cambios antropométricos consecuentes a la pérdida de peso (8,14). En cuanto al índice HOMA, los datos de la presente revisión demuestran una tendencia a una mejora significativa en comparación con los datos de la línea de base, pero no una superioridad del AI sobre la REC.
Con respecto al perfil lipídico, los resultados obtenidos no manifestaron una clara superioridad por parte de ninguna de las dos intervenciones, asimismo, estos resultados coinciden con estudios previos (14,24,33,43).
Variables clínicas
En concordancia con la revisión realizada por Cioffi I et al.(24) los valores de PAS y PAD no presentaron cambios significativos entre la intervención y el grupo comparador. Cabe aclarar que estas variables no fueron medidas en la mayoría de los ECA incluidos en este estudio ni en los estudios anteriores.
Comparación indirecta de protocolos de AI: ADA vs. 5:2
Los seis estudios que utilizaron el protocolo de ADA (28,29,37-40) como los cinco que realizaron el denominado 5:2 (16,17,34,41,42) lograron un descenso estadísticamente significativo de peso. Por otro lado, al comparar la efectividad en el descenso del peso, de los cuatro ECA que resultaron en una superioridad del protocolo de AI por sobre la REC, tres corresponden al protocolo ADA (28,37,39) y uno al 5:2 (41).
Considerando los datos de la intervención dietética proporcionados por los ECA de la presente revisión, se ha podido detectar mayor restricción energética semanal en todos los estudios que realizaron el protocolo de ADA comparado con la intervención 5:2, que conllevó a su vez a una mayor pérdida de peso. De igual modo, estas son tendencias basadas en los ECA analizados, se requieren futuros estudios que realicen una comparación directa de estos protocolos para poder arribar a conclusiones fehacientes.
Fortalezas y limitaciones
Este estudio se basa en la comparación del AI con la REC, intervención actualmente recomendada por las GPC para el tratamiento del sobrepeso y la obesidad, contribuyendo de este modo con información actualizada a esta problemática mundial de salud. Se incluye también la comparación indirecta de protocolos de AI utilizados en los ECA incluidos en esta revisión, lo que constituye un aspecto novedoso de la misma. Si bien no hay evidencia suficiente para dar conclusiones certeras, busca sentar bases para investigaciones futuras. La falta de uniformidad al implementar los diferentes protocolos de AI, encontrándose múltiples variantes de ayuno y realimentación, junto con tiempos acotados de investigación, tamaños muestrales pequeños, imposibilidad para determinar el balance energético real debido a términos ambiguos, conforman las limitaciones de la presente revisión.
Además, no fue posible comparar todos los tipos de protocolo de AI existentes con la REC debido a que las investigaciones no cumplían los criterios de inclusión y por la escasa evidencia actual.
Conclusión
Está revisión concluye que el AI como intervención dietoterápica es eficiente para el descenso de peso en población con sobrepeso y obesidad sin patologías asociadas, en el corto plazo. No fue posible evaluar la efectividad del AI en el largo plazo. En cuanto a la comparación indirecta de los protocolos de AI, ADA demostraría una mayor efectividad con respecto al protocolo 5:2 en el descenso de peso.
No es posible determinar la superioridad del AI con respecto a la REC en el cambio de peso, otras variables antropométricas ni en los efectos en la salud cardiometabólica. Futuros estudios serán necesarios para arribar a resultados concluyentes.