Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Geoacta
versión On-line ISSN 1852-7744
Geoacta v.35 n.1 Ciudad Autónoma de Buenos Aires ene./jun. 2010
Optimizacion de una técnica para la detección de patologías virales en Pleoticus Muelleri (Bate, 1988) en el estuario de Bahía Blanca, Argentina
Ana M. Roccamo1,3, Patricia M. Cervellini3*, M. Cintia Piccolo2,3 y Francisco J. Barrantes1,3
1CONICET - Instituto de Investigaciones Bioquímicas de Bahía Blanca
2CONICET- Instituto Argentino de Oceanografía,
3Universidad Nacional del Sur
aroccamo@criba.edu.ar, pcervell@uns.edu.ar
RESUMEN
La comercialización de animales acuáticos require la implementación de controles sanitarios para la detección de virus patógenos estipulados por la Organización Mundial para la Salud Animal (OIE). De acuerdo con sus normas, y específicamente en lo que se refiere la comercialización de crustáceos, la OIE determina como enfermedades de declaración obligatoria, entre otras, a las denominadas: virus del síndrome de la mancha blanca (WSSV), virus de la cabeza amarilla (YHV) y el virus del síndrome de Taura (TSV), las cuales son altamente peligrosas. El objetivo de este estudio fue determinar la presencia o ausencia de estas virosis en poblaciones de langostinos silvestres (Pleoticus muelleri) en el estuario de Bahía Blanca, aplicando metodologías bioquímicas, de biología molecular y genéticas. Los resultados demuestran que se ha logrado optimizar la metodología para la extracción y purificación de ADN y ARN de tejido y hemolinfa de langostinos y el correcto manejo en la captura, acondicionamiento y transporte de los animales al laboratorio. Los ensayos fueron debidamente convalidados por reacciones de control negativas y positivas. En las muestras estudiadas de Pleoticus muelleri se descarta la presencia de estas tres enfermedades virales. Esta metodología permite no sólo realizar una detección temprana y un diagnóstico de las tres patologías virales sino también establecer y asegurar un status libre de infección con el consiguiente beneficio sanitario para la región.
Palabras Clave: Virus; Pleoticus muelleri; WSSV; TSV; YHV
ABSTRACT
Trade in aquatic animals calls for the implementation of controls for the detection of pathogenic viruses in line with the regulations of the OIE, the World Organization for Animal Heath. In relation specifically to trade in crustaceans, the OIE identifies the following diseases: White Spot syndrome virus disease (WSSV); Yellow Head Virus disease (YHV); and Taura syndrome virus disease (TSV), all of which are highly dangerous. The purpose of this study was to determine whether these viruses occur in wild populations of Pleoticus muelleri in Bahía Blanca estuary, Argentina, using biochemical, molecular biology and genetics methods. The results show that the methods used for DNA and RNA extraction and purification from the tissue and hemolymph of these crustaceans, and the techniques for their capture, packaging and transportation to the laboratory have been optimized. Tests were properly validated by negative and positive controls. None of the named diseases were found in the wild populations of Pleoticus muelleri. The methodology followed in the present research not only enables early detection and diagnosis of the three viral pathologies but also ensures an infection-free status with the concomitant health benefits for the region.
Key words: Virus; Pleoticus muelleri; WSSV; TSV; YHV
INTRODUCCIÓN
La camaronicultura en América Latina ha sido una de las actividades económicas de mayor crecimiento productivo y económico durante los últimos15 anos. Esta actividad ha pasado por diversas dificultades de tipo sanitario y ecológico. Países como Ecuador, Méjico y Brasil han logrado niveles de desarrollo sobresalientes y presentan importantes posibilidades de incrementar su potencial productivo. Se destacan, en particular, Méjico y Brasil donde existen enormes extensiones susceptibles de ser dedicadas a esta actividad. Otros países como Colombia, Venezuela y Perú que también tienen un gran potencial, están incursionando en este rubro y avanzando rápidamente. Este es el caso de Argentina, país en el que existen especies excelentes para el desarrollo de esta actividad a pesar de estar actualmente en una etapa incipiente (Fenucci et al., 2002, Martinez et al., 2008) Pleoticus muelleri Bate es uno de los crustáceos decápodos más explotados comercialmente en toda la costa del Mar Argentino y sobre el cual se están llevando a cabo estudios con miras a su utilización en acuicultura (Martorelli, 2002; Harán et al., 2004, Mallo y Fenucci, 2004).
Este camarón es de hábitos bentónico demersales, vive aproximadamente dos anos y se distribuye desde los 23o00´ S (Río de Janeiro, Brasil) hasta el norte de la Patagonia 42o45 S (Boschi, 1997). Se pesca de junio a marzo en el litoral patagónico y en la costa de la provincia de Buenos Aires. La zona más importante de pesca se halla en las aguas del Golfo San Jorge (provincia de Santa Cruz). Las capturas máximas permisibles alcanzan 15000 tn y están reguladas por el Instituto Nacional de investigación y Desarrollo Pesquero (INIDEP) y el Ministerio de Asuntos Agrarios perteneciente a la provincia de Buenos Aires. Las enfermedades virales han impactado severamente en la industria camaronera del mundo, causando pérdidas significativas en su producción (Lightner, 1999, Bayot et al., 2008). En 1996 se reportaron 20 enfermedades virales que infectan a especies de camarones silvestres o de cultivos (Lightner, 1996). En el continente americano los principales virus que han sido identificados en las poblaciones de camarones son: el síndrome de Taura (TSV), el virus de la necrosis infecciosa hipodérmica y hematopoyética (IHHNV), de la mancha blanca (WSSV) y el virus de la cabeza amarilla (YHV) (Bonami et al., 1997, Chapman et al., 2004, Mc Clennen, 2004, Lotz et al., 2005, Boada, et al., 2008, Hasson et al., 2009, Lotz et al., 2005, Martorelli et al., 2010).
El interés en la comercialización de animales acuáticos motiva la implementación y desarrollo de controles sanitarios requeridos obligatoriamente por la Organización Mundial de Sanidad Animal (OIE, 2008). Esta entidad elabora y establece las normas aplicables al comercio internacional de animales vivos, acuáticos o terrestres y sus productos. De acuerdo con estas normas, específicamente, en lo que se refiere a la comercialización de crustáceos, la organización determina como enfermedades de declaración obligatoria, entre otras, a las denominadas: virus del síndrome de la mancha blanca (WSSV), virus del síndrome de Taura (TSV) y el virus de la cabeza amarilla (YHV) (OIE, 2008). Estas enfermedades de naturaleza viral son consideradas por la OIE como enfermedades patógenas extremadamente peligrosas que impiden su comercialización e ingesta. Para el diagnóstico se utilizan diferentes técnicas, las más usadas son hibridación in situ, anticuerpos monoclonales y de biología molecular como la reacción de la polimerasa en cadena (PCR). Las técnicas de biología molecular son las de mayor especificidad y sensibilidad y aunque requieren una infraestructura más compleja para su implementación se las prefiere a los métodos tradicionales. Existen numerosos estudios en la literatura que reportan sobre el uso de técnicas para detectar la presencia de virus en poblaciones de peneidos en cautiverio. Sin embargo, son muy escasos los trabajos en poblaciones silvestres (Boada, et al., 2008).
En el estuario de Bahía Blanca (FIG. 1) existe una importante comunidad pesquera artesanal y comercial, que desarrolla su actividad utilizando principalmente los puertos de Ingeniero White y Coronel Rosales. Una de las especies que se capturan es el langostino Pleoticus muelleri que ingresa en el mercado de consumo de las principales ciudades de Argentina como Buenos Aires y Mar del Plata. Es importante senalar que en nuestra región los desembarcos anuales de langostinos alcanzaron en los anos 2006 y 2007 las cifras de 93,6 y 21,9 tn (SAGPyA, 2008). Si bien estas cifras son menores a la producción total del país, significan un aporte importante en la provincia de Buenos Aires. Para lograr una mejor comercialización y exportación de este recurso se requiere del relevamiento de las patologías virales determinadas por la OIE (2008) que permitan establecer y asegurar un status libre de infección en la población de langostinos natural del estuario. Hasta el presente se ha reportado un solo trabajo sobre las enfermedades virales en crustáceos en el estuario de Bahía Blanca con técnicas realizadas en otros países (Martorelli et al., 2010). Por lo tanto, el objetivo de este trabajo fue optimizar una técnica de diagnóstico de estas enfermedades en esta especie en Argentina realizando el relevamiento de las tres patologías virales mencionadas anteriormente.

Figura 1. Localización del estuario de Bahía Blanca
MATERIALES Y MÉTODOS
Obtención de la muestra
Las ejemplares de langostinos fueron recolectados en el estuario de Bahía Blanca (38° 40' S; 62° 25' W) durante los meses de diciembre a junio del ano 2007 con redes de pesca camaroneras a bordo de lanchas de 14 m de eslora. Las muestras se tomaron en dos zonas típicas de captura de langostino en el estuario de Bahia Blanca Estas zonas son la zona externa del estuario y la denominada Riacho Azul (FIG. 1). Se capturó un total de 100 ejemplares adultos de un tamano estimado en 30 mm considerando el largo del caparazón sin el rostro. Las muestras no presentaron ejemplares enfermos, moribundos o con lesiones externas características de las virosis mencionadas. Los animales, luego de ser capturados se colocaron individualmente en bolsas plásticas, correctamente identificadas y envueltas en papel absorbente para evitar pérdida de material. Inmediatamente, las muestras fueron colocadas en hielo para su posterior procesamiento. De no ser así, los animales llegados al laboratorio se colocaron en doble bolsa, se congelaron en hielo seco y se mantuvieron en congeladora de -70°C.
Los controles positivos utilizados para la detección WSSV y TSV fueron adquiridos en el laboratorio del Dr. Donald V. Lightner (Texas Agricultural Experiment Station University of Arizona). El material genético adquirido consistió en dos entidades plasmídicas que contenían parte del genoma viral. El mismo fue ampliado y purificado para realizar los ensayos de PCR. El control positivo para la detección de YHV se obtuvo de pleópodos infectados originarios de Tailandia, enviados en etanol. Cada ejemplar fue procesado en el laboratorio para el aislamiento y purificación del ARN utilizado en los ensayos de RT-PCR. En éstas condiciones, además de su perfecto estado de conservación, todo el material recibido carece de capacidad infectiva para humanos o animales.
Obtención de ADN
Para la extracción de ADN de tejido, se emplearon ejemplares vivos, enfriados en hielo, congelados y/o preservados en alcohol. Una porción del tejido fue macerada con N2 líquido hasta la obtención de un polvo fino, del cual se utilizaron 100 a 200 mg. A la muestra, colocada en un tubo de centrífuga se le agregó 600ml de buffer de lisis: 100 mM NaCl, 10 mM tris/Cl, pH8, 25mM EDTA, 0,5% de SLS (N-lauril sarcosinato de Na) ó 2% de SDS (dodecilsulfato de Na) y 0,5 mg/ml de proteinasa K. Se incubó a 65°C durante 1h y se agregaron inmediatamente 100ml de NaCl 5M y 70 ml de CTAB (bromuro de hexadeciltrimetil amonio) 10% / en 0,7M de NaCl. Luego de 10 minutos se agregó un volumen igual de cloroformo/alcohol isoamílico 24:1, mezclando suavemente. Se centrifugó a 13.000xg por 5 minutos y al sobrenadante se le agregó 1x volumen de fenol. La fase superior se recuperó en un tubo, se agregaron dos volúmenes de cloroformo/alcohol isoamílico 24:1 y en el sobrenadante el ADN fue precipitado por el agregado de 2 volúmenes de etanol absoluto en frío. El precipitado de ADN se lavó con etanol al 70% y luego de un período de secado se resuspendió en 100 ml de agua bidestilada estéril. El ADN obtenido se cuantificó por espectrofotometría a 260 nm y se evaluó la pureza por la relación 260 nm/280 nm.
Obtención de ARN
Para la extracción de ARN de hemolinfa se utilizaron animales descongelados en hielo. De cada ejemplar se extrajeron entre 50ml - 100 ml. La muestra fue colocada inmediatamente en tubo de centrífuga con 175 ml del buffer de lisis (kit 2SV Total ARN Isolation System Promega2). El ARN se precipitó con etanol 95% y se purificó por medio de una columna de afinidad provista por la firma. Se eluyó con 100 ml de agua ultrapura libre de nucleasas y fue conservado a -70 °C hasta la realización de la reacción de RT-PCR. Para la obtención del ARN de tejido, se seccionó una porción del pleón de un ejemplar congelado. La muestra pulverizada (30mg) fue transferida a un tubo de centrífuga con 175 ml de buffer de lisis y beta -mercaptoetanol, diluída con 350ml de buffer, se incubó durante 3 minutos a 70°C. Luego de una centrifugación a 14000 xg el ARN se purificó por columna (2SV Total ARN Isolation System2). Se recuperó con un volumen de 100 ml de agua y se conservó a -70°C hasta su utilización en la reacción de RT-PCR.
Control del ADN de Crustáceos por PCR
Para evaluar el grado de pureza e integridad del ADN se realizó un ensayo de PCR con oligonucleótidos disenados para tal fin. Se utilizaron 0,4mg de ADN en 100ml de mezcla de reacción: Tris/ClH, pH 8,8, 50 mM de ClK, 1,5 mM de Cl2 Mg, 0,1% de Tritón X-100, 200 mM de cada dNTPs, 100 pmoles de cada cebador y 2 unidades de ADN polimerasa termoestable. Los cebadores:
143 F 5'-TGC CTT ATC AGC TNT CGA TTG TAG -3'
145 R 5'-TTC AGN TTT GCA ACC ATA CTT CCC-3'
son específicos para decápodos, producen un replicón de 848 bp y permiten verificar el estado de pureza e integridad del genoma aislado del crustáceo.
La reacción fue desarrollada según un programa de amplificación optimizado, con una concentración de MgCl2 de 1.5 mM y una temperatura de hibridación de 53°C, por 40 ciclos. Luego de la reacción, la muestra fue mantenida a 4°C hasta la realización de la electroforesis en un gel de agarosa al 1%.
Reacción de PCR de tejido de langostinos para el diagnóstico del virus de la mancha blanca (WSSV)
Se determinaron las condiciones óptimas de la reacción con el control positivo y luego se ensayaron las muestras de ADN aislado y purificado de animales capturados en el estuario. Para la reacción de PCR se utilizaron dos juegos de cebadores (según el Código OIE 2008):
a) 146 F1 5' ACT ACT AAC TTC AGC CTA TCT AG 3'
146 R1 5' TAA TGC GGG TGT AAT GTT CTT ACG A 3'
b) 146 F2 5' GTA ACT GCC CCT TCC ATC TCC A 3'
146 R2 5' TAC GGC AGC TGC TGC ACC TTG T 3'
La reacción se realizó en dos etapas, en la primera se usó: 2 ml ADN plasmídico,diluído 1:700, 200mM de c/u de los dNTPs, 10ml de buffer 10X (10mM Tris/ClH, pH 8.8, 50mM ClK, 1.5 mM Cl2Mg, 0.1% de Tritón X100),100 pmoles de cada cebador (a) y 2 unidades de ADN polimerasa estable en 100ml de volumen final. La reacción fue programada en un ciclador térmico, con una desnaturalización inicial de 5 minutos y 40 ciclos de 94°C por 30 segundos, una temperatura de hibridación de 53°C por 30 segundos y 68°C por 2 minutos, para la fase de síntesis. Finalizados los ciclos se programó una extensión adicional de 5 minutos a 68°C. El producto de esta reacción genera un replicón de 1447bp.
Utilizamos además el segundo par de cebadores (b) que hibridan en una secuencia interna al replicón anterior y permiten corroborar la presencia del virus por una técnica denominada PCR anidada (nested PCR). La reacción contiene: 10ml del producto de la PCR anterior como muestra patrón y la misma mezcla de reacción. Se utilizaron los cebadores 146F2 y 146R2 a la misma concentración, con el mismo protocolo de amplificación utilizado en la primera reacción de PCR. El resultado esperado es un amplicón de 941 bp. Ambos fueron corroborados en un gel de agarosa 1% con Bromuro de Etidio.
RT-PCR de tejido de langostinos para determinar la presencia del virus del sindrome de Taura (TSV)
Para la detección de esta virosis se utilizó hemolinfa y/o ARN total extraído de hemolinfa y de tejido. Para la reacción de RT-PCR se agregó 1ml de hemolinfa ó 10ml de ARN total (10 pg), Buffer AMV/Tfl 5x, 200mM de cada uno de los dNTPs, 1mM de SO4Mg, 50pmol de cada cebador, 5U de AMV (transcriptasa reversa) y 5U de Tfl (ADN polimerasa) en un volumen final de 50ml.
Los oligonucleótidos disenados para la detección de esta virosis son (según el Código OIE 2008):
9195 5' TCA ATG AGA GCT TGG TCC 3'
9992 5' AAG TAG ACA GCC GCG CTT 3'
El ciclador térmico fue programado primero para la síntesis de ADN y para la desnaturalización de la transcriptasa reversa: 45°C por 45 minutos y 94°C por 2 minutos. Luego se realizaron 40 ciclos de amplificación: 94°C por 30 segundos, 60°C por 1 minuto, 68°C por 2 minutos y una extensión adicional a 68°C por 7 minutos. Finalizado el programa de amplificación, se mantuvo la muestra a 4°C hasta la corrida electroforética en un gel de agarosa al 2%.
RT-PCR de hemolinfa de langostinos para la detección del virus de la cabeza amarilla (YHV)
Para la detección de esta virosis se utilizó el ARN de hemolinfa. La reacción de RT-PCR fue preparada según el protocolo utilizado para la detección del virus del sindrome de Taura. La estructura de los cebadores utilizados es:
10F 5' CCG CTA ATT TCA AAA ACT ACG 3'
144R 5' AAG GTG TTA TGT CGA GGA AGT 3'
El programa desarrollado para la reacción de la síntesis de ADN y la posterior amplificación responde al mismo protocolo seguido para TSV. No obstante, fue necesario modificar la temperatura de hibridación de acuerdo con la secuencia y cantidad de bases de los cebadores, establecida finalmente en 58°C. El amplicón característico que resulta de esta amplificación tiene un valor de 135 bp y fue corroborado en un gel de agarosa al 2%. La reacción se realizó en paralelo con un control negativo como en todos los casos.
RESULTADOS Y DISCUSIÓN
El resultado de las muestras de ADN y ARN obtenidas en el laboratorio con muestras de animales del estuario se presenta en la FIG. 2. La electroforesis fue realizada como control de la metodología y del manejo de las muestras. La línea 2 corresponde a una alícuota de la reacción de PCR con los cebadores específicos para decápodos (143F, 145R). Se muestra luego de la amplificación la obtención de un replicón de 848 bp, como se espera para un ADN no degradado.

Figura 2. Control de ADN y ARN de decápodos. 1) Marcador de peso molecular l/hind iii. 2) PCR del ADN aislado y purificado de animales del estuario. 3 y 4) resultados del aislamiento y purificación de ARN de hemolinfa. 5 y 6) resultados de distintas extracciones de ADN de langostinos.
Las líneas 3 y 4 muestran que la extracción de hemolinfa fue realizada sin danar tejidos y no muestra la presencia de ADN o ARN. Las líneas 4 y 5 corresponden a alícuotas de ADN purificado de langostinos utilizado para el control de la integridad de las muestras.
Resultado de la detección del virus de la mancha blanca (WSSV)
El resultado de la reacción de PCR optimizada para la detección del WSSV se presenta en la FIG. 3. En la línea 2 se utilizaron los cebadores146 F1/R1 sobre una muestra control (plásmido que contiene parte del genoma viral de WSSV). Se observa claramente el amplicón de 1447bp esperado. La línea 3 representa el resultado de la reacción de PCR anidada, utilizando 10ml de la reacción de PCR anterior (2) con los cebadores 146 F2/R2. Se obtuvo una sola banda de 941 bp, que demuestra la optimización de la técnica para la detección viral. Las líneas 4 y 5 corresponden a las reacciones 2 y 3 respectivamente con muestras de ADN de langostinos del estuario. Demostramos de esta manera la negatividad de la reacción y se descarta la presencia del virus en los animales controlados. En la línea 6 se sembró una alícuota del plásmido WSSV+, control amplificado y purificado en el laboratorio. Las líneas 7 y 8 corresponden a más ejemplares y las cuatro últimas líneas 12 a 15 corresponden a controles negativos (FIG. 3). Se demuestra la negatividad de la reacción y se descarta la presencia del virus en los animales controlados.
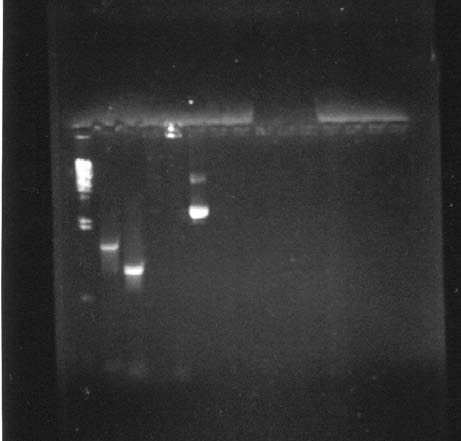
Figura 3. Detección y diagnóstico de WSSV. 1) Marcador peso molecular, 2) Control positivo WSSV (10ml reacción de pcr utilizando una dilución 1:700 del plásmido que contiene parte del genoma viral de WSSV con los cebadores 146 f1/r1, 3) Resultado de 10ml de reacción de PCR anidada. Se utilizaron 10ml de la reacción de pcr anterior (2) con los cebadores 146 f2/r2, 4 y 5) corresponden a las reacciones 2 y 3 realizadas con ADN de langostinos del estuario y 6) control WSSV+ (0,5ml del plásmido).
Resultado de la detección del virus del síndrome de Taura (TSV)
Los resultados de la reacción de RT-PCR sobre muestras de ARN de hemolinfa obtenida a partir de animales del estuario se muestran en la Fig 4. La línea 9 del gel de agarosa es el resultado de 10ml de la reacción de PCR desarrollada con plásmido que contiene parte del genoma viral de TSV+ con los cebadores 9195/9992. Se puede observar una única banda que junto con el resultado de la línea 3, certifica la validez de la reacción. El resultado de PCR con ADN de langostinos mostró la negatividad de la presencia viral.
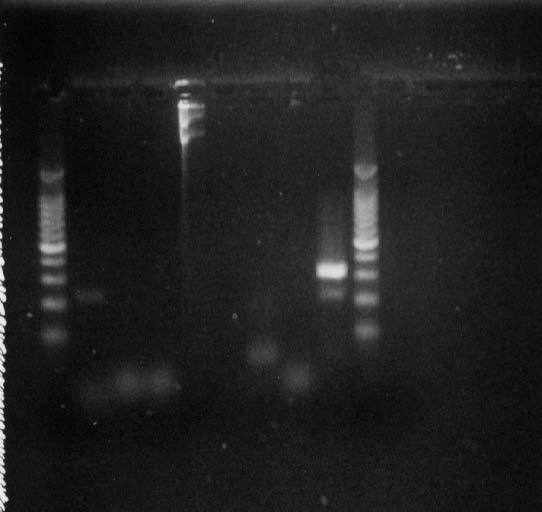
Figura 4. Detección del virus del síndrome de Taura. 1) Marcador 100bp DNA ladder de promega (4ml), 2) control negativo, sin el agregado de adn a la muestra de reacción, 3, 4, 7 y 8) muestras analizadas, 5) plásmido tsv+ (0,5ml), 6) muestra de ARN de hemolinfa, 9) resultado de la PCR con el plásmido tsv+ y los cebadores 9195/9992 y 10) marcador 100bp DNA ladder de promega (4ml).
Resultado de la reacción de PCR y RT-PCR para la detección de YHV
La línea 2 muestra el resultado de la reacción de RT-PCR con una muestra de ARN extraído de pleópodos infectados con el virus de la cabeza amarilla en un gel de Agarosa 2% (control positivo, Fig. 5). Se observa la banda del amplicón esperada estimada teóricamente en 135 bp, prueba de la optimización de la reacción. La posición 3 del gel fue sembrada con una alícuota de la reacción de RT-PCR que contenía ARN aislado de langostinos del estuario de Bahía Blanca. Se determina la negatividad de la reacción y se descarta la presencia viral. Para convalidar el ensayo se utilizó un control positivo externo dado para controlar la reacción de RT.

Figura 5. Reacción de PCR y RT-PCR para la detección de YHV. 1) Marcador de peso molecular 100 bp de promega. 2) RT-PCR de arn extraído de pleópodos infectados con el virus YHV (amplicón de 135 bp). 3) RT-PCR de ARN aislado de langostinos del estuario. 4) control positivo externo.
CONCLUSIONES
En el presente trabajo se optimizó la metodología de detección y diagnóstico de tres enfermedades virales de los langostinos: YHV, TSV y WSSV. Estas tres enfermedades fueron seleccionadas en base a la importancia que revisten para el consumo y comercialización de estos crustáceos de acuerdo a la declaración de la OIE (2008). En particular, su importancia para el consumo no está relacionada con la posibilidad de trasmitir al hombre sino solamente en el peligro que para la acuicultura representan los desechos de crustáceos que pueden transmitir el virus al medio ambiente, dado que se debe tener en cuenta que algunos de ellos (ej., WSSV) son resistentes al congelado.
Para ello se utilizó la técnica de PCR por ser la más sensible y específica para la detección de estas enfermedades virales. Los controles positivos y negativos realizados permiten convalidar el diagnóstico mediante esta técnica de biología molecular. Los resultados presentados demuestran que se ha logrado optimizar la metodología para la extracción y purificación de ADN y ARN de tejido y hemolinfa de langostinos y el correcto manejo en la captura, acondicionamiento y transporte de los animales al laboratorio. Los ensayos para la detección están debidamente convalidados por reacciones de control negativas y positivas. Los resultados de este trabajo permitirán realizar la detección temprana y el diagnóstico de las tres patologías virales. Esta metodología nos permitirá efectuar un futuro análisis exhaustivo de las especies silvestres para establecer el estado sanitario de estas especies en el estuario de Bahia Blanca y eventualmente la detección temprana de estas enfermedades patógenas con mayor precisión.
AGRADECIMIENTOS
Esta investigación fue financiada por el proyecto PGI TIR N° 24/TB06 otorgado por la Universidad Nacional del Sur, Argentina.
REFERENCIAS
1. Bayot ,B, Sonnenholzner S., Ochoa , X, J Guerrerro , J, Vera, T, Calderón , J, De Blas I, Cornejo-Grunauer , Mp. Stern , S Y Ollevier .F., 2008. An online operational alert system for the early detection of shrimp epidemics at the regional level based on real-time production. Aquaculture 277: 164-173. [ Links ]
2. Boada, M, Donato M.D. y Rodulfo H., 2008. Detection of the Infectious Hypodermal and Hematopoietic Necrosis Virus (IHHNV) in Asymtomatic Cultured White Shrimp, Litopenaeus vannamei (Boone), in Venezuela. Rev. Científica, FCV-LUZ . XVIII, No 1: 7 - 11. [ Links ]
3. Bonami, J.R.; Hasson, K.W.; Mari, J.; Poulos, B.T. and D.V. Lightner.,1997. Taura Syndrome of marine penaeid shrimp: characterization of the viral agent. J. Gen. Virol. 78: 313-319. [ Links ]
4. Boschi E.E., 1997. Las pesquerías de crustáceos decápodos en el litoral de la República Argentina. Invest. Mar. 25: 19-40. [ Links ]
5. Chapman, R. W., Browdy, Cl, Savin, S, Prior, S Y Wenner. E., 2004. Sampling and evaluation of white spot syndrome virus in commercially important Atlantic penaeid shrimp stocks diseases of aquatic organisms. Dis Aquat Org, 59: 179-185. [ Links ]
6. Fenucci, J.L., Mallo, J.C. Y Galarza, C.M., 2002. Larval culture and growth in ponds of the Argentine shrimp Pleoticus muelleri Bate (Crustacea, Penaeoidea). Aquaculture World Aquaculture Society. San Diego. California. USA, pág. 106. [ Links ]
7. Harán, N, Mallo Jc., Fenucci .J., 2004. Density influence on growth and development of the petasma in juvenile shrimps Pleoticus muelleri (Decapoda, Penaeoidea). Invest. Mar. 32(1): 11-18. [ Links ]
8. Hasson K.W., Lightner D.V., Mohney L.L., Redman R.M., Poulos B.T., Mari J. Y Bonami J.R., 2009. The geographic distribution of Taura Syndrome Virus (TSV) in the Americas: determination by histology and in situ hybridization using TSV-specific DNA probes. Aquaculture, 171:13-26. [ Links ]
9. Lightner D.V., 1999. A Handbook of Shrimp Pathology and Diagnostic Procedures for Diseases of Cultured Penaeid Shrimp. En: Lightner D.V. (Ed.). World Aquaculture Society, Baton Rouge, Louisiana, USA. 304 p. [ Links ]
10. Lightner, D.V., 1996. Epizootiology, distribution and the impact on international trade of two penaeid shrimp viruses in the Americas. Revue Scientifique et Technique Office International des Epizooties 15: 579-601. [ Links ]
11. Lotz J.M., Anton, L.S. y Soto M.A., 2005. Effect of chronic Taura syndrome virus infection on salinity tolerance of Litopenaeus vannamei. Dis. Aquat. Org., 65, 75-78. [ Links ]
12. Mallo, J.C. y Fenucci J.L., 2004. Alimentación de protozoeas de Pleoticcus muelleri Bate utilizando diferentes microencapsulados y especies de microalgas Rev. de Biol Mar y Oceanografia 39 (1): 13-19. [ Links ]
13. Martínez, B.; Koloffon Tella, S.; Mcgladdery, S. Y Enríquez, R., 2008. Políticas, marco de trabajo y lineamientos del Comité Interamericano de Sanidad de los Animales Acuáticos Rev. Sci. Tech. Off. int. Epiz., 27 (1):65-70. [ Links ].
14. Martorelli, S. R., Overstreet, R. M. and Jovonovich, J. A., 2010. First report of viral pathogens WSSV and IHHNV in argentine crustaceans. Bulletin Of Marine Science, 86(1): 117-131 [ Links ]
15. Martorelli S.R., 2002. Parásitos y epibiontes del Langostino Pleoticus muelleri (Bate 1888) en el Atlántico Sud-occidental. Congreso Virtual de Acuicultura: 647-665. http://www.revistaaquatic.com/civa2002/ CIVA. [ Links ]
16. Mcclennen C., 2004. White spot syndrome virus. The economic, environmental and technical implications on the development of Latin American shrimp farming. Master of Arts in Law and Diplomacy Thesis, 106 pp. [ Links ]
17. OIE, 2008. Código Sanitario para los animales acuáticos. http://www.oie.int/esp/normesfcode/E_INDEX. [ Links ]
18. SAGPyA Pesca Marítima, 2008. Especies. http://www.sagpya.mecon.gov.ar/ [ Links ]














