Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de radiología
versión On-line ISSN 1852-9992
Rev. argent. radiol. vol.75 no.2 Ciudad Autónoma de Buenos Aires abr./jun. 2011
MAMA
Estudio de la subestimación histológica e incidencia de falsos negativos en biopsias de mama por vacío con guía estereotáxica
Javier Rodríguez Lucero, Carolina Espinosa, Mercedes Franco, Marcelo García Arnedo, Juan Neuman, Isabel Vaselli
Intituto Gamma - Entre Ríos 330 - Rosario - Santa Fe - Argentina
Correspondencia: Dr. Javier Rodríguez Lucero -jrodluc@hotmail.com
Recibido: noviembre 2010; aceptado: marzo 2011
Received: november 2010; accepted: march 2011
©SAR-FAARDIT
Resumen
Objetivo. Comparar los resultados histológicos en biopsias percutáneas bajo guía mamográfica y sistema de vacío con los resultados anatomopatológicos de las ulteriores cirugías. Evaluar falsos negativos al control mamográfico tras seis meses del procedimiento.
Materiales y Métodos. Entre mayo de 2008 y mayo de 2010 en 148 mujeres se realizaron 157 biopsias. Del total biopsiado, se obtuvieron 137 grupos cálcicos, 6 nódulos, 9 densidades focales asimétricas y 5 blancos mixtos. Se colocaron clips en 85 blancos (85/157; 54,14%). Se compara la histología obtenida por punción con la surgida de las cirugías para analizar discrepancias o subestimaciones.
En las biopsias negativas se indica control mamográfico a los 6 meses para evaluar falsos negativos.
Resultados: En 41 pacientes (41/157; 27,70%) se decidió completar con cirugía por el resultado histológico de la punción. Accedimos al resultado histológico quirúrgico en 34 casos, observando una concordancia entre la anatomía patológica de la punción y la quirúrgica en los 34 casos.
De los 116 casos en los que no se realizó cirugía, logramos seguir mamográficamente a 67 mujeres reconociendo 1 falso negativo (1/67; 1,49%) vinculado a un grupo cálcico.
Conclusiones. Encontramos una correlación histológica en el 100% de los casos en los que accedimos a la anatomía patológica quirúrgica y pudimos reconocer durante el seguimiento posbiopsia 1 falso negativo. En el grupo que pudo evaluarse no hallamos subestimación. El falso negativo fue en una de las primeras pacientes biopsiadas, por lo que podría interpretarse como probable causa la falta de experiencia con el sistema. Creemos conveniente contar con grupos poblacionales más numerosos para obtener mayores conclusiones.
Palabras clave. Biopsia; Mama; Mamografía; Sistema de vacío.
Abstract
Evaluation of the histological underestimation and incidence of false-negative using vacuum assisted breast biopsy and stereotactic equipment
Objective. To compare the histological findings in percutaneous biopsies under stereotactic guidance and vacuum assisted breast biopsy, with the pathological results from subsequent surgery. To evaluate false negative results in mammographic follow- up, six months after the procedure.
Material and Methods. Between May 2008 and May 2010, 157 biopsies were performed in 148 women. Of all the biopsies, there were 137 calcification clusters, 6 masses, 9 focal asymmetric densities and 5 mixed targets. Clips were placed in 85 targets (85/157, 54.14%). The histology obtained by needle biopsy is compared with that emerging from surgeries in order to discuss discrepancies or underestimation. On the negative biopsies, mammographic control is indicated to assess false negatives after 6 months.
Results. In 41 patients (41/157, 27.70%), performing surgery was decided according to the histological result of the percutaneous biopsy. We agreed to surgical histological results in 34 cases, noting consistency between the pathological findings of percutaneous biopsy and those from surgery, in the 32 cases previously mentioned.
Of the 116 cases in which no surgery was performed, we were able to do a follow up of 67 women with mammography, recognizing 1 false negative (1/67, 1.49%) linked to a calcification cluster.
Conclusion. There was a histological correlation in 100% of cases in which we agreed to the surgical anatomopathological results and we could recognize 1 false negative, during post biopsy follow-up. As regards the group that could be assessed, no underestimation was found. The false negative was in one of the first patients who had undergone biopsy; therefore, the lack of experience with the system could account for this false negative. We think it is convenient to have more numerous population groups for further and wider conclusions.
Key words. Biopsy; Breast; Mammography; Vacuum system.
INTRODUCCIÓN
Inicialmente la única forma de obtener material de la mama para su estudio por anatomía patológica era la cirugía. El Diagnóstico por Imágenes adquirió progresivamente un rol más activo en esta área, primero a través de la biopsia radioquirúrgica y, luego, mediante la realización de procedimientos percutáneos empleando diferentes sistemas y calibres de agujas, bajo guía de mamografía (MX), ultrasonido (US) y, en los últimos años, también a través de la Resonancia Magnética (RM) (1).
La biopsia percutánea de mama es una alternativa con ventajas sobre la biopsia quirúrgica, ya que por ejemplo es menos costosa e invasiva. Aproximadamente el 2% de las mujeres que realizan screening mamario necesitará biopsia (2).
Existe consenso surgido en múltiples publicaciones de las ventajas que ofrecen los sistemas de biopsias asistidos por vacío (vacuum-assisted breast biopsy: V.A.B.B.) en relación a sistemas con agujas de corte (3).
Por lo expuesto, creemos conveniente evaluar los resultados de nuestra experiencia con sistemas de biopsia por vacío bajo guía de mamografía, comparar los resultados histológicos de las biopsias percutáneas con los informes de la anatomía patológica quirúrgica y estudiar la incidencia de falsos negativos.
MATERIALES Y MÉTODOS
Entre los meses de mayo de 2008 y mayo de 2010 abordamos en nuestro servicio 157 blancos mamarios en 148 mujeres guiados por imágenes de mamografía.
Todos los procedimientos se realizaron en mesa prona Multi Care Platinum de Lorad con sistema de estereotaxia e imágenes digitales indirectas, Digital Spot Mammography (D.S.M.) empleando tecnología Couple Charge Device (C.C.D.). En todos los casos se empleó Sistema Suros (ATEC Breast Biopsy and Excision System, SUROS, Hologic Company, Indianapolis, IN USA) (Fig. 1).
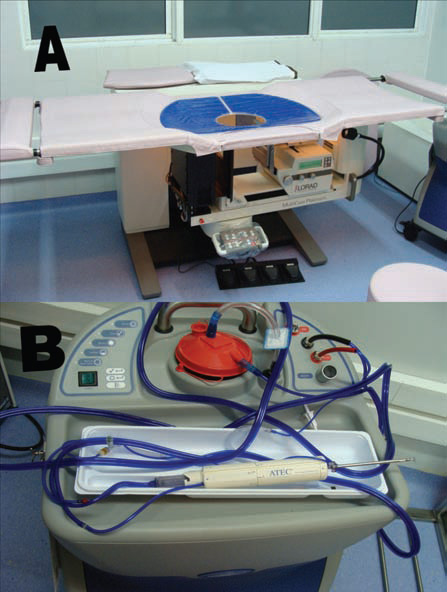
Fig. 1: (a) Mesa prona Multi Care Platinum de Lorad con sistema de estereotaxia e imágenes digitales indirectas, Digital Spot Mammography (D.S.M.). (b) Sistema Suros (ATEC Breast Biopsy and Excision System, SUROS, Hologic Company). Hand-piece montado en consola.
Las pacientes presentaron entre 33 y 81 años (promedio: 44 años) y fueron biopsiados 85 blancos en mamas derechas y 72 en izquierdas.
En todos los casos se solicitaron exámenes de coagulación y firma de consentimientos informados. Se indicó suspensión de toma de ácido acetil salicílico y derivados durante la semana previa al examen (4).
Fueron biopsiados en total 137 agrupamientos cálcicos, 6 imágenes nodulares, 9 densidades focales asimétricas y 5 blancos mixtos (nódulos y calcificaciones).
Se emplearon agujas 9 gauge (G) estándar en 76 casos (48,40%), 9 G petite en 12 mujeres (7,64%) y 12 G en 69 biopsias (43,94%).
En primera instancia, realizamos antisepsia cutánea seguida de anestesia local superficial (4-8 cc de lidocaína) y luego anestesia profunda (4-8 cc de lidocaína/epinefrina). En cuatro casos se administró mayor dosis de anestesia durante el procedimiento, a través de una válvula en "Y" que presenta el sistema de tubuladuras, por referir molestias en la toma de muestras. En otros 5 casos se administró por observarse mayor sangrado que el habitual a través del punto de ingreso y/o el receptáculo posterior del hand-piece.
Empleando un bisturí se procedió a realizar una mínima incisión cutánea para ingresar la aguja hasta la posición prefire. Se adquirieron imágenes 15 grados derecha-izquierda para luego gatillar el stage, sobre el cual se monta la aguja, y a continuación obtener imágenes postfire. En el caso de observarse óptima localización del extremo de la aguja con respecto al blanco se obtuvieron las muestras, en general 12 muestras por blanco (Figs. 2 y 3).
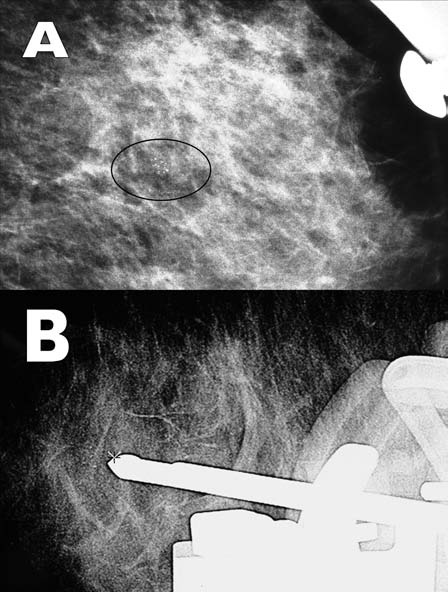
Fig. 2: (a) Imagen digital directa grupo cálcico previo a biopsia. (b) Imagen postfire, aguja sobre blanco de calcificaciones.

Fig. 3: (a) Aguja dentro de mama durante procedimiento. (b) Extracción de especímenes para su control radiológico.
En los casos en los que se biopsiaron microcalcificaciones se hicieron controles magnificados sobre las muestras, empleando equipo digital directo Selenia de Hologic, para corroborar la presencia de calcio en las mismas.
Se obtuvieron placas de control sobre los blancos para evaluar la persistencia o no de calcificaciones y el estado del sector abordado (Fig. 4). Los casos en los que se documentaba escisión completa o prácticamente completa del agrupamiento cálcico fueron marcados con un clip de titanio (ATEC TriMark TD 13-12 Biopsy Site Marker). La situación del mismo se documentó con placas de control en mesa prona y, a continuación, con placas perfil estricto y cráneo caudal con equipo digital directo (Fig. 5).

Fig. 4: (a) Control de especímenes con equipo digital directo que certifica la presencia de calcificaciones en los mismos (entre óvalos). (b)
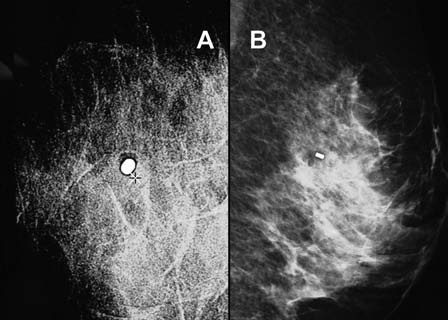
Fig. 5: Control colocación del clip: (a) en mesa prona; (b) en equipo digital directo, perfil estricto.
Procedimos a colocar clips en 85 de los blancos abordados (85/157; 54,14%).
Se recomendó un control mamográfico a los seis meses del examen para evaluar la potencial incidencia de falsos negativos en aquellos casos con histología negativa en la biopsia.
En los casos con biopsias con resultados que requerían una ulterior cirugía se correlacionó la anatomía patológica inicial (percutánea) con la definitiva (quirúrgica).
RESULTADOS
De los 179 exámenes solicitados inicialmente, se concretaron 157 (157/179; 87,70%) que son los que sirven de base a este trabajo. Las causas de la no realización de los procedimientos fueron: espesor mamario insuficiente (3 casos), blanco profundo (10 mujeres), imagen visible originalmente por técnica digital directa no reconocida por sistema indirecto de la mesa (2), no persistencia de densidades originalmente descriptas (2), proyección cutánea de calcificaciones (3 pacientes), superposición con estructura arterial prominente no evitable (1), proyección superficial (1 procedimiento). Muchos de estos casos consultaron con exámenes de otras instituciones, algunos se rechazaron inicialmente y en otros se intentó realizar el examen sin poder concretarse por algunas de las causas comentadas (Gráfico 1).
Gráfico 1: Población.
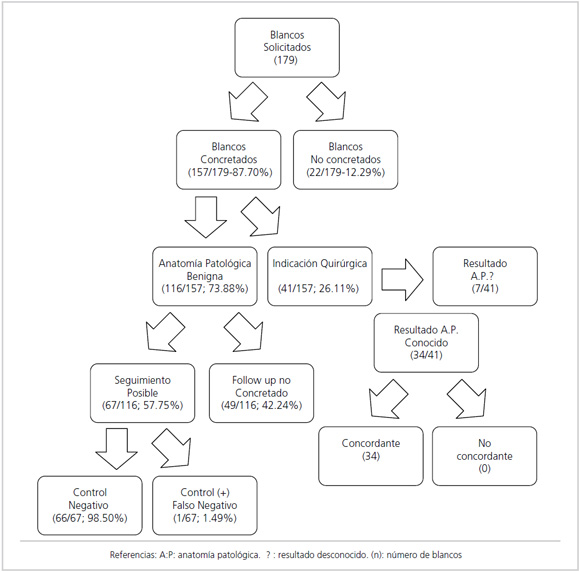
Referencias: A:P: anatomía patológica. ? : resultado desconocido. (n): número de blancos
Los procedimientos fueron muy bien tolerados por parte de las pacientes. Se observó un episodio de hipotensión leve durante el procedimiento y en otro caso luego del mismo. Ambos se resolvieron de manera rápida y espontánea.
El sangrado fue leve en la mayoría de los casos. Los controles pospunción presentaron cambios inherentes al procedimiento. Una paciente consultó por presentar un área indurada en el plano biopsiado tres días después de la punción, reconociéndose al rastreo por ultrasonido hematoma de 33 mm que resolvió en forma favorable y espontánea. No se observaron complicaciones infecciosas.
El informe de anatomía patológica describió hallazgos benignos, en general cambios fibroquísticos y/o fibroadenomas, en 116 pacientes (72,30%).
Estas pacientes recibieron indicación en el informe de un control mamográfico del área biopsiada a los 6 meses. En 67 de los 116 casos (57,75%) este control se concretó y las restantes no retornaron al control, o bien al cerrarse este trabajo aún no habían cumplido el plazo de 6 meses establecido para el seguimiento.
Se colocó clip en más del 54% de los casos. Analizando el número de clips colocados a lo largo de la serie observamos que fue cada vez más frecuente su empleo, probablemente por la mayor experiencia adquirida en el uso del sistema y por lograr una extracción completa de los blancos mamográficos cada vez con mayor asiduidad.
En 41 mujeres del total de 157 blancos abordados (27,70%), los hallazgos por anatomía patológica de la biopsia percutánea requerían cirugía; de éstos 41 casos, en 34 mujeres (82,9%) se obtuvo la histología definitiva y en los 7 casos restantes no fue posible rastrear la información acerca de la histología posquirúrgica.
Para patología el material resultó apto para su análisis en todos los casos del grupo evaluado (Fig. 6).
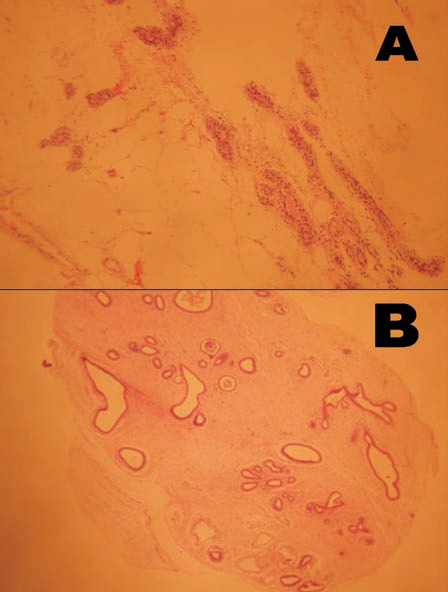
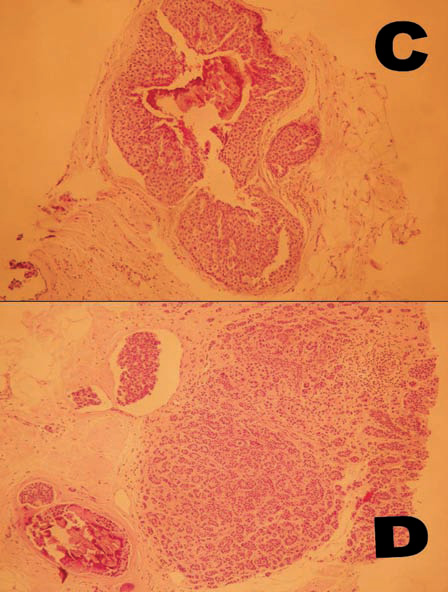
Fig. 6: Anatomía patológica. (a) Tejido mamario normal; (b) fibroadenoma; (c) carcinoma intraductal con calcificación central; (d) carcimoma lobulillar infiltrante con embolia linfática y calcificaciones en ductos.
En este grupo de 41 pacientes se describió carcinoma ductal in situ en 13 mujeres (31,70%), carcinoma ductal invasor en 10 (24,39%), hiperplasia ductal atípica en 8 pacientes (19,51%), lesiones esclerosantes complejas en 4 (9,75%), papilomas en 2 (4,87%), carcinoma ductolobulillar in situ en 2 (4,87%), carcinoma ductolobulillar invasor en 1 (2,43%) y neoplasia papilar infiltrante en 1 caso (2,43%).
En las 34 mujeres en las que pudo correlacionarse la anatomía patológica de la biopsia percutánea con la quirúrgica hubo coincidencia, sin observarse casos de subestimación o discrepancia.
En dos pacientes con informe de hiperplasia ductal atípica por punción se describieron, en la anatomía patológica quirúrgica, hallazgos benignos asociados a la presencia de cambios por la punción previa, sin persistencia de los hallazgos histológicos iniciales.
En las pacientes con biopsia percutánea negativa, que fueron pasibles de seguimiento, pudo reconocerse un falso negativo: paciente de 73 años biopsiada por grupo cálcico en abril de 2009 con histología benigna y control radiológico de las muestras obtenidas con escasa presencia de calcificaciones, que al control de los 9 meses presentaba, en relación al blanco biopsiado, un aumento del número de calcificaciones en relación al examen previo y la presencia de una densidad asimétrica no presente inicialmente. Se realizó RM donde se reconoció área nodular de 15 mm con realce heterogéneo y curva tipo II. Se decidió realizar una biopsia radio quirúrgica que demostró un carcinoma ductal infiltrante.
DISCUSIÓN
Las opciones disponibles a la hora de planear una punción percutánea en mama incluyen a la Punción Aspirativa con Aguja Fina (PAAF), las biopsias con agujas de corte (trucut), las agujas con sistema de vacío (Suros, Mammotome) y los sistemas escisionales.
Desde la introducción del Mammotome en la década del 90 la biopsia con sistemas de vacío ha crecido gracias a la calidad del material que permite obtener, óptimo para su evaluación por anatomía patológica, tanto desde el punto de vista cualitativo como cuantitativo. Otra ventaja es que, en general, no requieren reinserción para la toma de cada muestra.
También se emplean por guía de MX, US y RM y se utilizan agujas cuyos calibres van desde los 7 a los 14G.
Se ha demostrado la superioridad de los sistemas de vacío en relación a las agujas de corte en diferentes escenarios. La incidencia de subestimación histológica es menor empleando sistemas de vacío que sistemas de agujas de corte (6).
Los sistemas de vacío han demostrado mayor precisión en el manejo de calcificaciones. La sensibilidad de la biopsia con sistema de vacío es de un 98% y su especificidad cercana al 100% (7).
Según reportes previos, aproximadamente el 20% de las lesiones sospechosas que se someten a biopsia resultan malignas a la evaluación histológica (8, 9).
En diferentes publicaciones la incidencia de falsos negativos es inferior al 5%. Uno de los puntos más importantes a tener en cuenta para reducir los falsos negativos en procedimientos de intervencionismo mamario es la correcta selección del paciente. También debe elegirse el tipo de aguja a emplear y la guía de imágenes más conveniente según la particularidad del caso (6).
Es esencial la comunicación permanente entre los servicios de mamografía y anatomía patológica. El material debe remitirse dejando constancia del blanco biopsiado, sus características, localización y categorización BI-RADS. Asimismo, también se remite información acerca de los antecedentes familiares y si fue positivo o no el control de los especímenes en el caso de biopsiar calcificaciones.
Resulta fundamental saber reconocer aquellas lesiones que resulten de biopsias percutáneas y que requieran ulterior cirugía, además de las lesiones invasoras. Pueden mencionarse: hiperplasia ductal atípica, carcinoma ductal y lobulillar in situ, lesiones papilares con atipia y lesiones esclerosantes complejas. Debe aclararse que la indicación deberá contemplar la situación y el contexto general de cada paciente.
Ante el diagnóstico de hiperplasia ductal atípica y carcinoma intraductal, la subestimación en relación a la biopsia por ulterior cirugía es del 15 al 25% (10). Estas diferencias entre la anatomía patológica de la biopsia percutánea y la quirúrgica no se consideran un falso negativo sino una subestimación (11).
La explicación de los casos con subestimación vía percutánea es la extracción de especímenes de sectores con lesiones menos agresivas que otros adyacentes potencialmente reconocibles en la ulterior biopsia por cirugía (1).
Según un reciente metaanálisis, a cargo de Ying-Hua Yu y colaboradores, la incidencia de subestimación es de 20,9% para la hiperplasia ductal atípica (por poder asociarse a lesiones in situ o invasoras) y de 11,2% para el carcinoma intraductal (potencialmente asociado a carcinoma invasor) (7).
La extracción completa de la imagen blanco del procedimiento no exime de la cirugía, ya que ésta puede subestimar la real extensión de la lesión (Fig. 7). Además, el propósito de la biopsia percutánea es diagnóstico y no terapéutico en la gran mayoría de los casos, salvo situaciones excepcionales como podría ser el manejo de algunos fibroadenomas (4, 6, 12).

Fig. 7: Biopsia nódulo espiculado; anatomía patológica: carcinoma ductal infiltrante. (a) Imágenes estereotácticas derecha-izquierda. (b) Control post punción.
La presencia de lesiones "precursoras" con tanta frecuencia en biopsias percutáneas es una medida de lo precoz que resulta el diagnóstico cuando se combina screening mamográfico con biopsias percutáneas. Mientras que antes de la introducción de programas de screening la detección de carcinomas ductales in situ era de sólo el 5% del total de las lesiones malignas de la mama, actualmente esta proporción asciende a 20-40% (13).
La incidencia de complicaciones serias (hematomas que requieren cirugía) son inferiores al 0,5%. Se han descrito también neumotórax, infección, reacciones vagales, pseudoaneurismas arteriales, etc. La posibilidad de propagación de células tumorales por el trayecto de la aguja ha sido reportada, excepcionalmente, en mama. Por este motivo, tratamos de utilizar el mismo acceso durante arponajes que el empleado inicialmente durante una biopsia positiva. El objetivo es que en la pieza quirúrgica sea además extraído el trayecto de la punción (2, 4, 14).
La reducción de falsos negativos en procedimientos percutáneos requiere de estrecha colaboración interdisciplinaria entre el ginecólogo-mastólogo a cargo de la paciente, el médico imagenólogo y el patólogo. Es importante correlacionar el informe de anatomía patológica con la imagen estudiada y evaluar si se considera al procedimiento como satisfactorio o insatisfactorio. En esta última situación, hay que contemplar la posibilidad de realizar retomas o considerar la cirugía.
A su vez, es importante el seguimiento pospunción de biopsias negativas para reducir las chances de falsos negativos. Cerca del 77% de éstos son reconocidos a corto plazo, por lo que se recomienda un control mamográfico a los 6 meses del procedimiento (15).
En lo que respecta al falso negativo detectado en nuestro grupo (Figs. 8 y 9), el procedimiento fue el octavo realizado por el operador a cargo del examen. Para Liberman, la curva de aprendizaje de un operador para biopsias con sistema de vacío requiere de al menos 15 procedimientos (16).

Fig. 8: Falso Negativo, mamografías. (a) Calcificaciones previas a punción centrales en mama izquierda. (b) Control nueve meses después del procedimiento, se agregan calcificaciones y densidad al área biopsiada.
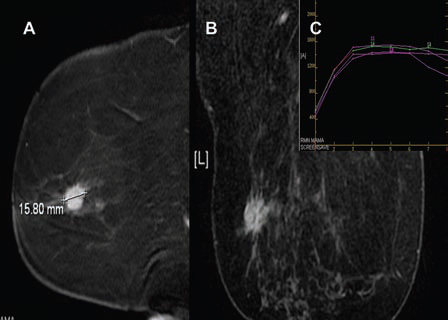
Fig. 9: Falso Negativo, RM. (a) Nódulo irregular de 15 mm en imagen sagital sobre mama izquierda. (b) Correlación axial. (c) Cinética con curvas tipo II a nivel del nódulo.
Si bien el profesional a cargo tenía experiencia previa en procedimientos con agujas de corte y sistema Mammotome en sistemas verticales, el falso negativo era uno de sus primeros procedimientos con mesa prona y Sistema Suros. Esto podría explicar la evolución ulterior.
Otros datos surgidos del trabajo y que demuestran el impacto de la experiencia en la realización de los procedimientos son la observación de la necesidad de poner, cada vez con mayor frecuencia, clips por extracción completa de los blancos a lo largo de la serie; como así también el empleo cada vez más frecuente de agujas de mayor calibre. También se destaca la disminución del número de exámenes no concretados. Estos resultados podrían interpretarse como secundarios al aumento de confianza en el método por parte de los operadores.
La mayoría de los trabajos sobre biopsias con sistemas de vacío fueron realizados empleando sistemas de agujas Mammotome. La disponibilidad de trabajos realizados utilizando agujas Suros en mamografía es escasa y la mayor parte de las publicaciones basadas en el uso de sistema Suros habla de experiencias en biopsias bajo guía de RM. No hemos encontrado bibliografía que compare diferentes sistemas de biopsias por vacío entre sí (17, 18, 19, 20).
La importancia del seguimiento de lesiones con histología benigna ha sido señalada en trabajos previos y creemos importante dejar asentado en el informe la recomendación de un control a los 6 meses para poder reconocer así un potencial falso negativo a corto plazo (20).
CONCLUSIONES
El permanente desarrollo de nuevas tecnologías, tanto en lo que concierne a la obtención de imágenes como en lo referente a intervencionismo, se acompaña de disponibilidad de equipamiento cada vez más preciso y rápido.
Este constante desarrollo debe acompañarse de formación continua por parte de los profesionales intervinientes.
La conjunción de personal capacitado y tecnología de punta permite realizar de manera rápida, precisa y sin mayores complicaciones un diagnóstico precoz en patología mamaria con todo lo que ello implica para la salud de las pacientes.
Nuestra serie mostró excelente correlación entre los resultados histológicos de la biopsia percutánea empleando sistema de vacío y la biopsia quirúrgica, sin subestimación en ningún caso.
En el grupo estudiado se reconoció sólo un falso negativo, tras biopsiar un agrupamiento cálcico. Esto equivale al 1,49%, incidencia similar a la reportada por publicaciones previas (7, 21).
Trabajos con poblaciones mayores y seguimiento a largo plazo podrán medir el verdadero impacto de la utilización del sistema de biopsias percutáneo asistido por vacío en el manejo de la patología mamaria.
1. Dershaw DD. Equipment Technique, Quality, Assurance and accreditation for Imaging-Guided Breast Biopsy Procedures. Radiol Clin North Am 2000; 38 (4):773-90. [ Links ]
2. Comstock CE. Biopsia Guiada por Estereotaxia con Aguja Gruesa. En: Venta Luz A, ed. Mamografía Intervención e Imagen. Philadelphia:Lippincott Williams & Wilkins; 2000:219-34. [ Links ]
3. Vega Bolivar A. Intervencionismo Mamario; técnica e instrumental. En: Rostagno R, Castro Barba M, eds. Avances en Diagnostico por Imágenes: Mama. Buenos Aires: Journal; 2010:121-32. [ Links ]
4. Berg WA. Image-Guided breast biopsy and management of High-risk lesions. Radiol Clin North Am 2004; 42(5):935-46, vii. [ Links ]
5. López Ruiz JA. Punciones con Aguja Fina: actualidad y controversias. En: Rostagno R, Castro Barba M, eds. Avances en Diagnostico por Imágenes: Mama. Buenos Aires: Journal; 2010:133-40. [ Links ]
6. Liberman L. Clinical Management Issues in Percutaneous core Breast Biopsy. Radiol Clin North Am 2000; 38(4):791-807. [ Links ]
7. Yu YH , Liang C, Yuan XZ. Diagnostic value of Vacuum-assisted breast biopsy for breast carcinoma: a meta-analysis and systematic review Breast Cancer Res Treat 2010; 120(2): 469-79. [ Links ]
8. Elmore JG, Moceri VM, Barton MB, Polk S, Arena Pj, Fletcher SW. Ten years reik of false-positive screening mammograms and clinical breast examination. N Engl J Med 1998; 338(16):1089-96. [ Links ]
9. Kopans DB. The positive predictive value of mammography. AJR Am J Roentgenol 1992; 158(3): 521-6. [ Links ]
10. Liberman L. Percutaneous image-guided core breast biopsy.Radiol. Clin North Am 2002; 40: 483-500. [ Links ]
11. Sewell Whitaker C. Pathology of High-risk breast lesions and ductal carcinoma in situ. Radiol Clin North Am 2004; 42(5):821 - 30, v. [ Links ]
12. Lee JM, Kaplan JB, Murray MP, Liberman L. Complete Excision of the MRI Target lesion at MRI-Guided Vacuum-Assisted Biopsy of Breast Cancer AJR Am J Roentgenol 2008; 191(4): 1198-202. [ Links ]
13. Feig SA. Adverse Effects of Screening Mammography. Radiol Clin North Am 2004; 42(5):807-19, v. [ Links ]
14. Rodríguez Lucero J, Maffei LD, Riege RM, Vaselli I. Pseudoaneurisma Arterial Mamario tras Biopsia Percutánea: Diagnóstico y Tratamiento no Quirúrgico. RAR 2002; 66:63-7. [ Links ]
15. Jackman RJ, Nowels KW, Rodriguez-Soto J, Marzoni FA Jr, Finkelstein SI, Shepard MJ. Stereotactic, automated, large-core needle biopsy of nonpalpable breast lesions: False-negative and histologic underestimation rates after long-term follow-up. Radiology 1999; 210(3):799-805. [ Links ]
16. Liberman L, Benton CL, Dershaw DD, Abramson AF, La Trenta LR, Morris EA. Learning Curve for stereotactic Breast Biopsy: how many cases are enough? AJR Am J Roentgenol 2001; 176(3):721-7. [ Links ]
17. Liberman L, Morris E, Dershaw DD, Thornton CM, Van Zee KJ, Tan LK. Fast MRI-Guided Vacuum-Assisted Breast Biopsy: Initial Experience. AJR Am J Roentgenol 2003; 181(5):1283-93. [ Links ]
18. Lehman CD, Deperi ER, Peacock S, McDonough MD, Demartini WB, Shook J. Clinical Experience with MRI-Guided Vacuum-Assisted Breast Biopsy. AJR Am J Roentgenol 2005; 184(6):1782-7. [ Links ]
19. Schrading S, Simon B, Braun M, Wardelmann E, Schild HS, Kuhl C MRI-Guided breast Biopsy: Influence of choice of Vacuum biopsy System on the Mode of Biopsy Of MRI-Only Suspicious Breast Lesions. AJR Am J Roentgenol 2010; 194(6):1650-7. [ Links ]
20. Han BK, Schnall MD, Orel SG, Rosen M. Outcome of MRI-Guided Breast Biopsy. AJR Am J Roentgenol 2008; 191(6):1798-804. [ Links ]
21. Peter D, Grünhagen J, Wenke R, Schäfer, FKW Scheer I. False-negative results after stereotactically guided vacuum biopsy. Eur Radiol 2008; 18(1): 177-82. [ Links ]
Los autores Javier Rodríguez Lucero e Isabel Vaselli declaran como un potencial conflicto de interés ser co-autores de un artículo al que se hace referencia en este estudio.














