Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista argentina de radiología
versão On-line ISSN 1852-9992
Rev. argent. radiol. vol.76 no.2 Ciudad Autónoma de Buenos Aires abr./jun. 2012
MEDIOS DE CONTRASTE
Gadolinio y fibrosis sistémica nefrogénica
Claudia Cejas (1), Cecilia Acuña (1)
(1) Fundación para el estudio de enfermedades neurológicas Dr. Raúl Carrea (FLENI). Montañeses 2325, CABA, Argentina.
Correspondencia: Dra. Claudia Cejas - ccejas@fleni.org.ar
Recibido: junio 2011; aceptado: marzo 2012
Received: june 2011; accepted: march 2012
©SAR
Resumen
Inicialmente llamada dermopatía fibrosante nefrogénica, la fibrosis sistémica nefrogénica (FSN) está fuertemente ligada a la inyección endovenosa de medios de contraste -basados en gadolinio- en pacientes con insuficiencia renal. En esta revisión corta se analiza la fisiopatología y la clínica, la responsabilidad del radiólogo en la prevención a través de la puesta en práctica de las reglamentaciones vigentes y, por último, se mencionan algunos conceptos sobre el tratamiento de los pacientes con insuficiencia renal crónica que deben exponerse a la inyección de gadolinio.
Abstract
Gadolinium and nephrogenic systemic fibrosis.
Nephrogenic systemic fibrosis (NSF), initially called nephrogenic fibrosing dermopathy, is strongly linked to the intravenous injection of gadolinium-based contrast agents in patients with renal insufficiency. In this short review, we analyze the pathophysiology and clinical signs and symptoms, the medical responsibility of the radiologist in prevention through the implementation of the existing regulations and, finally, some concepts on the treatment of patients with chronic renal insufficiency who must receive a gadolinium injection.
INTRODUCCIÓN
Inicialmente llamada dermopatía fibrosante nefrogénica, la fibrosis sistémica nerfrogénica (FSN) fue descrita por primera vez en la literatura médica en el año 2000 (1). Desde ese momento, fue definida por numerosos autores de todo el mundo como una entidad asociada a la exposición de gadolinio (Gd) en los estudios de RM en pacientes con insuficiencia renal. Luego de varios años de investigación sobre el uso de este elemento químico, se ha determinado que la administración intravascular de Gd tiene los siguientes riesgos: nefrotoxicidad (pudiendo requerir diálisis), fibrosis sistémica nefrogénica, reacciones anafilactoideas y anafilácticas (que requieren intervención inmediata) y reacciones en el sitio de inyección (2-7).
PREVALENCIA Y CLÍNICA
La FSN típicamente afecta a pacientes con insuficiencia renal (IR) en estadio terminal, incluyendo a aquellos que se encuentran bajo tratamiento regular con diálisis. Esta enfermedad no tiene predilección por género, raza o edad, y se observa tanto en niños como en adultos. Se ha reportado una incidencia del 3 al 7% en pacientes con una función renal disminuida (VFG < 30mL/min).
El clearence de creatinina es una prueba muy útil, aceptada como medida del filtrado glomerular. Ésta, si se conocen la creatininemia, el peso teórico y la edad del paciente, puede predecirse a través de la fórmula de Cockroft- Gault:
Cl cr (hombre) en ml/min= (140- edad) x PCI / (72 x Crs)
Cl cr (mujer) en ml/min= (140-edad) x PCI x 0,85 / (72 x Crs)
Donde: Crs = creatinina sérica (mg/dl), Cl cr = clearence de creatinina, PCI = peso corporal ideal (8).
La Sociedad Española de Nefrología tiene una útil calculadora online que, introduciendo los datos (edad, sexo, creatininemia, peso y talla), brinda un cálculo inmediato (9).
Sin embargo, es importante saber que la creatininemia y el clearence de creatinina son datos indirectos e insuficientes y, en tanto dependen de los factores ya mencionados, resultan sumamente variables, sobre todo en los grupos de riesgo donde es indispensable la estimación del volumen del filtrado glomerular (VFG) o la tasa de filtrado glomerular (TFG). La prevalencia de FSN aumenta con el grado de disfunción renal, la dosis de inyección y la cantidad de veces que se haya administrado (supone una dosis acumulativa) (2,10).
Los pacientes pueden desarrollar síntomas de FSN (Tabla 1) desde el día de exposición al gadolinio hasta muchos meses después (2-75 días; media: 25 días). En general, predominan las manifestaciones cutáneas. Éstas suelen ser simétricas y afectan en particular las extremidades y el tronco, y raramente la cara; también es posible observar edema de miembros inferiores.
Tabla 1: Signos y síntomas de la FSN (11-13).

La fibrosis es el desenlace final y, además de la piel, puede afectar múltiples órganos y desencadenar, como consecuencia, una falla multisistémica. Se ha comunicado una mortalidad del 31%, pero aún no se conoce la cifra exacta, ya que es probable que existan menos casos reportados de los que verdaderamente hay (10-12).
MECANISMO DE ACCIÓN Y BIODISTRIBUCIÓN DEL GADOLINIO
Grobner (3) fue el primero en sugerir que la Resonancia Magnética (RM) con inyección de gadolinio podía ser la causante de este tipo de fibrosis. Recientemente, algunos investigadores han documentado la presencia del químico en biopsias de pacientes con FSN (13,14). Existen evidencias de que los quelantes del Gd estimulan la proliferación de fibroblastos y, debido a la afectación del tejido celular subcutáneo y músculos subyacentes, es necesaria una biopsia dérmica profunda para confirmar el diagnóstico clínico. Asimismo, especímenes histológicos demostraron engrosamiento del colágeno, depósito de mucina, proliferación de células en huso y fibroblastos (15).
Dada la existencia de depósitos de Gd en los tejidos afectados (tinción de fibrocitos CD34+ en biopsia cutánea), el papel patógeno de este elemento químico ha quedado evidenciado (16).
El Gd libre (GD+++) es altamente tóxico in vivo, no es iónico ni es tejido específico. Cuando es administrado por vía endovenosa, se distribuye por la sangre y el espacio extracelular, transitando a través de los órganos excretores. En estudios experimentales (17,18), se ha probado que todos los componentes del Gd son excretados intactos y en forma rápida (Fig. 1) (3).

Fig. 1: Distribución y eliminación del gadolinio administrado por vía endovenosa.
El Gd se distribuye principalmente por el hígado, el tejido linfático y el hueso, y puede llegar a producir necrosis hepática. Obstruye el paso de calcio en células musculares y nerviosas e interfiere en la neurotransmisión y, con enzimas intracelulares y membranas celulares, en el proceso de transmetilación (donde el GD+++ reemplaza a metales como el zinc y el cobre). Este proceso facilita una mayor permanencia en el organismo, por lo que se lo utiliza ligado a quelantes (por ejemplo, el ácido dietilen triamino pentaacético -DTPA-). Estos lo convierten en una molécula más estable y reducen su toxicidad (19).
La configuración de la molécula puede ser lineal o cíclica. La diferencia radica en la estabilidad química y su capacidad para liberar iones de Gd (20,21). En el caso de las cíclicas, éstas tienen mayor ligazón con el GD+++, no requieren exceso de quelato y poseen mayor vida media de disociación (17) (Tabla 2).
Tabla 2: Características de los contrastes basados en gadolinio y su relación con FNS*.
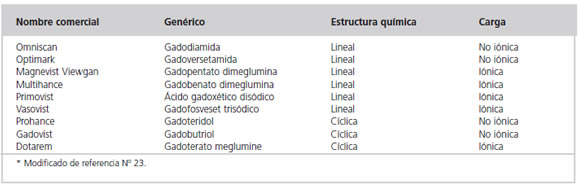
Estudios experimentales han demostrado que la dosis letal 50 de gadolinio libre es 50 veces mayor que la del gadolinio quelado (18, 22).
La vida media del Gd es de 1,3 h, pero en pacientes con insuficiencia renal puede extenderse hasta las 30 ó 120 h, dependiendo de la función del riñón. Esta persistencia genera el depósito del gadolinio en la piel y en los órganos internos (23)
.La mayoría de los casos reportados de FSN sucedieron luego de una inyección con dosis alta de gadolinio (sobre todo en estudios de Angio RM) o en pacientes que recibieron reiteradamente, en un corto período, cantidades habituales. Por este motivo, es importante generar protocolos que minimicen el volumen de contraste, especialmente en pacientes vulnerables (24).
Debido a los síntomas inespecíficos de la FSN, no es habitual estudiar a estos pacientes con exámenes radiológicos. Sin embargo, tanto en ecografía (US) y Tomografía Computada (TC) como en RM, se ha descrito un engrosamiento difuso de la piel con estratificación de la grasa. Asimismo, en estudios de medicina nuclear con 99mTc se ha comunicado hipercaptación del trazador en piel y músculos (25).
REGLAMENTACIONES
Dada la asociación descrita entre el Gd y el desarrollo de FSN, la Administración de Drogas y Alimentos de los Estados Unidos (FDA), en diciembre de 2006, emitió las primeras recomendaciones sobre la utilización de agentes de contraste, basados en gadolinio, en pacientes con IR aguda o crónica, con un VFG < 30mL/min /1,73 m2, con falla renal aguda causada por síndrome hepatorrenal o en aquellos en período perioperatorio de trasplante hepático (30). Si bien la FDA no hizo distinciones sobre qué tipo de Gd debía ser evitado, reconoció que el agente más reportado era el gadodiamide (Omniscan®) (26).
Por otra parte, en el 2007 la Sociedad Europea de Radiología Urogenital (ESUR) publicó las guías para el uso de gadolinio. En éstas, se discutían especialmente los diferentes tipos de medios de contraste con Gd que debían evitarse en pacientes con estadios 4 ó 5 de enfermedad renal crónica o en aquellos con trasplante hepático y función renal disminuida. A su vez, recomendaban tomar precauciones tanto en el estadio 3 de una IR crónica como en mujeres embarazadas y niños menores de un año (27).
En septiembre de 2010, la FDA publicó las nuevas guías restrictivas para el empleo de gadolinio (28). A partir del análisis de Wang et al., elaborado con un total de 52.954 RM con inyección endovenosa de Gd, se determinó la solicitud de creatinina sérica para todo paciente de 60 años (o más) y/o con riesgo de enfermedad renal. También se decidió restringir al máximo la dosis administrada de Gd en los pacientes con VFG < 60 mL/min/1,73 m2 y, exceptuando las situaciones de emergencia que justifiquen su uso, se planteó la obligación de evitar la utilización del gadolinio en pacientes con VFG < 30mL/min/1,73 m2 o con IRC en tratamiento de diálisis (29).
A su vez, la ESUR en las recomendaciones de la última versión (7.0) contraindica la inyección de gadolinio en los casos de alto riesgo. Estos son: trasplantados hepáticos y pacientes en diálisis o que tienen un VFG < 30ml/min/1,73 m2. Además, advierte la necesidad de tomar precauciones en los pacientes con VFG 30-60ml/min/1,73 m2 y en los niños menores de un año. Sobre estos últimos, recomienda medir la creatinina sérica antes de la administración del contraste (30).
En la Argentina, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) (31) -órgano oficial con competencia en el control y fiscalización de la sanidad y calidad de las drogas, medicamentos, productos médicos, reactivos de diagnóstico, cosméticos, suplementos dietarios y productos de uso doméstico- emitió, en el 2007, la Disposición Nº 5555/07-Gadolinio. Allí, se establece que no deben usarse contrastes con gadolinio o derivados (tales como la gadodiamida u otros quelatos diferentes de gadodiamida) en pacientes con insuficiencia renal severa y en aquellos que han recibido -o van a recibir- un trasplante hepático. En este sentido, el documento estipula:
"Contrastes para RM con gadodiamida: su uso está contraindicado en pacientes con insuficiencia renal severa (tasa de filtración glomerular < 30 ml/min/1,73 m2) y en pacientes sometidos, o que van a someterse, a trasplante hepático. En neonatos y en niños de hasta un año de edad sólo debe administrarse tras una cuidadosa valoración, debido a la inmadurez de su función renal.
Contrastes para RM a base de otros quelatos de gadolinio diferentes a gadodiamida: la administración de estos contrastes en pacientes con insuficiencia renal severa (tasa de filtración glomerular < 30 ml/mn/1,73 m2) sólo debe realizarse después de una cuidadosa valoración del balance beneficio-riesgo para cada paciente individual".
El riesgo de desarrollar una FSN en pacientes con insuficiencia renal moderada (filtración glomerular 30-59 ml/min/1,73 m2) es desconocido, por lo que, en estos casos, el gadolinio debe utilizarse con cautela.
Tanto la ANMAT (a través de Farmacovigilancia) como la FDA instan a los profesionales de la salud y a los pacientes a comunicar, en casos de insuficiencia renal, cualquier evento adverso ocurrido con agentes de contraste que contengan gadolinio. La página para este propósito es http://www.anmat.gov.ar/farmacovigilancia y el número de teléfono y fax 4340-0866. Hasta la actualidad (noviembre 2011), se han reportado 194 pacientes con FSN (dato obtenido por pedido expreso para los fines de esta publicación).
RESPONSABILIDAD MÉDICA EN LA PREVENCIÓN
En primer lugar, para minimizar el riesgo de FSN es necesario identificar, siguiendo las guías mencionadas (29-31), a los pacientes de riesgo. También es importante que el médico, antes de la aplicación del agente de contraste para RM con gadolinio en su estructura, determine la función renal del paciente (sea a través de la historia clínica y/o por pruebas de laboratorio), ya que hay que tener en cuenta el VFG independientemente de la edad, raza o sexo. Asimismo, es necesario recordar que no debe haber pasado más de un mes del último resultado de laboratorio en pacientes de riesgo (20).
Otro punto a definir en este tipo de casos es la relación riesgo-beneficio de la inyección de contraste. Un paciente con posibilidades de padecer FSN puede recibir gadolinio siempre que las ventajas del estudio superen claramente el o los peligros. Esto deberá ser evaluado entre el radiólogo y el especialista solicitante, y la decisión tiene que quedar documentada con un consentimiento informado.
Por otra parte, a menos que la información diagnóstica sea esencial y no se consiga con una imagen de RM sin contraste, se debe evitar el uso de compuestos derivados del gadolinio. Su utilización no siempre resulta ineludible, por lo que realizar el estudio sin contraste es una buena práctica. Quien tiene que determinar su uso o no es el radiólogo experto; pero, aun en aquellos casos en los que resulte necesario, hay que tratar de disminuir la dosis al mínimo posible (32) (dosis recomendada: 0,1mmol/Kg). Una vez inyectada y antes de cualquier readministración, se debe esperar un plazo suficiente para la eliminación del gadolinio, ya que las dosis repetidas o mayores a las recomendadas son factores que pueden aumentar el riesgo de desarrollar una FSN.
En los recién nacidos e infantes de hasta 1 año de edad, el Gd sólo debe utilizarse luego de una cuidadosa consideración, ya que la función renal todavía se encuentra inmadura.
Para prevenir incidentes y accidentes es imprescindible capacitar a los técnicos radiólogos en el uso de la dosis apropiada para cada caso. En este sentido, cabe destacar que en los últimos tres años, desde que se establecieron las regulaciones sobre el uso de gadolinio en pacientes con insuficiencia renal, no se han reportado nuevos casos en los centros que adhieren a estas normas (20).
TRATAMIENTO
No existe un tratamiento efectivo para la FSN. Los estudios multicéntricos con corticoides, féresis, plasmaféresis, talidomida, tiosulfato y metotrexate no han demostrado resultados consistentes y, si bien la administración de imatinib disminuye la fibrosis y produce una rápida mejoría de los cambios dérmicos y articulares en pacientes con estadio 5 de IRC, se ha observado recurrencia cuando se discontinúa el tratamiento, por lo que tampoco se ha podido determinar la duración del mismo (33).
Asimismo, la hemodiálisis puede ser efectiva para remover el gadolinio circulante, pero no hay evidencias sobre su eficacia en la protección contra el desarrollo de la FSN. Por este motivo, no es recomendado como tratamiento preventivo tras la inyección de gadolinio. En los casos de pacientes dializados inyectados, se debe comenzar la diálisis tan pronto como sea posible, idealmente dentro de las 3 primeras horas después de la administración del contraste. La segunda sesión se hará dentro de las 24 h y se completará con un tercer ciclo a las 48 h. La hemodiálisis pareciera ser más efectiva que la diálisis peritoneal (34).
Según recomienda la ANMAT, "para los pacientes que realizan hemodiálisis, los profesionales del cuidado de la salud pueden considerar la práctica inmediata de este tratamiento luego de la administración de gadolinio para aumentar la eliminación del agente de contraste". A pesar de que admiten desconocer si la hemodiálisis previene la aparición de la fibrosis sistémica nefrogénica, informan que "de la primera a la tercera sesión, las tasas de eliminación promedio reportadas fueron 78%, 96% y 99%" (31).
CONCLUSIONES
El propósito de esta revisión corta fue hacer una breve descripción de la FSN, los mecanismos de acción de los agentes de contraste basados en gadolinio, la sintomatología, el tratamiento y las disposiciones vigentes a nivel nacional e internacional para su prevención. Sin embargo, aún existen muchas preguntas sin responder acerca del mecanismo de acción del gadolinio en pacientes con insuficiencia renal.
Es de vital importancia que el radiólogo tome conciencia de la responsabilidad que le cabe en este tema y que tenga en cuenta las recomendaciones de la FDA, ESUR y la ANMAT, con el fin de evitar la inyección de gadolinio en pacientes de riesgo. En caso de ser necesaria su administración (riesgo-beneficio), es obligatorio contar con el consentimiento informado del paciente.
1. Cowper SE, Robin HS, Steinberg SM, Su LD, Gupta S, LeBoit PE. Scleromyxoedema-like cutaneous diseases in renaldialysis patients. Lancet 2000; 356:1000-1. [ Links ]
2. Thomsen HS. Nephrogenic systemic fibrosis: history and epidemiology. Radiol Clin N Am 2009; 47:827-31. [ Links ]
3. Grobner T. Gadolinium -- a specific trigger for the development of nephrogenic fibrosing dermopathy and nephrogenic systemic fibrosis? Nephrol Dial Transplant 2006; 21(4):1104-8. [ Links ]
4. Vakil V, Sung JJ, Piecychna M, et al. Gadolinium-containing magnetic resonance image contrast agent promotes fibrocyte differentiation. J Magn Reson Imaging 2009; 30:1284-8. [ Links ]
5. Agarwal R, Brunelli SM, Williams K, Mitchell MD, Feldman HI, Umscheid CA. Gadolinium-based contrast agents and nephrogenic systemic fibrosis: a systematic review and metaanalysis. Nephrol Dial Transplant 2009; 24:856-63. [ Links ]
6. Braverman IM, Cowper S. Nephrogenic systemic fibrosis. F1000 Med Rep 2010; 2:84. [ Links ]
7. Cowper SE. Nephrogenic systemic fibrosis: a review and exploration of the role of gadolinium. Adv Dermatol 2007; 23:131-54. [ Links ]
8. Zalazar M, Tobia N, Guerra E, et al. Contrastes yodados intravenosos y metmorfina: interacciones y precauciones. Rev Arg Radiol 2011; 75:79-81. [ Links ]
9. Sociedad Española de Nefrología. Calculadora. Disponible en (Available at): http:/www.senefro.org/modules.php?name=calcfg. Accedido (Accessed): diciembre 10, 2011. [ Links ]
10. Sadowski EA, Bennett LK, Chan MR, et al. Nephrogenic systemic fibrosis: risk factors and incidence estimation. Radiology 2007; 243:148-57. [ Links ]
11. Marckmann P, Skov L, Rossen K, et al. Nephrogenic systemic fibrosis: suspected causative role of gadodiamide used for contrast-enhanced magnetic resonance imaging. J Am Soc Nephrol 2006; 17:2359-62. [ Links ]
12. Gibson SE, Farver CF, Prayson RA. Multiorgan involvement in nephrogenic fibrosing dermopathy: an autopsy case and review of the literature. Arch Pathol Lab Med 2006; 130:209-12. [ Links ]
13. Boyd AS, Zic JA, Abraham JL. Gadolinium deposition in nephrogenic fibrosing dermopathy. J Am Acad Dermatol 2007; 56:27-30. [ Links ]
14. High WA, Ayers RA, Chandler J, Zito G, Cowper SE. Gadolinium is detectable within the tissue of patients with nephrogenic systemic fibrosis. J Am Acad Dermatol 2007; 56:21-6. [ Links ]
15. Edward M, Quinn JA, Burden AD. Effect of different classes of gadolinium-based contrast agents on control and nephrogenic systemic fibrosis-derived fibroblast proliferation. Radiology 2010; 256:735-43. [ Links ]
16. Bourlon Cuellar R, Castro Quiróz O, Bourlon de los Ríos Ch, et al. Fibrosis Nefrogénica Sistémica. Med Int Mex 2009; 25: 210-6. [ Links ]
17. Bousquet JC, Saini S, Stark DD, et al. Gd-DOTA: characterization of a new paramagnetic complex. Radiology 1988; 166:693-8. [ Links ]
18. Cacheris W, Quay S, Rocklage S. The relationship between thermodynamics and the toxicity of gadolinium complexes. Magn Reson Imaging 1990; 8:467-81. [ Links ]
19. Morcos SK. Nephrogenic systemic fibrosis following the administration of extracellular gadolinium based contrast agents: is the stability of the contrast agent molecule an important factor in the pathogenesis of this condition? Br J Radiol 2007; 80:73-6. [ Links ]
20. García Mónaco R, Paganini L, Ocantos J. Medios de contraste radiológicos/ lo que un médico radiólogo no puede dejar de conocer. Buenos Aires: Editorial Journal; 2011. [ Links ]
21. La Forgia M, Arias M, Buonsante ME. Fibrosis sistémica nefrogénica vinculada a gadolinio con evolución fatal. Dermatología Argentina 2007; 13:246-51. [ Links ]
22. Aime S, Caravan P. Biodistribution of gadolinium-based contrast agents, including gadolinium deposition. J Magn Reson Imaging 2009; 30:1259-67. [ Links ]
23. Ersoy H, Rybicki FJ. Biochemical safety profiles of gadolinium- based extracellular contrast agents and nephrogenic systemic fibrosis. J Magn Reson Imaging 2007; 26:1190-7. [ Links ]
24. Prince MR, Zhang HL, Prowda JC, Grossman ME, Silvers DN. Nephrogenic systemic fibrosis and its impact on abdominal imaging. RadioGraphics 2009; 29: 1565-74. [ Links ]
25. U.S. Food and Drug Administration. Public health advisory: update on magnetic resonance imaging (MRI) contrast agents containing gadolinium and nephrogenic fibrosing dermopathy. Disponible en (Available at): http://www.fda.gov/cder/drug/InfoSheets/HCP/gcca_20 0612HCP.htm. Accedido (Accessed): febrero 20, 2007. [ Links ]
26. U.S. Food and Drug Administration. Important drug warning for gadolinium-based contrast agents. September 2007. Disponible en (Available at): http://www.fda.gov/downloads/Safety/MedWatch/SafetyInformation/SafetyAlertsfor HumanMedicalProducts/UCM154532.pdf. Accedido (Accessed): marzo 11, 2009. [ Links ]
27. Thomsen HS. ESUR guideline: gadolinium-based contrast media and nephrogenic systemic fibrosis. Eur Radiol 2007; 17:2692-6. [ Links ]
28. U.S. Food and Drug Administration. New warnings required on use of gadolinium-based contrast agents. September 9, 2010. Disponible en (Available at). http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm22528 6.htm. Accedido (Accessed): noviembre 16, 2011. [ Links ]
29. Wang Y, Alkasab TK, Narin O, et al. Incidence of nephrogenic systemic fibrosis after adoption of restrictive gadolinium- based contrast agent guidelines. Radiology 2011; 260:105-11. [ Links ]
30. European Society of Urogenital Radiology (ESUR). ESUR guidelines on contrast media. Versión 7.0. Agosto 2010. Disponible en (Available at): http://www.esur.org/Contrastmedia.51.0.html. Accedido (Accessed): agosto 7, 2011. [ Links ]
31. Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT). Disposición 5555-Gadolinio. Boletín para profesionales 2007; 15:33-48. Disponible en (Available at): http://www.anmat.gov.ar/webanmat/Publicaciones/Bolet ines/Profesionales/Boleprof_noviembre_2007.pdf. Accedido (Accessed): noviembre 16, 2011. [ Links ]
32. Shellock GF, Spinazzi A. MRI safety update 2008: part 1, MRI contrast agents and nephrogenic systemic fibrosis. AJR Am J Roentgenol 2008; 191:1129-39. [ Links ]
33. Kay J, High WA. Imatinib mesylate treatment of nephrogenic systemic fibrosis Arthritis Rheum 2008; 58:2543-8. [ Links ]
34. Kuo PH, Kanal E, Abu-Alfa AK, Cowper SE. Gadoliniumbased MR contrast agents and nephrogenic systemic fibrosis. Radiology 2007; 242:647-9. [ Links ]














