INTRODUCCIÓN
Los ostrácodos (Clase Ostracoda Latreille, 1802) son unos pequeños crustáceos que poseen un caparazón conformado por dos valvas que se articulan dorsalmente y cuya composición quími ca es esencialmente carbonato de calcio (CaCO3) y quitina. Estos organismos están ampliamente distribuidos en ambientes acuáticos, tanto mari nos como continentales, con especies y géneros que viven en rangos de salinidad bien definidos, desde el agua dulce hasta rangos hiperhalinos (Amstrong & Brasier, 2005). Los ostrácodos exhiben una gran variedad de hábitos alimenti cios; algunas especies son filtradoras, otras son carroñeras, detritívoras, herbívoras, predadoras carnívoras, incluso parásitas o comensales de otros crustáceos (Athersuch et al., 1989). Su re producción es sexual, partenogenética o mixta. Hasta el presente se han descripto 30.000 espe cies actuales (Brusca et al., 2016). Si bien poseen aplicaciones en disciplinas como la acuicultura y la ecotoxicología (Moguilevsky & Whatley, 1995), las especies pertenecientes al Orden Podocopida (Sars, 1866) son utilizadas mayormente como in dicadores paleoambientales; particularmente en ambientes marino marginales y en la definición de antiguas líneas de costa (Frenzel & Boomer, 2005).
En Argentina el conocimiento acerca de las especies presentes en diferentes ambientes es escaso. En la provincia de Mendoza, D’Ambrosio (2014) y D’Ambrosio et al. (2017) llevaron a cabo el muestreo y el análisis de la ostracofauna de la laguna, los bañados y los ríos de la cuenca de la Laguna Llancanelo, que permitió reconocer 12 especies pertenecientes a 9 géneros; mientras que Kihn et al. (2020) estudiaron la composición taxonómica de 5 lagos someros de la provincia de La Pampa, dónde se registraron 10 taxa, algunos hallados previamente en la provincia de Buenos Aires. Por otro lado, entre las investigaciones más recientes llevadas a cabo en la Patagonia, cabe destacar un relevamiento efectuado en 40 siste mas acuáticos, donde se registraron 22 especies, tres de las cuales fueron reportadas por primera vez en la región neotropical y una en Argentina (Ramón Mercau et al., 2012); un estudio sobre la hidroquímica de 10 cuerpos de agua, que per mitió identificar la presencia de 15 especies de ostrácodos (Coviaga et al., 2017); y 28 especies determinadas a partir de la caracterización de la ostracofauna actual en 69 ambientes lacustres (Cusminsky et al., 2020). Particularmente, en la provincia de Buenos Aires, los antecedentes se limitan a la cuenca del Salado y a la región de Bahía Blanca. Laprida (2006) reportó la presen cia de 20 especies de ostrácodos no marinos en 15 cuerpos de agua continentales de la Pampa Deprimida; en tanto en el estuario de Bahía Blanca se identificaron 37 especies en bioceno sis y tanatocenosis de canal de marea (Martínez, 2005), y 11 géneros representados por 13 espe cies bentónicas (Kihn et al., 2016, 2017a) a par tir del estudio de la ostracofauna en muestras de sedimentos superficiales de ambientes actuales.
Si bien los ostrácodos están siendo utiliza dos como indicadores paleoambientales en am bientes costeros de la provincia de Buenos Aires (Bertels-Psostka & Laprida, 1998; Bertels & Martínez, 1990, 1997; Ferrero, 1996, 2006, 2009; Laprida, 1998; Laprida y Valero-Garcés, 2009), son prácticamente inexistentes los estudios so bre las faunas modernas en estos mismos tipos de ambientes (estuarios y lagunas costeras), lo que impide contar con una buena caracterización ecológica y ambiental que pueda ser usada como análogo moderno para realizar inferencias pa leoambientales. En este sentido, de los ambien tes mixohalinos de la Argentina, Mar Chiquita es relevante por ser la única albufera del país, y por lo tanto el único análogo moderno de muchos de los ambientes que se desarrollaron en la costa de la provincia de Buenos Aires durante la última transgresión marina.
El objetivo del presente trabajo fue conocer la composición taxonómica de las comunidades de ostrácodos vivientes de la laguna costera Mar Chiquita.
MATERIALES Y MÉTODOS
Área de estudio
La laguna costera Mar Chiquita, declarada Reserva Mundial de Biosfera por Unesco en el año 1996, cuenta con una cuenca tributaria de 10.000 km2 y posee una superficie de 60 km2. La laguna se localiza en el partido de Mar Chiquita, provincia de Buenos Aires (37°42´S; 57°25´O). En la laguna Mar Chiquita descargan varios cur sos de agua poco caudalosos (arroyos Grande, Canal 7, Dulce y Vivoratá; Fig. 1) haciendo que la laguna sea el principal reservorio que conecta los mismos con el océano. La laguna puede ser dividida en dos ambientes bien diferenciados, un cuerpo lagunar, donde la acción de la marea es insignificante; y un sector de características netamente estuariales. El límite entre ambos ambientes es sumamente variable, definiéndose por la conjunción de la amplitud de mareas, las condiciones meteorológicas (viento y precipita ciones) y el aporte de agua dulce de los arroyos (Reta et al., 2001).
Muestreo de campo
Se tomaron muestras de ostrácodos vivien tes y se determinó la conductividad en siete si tios representativos del gradiente estuárico, en invierno, primavera, verano y otoño (2017-2018) durante la bajamar. Los sitios fueron numerados de acuerdo a su distancia respecto de la desembo cadura (sitios 1-7; Fig. 1 y Fig. 2; Tabla 1).
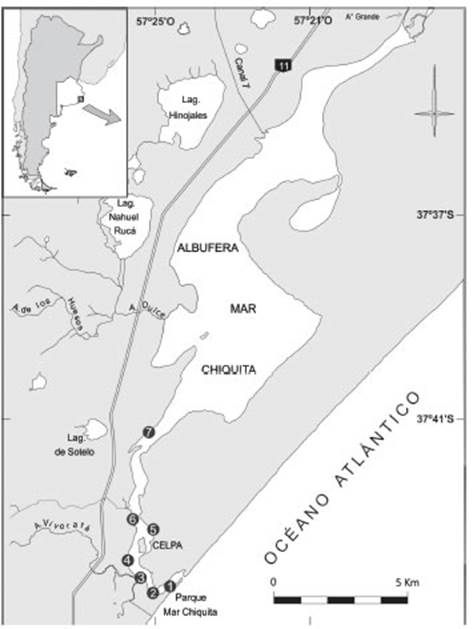
Fig. 1 Laguna costera Mar Chiquita, sureste de la provincia de Buenos Aires. Los círculos del 1 al 7 indican los distintos sitios de muestreo.

Fig. 2 Vista general de los sitios de muestreo. Sitio 1 (A). Sitio 2 (B). Sitio 3 (C). Sitio 4 (D). Sitio 5 (E). Sitio 6 (F). Sitio 7 (G).
La extracción de las muestras se llevó a cabo con una red con copo colector de 200 μm de aber tura de malla. Las muestras fueron conservadas en alcohol al 70%, y posteriormente lavadas con agua corriente a través de un tamiz. Utilizando lupa binocular (Wild Heerbrugg, aumento 50X) se recuperaron los ostrácodos presentes, que posteriormente fueron conservados en frascos con alcohol al 70%. Los individuos fueron deter minados, a partir de sus caparazones, a nivel de especie o subespecie basados en los trabajos de Sandberg (1964), Ramírez (1967), Whatley & Moguilevsky (1975), Whatley et al. (1988, 1997), Ferrero (2006) y Ramón Mercau et al. (2014). Se determinó el alto, el largo y el ancho medio de los caparazones. A los fines de estandarizar las me didas, todas las mediciones fueron efectuadas en 6 individuos adultos de cada taxón, informándo se la media y el rango de valores. Los ejemplares ilustrados se encuentran depositadas en la co lección del Instituto de Geología de Costas y del Cuaternario de la Universidad Nacional de Mar del Plata, bajo los números CGC-0- N° 145 al 148.
RESULTADOS
Los sitios de muestreo presentaron valores de conductividad entre 0,90 y 45,35 mS/cm (Tabla 2). Se hallaron cuatro taxones de ostrácodos pertenecientes al Orden Podocopida; siendo las mismas en orden decreciente de abundancia: Cyprideis salebrosa hartmanni, Callistocythere asperereticulata, Cytherura dimorphica y Limnocythere cusminskyae (Fig. 3).

Tabla 2 Valores de conductividad (en mS/cm) de los sitios de muestreo. Se muestran promedios de valores tomados en cada estación del año con su correspondiente desviación estándar y el rango de valores.

Fig. 3 Vista externa lateral de valvas de los taxones de ostrácodos presentes en la zona estuárica de la laguna cos tera Mar Chiquita. Cyprideis salebrosa hartmanni, macho (A) hembra (B) CGC-O-145/1-2; Cytherura dimorphica, macho (C) hembra (D) CGC-O-146/1-2; Callistocythere asperereticulata (E) CGC-O-147; Limnocythere cusminsk yae, macho (F) CGC-O-148. La flecha indica el extremo anterior. La barra indica 50 μm para C, D y E; y 100 μm para A, B y F.
Las mayo res abundancias de ostrácodos tuvieron lugar en primavera y otoño, particularmente en los sitios 5 y 6. No se halló ningún ostrácodo en el sitio 1 durante el invierno (Tabla 3).
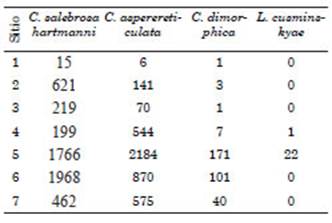
Tabla 3 Número total de individuos de cada ta xón por sitio de muestreo en 30 ml de muestra procesada.
Si bien los primeros 3 taxones referidos se hallaron representados en todos los sitios de muestreo, Cyprideis salebrosa hartmanni fue dominante en los sitios más cercanos a la des embocadura de la laguna y Callistocythere aspe rereticulata en los sitios más cercanos al cuerpo lagunar.
Lista taxonómica de los ostrácodos repor tados
Cyprideis salebrosa hartmanniRamírez, 1967
(Fig. 3. A-B)
1967. Cyprideis hartmanni Ramírez, pp. 40-42, lám. 11, figs. 74-79; lám. 12, figs. 80-89.
1983 Cyprideis salebrosa hartmanni Ramirez - emend. Ornellas & Würdig, subsp.nov. - Ornellas & Wür dig, pp. 94-112, láms. 1-6.
1987. Cyprideis salebrosa Van den Bold - Zabert & Her bst, p. 218, lám. II, fig. 5 a-e; lám. III, fig. 14 a-b.
1988. Cyprideis salebrosa Van den Bold - Dias Brito et al., lám. 1, fig. 14.
1990. Cyprideis hartmanni Ramírez - Bertels & Martínez, lám. 1, fig. 7.
1996. Cyprideis salebrosa hartmanni Ramírez - Ferre ro, p. 216, lám. 2, figs. 1a-1b.
1997. Cyprideis hartmanni Ramírez - Bertels & Martínez, pp. 35-36, lám. 1, figs. 10-11.
1997. Cyprideis salebrosa Van den Bold - Whatley et al., p. 24, lám. 3, figs. 1-2.
2006. Cyprideis salebrosa Van den Bold - Laprida, p. 194, fig. 3 D-E; fig. 6 B-D.
2009. Cyprideis salebrosa hartmanni Ramírez - Ferre ro, p. 655, fig. 9.5.
2015. Cyprideis salebrosa hartmanni Ramírez - Kihn & Gómez, p. 288, fig. 2 B.
2016. Cyprideis salebrosa Van den Bold - Márquez et al., p. 29, fig. 3 L-M.
2017. Cyprideis salebrosa Van den Bold - Kihn, p. 649, fig. 2, 1-3.
2017a. Cyprideis salebrosa hartmanni Ramírez - Kihn et al., p. 95, fig. 3 C.
2018. Cyprideis salebrosa hartmanni Ramírez - Kihn et al., p. 248, fig. 3 C-D.
2019. Cyprideis salebrosa hartmanni Ramírez - Ramos et al., p. 166, fig. 5 a-b.
2020. Cyprideis salebrosa Van den Bold - D´Ambrosio et al., p. 5, fig. 3 K.
2021. Cyprideis salebrosa Van den Bold - Campos et al., p. 84, fig. 4 L-M.
Material estudiado: Adultos: 470, Juveniles: 4780
Dimensiones:
Macho Lm: 1,17 mm (1,12-1,21); Hm: 0,62 mm (0,59-0,64); Am: 0,47 mm (0,44-0,50)
Hembra Lm: 1,03 mm (0,99-1,08); Hm: 0,60 mm (0,58-0,63); Am: 0,51 mm (0,48-0,55)
Ejemplares ilustrados:
CGC-O-145/1 valva izquierda macho, L: 1,05 mm, H: 0,57 mm
CGC-O-145/2 valva derecha hembra, L: 0,99 mm, H: 0,57 mm
Observaciones: Se identificaron individuos ju veniles y adultos, tanto hembras como machos. Con relación a sus características ecológicas, esta subespecie ya había sido referida como eurihali na y propia de ambientes mixohalinos. Coimbra et al. (2007) afirman que es más abundante en aguas mixomesohalinas a mixoeuhalinas, que en ambientes mixooligohalinos a oligohalinos. No obstante, su amplio nicho ecológico le permiti ría desarrollarse también en condiciones de baja salinidad (Ramírez, 1967; Laprida, 2006). Por otro lado, Laprida (2006) sugiere que la subes pecie solo puede vivir en ambientes con estabi lidad temporal (cuerpos de agua permanentes), estando ausente en cuerpos de agua temporarios y semipermanentes.
Distribución geográfica y estratigráfica: En Argentina, ha sido registrada en la laguna Chascomús (Buenos Aires), viviendo sobre ve getación litoral (Ramírez, 1967; Laprida, 2006). Whatley et al. (1997; 1998) la registraron en am bientes litorales y de plataforma, entre 35º43´S y 40º40´S en el estuario del Río de la Plata, Playa Grande (Mar del Plata, Buenos Aires), Bahía San Blas (Buenos Aires) y San Antonio Oeste (Río Negro). La subespecie ha sido registrada en el Pleistoceno Tardío en las provincias de Entre Ríos (arroyo Perucho Verna; Zabert & Herbst, 1987), Santa Fe (río Carcaraña; Segovia, 2014), Mendoza (laguna Llancanelo; D´Ambrosio, 2014) y Buenos Aires: río Luján (De Francesco & Blasi, 2012), río Salto-Arrecifes (Blasi et al., 2016, 2020) y cantera “Nicolás Vignogna III”, en el partido de Marcos Paz (Iacona & Carignano, 2018). En el Holoceno, se registra en las provin cias de San Luis (Salinas del Bebedero; Calvo Marcilese et al., 2019), Santa Fe, Entre Ríos (Segovia, 2014), Catamarca (Espíndola, 2019), Jujuy (lago Runtuyoc; D´Ambrosio et al., 2020) y Buenos Aires. En esta última provincia se presenta en sedimentos continentales del río Quequén Grande (Zárate et al., 1998; Ferrero, 1996), laguna del Sauce Grande (Fontana, 2005), arroyo San Miguel (Ramos et al., 2019) y laguna Blanca Grande (López Blanco et al., 2021) y tam bién en sedimentos estuáricos de Bahía Blanca (Bertels & Martínez, 1990, 1997; Gómez et al., 2005; Martínez, 2005; Cusminsky et al., 2006; Kihn et al., 2011, 2017a, 2018; Kihn, 2015, 2017; Kihn & Gómez, 2015).
Callistocythere asperereticulataWhatley & Moguilevsky, 1973
(Fig. 3. E)
1973. Callistocythere asperereticulata Whatley & Mo guilevsky, pp. 489-493, figs. 1-8.
1975. Callistocythere n. sp. C Whatley & Moguilevsky, pp. 516-517, lám. 2, figs. 6-9; lám. 3, figs. 23, 25, 28.
1997. Callistocythere asperereticulata Whatley & Mo guilevsky - Whatley et al., p 45-46, lám. 7, figs. 1-3.
Material estudiado: Adultos: 4077, Juveniles: 313
Dimensiones: Lm: 0,43 mm (0,42-0,44); Hm: 0,24 mm (0,23-0,25); Am: 0,21 mm (0)
Ejemplar ilustrado: CGC-O-147 valva dere cha, L: 0,44 mm, H: 0,25 mm
Observaciones: Se identificaron juveniles y adultos, no habiéndose podido efectuar el sexado debido a dificultades metodológicas para acceder a las partes blandas.
Distribución geográfica: Si bien no se co nocen demasiados datos en torno a la distribu ción geográfica y características ecológicas de la especie, Whatley & Moguilevsky (1975) y Whatley et al. (1997) reportaron su presencia en Punta Ramírez (Buenos Aires), Arroyo Jabalí (Buenos Aires), Las Grutas (Río Negro) y Punta Delgada (Chubut) usualmente en asociaciones fitales (sobre la superficie de algas); estando particularmente asociada a los géneros Ulva, Enteromorpha, Ceramium y Polisiphonia. El ho lotipo de la especie corresponde a una valva ha llada en la laguna costera Mar Chiquita.
Cytherura dimorphicaBertels & Martínez, 1997
(Fig. 3. C-D)
1990. Cytherura sp.n. - Bertels & Martínez, lám. 3, fig. 22.
1996. Cytherura sp. - Ferrero, p. 219, lám. 2, figs. 4 a-b.
1997. Cytherura dimorphica - Bertels & Martínez, p. 43, lám. 3, figs. 2-5; lám. 6, fig. 10.
1998. Cytherura dimorphica Bertels & Martínez - La prida, p.468, lám. 3, fig. 9.
2006. Cytherura dimorphica Bertels & Martínez. - La prida, p. 196, fig. 3 G, fig. 7 G-I.
2016. Cytherura dimorphica Bertels & Martínez - Már quez et al., p. 29, fig. 3 R.
2019. Cytherura dimorphica Bertels & Martínez - Ra mos et al., p. 166, fig. 5 g.
Material estudiado: Adultos: 324, Juveniles: 0
Dimensiones:
Macho Lm: 0,45 mm (0,43-0,47); Hm: 0,21 mm (0,20-0,22); Am: 0,18 mm (0,17-0,19)
Hembra Lm: 0,42 mm (0,40-0,46); Hm: 0,23 mm (0,20-0,23); Am: 0,20 mm (0,19-0,21)
Ejemplares ilustrados:
CGC-O-146/1 valva derecha macho, L: 0,44 mm, H: 0,21 mm
CGC-O-146/2 valva derecha hembra, L: 0,44 mm, H: 0, 23 mm
Observaciones: Solo se identificaron indivi duos adultos, machos y hembras. Con relación a sus características ecológicas, esta especie ya ha bía sido referida como una especie marino-litoral típica de ambientes salobres poco profundos y con variaciones de salinidad marcadas. Laprida (2006) señala la misma como especie indicadora de aguas oligomesohalinas a polihalinas, Cl-/Na+ dominadas, sometidas a fuertes variaciones dia rias de la salinidad; características propias de los ambientes estuáricos. Martínez (2005) reportó su presencia en planicies de marea del estuario de Bahía Blanca; dentro de poblaciones con una reducida proporción de juveniles. Whatley et al. (1988) propusieron la posibilidad de que estos organismos posean filamentos de fijación al sus trato que evitan sus desplazamientos, lo que les permitiría habitar ambientes de mayor energía donde el sustrato resulta más inestable.
Distribución geográfica y estratigráfica: Se reportó la presencia de ejemplares vivos en las planicies de mareas del estuario de Bahía Blanca (Martínez, 2005), Punta Rasa (Buenos Aires) y Canal 15 (Buenos Aires) (Laprida, 2006). La es pecie ha sido registrada en la provincia de Buenos Aires en sedimentos del Pleistoceno Tardío de la laguna costera Mar Chiquita (Ferrero, 2009) y en sedimentos holocenos de la Bahía Samborombón (Laprida, 1998), el río Quequén Grande (Ferrero, 1996), el arroyo Las Brusquitas (Márquez et al., 2016), el arroyo San Miguel (Ramos et al., 2019) y el estuario de Bahía Blanca (Bertels & Martínez, 1990, 1997; Cusminsky et al., 2006; Kihn et al., 2011; Kihn, 2015).
Limnocythere cusminskyaeRamón-Mercau et al., 2014
(Fig. 3. F)
1990. Limnocythere sp.n. Bertels & Martínez, fig. 11.
1996. Limnocythere staplini Gutentag & Benson - Fer rero, fig. 4, 1a-1d.
1997. Limnocythere sp. Bertels & Martínez, lám. V, fig. 2-3; lám. VI, figs. 16-17.
1998. Limnocythere sp. 1. Bertels-Psotka & Laprida, fig. 1.
1998. Limnocythere staplini Gutentag & Benson - Laprida, fig. 14.
2006. L. aff. L. staplini. Laprida, fig. 3, J-L. Limno 185
cythere sp. Laprida, fig. 3, H.
2009. Limnocythere staplini Gutentag & Benson - Fer rero, fig. 10, 5-6.
2014. Limnocythere cusminskyae Ramón Mercau et al., p. 29, fig. 2 a-h.
2016. Limnocythere cusminskyae Ramón Mercau et al. - Márquez et al., p. 29, fig. 3 N-O.
2017b. Limnocythere cusminskyae Ramón Mercau et al. - Kihn et al., p. 378, fig. 3 H-J.
2017. Limnocythere cusminskyae Ramón Mercau et al. - Coviaga et al, p. 7, fig.2 S-T.
2019. Limnocythere cusminskyae Ramón Mercau et al. - Ramos et al., p. 166, fig. 5 c-d.
Material estudiado: Adultos: 20, Juveniles: 3
Dimensiones: Lm: 0,62 mm (0,58-0,64); Hm: 0,29 mm (0,27-0,30); Am: 0,20 mm (0,19-0,21)
Ejemplar ilustrado: CGC-O-148 valva derecha macho, L: 0,61 mm, H: 0,29 mm
Observaciones: Todos los individuos recolecta dos fueron machos, lo que puede deberse al pe queño tamaño de la muestra colectada. Algunos estudios llevados a cabo en la región pampeana sobre sucesiones holocénicas coinciden al señalar la especie como indicadora de ambientes salobres someros, con elevado contenido de bicarbonato y sodio (Laprida, 2006; Ramón Mercau et al., 2014).
Distribución geográfica y estratigráfica: Se encontraron especímenes vivos en las lagu nas bonaerenses de Chascomús, Salada Grande, Los Horcones, del Monte y en el Arroyo Grande (Laprida, 2006); en la laguna Asansa (Río Negro) (Coviaga, 2015) y en las lagunas Monte de Caldén, General Campos y Don Tomás (La Pampa) (Kihn et al., 2017b). La especie ha sido registrada en la provincia de Buenos Aires en sedimentos del Pleistoceno Tardío de la laguna Mar Chiquita (Ferrero, 2009) y de la cantera “Nicolás Vignogna III”, en el partido de Marcos Paz (Iacona & Carignano, 2018) y en sedimentos holocenos de los ríos Napostá Grande (Bertels & Martínez, 1990, 1997) y Quequén Grande (Ferrero, 1996; Zárate et al., 1998), las lagunas Hinojales (Prieto et al., 1998), La Brava (Plastani, 2016; Laprida et al., 2014), La Barrosa (Plastani, 2016; Plastani et al., 2019), Cabeza de Buey (Plastani, 2016) y Blanca Grande (López Blanco et al., 2021), los arroyos Chico (Plastani, 2016) y San Miguel (Ramos et al., 2019) y el Canal 15 (Laprida, 1998; Bertels-Psotka & Laprida, 1998).
DISCUSIÓN
La fauna de ostrácodos de la laguna costera Mar Chiquita se destaca por la dominancia de Cyprideis salebrosa hartmanni y Callistocythere asperereticulata en un rango salino de 1 a 45 mS/ cm. Los taxones mencionados son representan tes de dos géneros muy frecuentes en sistemas estuáricos. Estos resultados son coincidentes con los obtenidos en estudios ecológicos llevados a cabo en el estuario de Bahía Blanca (Kihn et al., 2016), donde se observó la coexistencia de Cyprideis salebrosa hartmanni y Callistocythere litoralensis (Rossi De García, 1966) formando parte de comunidades poco desarrolladas en cu betas salinas o salt pan del Canal Maldonado y Villa del Mar; con salinidades variables inferio res a 34,8%. Además, Cyprideis salebrosa hart manni y Callistocythere nucleoperiscumWhatley, Moguilevsky, Toy, Chadwick & Ramos, 1998 se hallaron formando parte de sedimentos areno sos finos y pelíticos en el intermareal bajo y me dio del canal de marea principal del estuario de Bahía Blanca, bajo condiciones de salinidad rela tivamente estables y elevadas; en un rango de 28 a 35 ups (Kihn et al., 2017a).
Callistocythere asperereticulata, especie cu yas características han sido escasamente descrip tas en la bibliografía existente, se halló en abun dancia y ampliamente distribuida en todas las estaciones del año y en todos los sitios de mues treo; dominando los ensambles más alejados a la desembocadura, en un rango salino de 7 a 21 mS/ cm. Estos resultados sugieren una tolerancia a condiciones de salinidad variable.
Algunos taxones de la laguna costera Mar Chiquita se han registrado viviendo en otros sis temas hídricos de la provincia de Buenos Aires. Tal es el caso de Cyprideis salebrosa hartmanni, cuya presencia fue previamente reportada en la Pampa bonaerense, tanto en ambientes estuári cos como en lagunas permanentes sin conexión marina; y Cytherura dimorphica, hallada solo en ambientes estuáricos de la Pampa Austral y la Pampa Deprimida (Martínez, 2005; Laprida, 2006). Por otro lado, si bien la presencia de ejem plares vivos de Limnocythere cusminskyae en lagunas de la provincia de Buenos Aires fue pre viamente interpretada como potencial indicado ra de ambientes permanentes oligo-mesoalinos (Laprida, 2006); el presente trabajo constituye el primer registro de la especie en un ambiente estuárico.
La composición faunística y las variaciones cuantitativas de los ostrácodos pueden relacio narse con la energía en las áreas submareales; mientras que, en las planicies de marea, la varia ción de la salinidad, la topografía, la sedimento logía y la vegetación son las variables más rele vantes (Kihn et al., 2016, 2017a). En el presente estudio, si bien la salinidad no presenta marca das diferencias entre los sitios muestreados, los valores de conductividad obtenidos dan cuenta de que dicha variable es ampliamente fluctuante temporalmente para cada sitio; excepto el sitio 7, el cual presenta una mayor estabilidad en los rangos salinos. Estos resultados coinciden con datos previamente obtenidos en la laguna costera Mar Chiquita, donde se observaron patrones es tacionales muy variables de salinidad (Reta et al., 2001; De Francesco & Isla, 2003; Marcovecchio et al., 2006; Hassan et al., 2009).
Según Kihn et al. (2017a) la salinidad es una de las variables ambientales más relevantes que rigen la distribución de las especies de ostráco dos en ambientes estuáricos. Esto coincide con lo propuesto previamente por Engel & Swain (1967), Keyser (1977), Cronin (1979), Frenzel & Boomer (2005) y Coimbra et al. (2007), quienes postulan que la adaptación a variaciones en la salinidad es el factor con mayor incidencia en el control ecológico de la estructuración de las po blaciones de ostrácodos y su distribución en am bientes estuáricos. Horne et al. (2021) señalan a la salinidad, junto a las mareas y a los cambios meteorológicos, como un factor relevante a tener en consideración en la caracterización comple ta, desde un punto de vista espacio-temporal, de la riqueza específica de la ostracofauna en am bientes vinculados a los estuarios. Este esquema responde tanto a las características de la laguna costera Mar Chiquita, caracterizada por sus am plias variaciones diarias en la salinidad; como a los resultados obtenidos en el presente trabajo, dónde existe una preponderancia de taxones eu rihalinos y la riqueza especifica es reducida tanto espacial como temporalmente.
CONCLUSIÓN
La ostracofauna viviente de la zona estuá rica de la laguna costera Mar Chiquita se halla caracterizada por su reducida diversidad, y la presencia de Cyprideis salebrosa hartmanni, Callistocythere asperereticulata, Cytherura di morphica y Limnocythere cusminskyae; taxones típicos de ambientes estuáricos y de mezcla, tole rantes a rangos variables de salinidad.












 uBio
uBio 


