INTRODUCCIÓN
La reciente aparición del nuevo virus SARS-CoV-2 plantea un gran desafío para los planificadores y decisores en salud, que deben movilizar recursos finitos, reorganizar los sistemas de atención y tomar decisiones sobre el funcionamiento de la sociedad en un contexto de gran incertidumbre.
Los modelos matemáticos son herramientas invaluables para la planificación; al hacer explícitos los supuestos en los que se basan, pueden probar diferentes hipótesis y cuanti-ficar los riesgos, beneficios y costos anticipados asociados con las actividades de control de enfermedades1.
Los modelos matemáticos de las enfermedades humanas tienen una larga historia. En 1760 Bernoulli comenzó a usar modelos matemáticos para estudiar la propagación de la viruela por vacunación2. Hamer construyó un modelo temporal para el estudio de epidemias recurrentes de sarampión en 19063. Kermack y McKendrick4 establecieron un principio fundamental cuando afirmaron que el nivel de susceptibilidad en la población debe ser suficientemente alto para que se desarrolle una epidemia. De este principio se derivó un modelo simple, que describe la dinámica de transmisión de la enfermedad entre individuos en una población mixta homogénea: el denominado modelo epidémico SIR (Susceptibles-Infectados-Recuperados) clásico5, que hoy sigue siendo utilizado para modelizar la infección COVID-19. La validez del modelo SIR ha sido probada por los datos de múltiples epidemias a gran escala. Sobre la base del SIR se propuso la teoría del umbral6, según la cual la introducción de individuos infecciosos dentro de una población de susceptibles podrá originar una epidemia sólo si la densidad de susceptibles sobrepasa un cierto valor crítico o umbral. Si se excede el umbral, sobreviene el brote; de lo contrario, desaparece. Aron y Schwartz propusieron el modelo SEIR (Susceptibles-Expuestos-Infectantes-Recuperados) en 19847. Este modelo asume que la latencia de las enfermedades infecciosas también tiene un impacto en las epidemias, por lo que algunos consideran que es más realista8. En un esfuerzo por incorporar información relevante del manejo de las epidemias modernas, se han ido proponiendo modelos cada vez más complejos9, como el SEQIJR (Susceptible-Ex-puesto-Cuarentena-Infectante-Aislado-Recuperado) y el SEIRP (Susceptible-Expuesto-Infectante-Recuperado-Preservado), para analizar un brote de SARS y los efectos del aislamiento y de una posible vacuna10,11.
La modelización matemática se ha convertido en un enfoque muy utilizado para evaluar el impacto de las estrategias de intervención de salud pública y sugerir el curso de acción óptimo en el abordaje de enfermedades emergentes, como ocurrió con el SARS, el H1N1 y el ébola12,13. Los modelos pueden intentar proyectar la evolución natural de un fenómeno, pero con frecuencia incluyen una o varias intervenciones sanitarias para poner a prueba su posible efecto14-15. El modelado matemático resalta los factores clave y proporciona predicciones cuantitativas para la efectividad y los costos y consecuencias de las políticas de control de enfermedades.
Este estudio apuntó a revisar la evolución de los distintos tipos de modelos predictivos existentes, sus características principales, limitaciones y vinculación con la toma de decisiones en contexto de pandemia en Argentina y otros países.
MÉTODOS
Se realizó una búsqueda bibliográfica en Cochrane, en la base de datos de la Organización Mundial de la Salud16, en PubMed y LILACS sobre las publicaciones relacionadas con modelos matemáticos aplicados a la salud y específicamente sobre la evolución de esta pandemia al 9 de mayo de 2020. Se excluyeron los modelos de predicción o pronóstico para ser aplicados sobre individuos. Se identificó el número de publicaciones en Medline desde 1945 hasta el 9 de mayo de 2020, indexadas bajo los términos MESH ("Models, Statistical"[Mesh]) OR "Models, Theoretical"[Mesh]. La Tabla 1 muestra los sitios y estrategias de búsqueda y los resultados sobre modelos relacionados con la pandemia por COVID-19.
Los resultados obtenidos fueron analizados para identificar los tipos de modelos utilizados y sus características principales.
Se analizaron los proyectos presentados para financia-mlento del Ministerio de Ciencia, Tecnología e Innovación (MinCyT) en la convocatoria COV1D, estimando qué porcentaje de ellos correspondían a modelos.
Se clasificaron y describieron los tipos de modelos más utilizados, como los determinísticos y los estocásticos. Se comentaron los supuestos asumidos y las principales teorías subyacentes. Se explicaron los componentes principales de los modelos como el número reproductivo básico ( R0), los programas de software utilizados y los abordajes para manejar la incertidumbre.
RESULTADOS
En Medline-PubMed el número de publicaciones con alguno de los dos términos MESH ("Models, Statistical"[Mesh]) OR "Models, Theoretical"[Mesh] arrojó un total de 1 749 791 estudios publicados desde 1945. En el siguiente gráfico se ilustra la evolución temporal de las publicaciones científicas relacionadas con el uso de modelos aplicados a la salud humana, indexadas con alguno de esos dos términos de búsqueda (ver Gráfico 1). En el mismo se observa un incremento sostenido en las publicaciones vinculadas con modelos en salud.
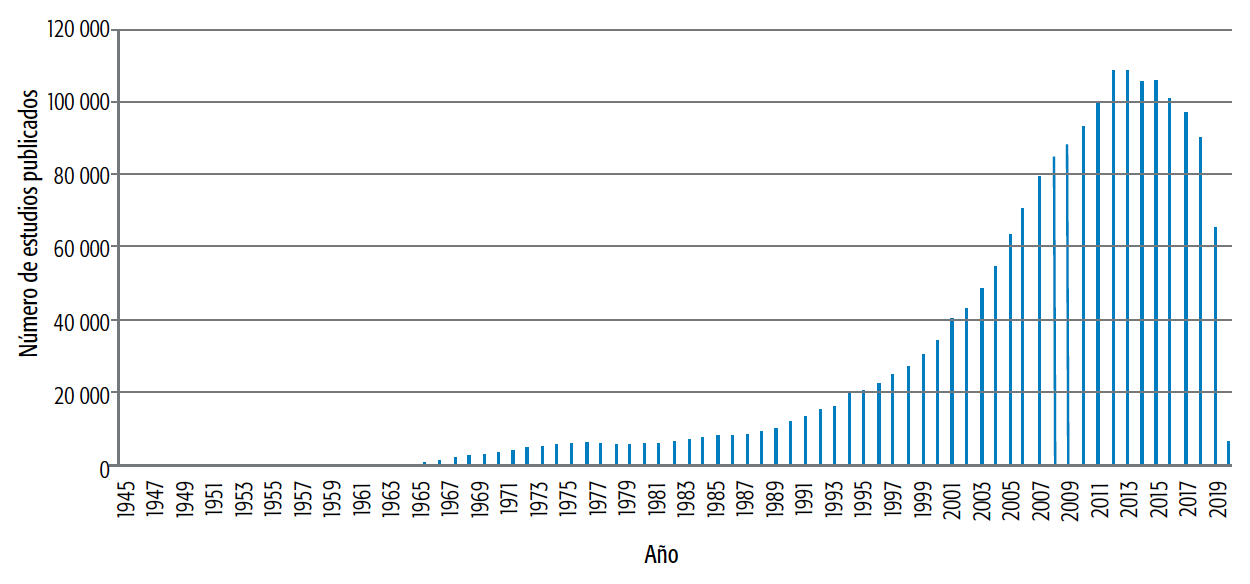
GRÁFICO 1 Publicaciones en Medline desde 1945 hasta el 9/5/2020 indexadas bajo MESH ("Models, Statistical"[Mesh]) OR "Models, Theoretical"[Mesh ].
En ninguna de las cuatro bases de datos bibliográficas consultadas se encontraron publicaciones de Argentina. Dos grupos técnicos, en los que participan los autores, se reúnen semanalmente para compartir modelos predictivos en el marco de la Organización Mundial de la Salud (OMS) y la Organización Panamericana de la Salud (OPS). Diversos investigadores argentinos participan y han publicado sus modelos en sitios web como material preimpreso sin revisión de pares17,18 (como https://www.medrxiv.org/, https://arxiv.org/, https://www.researchgate.net/), en las páginas web de sus instituciones19 o de sitios colaborati-vos (como https://github.com/), muchos de ellos de libre acceso. En estos espacios, que pueden catalogarse como "literatura gris"20, se identifica una prolífica producción de modelos predictivos nacionales. En la reciente convocatoria extraordinaria del MinCyT de Argentina para financiar Ideas-Proyecto COV1D-19, hubo 986 postulaciones, de las cuales 19 correspondieron a modelos matemáticos. De los 41 proyectos seleccionados, 3 (7%) incluyen el análisis a partir de modelos predictivos21.
No se encontraron revisiones sistemáticas sobre modelos predictivos de evolución de la pandemia por COV1D-19 a nivel poblacional, pero una revisión sistemática analizó modelos predictivos de diagnóstico y evolución clínica en individuos con COV1D-1 922. Si bien el objetivo de la revisión era otro tipo de modelos, se destacan las conclusiones de los revisores, que consideran que la mayoría de los modelos publicados tienen déficit en la calidad del reporte y presentan alto riesgo de sesgos. La Colaboración Cochrane no ha publicado revisiones sistemáticas sobre modelos, pero dentro de su repositorio "Evidencias COV1D-19" incluyó el documento "Respuestas COV1D-19", con revisiones rápidas de la literatura que responden preguntas prioritarias. En el documento titulado "¿Qué ofrecen los modelos matemáticos para estimar la necesidad de hospitalización y/o tratamiento en las unidades de cuidados intensivos debido a la COV1D-19?"23, los autores identificaron 10 modelos publicados en revistas sin revisión de pares, la mayoría modelos tipo SE1R.
Se identificaron modelos publicados programados en R-project, earlyR, Excel, Data Tree Age, Python y Fortran, entre otros. Muchos de los autores de modelos han dejado sus programaciones abiertas y disponibles para ser
compartidas24,25.
La mayoría de los modelos compartimentados analizaron como variables dependientes la evolución en el tiempo del total de susceptibles, infectados y recuperados; a partir de estos datos estimaron los hospitalizados en sala general, terapia intensiva, con necesidad de asistencia respiratoria mecánica y muertes. Muchos modelos incorporaron la capacidad de sus sistemas de salud para evaluar el grado de saturación, aunque pocos evaluaron los costos y la costo-efectividad comparativa de las diversas intervenciones26.
Como variables independientes se utilizaron distintas medidas no farmacológicas, como cierre de escuelas, de bares y restaurantes, del transporte público, de fábricas y fronteras, y distintos grados de adherencia al distanciamiento social, entre otras.
Se identificaron dos grandes tipos de modelos matemáticos epidemiológicos: deterministicos y estocásticos. En un modelo determinista es posible controlar todos los factores que intervienen en el estudio del fenómeno y predecir sus resultados con exactitud; bajo este modelo, un solo sujeto causa una epidemia generalizada. En un modelo estocásti-co no es posible controlar todos los factores concurrentes, de manera que los resultados no son únicos, y existe la posibilidad de que la epidemia se extinga27. En la teoría de la probabilidad, un proceso estocástico es un concepto matemático que sirve para usar magnitudes aleatorias que varían con el tiempo o para caracterizar una sucesión de variables aleatorias (estocásticas) que evolucionan en función de otra variable, generalmente el tiempo. Cada una de las variables aleatorias del proceso tiene su propia función de distribución de probabilidad, y ellas pueden o no estar correlacionadas entre sí. Cada variable o conjunto de variables sometidas a influencias o efectos aleatorios constituye un proceso estocástico. Se pueden utilizar simulaciones como la de Monte Carlo o la simulación de eventos discretos para someter a una población imaginaria a una serie de sucesos, algo así como tirar los dados o la moneda cada vez que uno de los pacientes imaginarios pasa un día, para definir si ese paciente se enferma o no.
En una primera clasificación de los modelos utilizados para la proyección de la pandemia, se pueden nombrar los modelos determinísticos, como los SIR o SEIR, que resuelven ecuaciones diferenciales ordinarias en compartimentos; los estadísticos, que aplican el análisis de series de tiempo (ARMA, ARIMA28), así como los que utilizan análisis regresivos (de Poisson, de Boltzmann29); y los modelos estocásticos, que consideran aleatoriedad en el proceso de infección. Estos últimos pueden aplicar cadenas markovianas al análisis de series de tiempo, o incorporan aleatoriedad a las variables generando "casos" mediante simulaciones de Monte Carlo y una distribución estadística propia de la variable que consideran aleatoria. También se pueden nombrar otros modelos estocásticos más complejos, que adoptan procesos estocásticos o intentan resolver ecuaciones diferenciales con variables aleatorias.
Los modelos son simplificaciones de la realidad y, por lo tanto, se basan en ciertas asunciones, que deben ser explicitadas. Por ejemplo, en la mayoría de los modelos publicados se asumió que no habrá nacimientos y muertes por otras causas en la población estudiada (lo cual facilita el análisis) y que toda la población es homogénea en cuanto a edad, riesgo de contagio, riesgo de presentar formas graves de la enfermedad, etc. Además, la mayoría de los modelos identificados plantearon el análisis a nivel país, lo que presume un comportamiento similar de todas las provincias. Los modelos de compartimentos suponen que la población está homogéneamente mezclada (una suposición razonable para países pequeños, pero dudosa para otros más grandes y heterogéneos como Argentina). Se encontraron modelos más complejos, que simularon las interacciones cotidianas de millones de personas y podrían resultar más adecuados. La mayor parte de los modelos asumieron que las fronteras permanecen cerradas, aunque algunos analizaron la transmisión interna y externa por movimientos a través de fronteras30. Algunos modelos utilizaron matrices de contacto31, que incorporaron al análisis los posibles contactos entre diferentes grupos sociales en distintos ámbitos, como el hogar, el trabajo, la escuela o un geriátrico y, por ende, permitieron evaluar con mayor precisión las posibilidades de contagiar y transmitir la enfermedad.
Por su amplia utilización en los modelos, se describen el número reproductivo básico o R0 y las ecuaciones diferenciales. El modelo SIR se define por un sistema de tres ecuaciones diferenciales ordinarias, a saber:
1) dS/dt = - ΒIS/N
2) dI/dt = ΒIS/N - y*I
3) dR/dt = y*I
donde Β es la tasa de transmisión, y es la tasa de recuperación (o la inversa del período infeccioso) y N es el tamaño total de la población, de manera que N=S+I+R. En el modelo ordinario de la ecuación 1 se da por sentado que no hay nacimientos ni muertes. Al comienzo del brote o epidemia (t=0), se supone que la población está constituida totalmente por individuos susceptibles y un solo individuo infeccioso.
El R0 se generaliza al número de reproducción básico, que se define como el número promedio de casos secundarios generados por un caso infeccioso a lo largo del período. Si se lo va estimando durante la epidemia, en un momento específico t se lo denomina Rt. Este valor cambia a medida que la población se inmuniza, ya sea por inmunidad individual después de la infección, por vacunación o muerte, y también a partir de las políticas públicas establecidas para frenar la transmisión del virus (cierre de escuelas, aislamiento, etc.). Se considera que la epidemia está bajo control cuando Rt<1, y en aumento cuando Rt>1. Este número ayuda a estimar la velocidad con que una enfermedad puede propagarse en una población. El valor de R0 depende tanto de la enfermedad como de la población huésped, de manera que para una misma enfermedad puede variar según el grupo poblacional debido a diferencias demográficas, gradientes rurales-urbanos y estructuras de contacto32. En una población cerrada, una enfermedad infecciosa con un R0 conocido producirá una epidemia sólo si existe una fracción umbral de susceptibles mayor a 1/R33.
El R0 de la COVID-19 ha sido estimado entre 1,5 y 334,35. En epidemias en las cuales los datos se actualizan continuamente, esto es muy dependiente del sistema de vigilancia implantado (cada uno de ellos tiene puntos fuertes y flacos, que deben tenerse en cuenta sobre todo en el contexto del sistema de salud). En epidemias previas, como la de H1N1, se observó una heterogeneidad considerable en los valores del R0 de diferentes regiones del mundo. Casi no hay datos científicos que indiquen que el R0 de una zona geográfica sea aplicable a otra, y muchos estudios efectuados en una misma región han arrojado una gran variedad de resultados36. Estudios recientes plantean que las disparidades encontradas entre el estimado en Wuhan y el estimado en Lombardía se deberían principalmente a diferencias en el grado de subregistro de casos asintomáticos entre esas regiones37.
En la Tabla 2 se ilustran los parámetros con los que se construye el R0 a nivel nacional, como el tiempo de duplicación de casos y el parámetro B, y como han ido cambiando desde el inicio de la pandemia.
Un modelo puede diseñarse para intentar predecir la evolución de la pandemia en los próximos meses o años. Cuanto más largo el horizonte temporal, mayor incertidumbre se debe incorporar y tolerar, ya que aumentan los interrogantes respecto a muchos aspectos, como la inmunidad en los infectados o la evolución de los contagios al relajar las medidas de aislamiento. Muchos modelos publicados fijaron un horizonte temporal hasta diciembre de 2020; los que lo prolongaron a uno o dos años, se plantearon si esta enfermedad habrá de presentar variaciones estacionales que, en caso de comprobarse, requerirán su consideración38.
Los modelos compartimentados, como el SIR, el SEIR u otros más complejos, incluyeron diversas intervenciones, como el uso de vacunas, barbijos, lavado de manos, cierre de escuelas, distanciamiento social, aislamiento o cuarentena; y evaluaron el grado de potencial utilización de recursos, como camas de hospital, internaciones en terapia intensiva, necesidad de respiradores mecánicos o de hemodiálisis. Dado que todas estas variables dependen de muchos factores, algunos de ellos culturales, políticos y sociales, sería poco confiable un modelo que asegure exactamente cuántos respiradores necesitará un sistema de salud en una determinada fecha o en cuánto se reducirá la tasa de contagios al decretar el cierre de escuelas. Por tal motivo, la mayoría de los modelos publicados incorporaron la incertidumbre y la delimitaron, por ejemplo, planteando intervalos o rangos dentro de los cuales se consideró que el parámetro podría encontrarse, con un determinado nivel de confianza.
En los lugares donde aún no se ha llegado al pico máximo de casos, el tiempo y el ancho del pico son inciertos debido a la estocasticidad en la dinámica temprana, a heterogeneidades en los patrones de contacto, a la variación espacial y a la incertidumbre en los parámetros epidemiológicos clave38. Allí donde se ha presentado un buen control de la pandemia con intervenciones de distanciamiento social estricto, muchos modelos prevén un rebrote al relajar estas medidas, incluso después de 12-18 meses39.
El Centro Universitario de Estudios de Salud, Economía y Bienestar40 ha elaborado modelos (SIR y SEIR) que se encuentran abiertos y disponibles, y están siendo utilizados por sistemas de salud provinciales, regionales y municipales41. Participa semanalmente de grupos de discusión técnica de modelos para COVID en el marco de la OPS y de la OMS, donde se encuentran y colaboran múltiples equipos de diversas profesiones que buscan transferir conocimiento de la academia hacia los niveles de toma de decisión.
DISCUSIÓN
Una importante cantidad y diversidad de modelos predictivos sobre la evolución de la pandemia por COVID-19 han sido publicados a nivel mundial. Si bien no se identifican modelos realizados en Argentina en publicaciones indexadas, muchas universidades, centros de estudios y redes colaborativas se encuentran desarrollando modelos con este fin, algunos con financiamiento del Estado nacional.
La vinculación entre los modelos matemáticos y la toma de decisiones es un área controvertida. Ha habido autoridades sanitarias de países que modificaron su estrategia ante la pandemia sobre la base de la publicación de modelos predictivos. Tal vez la más renombrada fue la del Reino Unido42, que inicialmente había recomendado favorecer la inmunidad de rebaño permitiendo los contagios controlados y luego viró radicalmente hacia un distanciamiento social y restricción del movimiento poblacional. Según las autoridades, este giro se basó en proyecciones de los modelos nuevos43, que predecían cientos de miles de muertes evitables con las nuevas medidas. De todas formas, el porqué de ambas decisiones llama a reflexionar sobre la necesidad de hacer modelos más transparentes, basados en las mejores evidencias disponibles, y acompañarlos de mejores comunicaciones públicas sobre las decisiones políticas44. Probablemente el giro en la estrategia no se debió solamente a la publicación del modelo45, pero evidentemente este fue incorporado como un insumo de gran importancia para el proceso de toma de decisión. Hay quienes consideran que se está dando demasiada importancia a los modelos, mientras que otros sostienen que sin predicción matemática los tomadores de decisión se encuentran a ciegas46.
El impacto de las intervenciones no farmacológicas sobre la evolución de la pandemia dependerá en gran medida del contexto sociocultural y político. Se plantea que en países asiáticos la adherencia a estas intervenciones fue muy elevada, mientras que en sociedades occidentales sería menor. Diversos autores estiman que en Wuhan el distanciamiento social y otras medidas de mitigación demostraron reducir la tasa de transmisión del Rt desde valores de entre 2,38 y 3,1 a valores de entre 0,5 y 1 en pocas semanas47-49. Autores norteamericanos consideran que en sociedades occidentales la reducción en la transmisión sería de 3,0 a 1,6, en línea con medidas de distanciamiento social menos estrictas38. En Argentina se utilizaron diferentes escenarios para analizar a partir de un modelo SE1R las posibles implicancias de diversas políticas de salida de la cuarentena en forma escalonada50.
Las actividades de traducción del conocimiento siguen siendo un componente clave de los esfuerzos de modelado para guiar la Salud Pública en tiempos de crisis e informar a los responsables de la toma de decisiones sobre la efectividad de las políticas y los posibles resultados de diferentes escenarios. En palabras de Neil Ferguson, con los modelos "estamos construyendo representaciones simplificadas de la realidad. Los modelos no son bolas de cristal"51. Se requiere, hoy más que nunca, una comunicación efectiva entre los modeladores, los planificadores y los encargados de formular políticas para que el modelado sea más adecuado y aplicable a las necesidades de planificación de la Salud Pública y la toma de decisiones.
















