INTRODUCCIÓN
La enfermedad por el coronavirus 2019 (COVID-19, por su sigla en inglés) es una enfermedad respiratoria de los seres humanos producida por un nuevo coronavirus identificado con la sigla SARS-CoV-21.
El primer registro de la infección por COVID-19 se realizó el 31 de diciembre de 2019 cuando la Comisión Municipal de Wuhan informó a la Organización Mundial de la Salud (OMS) sobre varios casos de neumonía de etiología desconocida. El 13 de enero de 2020 se confirmó de forma oficial en Tailandia el primer caso de COVID-19 fuera de China2. El 11 de marzo de 2020, la OMS declaró la COVID-19 como una pandemia2. Desde ese momento, y hasta el 10 de noviembre, se informó su circulación en más de 200 países, con más de 13 983 099 casos activos a la fecha y más de 37 530 250 casos cerrados, de los cuales el 3% murió (1 273 385 casos)3.
Este crecimiento rápido de la enfermedad a nivel mundial llevó a la creación de varios modelos para la estimación de su impacto en distintos países 4-7. Estos modelos fueron de distinta complejidad y buscan no solo la proyección de casos y fallecidos de la pandemia sino, además, influir en la toma de decisiones para buscar las mejores estrategias y momentos para la implementación de las distintas intervenciones destinadas a la disminución de la propagación y la mortalidad asociada a esta enfermedad.
Muchos de los modelos epidemiológicos usados durante la pandemia provienen de una base de modelos compartimentales como los modelos SIR (susceptibles, infectados, recuperados) o SEIR8-10. Estos últimos posicio-nan a los individuos en cuatro compartimientos relevantes que determinan el curso de la epidemia: susceptibles (S), expuestos (E), infectados (I) y recuperados (R). El compartimiento S se refiere al número de personas vulnerables a infectarse; es decir, sin inmunidad preexistente, y que pueden tener contacto con el virus. Los expuestos (E) son las personas expuestas a una persona con la enfermedad, pero no capaces de transmitirla. Los infectados (I) son los individuos infectados capaces de dispersar la enfermedad; y los recuperados (R) son los individuos con inmunidad y no se infectan11,12.
Es posible aumentar la complejidad de estos modelos mediante la inclusión de otros parámetros como intervenciones, uso de vacunas, barbijos y medidas no farmacológicas, entre otras, para proveer aun más información13-15.
Todos estos modelos se desarrollan con base en parámetros o insumos de información epidemiológica y clínica que permiten realizar las estimaciones. Mientras más precisos y menos sesgados sean estos parámetros, más correctas serán las estimaciones de los modelos. Esto genera la necesidad de buscar la mejor fuente de información para estas variables, con el fin de construir modelos más precisos para cada situación, y así, favorecer la toma de decisiones político-sanitarias con base en información adecuada.
Sin embargo, las estimaciones sobre estos parámetros esenciales varían de manera relevante en los informes presentes en la literatura científica; esto se debe, por una parte, al momento particular de la pandemia y, por otra, a atributos propios de cada región. Esta variabilidad de parámetros y comportamiento de la pandemia explica en gran medida que los distintos países muestren diferentes dinámicas epidemiológicas en el transcurso de la pandemia; por ejemplo, Italia tuvo sus primeros casos la semana del 17 de febrero del 2020 y su primer pico la semana del 23 de marzo, aproximadamente un mes después; en cambio, Argentina presentó sus primeros casos durante la semana del 2 de marzo y aún (seis meses después) no tiene un pico definible.
Si bien algunos de los parámetros propios de la biología del virus se pueden pensar como constantes (por ejemplo, el tiempo de infecciosidad y el tiempo de incubación, entre otros), muchos otros parámetros utilizados para la predicción en cada jurisdicción se deben analizar en un contexto geográfico, y no siempre se pueden utilizar aquellos procedentes de otras regiones. Por estos motivos, es fundamental hacer un relevamiento de dicha información para determinar la estimación más precisa que se adecue a cada región. En el caso de Argentina, muchos de estos parámetros no están estimados, se desconocen o provienen de estimaciones no siempre adecuadas a la situación del país16.
Dado el interés y el uso creciente de este tipo de modelos para informar la toma de decisiones, sería importante promover el uso de la mejor evidencia y un set de parámetros adecuados entre los diferentes modelos y grupos. Es por ello que, en este trabajo, se presenta una revisión rápida de aquellos parámetros epidemiológicos esenciales potencialmente utilizables para alimentar modelos predictivos relevantes para Argentina, con foco en los parámetros relacionados con la propagación y los parámetros clínicos.
MÉTODOS
Para la realización y el diseño de las estrategias de búsquedas bibliográficas, se seleccionó, en primer lugar, una lista con los parámetros de interés. Una vez determinados estos, se seleccionaron los sitios de búsqueda con sus respectivas estrategias, se determinaron criterios de selección y aplicabilidad y, luego, se evaluó el riesgo de sesgo en base a herramientas para los distintos tipos de estudios. Por último, se valoró el conjunto de opiniones del grupo de epidemiólogos del Instituto de Efectividad Clínica y Sanitaria en relación con la calidad y la aplicabilidad del dato al contexto. La valoración de los datos identificados contó con el asesoramiento de expertos infectólogos y epidemiólogos de Argentina.
PARÁMETROS INCORPORADOS
Los parámetros considerados para este trabajo fueron los relevantes para dos objetivos, los que determinan la propagación de la pandemia y los que afectan su impacto en los sistemas de salud.
Para evaluar la propagación de la pandemia se consideraron los parámetros relativos a la dinámica de la transmisión: el período de incubación, el período de infeccio-sidad y número básico de reproducción (R0) y la tasa de fatalidad entre los infectados.
Las variables relacionadas con el impacto en el sistema de salud fueron los parámetros de índole clínica, como el tiempo de internación hospitalaria, el tiempo de internación en unidad de cuidados intensivos (UCI) y la proporción de pacientes que requieren UCI, entre otros.
BÚSQUEDA BIBLIOGRÁFICA
A medida que se seleccionaban estos parámetros, se realizó una búsqueda de información en las principales bases de datos bibliográficas (Medline, Embase, Lilacs), Scopus y Google Scholar, bases de datos de artículos en estado preimpresión (preprínts) como Medrxiv, Biorxiv, Arxiv, China Xiv, un metabuscador de las mismas referencias encontradas a partir de los principales modelos de simulación utilizados a nivel mundial, listas de referencias de artículos relevantes, literatura gris (reportes oficiales no indexados, bases de datos) y, por último, se realizó una búsqueda adicional en motores genéricos de Internet, medios de comunicación especializados, redes sociales y sitios web de diversos medios científicos pertinentes como sociedades y organizaciones científicas17. Las estrategias utilizadas para la búsqueda en PubMed (adaptadas para otras bases) para cada uno de los parámetros se detallan en el Anexo 1, disponible en: http://rasp.msal.gov.ar/rasp/ articulos/voll3supl/REV Argento Anexol.pdf
CRITERIOS DE SELECCIÓN
Los criterios para la selección de la bibliografía fueron la existencia de una definición precisa (por ejemplo, complacientes con una definición universalmente utilizada o aceptada, o al menos operacionalizable de manera adecuada) de cada parámetro, con estimaciones centrales y medidas de dispersión obtenida a partir de fuentes confiables (por ejemplo, registros oficiales de los países o de entidades nacionales e internacionales reconocidas) o verificables (por ejemplo, procedentes de estudios primarios) y la evaluación de la calidad metodológica de estos estudios luego de aplicarles una herramienta apropiada para cada tipo de diseño de estudio.
Otro de los criterios utilizados para la selección de la información fue la estimación de su aplicabilidad en América Latina. Se incluyeron datos provenientes de estudios primarios tanto como de estudios de simulación matemática de la Región. Se privilegiaron los datos recabados a partir de investigaciones primarias (como, por ejemplo, estudios de seroprevalencia, o datos de series de casos hospitalarias).
La información de cada uno de los estudios se extrajo en una plantilla desarrollada ad hoc: a) definición con estimador puntual e intervalo de confianza del 95% (05%); b) metodología de cálculo en caso de que estuviera disponible; y c) tipo de fuente de procedencia.
CRITERIOS DE APLICABILIDAD
En relación con la aplicabilidad de los parámetros para la población argentina, se valoraron los siguientes atributos en caso de que existiera o se informara el dato: estrategia de muestreo del país y representatividad, momento de la epidemia, presencia de intervenciones sanitarias concurrentes, estacionalidad, tipo de tests utilizados y población testeada.
EVALUACIÓN DEL RIESGO DE SESGO
Para todos los estudios publicados, se realizó una evaluación del riesgo de sesgo con una herramienta seleccionada para cada tipo de estudio.
Para los ensayos clínicos aleatorizados (ECA), se eligió la herramienta Cochrane oficial RoB2 para la evaluación del riesgo de sesgo18. Hasta el momento de la publicación, no se ha encontrado en esta revisión información de ningún ECA por fuera de una revisión sistemática, por lo que no se ha utilizado dicha herramienta.
Para los estudios observacionales, se utilizó la herramienta propuesta por el Instituto Nacional de Salud de Estados Unidos (NIH, por sus siglas en inglés)19. En cuanto a la evaluación del riesgo de sesgo de revisiones sistemáticas y metaanálisis, se utilizó la herramienta AMSTAR-2, una “herramienta de evaluación crítica de revisiones sistemáticas de estudios de intervenciones de salud”20. Para la información proveniente de estudios de modelos matemáticos con implicancia clínica y epidemiológica, se propuso analizarla con la lista de cotejo propuestos por Bhuia y Phillips21,22. Toda revisión de la literatura que no cumplía con los criterios Cochrane-DARE para ser considerada una revisión sistemática, fue catalogada per se como de “Muy baja calidad” debido a la ausencia de herramientas de evaluación de calidad para ellas23.
PARÁMETROS RELACIONADOS A LA DINÁMICA DE PROPAGACIÓN
Los parámetros centrales que se incluyeron fueron el período de incubación, el período de infecciosidad, la tasa de letalidad y el R0. Para el período de incubación, se consideró el tiempo desde la exposición al agente causal de la enfermedad hasta la aparición del primer signo o síntoma de la enfermedad24,25. Por otro lado, para el período de infecciosidad se consideró el intervalo durante el cual un agente infeccioso puede pasar de manera directa o indirecta de una persona infectada a otra persona24,25. La tasa de fatalidad en pacientes infectados se estableció como la relación entre los pacientes fallecidos por una enfermedad y la totalidad de los pacientes infectados con dicha enfermedad26. El R0 se definió como el número esperado de casos secundarios a un caso en una población completamente susceptible27.
PARÁMETROS CLÍNICOSLos parámetros adicionales que se incluyeron fueron la distribución de la gravedad de la enfermedad, el tiempo de internación, el tiempo desde la aparición de los síntomas hasta la internación, el tiempo de internación en la
UCI, la proporción de pacientes que requieren internación en la UCI, la proporción de pacientes que requieren ventilación mecánica invasiva (VMI), la proporción de pacientes que fallecen por la enfermedad y la efectividad de las intervenciones no farmacológicas. Para el caso de distribución de la gravedad de la enfermedad se consideró la proporción de pacientes asintomáticos, con sintomatolo-gía leve, moderada, grave y crítica de la OMS28.
Para este estudio no se consideró la tasa de mortalidad de casos diagnosticados, ya que su estimación varía de manera muy amplia con los criterios de diagnóstico y la gran diferencia de testeo de los distintos países29.
RESULTADOS
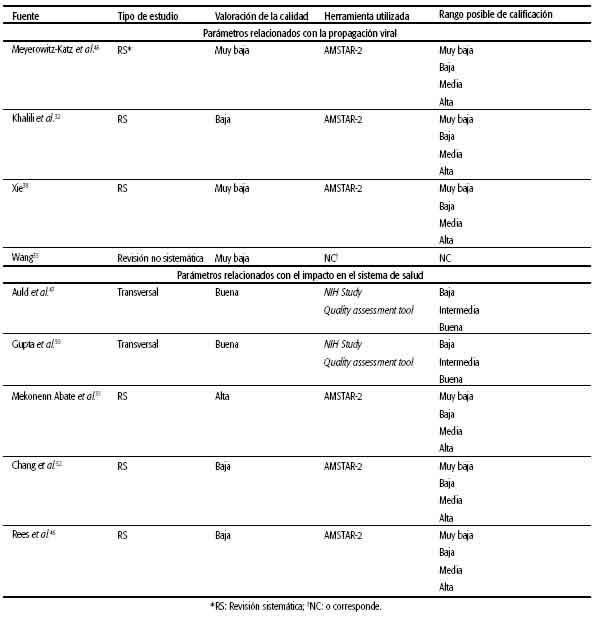
Se realizaron las búsquedas desde el 25 de abril de 2020 con actualizaciones periódicas cada 15 días; la última actualización presentada en este trabajo es hasta el 16 de septiembre de 2020. En la tabla 1 se muestran la cantidad de estimaciones halladas para cada variable con el rango encontrado para cada estimación y una aproximación de esta con base en valores más representativos de Argentina. En el sitio web relacionado con este proyecto se pueden consultar los datos de cada artículo con las estimaciones centrales y las medidas de incertidumbre y dispersión en los casos informados, además del hipervínculo a la fuente primaria. Este repositorio de parámetros se actualiza cada 15 días30. En la tabla 2 se muestra la evaluación de riesgo de sesgo de los principales estudios informados.
VARIABLES RELACIONADAS CON LA PROPAGACIÓN
- Periodo de incubación
Se relevaron 22 registros, 8 publicados y 14 de literatura gris, que expresaran el tiempo de período de incubación. El período de incubación de la mayoría de las estimaciones es de aproximadamente cinco a seis días, aunque hay estudios que informan hasta ocho días. Hay una variación pequeña entre los informes que expresan la medida en media o mediana (la primera es consistentemente mayor), McAloon informó una media de 5,8 días y una mediana de 5,1 días31. Se registraron cinco revisiones sistemáticas (RS) y una revisión rápida con metaanálisis, donde la media se aproximó, la mayoría de las veces, a 5,8 días. De estas, Khalili y col. realizaron una RS en la que evaluaron diversas variables clínicas y epidemiológicas de la pandemia, entre las que se encontraba el período de incubación. Los autores realizaron el metaanálisis de 14 estudios, de los cuales 12 fueron provenientes de datos de China, donde calcularon una media de tiempo de incubación de 5,8 días (IC95%: 4,83-6,85; medida de heterogeneidad I2 = 94,7%)32.
- Periodo de infecciosidad Se incluyeron 24 estudios que informaron el período de infecciosidad, de los cuales 5 fueron de artículos publicados y 19 de literatura gris. Se encontraron diversos criterios para determinar el tiempo de infecciosidad. Entre estos, encontramos artículos que evalúan este período en base al tiempo de actividad del virus medido desde el tiempo de inicio de los síntomas hasta la recuperación, fallecimiento o negativización de los tests para la enfermedad; en el caso de pacientes asintomáticos o presintomáticos, se considera el tiempo del test positivo hasta la presencia de tests negativos33. Byrne y col. refirieron un período de infecciosidad de 6,5 a 9,5 días para pacientes asintomáticos, mientras que para pacientes sintomáticos fue de 13,4 días (IC95%: 19,9-15,8)33. Otros autores estimaron este tiempo en base a modelos epidemiológicos, en los cuales también se encontró gran variabilidad intraestudio e interestudio con base en los criterios establecidos. Vattay estimó un período de infecciosidad para España, Italia y Nueva York de 16 días, mientras que para China este período fue de 6 días. Esta diversidad se explica por la diferencia de velocidad de detección y aislamiento34. Wang y col. realizaron una RS con análisis por tipo de artículo (preprínts y estudios publicados con revisión de pares) y en dos estadios temporales (del 23 de enero al 12 de febrero de 2020 y del 13 de febrero al 20 de marzo de 2020)35. El período de infecciosidad general fue de 6,25 días (IC95%: 5,097,51), menor en los artículos publicados que en los encontrados en las bases de preprints (5,25; IC95%: 3,32-7,25 y 6,54; IC95%: 5,24-8,08; respectivamente) así como en el segundo período en comparación con el primero (5,76 días; IC95%: 4,73-7,38; y 7,91 días; IC95%: 4,86-9,65; respectivamente).
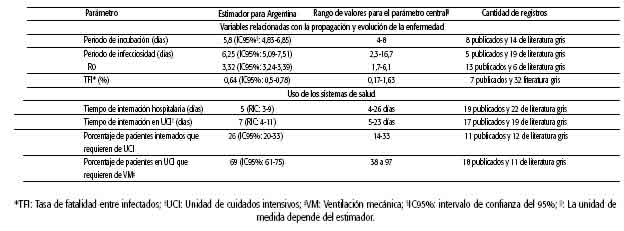
TABLA 1: Parámetros relacionados con propagación viral del SARS-CoV-2 y su impacto en el sistema de salud utilizables en Argentina.
- Número básico de reproducción (R0)De los 19 registros recolectados que informaron el R0, 13 fueron registros publicados con revisión por pares y 6 provinieron de la literatura gris. La estimación de este parámetro varía en la literatura entre 1,75 y 6,1. Esta amplia variedad puede deberse a diferencias metodológicas, regionales y temporales en las que se estimó el R0. Zhuang y col. estimaron un R0 de 2,6 y 3,3 para Italia; esta variación estaba determinada por el día de inicio de la pandemia (según se considerara el inicio de esta el 5 o el 10 de febrero de 2020)35. Por otra parte, Su y col. estimaron distintos R0 en el mismo período en Beijing, Shanghai, Guangzhou y Shenzhen (2,91; 2,78; 2,02 y 1,75; respectivamente)36. Cabe resaltar que el R en un tiempo particular (Rt) dado como una estimación en determinado momento está influenciado tanto por distintas medidas aplicadas para disminuir la pandemia como por la dinámica con base en la cantidad de gente susceptible a infectarse. Xie y col. realizaron una RS y MA donde incluyeron 127 artículos; para estimar esta variable, incluyeron 14 artículos a partir de los que calcularon un farmacológica vigente y considera al 100% de la población como susceptible. Se recomienda la estimación de un R0 propio de la región a modelar. Sin embargo, se debe tener en cuenta que, si el objetivo del modelo es no solo hacer proyecciones, sino también estimar el efecto de otros factores como las medidas no farmacológicas (por ejemplo, diversas políticas sanitarias) u otras variables como la vacunación, la estimación de un R(t) en un momento dado ya contempla un posible grado de inmunidad adquirida, así como el efecto de las medidas ya establecidas para esa región en ese momento dado. Es muy importante tener esto en cuenta para no sobreestimar el posible efecto de estas medidas en el modelado.
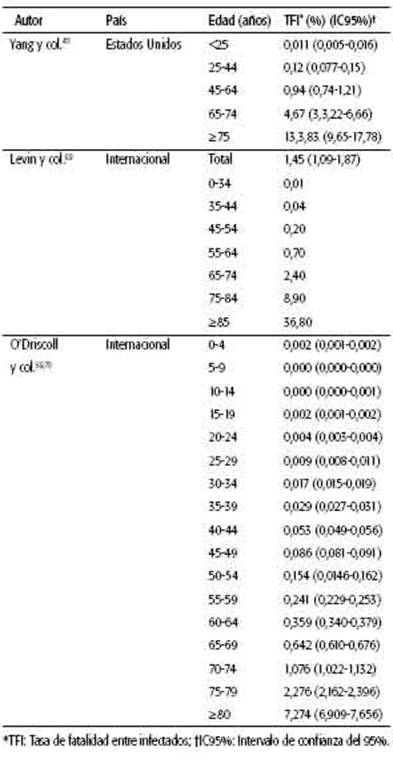
La TFI es una variable que puede ser influenciada por diversas cuestiones, como las características demográficas, la saturación del sistema de salud o la forma de calcular la cantidad de infectados. Se relevaron 39 registros, 32 de literatura gris y 7 publicados, que mencionan la TFI. Las estimaciones fueron muy variables en la literatura relevada, entre 0,17% y 1,63%. Los diversos estudios calcularon la TFI de diferentes maneras: algunos lo hicieron mediante estudios de seroprevalencia, mientras otros utilizaron modelos epidemiológicos. Algunos autores informaron la mortalidad según grupos etarios mostrando una relación entre la mortalidad y el aumento de la edad (ver Tabla 3); mientras otros expresaron la TFI en relación con la cantidad de muertos/habitantes, donde muestran un aumento en la TFI a mayor cantidad de muertos por habitantes39-41. Se encontraron pocos registros que informan la TFI en América Latina. Hallal y col. y Marra y col. calcularon la TFI para Brasil, ambos mediante estudios de seroprevalencia; sin embargo, las estimaciones fueron muy diferentes entre ellos: 0-2,4% para Hallal y 1,05 (IC95%: 0,96-1,17) para Marra. Almeida y col. estimaron una TFI para diferentes países de América Latina y calcularon para Argentina un 0,94% de mortalidad, valor considerablemente mayor que el del resto de países (0,09% para Colombia y 0,05% para Chile42-44. Meyerowitz-Katz y col. realizaron una RS y MA donde refieren una mortalidad del 0,68% (IC95%: 0,35-0,82). A su vez, realizaron un análisis por subgrupos donde la mortalidad fue del 0,53% (IC:95%: 0,35-0,78) en estudios con base en la serología y de 0,79% (IC95%: 0,58-1) en estudios en los que no se utilizó la serología. Los estudios serológicos con menor riesgo de sesgo demostraron TFI mayores que aquellos con mayor riesgo de sesgo45.
- Uso de los sistemas de saludSe relevaron 57 registros (26 de literatura gris y 31 publicados) que relevaron alguna variable de interés en cuanto al tiempo de internación (en sala general o en UCI), la proporción de pacientes que requieren internación en UCI y, de estos últimos, el porcentaje que requiere VMI. Una de las grandes dificultades en cuanto a la estimación de tiempo de internación es la falta de diferenciación del tiempo entre los pacientes que pasan tiempo en UCI y los que no; así como, de los pacientes que pasan tiempo internados en UCI, cuánto tiempo pasan internados fuera de ella.
Rees y col. realizaron una RS con MA para determinar el tiempo de internación, tanto en sala general como en UCI, de los pacientes con COVID-19. Incluyeron 52 artículos entre el 24 de diciembre de 2019 y el 16 de abril de 2020, de los cuales la mayoría fueron estudios de cohorte46. La mediana de tiempo de internación hospitalaria fue de 4 a 53 días en China y de 4 a 21 días para los registros fuera de China. El tiempo de internación entre los pacientes que fueron dados de alta y los que fallecieron fue de 4 a 21 días y 4 a 53 días, respectivamente. También mostraron un aumento en el tiempo de internación en los pacientes más graves. Con base en los distintos registros, los autores calcularon una mediana de tiempo de internación de 14 días (RIC: 10-19) para China y 5 días (RIC: 3-9) para el resto del mundo. En el caso del tiempo de internación en UCI, Rees y col. registraron una diferencia menor entre las medianas de días de internación de los pacientes que fueron dados de alta y los que fallecieron (5 días y 19 días, respectivamente). En su estimación, los tiempos de internación en UCI para China y para el resto del mundo fueron similares: 8 días (RIC: 5-13) y 7 días (RIC: 4-11), respectivamente. Algunos informes diferencian el tiempo de internación total en los pacientes que requirieron un período en la UCI47-49. Gupta y col. estudiaron una cohorte de 2 215 pacientes adultos con COVID-19 internados en UCI en 65 centros de Estados Unidos para evaluar factores asociados con la mortalidad y examinar la variación en el tratamiento y los resultados50. De los pacientes con resultado final (alta o fallecimiento) a los 28 días, tiempo en el cual 72,6% de los pacientes tuvieron un resultado final y 27,4% continuaban hospitalizados, el tiempo de internación en UCI fue en promedio de 9 días (RIC: 5-14) y el tiempo total de internación fue de 16 días (RIC: 1122). Al final del estudio, 93,8% de los pacientes fueron dados de alta o fallecieron; de estos, solo se informa el tiempo de internación en UCI y el total de los pacientes que fueron dados de alta: 12 días (RIC: 6 - 21) y 21 días (RIC: 13 - 33), respectivamente.
El porcentaje de pacientes que requieren internación en UCI entre los pacientes internados en los registros evaluados varía del 14% al 33%. Abate y col. realizaron una RS con MA en la que evaluaron el porcentaje de pacientes que requieren de internación en UCI por distintos coronavirus (SARS-CoV, MERS-CoV y SARS-CoV-2). Para COVID-19 estimaron, a partir de los datos obtenidos de 26 artículos, una prevalencia de UCI entre los pacientes internados del 26% (IC95%: 20-33; I2: 99,55%)51. Chang y col. realizaron una RS con MA con 28 artículos donde evaluaron, entre otras variables, la proporción de pacientes internados en UCI por COVID-19 que requieren VMI52. Para esta variable, detectaron 18 artículos con una población total de 10 240 pacientes en UCI, de los cuales el 69% requirió VM (IC95%: 6175). Cabe mencionar que, según los registros oficiales a nivel nacional hasta el 14 de octubre de 2020, solo el 13% de los pacientes requirió de internación en UCI y de estos, el 57,3% utilizó VMI53. A su vez, si bien los registros no contemplan datos como la fecha de alta, lo cual dificulta conocer el tiempo de internación de los pacientes, se pueden estimar parámetros como el tiempo de internación tanto en UCI como en sala general hasta el fallecimiento. La mediana del tiempo de internación en UCI para los pacientes que fallecen es de 9 días (RIC: 4-16), con un tiempo de internación total (UCI más sala general) de 11 días (RIC: 5-18). En cambio, en los pacientes que no requieren de UCI, la mediana del tiempo de internación hasta la muerte es de 8 días (RIC: 3-15). Es importante remarcar que estos tiempos solo contemplan datos de pacientes que fallecieron y, según la bibliografía consultada, los pacientes que reciben el alta suelen requerir de mayor tiempo de internación; sin embargo, este dato no siempre es consistente, ni resulta sencillo estimar cuánto tiempo más de internación requieren49,54,55. Los resultados preliminares de una investigación aún no publicada de la Sociedad Argentina de Terapia Intensiva, que evaluó el tiempo de internación de 500 pacientes en UCI, revelaron un tiempo internación en UCI de 13 días (RIC: 8-22) con 10 días de VM (RIC: 5-16). A su vez, informaron un tiempo más prolongado de internación en UCI (16 días RIC: 11-27 versus 10 días RCI: 6-17; p < 0,001) y de VM (12 días RIC: 6-18 versus 9 días RIC: 5-15; p < 0,005) en los pacientes sobrevivientes (n = 239) en comparación con los fallecidos (n = 261)56. Algunos de los parámetros del uso del sistema de salud, como se mencionó en el caso de la TFI, varían según el grupo etario considerado; por ejemplo, las personas de mayor edad tienen una mayor tasa de internación tanto en sala general como de UCI57.
En este trabajo se brindan parámetros para modelos relativamente simples; es así que en la Tabla 1 se contempla un estimador único para cada parámetro utilizable para todo el rango etario. Varios modelos matemáticos contemplan la compartimentalización de la población en grupos etarios debido a estas diferencias de riesgo. Para estos casos, en el anexo que acompaña a este artículo, así como en la página web covidstats.com.ar se puede encontrar información útil para la realización de un modelo compartimentalizado por edades30,57.
Otro dato de interés para muchos modelos es la proporción de personas infectadas según la gravedad de la enfermedad. Reportes de Wu y col., el Centro de Control y Prevención de Enfermedades de China y la OMS refieren que la distribución de gravedad de la enfermedad de los pacientes con COVID-19 es de aproximadamente 5% de casos críticos (casos que requieren internación en UCI), 14% de casos graves (casos que requieren internación hospitalaria pero no en UCI) y 81% de casos leves o moderados58-60. Sin embargo, estas estimaciones se realizan con base en los casos diagnosticados, por lo cual no necesariamente son proporciones atribuibles a todos los infectados. Según esta apreciación, es posible realizar una estimación de la cantidad de casos críticos y graves a partir del cálculo de la TFI de la proporción de pacientes que requieren de UCI y la mortalidad tanto en UCI como en sala general. En el caso de Argentina, según los datos oficiales, el 13% de los pacientes internados requiere UCI, con una mortalidad en UCI del 57,3% (esta mortalidad representa el 37,4% de la mortalidad total por COVID-19 en pacientes internados) y la TFI es de 0,64%. A partir de estos datos, se puede calcular la proporción de todos los infectados con enfermedad crítica y grave. Para los casos críticos, esta proporción es de 42%, calculada con la siguiente fórmula:
0,0064 (TFI) x 0,37 (proporción mortalidad total se da en UCI) / 0,57 (proporción de muertes en UCI).
A su vez, a partir de estos valores se puede estimar la cantidad de casos graves:
0,87 (proporción que no requieren UCI) x 0,42% (cantidad de críticos) / 0,13 (proporción de pacientes que requieren UCI) = 2,78%.
DISCUSIÓN
La presente revisión examina distintos parámetros relacionados con la dinámica de la transmisión del SARS-CoV2, el período de incubación, el período de infecciosidad, el R0, y otros parámetros vinculados al impacto en el sistema de salud en relación con diversos aspectos clínicos de la COVID-19, con miras a ser utilizados en modelos epidemiológicos predictivos para Argentina.
Debido a la gran heterogeneidad de las estimaciones, resulta difícil aproximar un valor puntual y hasta un rango de variabilidad para muchos de los parámetros. Esta dificultad es mayor en aquellos parámetros relacionados con el impacto en salud, y las posibles explicaciones estriban en la existencia de diferencias estructurales en los sistemas de salud, patrones de comportamiento de las poblaciones y variaciones en los perfiles de medidas sanitarias adoptadas por los países para afrontar la pandemia y también por la diversidad geográfica. Se realizó una evaluación de la calidad metodológica de aquellos estudios que el grupo de autores consideró más sólidos desde el punto de vista científico y con potencial relevancia para la realidad argentina.
Una cuestión de gran interés para los autores es la dificultad de una estimación de la TFI. Debido a que la tasa de fatalidad en contagios depende en gran medida de la cantidad de pacientes testeados, la TFI es una medida más robusta para conocer la gravedad de la pandemia. Sin embargo, su estimación es muy variada tanto por país como por el momento de la epidemia. La aparición de los estudios de seroprevalencia fue un gran avance para esto, ya que tienen un mejor desempeño en términos de sensibilidad y especificidad. Sin embargo, estos estudios pueden generar un subdiagnóstico en casos de pacientes asintomáticos o leves, ya que su sensibilidad puede ser menor en estas subpoblaciones61. En Argentina, se realizó un estudio de seroprevalencia en un barrio de bajos recursos en la Ciudad de Buenos Aires tres meses después de notificado el primer caso allí, donde se detectó una prevalencia del 53,4% según los niveles de anticuerpos de tipo IgG62. Sin embargo, las particularidades del barrio no permiten extrapolar estos datos al resto de la ciudad. Por este motivo, se requieren estudios de mayor magnitud con un muestreo probabilístico acorde para determinar la verdadera prevalencia en nuestro país.
Los datos del presente trabajo son de acceso libre y se encuentran en el sitio web del Instituto de Efectividad Clínica y Sanitaria (IECS) con la intención de que sean una herramienta disponible para trabajos de modelos de COVID-19 en Argentina63. La búsqueda de estos parámetros en particular surgió en el contexto de dos proyectos, “Proyección de tendencias y evaluación de escenarios de intervención para la epidemia COVID-19 en Argentina mediante modelado y simulación computacional: una plataforma para informar” y “Preparación y respuesta del sistema de salud COVID-19 en América Latina”; los cuales están destinados al modelado de la pandemia.
El primero es un proyecto interdisciplinario sobre COVID-19 en Argentina coordinado por el Instituto UBA-CONICET de Ciencias de la Computación de la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires (FECyN-UBA), junto a miembros del Instituto de Cálculo (FECyN-UBA) y el IECS y la participación de investigadores del Departamento de Matemáticas (FCEyN-UBA), la Universidad Nacional de San Martín, la Universidad Nacional de Rosario y el financiamiento de la Agencia Nacional de Promoción Científica y Tecnológica del Ministerio de Ciencia y Tecnología de la Nación (ANPCyT/MinCyT). El segundo, “Modelo Integral de Preparación y Respuesta de los Sistemas de Salud de Latinoamérica y el Caribe para estimar el impacto de la expansión de COVID-19” es desarrollado por el Centro de Implementación e Innovación en Políticas de Salud y el Departamento de Evaluaciones Económicas y de Tecnologías Sanitarias del IECS, y cuenta con el apoyo del Banco Interamericano de Desarrollo.
Otros estudios revisan este tipo de parámetros relacionados tanto con la propagación de la pandemia como con su relación en los sistemas de salud. Biggerstaff y col. realizaron una revisión de parámetros relacionados con la propagación de la pandemia, donde analizan variables no evaluadas en esta revisión, como los intervalos de serie o el tiempo de duplicación y la efectividad de medidas no farmacológicas; sin embargo, no contemplan variables relacionadas con el uso de recursos de salud, como el tiempo de internación o el porcentaje de pacientes que requieren internación en UCI64. Fonfria y col., por su parte, realizaron una revisión rápida con MA más orientada a las variables del sistema de salud, donde solo incluyeron el tiempo de incubación y el intervalo de serie como parámetros relacionados con la propagación del virus55. El estudio que aquí se presenta está más actualizado y orientado hacia el contexto argentino.
Si bien este trabajo no evalúa la efectividad de las medidas no farmacológicas para disminuir la propagación de la pandemia, el IECS desarrolló una evaluación de tecnología sanitaria (ETS) rápida sobre estas medidas65. Esta pertenece a un conjunto de ETS que son parte, junto a otros proyectos, de iniciativas para ofrecer una mejor respuesta al sistema de salud frente a la pandemia63. También existen otras revisiones importantes, como por ejemplo el trabajo del Robert Koch Institute, y el relevamiento de medidas sanitarias utilizada por el modelo de Oxford66,67. Este último permite un cálculo interactivo del Rt con base en distintas medidas sanitarias y una estimación del impacto posible de cada una de ellas66. Esto conlleva una gran ventaja para el modelado de la pandemia, ya que permite diferentes combinaciones de políticas y cambios de la efectividad de las medidas. Además, si bien las medidas más exhaustivas y estrictas son más efectivas, en un momento dado, la adición de medidas genera aumentos mínimos en su efecto68. Por este motivo, es primordial realizar un balance entre la efectividad de las medidas y sus factores colaterales negativos.
Otro factor de interés para muchos modelos son las matrices de contacto entre infectados, cuya consideración e inclusión podría mejorar la estimación de la dinámica de los contagios y tener implicancias en el desarrollo de la inmunidad de rebaño. Sin embargo, un análisis pormenorizado de estas matrices excede a los objetivos de esta revisión rápida de parámetros69-71.
Un aspecto para considerar, que podría tener un gran impacto para los modelos de COVID-19, es la reinfección de pacientes72. Si bien aún hay poca información sobre este fenómeno, parece ser poco frecuente. Sin embargo, podría existir un subdiagnóstico debido a la falta de criterios concretos de reinfección y la falta de su consideración en los programas de vigilancia epidemiológica.
Entre las fortalezas de este trabajo, cabe mencionar la exhaustividad de la búsqueda, la evaluación crítica de parámetros en relación con su adecuación para el país por un grupo experimentado de epidemiólogos y la evaluación de la calidad metodológica con herramientas según el diseño de estudio.
Por otra parte, como limitaciones, se puede mencionar el carácter de revisión rápida, dada la necesidad de información a medida que se desarrolla la pandemia en el país. Otro problema fue la limitación en el acceso a detalles de información local, en particular con relación a la disponibilidad y la fiabilidad de los resultados de las internaciones hospitalarias y de terapia intensiva en el país, que también es dispar. El presente estudio es una revisión rápida de la literatura, sin la metodología formal de una revisión sistemática, aunque muchos de los criterios que definen este tipo de estudios han sido debidamente cumplimentados como fue descrito.
La información obtenida en el presente trabajo, en sus anexos y repositorios conexos en Internet puede contribuir a informar futuros modelamientos y tableros de control para predecir la dinámica de la epidemia en Argentina. La investigación virológica, clínica y sanitaria tiene un desarrollo veloz en el mundo, y aún hoy es un desafío obtener datos actualizados de primera mano, relevantes para el país. Futuros emprendimientos deberían contemplar la posibilidad de realizar actualizaciones “vivas” o en tiempo real de estos parámetros.
CONTRIBUCIONES DE LOS AUTORES: FAR, AB, APR, LP, FaU y FRC participaron en la concepción y diseño de la revisión; FAR, AB, LP y FRC realizaron la recopilación de datos; FRC, LP y FAR realizaron y supervisaron el análisis; AB, FRC, LP y FAR participaron en la interpretación de los datos. Todos los autores aceptaron la publicación del presente trabajo.
AGRADECIMIENTOS: a Daniel Comandé, del Instituto de Efectividad Clínica y Sanitaria, por su importante colaboración con las búsquedas bibliográficas; a Adolfo Rubinstein (director del Centro de Implementación e Innovación en Políticas de Salud, CIIPS-IECS) y a Rodrigo Castro del Instituto de Investigación en Ciencias de la Computación.