Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Facultad de Ciencias Agrarias. Universidad Nacional de Cuyo
versión On-line ISSN 1853-8665
Rev. Fac. Cienc. Agrar., Univ. Nac. Cuyo vol.46 no.1 Mendoza ene./jun. 2014
Sesquióxidos de hierro en bosques templado húmedos del estado de Hidalgo, México
Sesquioxides of iron in moist temperate forests of the state of Hidalgo, Mexico
Otilio Arturo Acevedo Sandoval 1, 3, Enrique Cruz Chavez 1, Misael Cruz Sánchez 1, Francisco Prieto García 2, Judith Prieto Méndez 3
1 Centro de Investigaciones en Ciencias de la Tierra y Materiales. acevedo@uaeh.edu.mx
2 Centro de Investigaciones Químicas, Instituto de Ciencias Básicas e Ingeniería.
3 Instituto de Ciencias Agropecuarias. Universidad Autónoma del Estado de Hidalgo. Carretera Pachuca. Tulancingo Km. 4.5 Ciudad del Conocimiento. Colonia Carboneras, Mineral de la Reforma, Hidalgo, México. C. P. 42184. Teléfono +52 775 7533495, +52 771 7172000 ext 2461 fax 2466
Originales:
Recepción: 02/10/2013
Aceptación: 28/03/2014
Resumen
Se estudian las formas de hierro extraídas con oxalato ácido de amonio, pirofosfato de sodio, ditionito-citrato-bicarbonato, así como el hierro total en disolución en suelos Alisoles en el municipio de Acaxochitlán, Hidalgo, México. Los suelos estudiados soportan distintos tipos de vegetación forestal: Pinus patula Schlecht and Cham (Pp), Pinus teocote, (Pt) y Quercus spp, (Q). El objetivo del trabajo fue determinar si la vegetación influye significativamente sobre las diferentes fracciones de hierro (Fe) en el suelo. Los contenidos de Fe total son significativamente mayores en suelos bajo vegetación de Pp (14,5% de Fe2O3), el mayor porcentaje de ferrihidrita (38,0% del Fe total en suelo) y de complejos organominerales de Fe y óxidos amorfos de Fe (20,9% y 16,3% respectivamente del Fe total en suelo, se dio en el bosque de Pt. En los suelos bajo bosques de Pp predominaron formas de Fe lábil (56,7% del Fe total en suelo) y formas cristalinas de Fe (goetita/hematita). La vegetación de Q mostró mayor alteración de los suelos y en el caso de Pt y Pp se presentó una mayor evolución en el proceso de organización estructural de los oxihidróxidos de Fe. El tipo de vegetación forestal influye en el grado de evolución del suelo, y en la distribución, contenido y formas de óxidos de Fe. En un orden de mayor a menor el contenido de Fe total en el suelo fue Pinus patula > Quercus spp > Pinus teocote.
Palabras clave: Sesquióxidos de hierro; Bosque templado; Ferrihidrita; Goetita; Hierro amorfo
Abstract
Total iron dissolved and iron forms extracted with acid ammonium oxalate, sodium pyrophosphate and dithionate- citrate- bicarbonate were studied in Alisol soils in the municipality of Acaxochitlán, State of Hidalgo, México. The studied soils present different kind of forests: Pinus patula schlecht and Cham (Pp), Pinus teocote, (Pt) and Quercus spp, (Q). The objective of this investigation is to determinate if the vegetation modifies the different fraction of iron (Fe) in the soil. The highest total iron content (14.5% of Fe2O3) was observed in the soils with Pp vegetation, the highest percent of ferrihydrite (38.0% of total Fe present in the soil) and of iron-organic matter complex and amorphous iron oxides (20.9% and 16.3% respectively of total Fe in the soil) were found in the Pt forest. Free iron forms (56.7% of total Fe in the soil) and crystalline iron forms (goethite/ hematite) were predominant in the soils with Pp forest. The most weathered soil was the one with Q vegetation, a higher evolution in the process of iron oxi-hydroxides structural organization was found in the soils with Pt and Pp. The type of forest vegetation influences the degree of soil evolution, and distribution, content and forms of Fe oxides in order of highest to lowest total Fe content in the soil was Pinus patula > Quercus spp > Pinus teocote.
Keywords: Iron sesquioxides; Temperate forest; Ferrihydrite; Goethite; Amorphous iron
Introducción
Los suelos juegan un papel sustancial en la biogeoquímica de los ecosistemas forestales. Los suelos forestales son importante fuente de nutrimentos incluyendo nitrógeno (N), azufre (S), fósforo (P), calcio (Ca), potasio (K), magnesio (Mg) y algunos micronutrimentos (20, 22). El hierro (Fe) es uno de los elementos más frecuentes en las rocas, y en los suelos forestales y agrícolas. Las diversas formas de hierro ejercen una marcada influencia sobre las propiedades de los suelos, al tener una repercusión importante en la génesis y evolución de los mismos, y propiedades relacionadas con la fertilidad.
Prietzel et al. (2007) mencionan que el contenido de hierro en el suelo varia de 2 a 5 g kg-1 y en ciertos horizontes de suelo puede llegar a 400 g kg-1 (36) indican que los modelos de distribución de oxihidróxidos de hierro en suelos lateríticos de Brasil provee información de la historia pedogenética de estos suelos, desde una escala global a la nanométrica (45). Dixon (2000) reporta que los nódulos de Fe en los suelos probablemente contienen información cronológica acerca de la formación del suelo y los cambios ambientales (15).
La presencia o ausencia de minerales de Fe pedogénico en suelos, en los horizontes o en agregados del suelo, o bien su distribución espacial en el perfil se relaciona con las condiciones fisicoquímicas edáficas. Esto es debido a que el Fe puede experimentar reacciones redox, de adsorción, de protonación, o (co)precipitación con componentes orgánicos e inorgánicos de la solución del suelo y de la fase sólida del mismo (36). Los óxidos de Fe (incluyendo hidróxidos y oxihidróxidos) ayudan a describir el tipo, la dirección y la extensión de los procesos pedogenéticos. Propiedades inherentes a estos minerales como son hábito de cristalización, cristalinidad y sustitución isomórfica, pueden indicar las condiciones de medio ambiente en las cuales se formaron (1, 2). A título de ejemplo, la goetita y la hematita pueden almacenar información acerca del medio ambiente en el cual se desarrollaron, pues presentan baja solubilidad en condiciones aeróbicas de formación (18, 36, 42).
El Fe desempeña un papel importante en los procesos de ferralitización, laterización, podzolización, gleificación y solodización. A partir de la proporción de su contenido y formas en distintos horizontes, puede evaluarse el grado de desarrollo de los procesos edáficos antes indicados. El contenido, la química y la mineralogía de los óxidos de Fe varían con la clase de drenaje, la pendiente, la profundidad o la toposecuencia (1, 2, 32, 36, 37, 45). Varajâo et al. (2007) mencionan que cuando se presenta un drenaje libre y permanente, los óxidos de hierro son uniformemente distribuidos y el perfil del suelo es homogéneamente coloreado, la mayor concentración de óxidos de Fe se presenta en el horizonte B (45).
Agbenin (2003) reporta que en los suelos al norte de Guinea en Nigeria, los óxidos de hierro lábiles se movilizan y depositan en los perfiles formando moteados, concreciones y en ocasiones horizontes endurecidos (4).
Objetivo
• Determinar la influencia del tipo de vegetación, Pinus patula Schlecht and Cham (Pp), Pinus teocote, (Pt) y Quercus spp, (Q) en las distintas fracciones de hierro en suelos del municipio de Acaxochitlán, estado de Hidalgo, México.
• Conocer si el tipo de vegetación incide en el grado de evolución de estos suelos.
Materiales y métodos
Localización y características del área de estudio
El área de estudio se ubica en el municipio de Acaxochitlán, estado de Hidalgo, México, los perfiles se localizan entre las coordenadas 20°10'53" y 20°13'40" N y 98° 12'35" y 98°15'35" O, a una altura promedio de 2.300 m (figura 1). Esta zona se ubica dentro de la provincia geológica de la Faja Volcánica Transmexicana del Cenozoico y ambiente geotectónico de arco continental (19, 34). Los perfiles estudiados se encuentran en la Formación Atotonilco El Grande, constituidas por rocas basálticas del periodo terciario, compuestas por fenocristales de olivino (20%), augita (10%), óxidos de Fe-Ti (5%) y andesina (3%), el resto lo constituye la matriz, representada por un intercrecimiento de microfenocristales de andesina y augita (9, 19).

Figura 1. Localización de la zona de estudio.
Figure 1. Location of the study area.
El clima (Cm) es templado húmedo con abundantes lluvias en verano, precipitación anual de 1,200 mm y temperatura media de 15,5°C. (14). El régimen de humedad del suelo es údico y el de temperatura del suelo, mésico (41). En la región de estudio el uso dominante del suelo es forestal, donde la vegetación que predomina es Quercus spp (Q, Perfil 1), Pinus teocote (Pt, Perfil 2) y Pinus patula (Pp, Perfil 4).
Los bosques en general presentan una alta perturbación por actividades antropogénicas, tales como deforestación y cambio de uso del suelo. Los suelos se clasifican como Alisol Cutánico (Epieútrico), Alisol Cutánico Úmbrico (Hiperdístrico, Endocláyico), y Alisol Cutánico, Úmbrico (Hiperdístrico, Cláyico), respectivamente (3).
Muestreo de Suelos
Los suelos forestales objeto de este estudio son representativos de la región. Se eligieron tres sitios al noreste de la cabecera municipal de Acaxochitlán, estado de Hidalgo, México, a una altitud de 2250,3 m (Perfil 1, Q), 2100 m (Perfil 2, Pt) y 2244 m (Perfil 4, Pp). Cada perfil se describió morfológicamente (9, 16, 38). En cada horizonte, de cada perfil identificado en campo se colectaron tres muestras compuestas alteradas, éstas se llevaron al laboratorio donde se secaron al aire y tamizaron a través de una malla de 2 mm para sus respectivos análisis.
La determinación de los óxidos de Fe se realizó mediante extracciones químicas.
Sobre la base de la selectividad del extractante, debido a que diferentes métodos permiten recuperar formas con distinto grado de cristalinidad y asociado a diversas fracciones o compuestos del suelo (8). La extracción de Fe lábil se llevó a cabo con ditionito-citrato-bicarbonato (DCB), Fed (31); extracción de óxidos amorfos y óxidos hidratados con oxalato ácido de amonio, Feo (40); la extracción de Fe presente en complejos orgánicos se hizo con pirofosfato de sodio, Fep (40). El Fe en las respectivas soluciones se determinó por espectrometría de emisión en plasma de inducción acoplada, (ICP, marca Perkin Elmer 3000, modelo Lamda 2S). El análisis químico total de Fe (Fet) se realizó por fluorescencia de rayos x, con un espectrómetro secuencial de rayos x SIEMENS SRS 300.
Los análisis estadísticos de la varianza y comparación de medias (t student, p ≤ 0,05) se realizaron con el programa estadístico Graph pad v.3.0 (Tukey, p ≤ 0,05).
Reultados y discusión
Propiedades físicas y químicas de los suelo bajo bosques de Quercus sp, Pinus teocote y Pinus patula.
Los perfiles estudiados en general presentan un buen drenaje, las texturas que dominan son franco, franco arenoso y arcilloso. Todos los perfiles presentan un incremento de arcilla con la profundidad (30 a 50% de arcilla) (tabla 1, pág. 113), en el horizonte Bt. Éste se caracteriza por la presencia de películas de arcilla en las paredes de los poros y en la superficie de los agregados, producto de la acción de los factores de formación y de la ocurrencia combinada de los procesos dominantes de: a) acumulación y redistribución de arcilla, y b) desilificación y concentración de óxidos e hidróxidos de hierro y aluminio (10). El pH (1:2,5 en agua) varió de 6,7 a 4,9 de ligeramente ácido a muy ácido, con una ligera disminución de acidez al aumentar la profundidad en el perfil 2. En los perfiles 1 y 4 se presenta un incremento de la acidez con relación a la profundidad del suelo (tabla 1). Lilienfein et al. (26) mencionan que las coníferas incrementan la acidez del suelo y, asociada con ésta, se alteran procesos edáficos, al aumentar la hidrólisis ácida, la lixiviación de cationes básicos, la actividad fúngica, y disminuye la nitrificación.
Tabla 1. Algunas propiedades físicas y químicas de los suelos bajo bosques de Quercus sp, Pinus teocote y Pinus patula del municipio de Acaxochitlan, Hidalgo, México.
Table 1. Some physical and chemical properties of soil under Quercus sp, Pinus patula and Pinus teocote in Acaxochitlan Township, Hidalgo, Mexico.

Los resultados de la tabla 1 indican que el Perfil 2 tiene un alto contenido de materia orgánica en el horizonte superficial, el Perfil 4 se consideran medio y muy bajo para el Perfil 1, el porcentaje de materia orgánica decrece con la profundidad del suelo hasta llegar a valores considerados como muy pobres (5, 16).
En relación con las bases intercambiables el calcio, magnesio y potasio presentan valores bajos a muy bajos en los Perfiles 2 y 4, estos valores pueden ser considerados como un nivel crítico (por debajo de lo requerido). El Perfil 1 muestra contenidos altos de cationes intercambiables. El porcentaje de saturación de bases es mayor del 50% en el Perfil 1 y la tendencia de ésta fue disminuir con la profundidad del suelo, mientras que, en los Perfiles 2 y 4 es menor del 15% lo cual indica un bajo grado de saturación o de elevada eliminación de bases por lixiviación y lavado del suelo, aparentemente asociado a suelos más arenosos con menores capacidades de retención de agua. Esto puede estar asociado igaulmente a las especies de P. teocote y P. patula.
La capacidad de intercambio catiónico en general se puede considerar alta (promedio de 30 cmol + kg-1), lo que se atribuye, en gran parte, a la presencia de sesquióxidos (21), al contenido de materia orgánica, a la cantidad y naturaleza de las arcillas (15).
Extracción selectiva de hierro en suelos
Los resultados de la extracción selectiva de Fe se describen en las tabla 2 y tabla 3 (pág. 115), para los diferentes extractantes según el tipo de vegetación. Como se puede observar, la vegetación determina diferencias en los contenidos de Fed, Feo y Fep y el grado de alteración de los suelos.
Tabla 2. Extracción selectiva de hierro en suelos bajo diferentes tipos de vegetación del municipio de Acaxochitlan, Hidalgo, México.
Table 2. Selective extraction of iron in soils under different vegetation types in Acaxochitlan, Hidalgo, Mexico.

Tabla 3. Relaciones de hierro en suelos bajo diferentes tipos de vegetación del municipio de Acaxochitlan, Hidalgo, México.
Table 3. Relations iron in soils under different vegetation types Acaxochitlan Township, Hidalgo, Mexico.

Los tres suelos forestales poseen un contenido elevado de Fe, siendo el Fe total para Quercus spp de 3,6 a 4,82% (valor medio 4,14%), para Pinus teocote de 5,19 a 6,41% (valor medio 5,78%) y para Pinus patula de 5,44 a 5,98% (valor medio 5,76%), el tipo de vegetación influye significativamente en el contenido de Fet, donde Pp = Pt > Q (p ≤ 0,05) (tabla 4, pág. 116).
El porcentaje de Fe lábil extraído por ditionito-citrato-bicarbonato aumentó con respecto a la profundidad en los perfiles de Pt y Pp con excepción del perfil de Q, que disminuye en el horizonte C. En la tabla 2 (pág. 114) se observa un mayor porcentaje de Fed que de Feo y Fep, indica que la mayor cantidad de Fe liberado se da por la alteración e inestabilidad de los minerales ferromagnesianos (11, 18), donde el mayor porcentaje de Fed se presentó en Pp (valor promedio 56,7% del Fe total presente en el suelo) estadísticamente significativo.
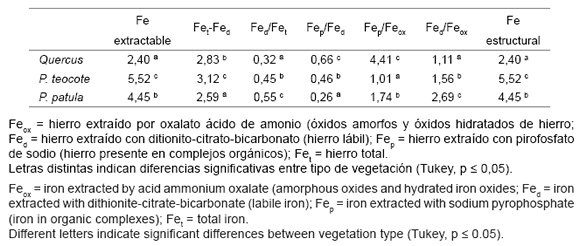
Tabla 4. Comparación de medias (en los primeros 50 cm aproximadamente) de hierro en suelos bajo diferentes tipos de vegetación del municipio de Acaxochitlan, Hidalgo, México
Table 4. Comparison of means (in the first 50 cm approximately) of iron in soils under different vegetation types Acaxochitlan Township, Hidalgo, Mexico.

La suma Feo+Fep, es superior en los tres perfiles estudiados a los valores de Fed, lo que indica que junto a complejos humus-Fe se presentan minerales de Fe cristalinos (goetita, hematita) (tabla 2, pág. 114)
El Fed muestra un aumento en el horizonte B de los tres perfiles acompañado con un incremento en el contenido de arcilla, lo que sugiere una migración conjunta desde el horizonte superficial, coincidentemente con el incremento de la relación arcilla/Fed (tabla 2, pág. 114) en los horizontes inferiores. Esto indica la presencia de procesos pedogenéticos de eluviación e iluviación de arcilla y óxidos de Fe. El tipo de vegetación influye significativamente (p ≤ 0.05) en la migración de arcilla en Q > Pp > Pt (tabla 4).
Levine y Golkosz (1983) estimaron el índice de acumulación de óxidos de Fe (IAFe) con la ecuación IAFe= (B-C)T; donde B, relación de Fed/Fet del horizonte superior; C, relación Fed/Fet del horizonte inferior siguiente; y T, ancho del horizonte (cm), para el perfil Pp el IAFe se presentó en horizonte Bt, con un valor de 4,23; 2,86 en horizonte Bt del perfil Q y 1,86 en horizonte Bt, del perfil Pt, lo que evidencia un predominio en la precipitación de óxidos de Fe (25).
La tabla 2 (pág. 114) presenta los resultados obtenidos para Fep. Para algunos horizontes su valor es mayor que el Feo, lo que evidencia una predominio de complejos Fe-húmico en los perfiles, sobre las formas amorfas inorgánicas.
Predomina en los horizontes inferiores un mayor contenido de Fep que de Feo, lo que evidencia que el 27% del perfil Q (horizonte Bt), el 24% del perfil Pt y Pp (horizonte Bt1 y Bt2 respectivamente) del Fe total presente en el suelo corresponde a Fe complejado por grupos funcionales orgánicos, por lo que óxidos de Fe no cristalinos son generalmente estabilizados por complejos orgánicos, situación similar reportaron Chiang et al. (11, 12) en suelos forestales de Taiwan. Liu y Chen (2004) informan que algunas sustancias solubles en agua (especialmente los ácidos fúlvicos) formados de la descomposición de la materia orgánica de la parte superficial del perfil complejan al Fe y éste es traslocado a través del perfil (27).
La acumulación de Fep en el horizonte Bt confirma los mecanismos de meteorización y procesos pedogenéticos que se presentan en la zona de estudio. Jansen et al. (20) y Schwertmann y et al. (42) reportan que la materia orgánica puede incrementar la concentración de materia orgánica disuelta y de ácidos fúlvicos, el cual aumenta la disolución total de metales vía reacciones de complejación en la solución del suelo, resultando en una alta movilidad del metal a través del perfil. El tipo de vegetación influye significativamente (p ≤ 0,05) en el contenido de Fep, donde Pt > Q = Pp (tabla 4, pág. 116).
Los valores obtenidos de Fe por oxalato (Feo) dan una aproximación del grado de acumulación de productos amorfos de reciente alteración Estos contenidos de Feo se asocian con suelos que presentan una alta carga dependiente del pH y una capacidad de fijar fósforo (30). El Feo es menor al contenido de Fep, lo que evidencia la presencia de complejos Fe-húmicos en los tres perfiles y un bajo contenido de formas amorfas inorgánicas sobre los complejos con la materia orgánica (tabla 2, pág. 114). Van Dam et al. reportan que óxidos de Fe amorfos (Feo) son considerados inestables sobre varias condiciones ambientales (44) y están presentes únicamente durante la formación inicial del suelo o con la presencia de silicatos y orgánicos que impiden la formación de óxidos de hierro cristalinos.
El contenido de Fe extraído con oxalato (Feo, óxidos de Fe amorfo) incremento ligeramente con la profundidad en Q y Pt excepto en los horizontes C y Bt1 respectivamente; mientras que, en el Pp disminuyó con relación a la profundidad.
Los bajos contenidos de Feo en los perfiles de Q y Pp, indican pequeñas cantidades de Fe amorfo que corresponde únicamente a 0,81 al 6,12% y 6,26 al 8,70% respectivamente del Fe total presente en el suelo (tabla 3, pág. 115). En el Pt, el Feo corresponde al 22,9; 18,8; 23,1; 24,7; 5,9 y 2,2% del Fe total presente en el suelo, se presenta en forma amorfa en los horizontes A1, A2, A3, A4, Bt1 y Bt2 respectivamente. El perfil Pt se dio el mayor contenido de Fe amorfo, siendo estadísticamente diferente (p ≤ 0,05) (tabla 4, pág. 116 y tabla 5, pág. 120) a Pp y Q.
Tabla 5. Comparación de medias (en los primeros 50 cm aproximadamente) de hierro en suelos bajo diferentes tipos de vegetación del municipio de Acaxochitlan, Hidalgo, México.
Table 5. Comparison of means (in the first 50 cm approximately) of iron in soils under different vegetation types Acaxochitlan Township, Hidalgo, Mexico.
Liu y Chen (2004) mencionan que algunas sustancias orgánicas solubles en agua (especialmente los ácidos fúlvicos) formados de la descomposición de la hojarasca de la parte superior del perfil, compleja el Fe y este es eluviado a través del perfil, situación que se presenta en el perfil Pt y Q (27).
Los valores mayores de 1,0 Feo indican la presencia de ferrihidrita (28), lo que significa que la meteorización de los aluminosilicatos primarios es alta en el perfil Pt, mientras que en Pp y Q (promedio 0,30) la meteorización es limitada en los minerales silicatados que contienen Fe.
Jones et al. (23) reportan que el contenido total de amorfos en los suelos es importante, porque estos se relacionan con problemas de manejo como la dispersión, floculación, agregación, infiltración, erosión, estabilidad de los terrenos, entre otros.
La relación Feo/Fed de los tres perfiles estudiados presenta valores altos en los horizontes A que en los B (tabla 3, pág. 115). Es posible que ello se deba a que la materia orgánica inhibe la transformación de la ferrihidrita hacia minerales cristalinos como la goetita/hematita. Las moléculas orgánicas en los suelos poseen grupos carboxil-hidroxilico, que en presencia de aniones silicatos y fosfatos y cationes cálcicos reaccionan química y físico-químicamente disminuyendo la tasa de transformación de la ferrihidrita hacia minerales férricos cristalinos (8).
Los valores de la relación Feo/Fed de la actividad del Fe, va de baja a muy baja (de 0,21 a 0,09) en los perfiles de Q y Pp, revelando poco contenido de Fe pedogenético y el predominio de los óxidos de Fe cristalinos (43), y un alto grado de alteración de los minerales relacionados con Fe. En Pt este valor varió de 0,56 a 0,37 en los primeros 69 cm, mostrando moderada cristalinidad de las fases de Fe (29). Cabria et al. (8) reportan que la formación de óxidos cristalinos de Fe es inhibido o retardada por la materia orgánica y que formas paracristalinas como la ferrihidrita (mayor del 32% del Fe total en los primeros 69 cm del perfil de suelo) (tabla 2, pág. 114) y tienden a ser dominantes sobre minerales como goetita y lepidocrocita (46). Por lo anterior, se considera que el perfil Pt y Pp presentan una mayor evolución en el proceso de organización estructural de los oxihidróxidos de Fe.
Mizota y van Reeuwijk (1989) determinan que con valores por debajo de 0,75 de la relación Feo/Fed puede considerarse a los suelos como antiguos. Por esta razón los perfiles estudiados en el presente trabajo entrarían en la categoría de suelos evolucionados, con valores inferiores en la mayoría de los casos a 0,56 (tabla 2, pág. 114).
Gamble y Daniels (17) reportan que valores de la relación Feo/Fed entre 0,16 y 0,20 indican la presencia de hematita, esta se presentó en el perfil de Q y Pp; mientras que en el perfil Pt únicamente en el horizonte Bt1 (17).
El Fe presente como goetita y hematita (óxidos de Fe cristalinos) se determinó mediante la diferencia en el contenido de Fed y Feo (35), en los perfile Pt y Pp se presentó un incremento de óxidos de Fe cristalinos en los horizontes profundos de 51,98% y 56,97% del Fe total presente en el suelo respectivamente, mientras que en el perfil de Q se observó un mayor contenido de óxidos de Fe cristalinos en el horizonte superior (25,8% del total de Fe presente en el suelo) y en el horizonte C, 8,64% del total de Fe presente en el suelo (tabla 2, pág. 114), lo que evidencia una limitada meteorización de los aluminosilicatos primarios (28).
La presencia de goetita y hematita en los horizontes Bt indica condiciones anaeróbicas, reducimorfismo, redepositación y de cristalización en el perfil (45) y un mayor tiempo de exposición al intemperismo de los minerales primarios (6).Malucelli et al. (29) reportan que la presencia de goetita/hematita en el suelo, debe al contenido de humedad y régimen de temperatura del suelo durante su formación (29). Vodyanitskii indica que tres factores favorecen la transformación de ferrihidrita en goetita: una baja temperatura, un clima húmedo y un pH ácido entre 4 a 6 (46). El perfil Pp presentó el mayor contenido de óxidos de Fe cristalino, estadísticamente diferente a Pt > Q (p ≤ 0,05) (tabla 3, pág. 115).
La relación (Fed-Feo)/Fet muestra la proporción de Fe total que forma parte de la red cristalina del silicato. Ochoa et al. (33) reportan que cuando se presentan valores altos de esta relación los suelos son menos alterados. Para el presente estudio los tres perfiles muestran valores inferiores a 0,57, revela que los silicatos ferromagnesianos contenidos en las rocas sobre la cual se desarrollan los suelos presentan una mediana a alta alteración, los valores promedios para Q (0,22), Pt (0,34) y Pp (0,49); donde Q influyen en mayor proporción en la alteración de los suelos (33).
La relación (Fed-Feo)/Fet expresa la proporción del hierro total en forma de oxihidróxidos (goetita y hematita). Esta relación guarda una estrecha vinculación con la edad de los suelos, así los valores altos, se presentan en los suelos más evolucionados En el estudio realizado, los valores son inferiores a 0,57 en la mayoría de los casos. Los tres perfiles presentan un bajo a moderado grado de evolución (33), al comparar la media de Q (0,22), Pt (0,34) y Pp (0,49), es de observarse que Pp presenta una tendencia a una mayor evolución.
La relación (Fet-Fed)/Fet indica el grado de evolución de los suelos estudiados, para el perfil Q se considera baja (valor medio 0,74) y moderada para Pt (valor medio 0,50) y Pp (valor medio 0,43).
Los valores obtenidos de la relación Fep/Fed mayores a 0,2 (tabla 2, pág. 114) indican la presencia de complejos organominerales de Fe de acuerdo con la bibliografía (39). Estos autores concluyen que para la formación de estos complejos se requieren valores de pH ácidos (< 4,9) y altos contenidos de materia orgánica, situación que se presenta en los tres perfiles estudiados.
En el perfil de Q el mayor porcentaje de Fe forma parte de las estructuras de los silicatos (Fet-Fed) que va del 70,2% en el horizonte superior a 90,5% en el horizonte inferior del Fe total presente en el suelo, esto coincide con las relaciones bajas de Fed/ Fet menores de 0,34 (tabla 2, pág. 114) indica que la mayoría de Fe no se encuentra en forma lábil (24), mientras que en los perfiles Pt y Pp la relación Fed/Fet fue mayor de 0,4 lo que muestra un mayor contenido de Fe lábil (Fed) que representa más del 40% del Fe total presente en el suelo en todo el perfil; por lo que el tipo de vegetación puede ejercer un efecto significativo Pt > Pp > Q (p ≤ 0,05) (tabla 3, pág. 115). La relación Fed/Fet varió de 0,09 a 0,64 en los tres perfiles, indica gran variación en el grado de alteración de los minerales primarios que contienen Fe.
Los valores altos de la relación Fep/Feo que se presentan en los tres perfiles (tabla 2, pág. 114) así como el contenido elevado de C orgánico muestra la presencia de complejos orgánicos de Fe que dominan sobre la fracción amorfa de Fe. En el perfil del suelo donde se desarrolla el bosque de Q se presentó el mayor porcentaje de complejos orgánicos de Fe siendo estadísticamente diferente (p ≤ 0,05) (tabla 5) a Pp > Pt.
Los valores mayores de 0,94 que se presentan en la relación Fep/Feo en los tres perfiles de suelo, sugieren la presencia de procesos naturales de reducción debido al contenido alto de arcilla y un pobre drenaje en los horizontes inferiores, bajo estas condiciones de los perfiles y un pH ácido se podría formar lepidocrocita en los horizontes Bt (27).
Si en estos perfiles se calcula el contenido de ferrihidrita (5Fe2O3 . 9H2O) mediante la proposición: ferrihidrita (%) = Feo(%)*1,7 (13) los porcentajes de ferrihidrita presentes en el perfil Pt varió de 38,9% en el horizonte superficial a 3,8% en el horizonte inferior del Fe total presente en el suelo; mientras que, en los perfiles Q y Pp los contenidos de ferrihidrita son menores del 10,4% y 14,8% del Fe total que se presenta en el suelo respectivamente. Jansen y col, (20) reportan que los ácidos orgánicos disuelven los minerales primarios y secundarios, y una parte del Fe liberado reacciona con la materia orgánica disuelta para formar complejos órgano-Fe (20). La otra forma óxidos de Fe cristalinos (goetita/hematita), los contenidos de ferrihidrita son estadísticamente diferente en el suelo dependiendo del tipo de vegetación presente Pt > Pp > Q (p ≤ 0,05) (tabla 4, pág. 116). Vodyanitskii (46) reporta que la ferrihidrita es termodinámicamente inestable y con el tiempo se convierte en óxido de Fe estable, comúnmente a goetita en climas templados. La ferrihidrita se forma por la precipitación de la solución del suelo con Fe y agentes orgánicos complejantes por oxidación rápida bajo la acción de microorganismos, y es típico de horizontes ácidos en pendientes húmedas; mientras que la formación de lepidocrocita y goetita se presenta en condiciones abióticas.
Álvarez et al. (7) reportan que la formación de goetita se da por la disolución de ferrihidrita y reprecipitación desde la solución del suelo; mientras que, la hematita se forma por la deshidratación y reordenamiento atómico de la ferrihidrita (7). La presencia de hematita y goetita en los horizonte Bt de Pp y Pt indica la presencia de condiciones anaeróbicas (45).
Los bajos porcentajes de ferrihidrita presentes en los perfiles indican que el Fe que se está liberando por meteorización de los componentes del suelo, una parte forma complejos con la materia orgánica y otra en la formación de minerales cristalinos de Fe (goetita-hematita). Tres importantes factores favorecen la transformación de ferrihidrita en goetita: una baja temperatura, un clima húmedo y un pH ácido entre 4 a 6 (46).
Conclusiones
El tipo de vegetación forestal influye en el grado de evolución del suelo, y en la distribución, contenido y formas de óxidos de Fe. En un orden de mayor a menor el contenido de Fe total en el suelo fue Pinus patula > Quercus spp > Pinus teocote. La solubilidad del Fe varió entre especies forestales, horizonte superficial y los subsuperficiales así como el grado de alteración. La distribución en los perfiles de suelo del Fe soluble en pirofosfato indica movimientos descendentes de complejos orgánicos de Fe. Los tres perfiles se caracterizan por la abundancia de materia orgánica que presenta un alto poder complejante, y que se estabiliza en los perfiles por el predominio de los complejos Fe-humus.
1 Acevedo-Sandoval, O. A.; Cruz-Sánchez, M.; Cruz-Chávez, E. 2002. Distribución de óxidos de Fe, Al y Si en horizontes endurecidos de origen volcánico. Agrociencia. 36: 401-409. [ Links ]
2 Acevedo-Sandoval, O. A.; Ortiz-Hernández, E.; Cruz-Sánchez, M.; Cruz-Chávez, E. 2004. El papel de óxidos de hierro en suelos. TERA Latinoamericana. (22)4: 485-499.
3 Acevedo-Sandoval, O. A.; Valera-Perez, M. A.; Prieto-García, F. 2010. Propiedades físicas, químicas y mineralógicas de suelos forestales en Acaxochitlán, Hidalgo, México. Rev. Universidad y Ciencia. 26(2): 137-149. [ Links ]
4 Agbenin, J. O. 2003. Extractable iron and aluminum effects on phosphate sorption in a Savanna Alfisol- Soil Science Society American Journal. 67: 589-595. [ Links ]
5 Aguilar-Santelises, A. 1988. Métodos de análisis de suelos. Sociedad Mexicana de la Ciencia del Suelo A. C. Chapingo, México.
6 Alcala de Jesús, M.; Hidalgo-Moreno, C.; Gutiérrez-Castorena, M. C. 2009. Mineralogía y retención de fosfatos en Andisoles. Terra Latinoamericana. 27: 275-286. [ Links ]
7 Alvarez, M.; Rueda, E. H.; Paiva-Santos, C. O.; Sileo, E. E. 2008.The influence of Mn (II) and aging time in the ferrihydrite to goethite transformation. The open mineralogy Journal. 2: 17-21. [ Links ]
8 Cabria, F. N.; Bianchini, M. R.; Mediavilla, M. C. 2005. Óxidos de hierro libres asociados a carbono orgánico en agregados de suelos del partido de Balcarce. Ci. Suelo (Argentina). 23: 23-29. [ Links ]
9 Castro-García, A.; Córdoba-Méndez, D. A. 1994 Estratigrafía del área volcánica de Tulancingo, Hidalgo, México. Pancromo 23, Revista de Investigación. Universidad Autónoma del Estado de Hidalgo. p. 26-39.
10 Chadwick, O. A.; Graham, R. C. 2000. Sesquioxides of iron in moist temperate forests of the state of Hidalgo, Mexico. Pedogenic processes p. E41-E75. In. Sumner, M.E. (Ed in Chief) Handbook of soil science. CRC Press USA.
11 Chen, Z. S.; Asio, V. B.; Yi, D. F. 1999. Characteristics and genesis of volcanic soils along a toposequence under a subtropical climate in Taiwan. Soil Science. 164: 510-525. [ Links ]
12 Chiang, H. C.; Wang, M. K.; Houng, K. H.; White, N.; Dixon, J. 1999. Mineralogy of B horizons in alpine forest soils of Taiwan. Soil Science. 164: 111-122. [ Links ]
13 Childs, C. W. 1985. Towards understanding soil mineralogy. II. Notes on ferrihydrite. N. Z. Soil Bureau Laboratory Report CM7, DSIR, New Zealand.
14 Diario Oficial del Estado de Hidalgo. 2001. Ordenamiento Ecológico Territorial. Estado de Hidalgo. Periódico Oficial (2 de abril de 2001) No. 14. Gobierno del Estado de Hidalgo. Poder Ejecutivo. 473 p.
15 Dixon, J. B. 2000. Functional roles of soil minerals. In R. Quintero-Lizaola, T. Reyna-Trujillo, L. Corlay-Chee, A. Ibáñez-Huerta, N. E. García-Calderón (Eds.) 2000. La edafología y sus perspectivas al siglo XXI. Tomo I Colegio de Postgraduados en Ciencias agrícolas, Universidad Nacional Autónoma de México, Universidad Autónoma de Chapingo, México.
16 FAO. 1990. Guidelines for soil profile description. Third edition (revised). Soil Resources Management and Conservation Service. Land and Water Development Division. FAO, Rome, Italy.
17 Gamble, E. D.; Daniels, R. B. 1972. Iron and silica in water, acid ammonium oxalate and dithionite extracts of some north Carolina coastal plain soil. Soil Science Society American Proceeding. 36: 939-943.
18 Heck, R. J.; Mermut, A. R. 1999. Mechanisms and rates of iron dissolution from Brazilian plinthustalfs by dilute hydrochloric and ascorbic acids. Soil Science. 164: 242-251. [ Links ]
19 INEGI. 1997. Acaxochitlán, Estado de Hidalgo. Cuaderno Estadístico Municipal. Edición 1996. Aguascalientes, Méx. 111 p.
20 Jansen, B.; Nierop, K. G. J.; Verstraten, M. 2005. Mechanisms controlling the mobility of dissolved organic matter, aluminium and iron in podzol B horizons. European Journal of Soil Science. 56: 537-550.
21 Johnson, C. E. 2002. Cation exchange properties of acid forest soils of the northeastern USA. European Journal of Soil Science. 53: 271-282.
22 Johnson, C. E.; Ruiz-Mendez, J. J.; Lawrence, G. B. 2000. Forest soil chemistry and terrain attributes in a Catskills Watershed. Soil Science Society American Journal. 64: 1804-1814. [ Links ]
23 Jones, R. C.; Babcock, C. J.; Knowlton, W. B. 2000. Estimation of the total amorphous content of Hawai’i soils by the Rietveld Method. Soil Science Society of American Journal. 64: 1100-1108.
24 Kleber, M.; Mikutta, R.; Torn, M. S.; John, R. 2005. Poorly crystalline mineral phases protect organic matter in acid subsoil horizons. European Journal of Soil Science. 56: 717-725.
25 Levine, E. R.; Ciolkosz, E. J. 1983. Soil development in till of various ages in Northeastern Pennsylvania. Quaternary Research. 19: 85-99.
26 Lilienfein, J.; Wilcke, W.; Ayarza, M. A.; Vilela, L.; do Carmo-Lima, S.; Zech, W. 2000. Soil acidificatión in Pinus caribea forest on Brazilian savanna Oxisols. Forest Ecology & Management. 128: 145-157.
27 Liu, J. C.; Chen, Z. S. 2004. Soil characteristics and clay mineralogy of two subalpine forest spodosols with clay accumulation in Taiwan. Soil Science. 169(1): 66-80.
28 Luzio, L. W.; Norambuena, P.; Casanova, M.; Vera, W. 2002. Génesis y propiedades de algunos suelos del altiplano de Chile. Suelo Nutrición Vegetal. 2: 35-52
29 Malucelli, F.; Terribile, F.; Colombo, C. 1999. Mineralogy, micromorphology and chemical analysis of andosols on the Island of Sao Miguel (Azores). Geoderma. 88: 73-98.
30 Mc Keague, J. A.; Day, J. H. 1966. Dithionite and oxalate extractable Fe and Al as aids in differentiating various classes of soils. Canadian. Journal Soil Science. 46: 13-22. [ Links ]
31 Mehra, O. P.; Jackson, M. L. 1960. Iron oxide removal from soils and clays by a dithionite-citrate system buffered with sodium bicarbonate. Clays and Clay Minerals. 7: 317-327. [ Links ]
32 Mizota, C.; van Reeuwijk, L. P. 1989. Clay mineralogy and chemistry of soils formed in volcanic material in diverse climatic regions. P 1-185 In: Soil monograph 2. International Soil Reference and Information Centre. Wageningen, The Netherlands.
33 Ochoa, H.; Bracho, H.; Oballos, J. 2000. Significación pedología del hierro en una secuencia de la estación experimental San Eusebio, Mérida, Venezuela. Agronomía Tropical. 50(4): 1-15.
34 Ortega, G. F.; Mitre, L. M.; Roldan, Q. J.; Aranda, G. J.; Morán, Z. D. J.; Alanís, A. S.; Nieto, S. A. 1992. Carta Geológica de la República Mexicana. Esc. 1: 2 000 000, con texto explicativo. 5ª Ed. Consejo de Recursos Minerales Instituto de Geología, U.N.A.M., México, D.F.
35 Parfitt, R. L.; Childs, C. W. 1988. Estimation of forms of Fe and Al: a review and analysis of contrasting soils by dissolution and Mossbaver methods. Australian J. Soil Research. 26: 121-144.
36 Prietzel, J.; Thieme, J.; Eusterhues, K.; Eichert, D. 2007. Iron speciation in soils and soil aggrgates by synchrotron based X-ray microspectroscopy (xanes, μ-xanes).
37 Rhoton, F. E.; Lindbo, D. L.; Rômkens, M. J. M. 1999. Iron oxides erodibility interactions for soils of the Memphis catena. Soil Science Society American Journal. 62: 1693-1703.
38 Schoeneberger, P. J.; Wysocki, D. A.; Benham, E. C.; Broderson, W. D. 2000. Libro de Campaña para Descripción y Muestreo de Suelos. Centro Nacional de Relevamiento de Suelos, Servicio de Conservación de Recursos Naturales, Departamento de Agricultura de los EE. UU., Lincoln, Nebraska. Argentina. Versión I.I.
39 Shoji, S.; Fujiwara, T. 1984. Active aluminum and iron in the humus horizons of Andosols from northeastern Japan: Their forms, properties and significance in clay weathering. Soil Science. 137: 216-226. [ Links ]
40 Smith, B. F. L. 1994. Characterization of poorly ordered minerals by selective chemical methods. In: Wilson, M.J. (ed). Clay Mineralogy Spectroscopic and Chemical Determinative Methods. Chapman and Hall. London, UK. p. 333-357.
41 Soil Survey Staff. 1999. Soil Taxonomy 2nd edition. Natural Resources Conservation Service, US Department of Agriculture. Madison, WI.
42 Schwertmann, U. 1985. Ocurrence and formation of ironoxides in various pedoenvironments. In: Iron in soils and clay minerals (eds J.W. Stucki, B.A.Goodmann & U. Schwertmann) pp 267-302.D. Reidel, Dordrecht. The Netherlands.
43 Taboada-Castro, M. T.; Silva-Hermo, B. M.; Barral-Silva, M. T. 1999. Relación entre formas de hierro y color rojo en suelos sobre calizas de Galicia. Cuaternario y Geomorfología. 13(3-4): 31-41.
44 Van Dam, R. L.; Harrison, J. B. J.; Hirschfeld, D. A.; Meglich, T. M.; Li, Y.; North, R. E. 2008. Mineralogy and magnetic properties of basaltic substrate soils: Kaho’olawe and Big island Hawaii. Soil Science Society of American Journal. 72: 244-257.
45 Varajâo, A. F. D. C.; Da Costa, G. M.; Varajâo, C. A. C.; Meunier, J. D.; Colin, F. 2007. Iron-bearing phases in a peat-derived duricrust from Brazil. European Journal of Soil Science. 58:1096-1106. [ Links ]
46 Vodyanitskii, Y. N. 2010. Iron hydroxides in soils: a review of publications. Eurasian Soil Science.43: 1244- 1254. [ Links ]














