Introducción
La estrategia de control de daños (ECD) es aceptada y tiene un alto índice de evidencia científica, cuando se aplica en pacientes gravemente lesionados en el contexto del traumatismo grave1-3.
A partir del año 2008, a causa del interés de cirujanos con experiencia en emergencias abdominales no traumáticas (EANT), esta estrategia comenzó a ocupar un lugar preponderante y generó cambios en el paradigma de atención para estos enfermos, más beneficiados al restituir la normalidad fisiológica que por resolver la lesión en un solo acto operatorio4-9.
Numerosas revisiones ofrecen informes que apoyan esta indicación, aunque para algunos autores son todavía insuficientes y de limitada evidencia4-11.
A fin de conocer los beneficios de la ECD en EANT en nuestro medio, los objetivos del presente estudio fueron: 1) describir las principales causas etiopatogénicas y las condiciones fisiopatológicas para su aplicación, 2) relacionar la mortalidad con la etiología, criterios de aplicación y factores de riesgo asociados y 3) comparar la mortalidad observada con la esperada según el score APACHE II.
Material y método
Se llevó a cabo un estudio observacional, retrospectivo, de pacientes mayores de 18 años, atendidos en forma consecutiva por EANT, y operados por especialistas en una institución de alta complejidad, entre enero de 2009 y diciembre de 2019.
En dicho lapso fueron evaluados 6632 pacientes con urgencias abdominales no traumáticas.
Los criterios de aplicación de la ECD fueron la presencia de signos, síntomas o resultados de estudios compatibles con: síndrome compartimental abdominal (SCA), sepsis abdominal y/o sistémica, acidosis metabólica y shock hipovolémico.
Los factores de riesgo de gravedad considerados fueron: edad ≥70 años, sexo, recuento de glóbulos blancos (GB) ≥ 10 000 x mm3, hemoglobina (Hb) ≤ 9 g/ dL, creatininemia ≥ 1,3 mg/dL, pH ≤ 7,25, ácido láctico ≥ 2,5 mmol/L, diabetes, puntuación de la Asociación Americana de Anestesiología (ASA) (≤ 3 versus ≥ 4), número de reoperaciones (≤ 3 versus ≥ 4) y cierre parietal versus no cerrado.
Se agrupó a los pacientes según el resultado del score APACHE II antes de aplicar la ECD y se comparó la mortalidad esperada con la observada en forma global y según grupos de puntuación.
Para su análisis estadístico, los datos fueron volcados en una base Microsoft Excel 97® y analizados empleando el programa estadístico R Core Team (2018), versión 4.0®.
Las variables incluidas fueron dicotomizadas y expresadas como frecuencia y porcentaje.
Las diferencias entre grupos se analizaron mediante la prueba asintótica para diferencia de proporciones y, cuando no se cumplieron los supuestos, por la prueba Chi2 y la prueba exacta de Fisher. Se consideraron significativas aquellas pruebas con un valor de p < 0,05; el intervalo de confianza fue del 95%.
Resultados
Con los criterios mencionados se encontraron 118 pacientes operados por EANT, 112 por peritonitis secundarias generalizadas (95%) y 6 por sangrados intraabdominales graves (5%).
Las peritonitis fueron secundarias a necrosis pancreática infectada (NPI) en 42 casos (37,5%), perforaciones intestinales no isquémicas (PINI), por causa diverticular, tumoral o dehiscencias anastomóticas, en 38 (34%), y perforaciones por isquemia intestinal grave (IIG) en 32 (28,5%).
Los sangrados intraabdominales graves fueron consecuencia de hemorragias en cirugías hepato-biliopancreáticas o pélvicas (5%).
La mortalidad global de la serie fue del 43,1% (51/118). La mortalidad ‒según la patología causal‒ fue: 65,6% (21/32) en la IIG, 42,8% (18/42) en las NPI y 31,5% (12/38) en las PINI. No existió mortalidad en los casos de sangrados intraabdominales graves. El análisis estadístico fue significativo a favor de la IIG como la causa con mayor mortalidad (p = 0,0027).
En cuanto a los criterios de aplicación y su influencia en la mortalidad, se observó que ‒con solo un criterio de aplicación‒ la mortalidad fue nula, con dos del 20%, con tres del 50%, con cuatro del 78% y con cinco del 100% (Fig. 1).
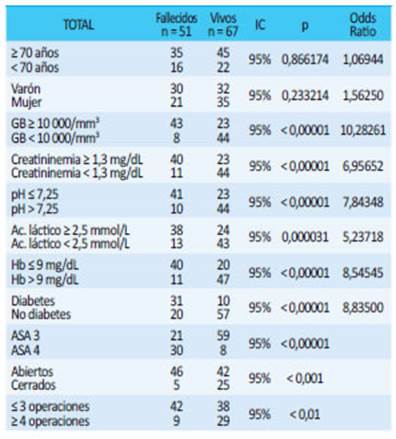
El análisis univariado de los factores de riesgo evidenció que el recuento de glóbulos blancos ≥ 10 000/mm3, creatinina ≥ 1,3 mg/dL, hemoglobina ≤ 9 g/ dL, pH ≤ 7,25, ácido láctico ≥ 2,5 mmol/L, presencia de diabetes, puntuación ASA ≥ 4 y ≥ 4 procedimientos operatorios, así como los pacientes que no fueron cerrados tempranamente, estuvieron relacionados en forma significativa con la mortalidad (Tabla 1).
El relevamiento global de la puntuación APACHE II en la serie registró una media 27,7 (rango entre 17 y 38 puntos) y una mediana de 28. La mortalidad esperada para una puntuación entre 25 y 29 puntos es del 53% y la observada fue del 43,1% (p = 0,118) (Tabla 2).
La comparación por grupos de puntuación mostró diferencias significativas en los grupos entre 20 y 24 (p = 0,004) y entre 25 y 29 puntos (p = 0,028). Con las demás puntuaciones no se registraron diferencias (Tabla 3).
Discusión
La estrategia de control de daños para el tratamiento de las EANT mantiene en la actualidad varios aspectos en controversia. Según algunos autores extranjeros, las principales indicaciones de esta estrategia son: las peritonitis generalizadas secundarias a perforación de vísceras huecas, las catástrofes vasculares abdominales (isquemia intestinal, aneurismas aórticos complicados y las hemorragias intraoperatorias), el síndrome compartimental abdominal (SCA), las infecciones parietales graves y las eventraciones agudas grado III1-16.
En la presente serie varias de estas fueron las causas involucradas. No registramos casos de aneurismas de aorta complicados. El SCA, las infecciones parietales graves y las eventraciones agudas grado III ocurrieron frecuentemente en la casuística aquí presentada y siempre fueron el resultado de una complicación séptica intraabdominal no controlada. Por este motivo fueron consideradas una consecuencia evolutiva de la enfermedad primaria y no un factor determinante por sí mismo. La mortalidad referida es muy variable entre las series y está fuertemente relacionada con la causa y a respuesta inflamatoria sistémica1,7,11,13,15-18. En comunicaciones previas sobre IIG, los autores manifestaron que la presentación clínica inespecífica y los métodos de diagnóstico no concluyentes llevan a diagnósticos erróneos y/o retrasados, que determinan estadios más avanzados con perforación intestinal, SCA, sepsis abdominal, sistémica o ambas, y falla multiorgánica17,18. Como se afirma en otras publicaciones, los autores coinciden en que la activación sucesiva de esta cascada de eventos en pacientes añosos, con comorbilidades graves y una menor reserva fisiológica, condicionan esta alta mortalidad19-25.
Esta alteración fisiológica ocurre en menor proporción en el caso de peritonitis secundarias a perforaciones intestinales de causa no isquémica (diverticular, tumoral o falla anastomótica). Es posible considerar que el diagnóstico y tratamiento más tempranos, la menor lesión fisiológica, los pacientes más jóvenes y con menor carga de enfermedades crónicas, son los responsables de la menor mortalidad. En cuanto a las infecciones graves en pancreatitis aguda, conocer mejor la historia natural de la enfermedad, la atención inicial agresiva, los potentes antibióticos y el desarrollo de tácticas de invasión mínima, mejoran las condiciones fisiológicas y sépticas del paciente, permitiendo reducir la necesidad de utilizar la ECD y disminuir la mortalidad14,20,21.
Los sangrados intraabdominales graves, en la presente serie, se resolvieron luego de maniobras de compresión y recomposición hemodinámica inicial. En estos pacientes, el compromiso hemodinámico, la acidosis metabólica y ‒en algunos casos‒ la hipotermia fueron rápidamente compensados y ello explica la ausencia de mortalidad, lo que coincide con lo observado por otros especialistas consultados19-26. El criterio de selección de los pacientes para indicar esta ECD en pacientes con EANT es un punto vital y clave en los resultados finales4-7,9,11. La agresión fisiopatológica y el choque sistémico difieren en los pacientes traumatizados y en las emergencias no traumáticas. En el traumatismo prevalecen la hemorragia y el daño tisular y, en las emergencias no traumáticas, la inflamación, la infección y la sepsis1-7,9,11.
Por este motivo, los especialistas consideran que aplicar solo la hipotensión, la hipotermia y la acidosis metabólica, como indicación en las EANT, es insuficiente4,5,21,29-31.
Hasta el momento no hay datos o evidencia que definan un grupo de criterios sobre los cuales sustentar la indicación para utilizar esta estrategia en las EANT, por lo cual la decisión sigue siendo compleja y desafiante, dependiendo fundamentalmente de la experiencia y juicio del cirujano. Se puede considerar que a la tríada letal deben agregarse otras variables que puedan evidenciar el deterioro fisiológico de estos enfermos11,21,27-31. Por tal motivo se incluyeron en la serie aquí expuesta, la presencia de signos, síntomas o resultados de estudios compatibles con un SCA, sepsis abdominal y shock séptico, como variables para indicar la ECD, que se activó por decisión del cirujano ante la presencia de al menos uno de los criterios mencionados.
Los resultados expresados en el Gráfico 1 permiten inferir que la mortalidad acompaña a la cantidad de criterios de indicación incluidos por cada caso.
Cuando se analizó el riesgo relativo de mortalidad según las variables de aplicación en toda la serie, se pudo concluir que, con cuatro o más criterios, el riesgo de morir es mayor y estadísticamente más significativo que en la población general. El mismo análisis efectuado según la causa especifica determinó que, en la IIG, el riesgo relativo de mortalidad aumentó a partir de tres criterios. Además, en el análisis de los fallecidos según patología causal, número de casos y cantidad de factores involucrados, también la IIG mostró mayor mortalidad que las otras patologías, aunque sin diferencias estadísticamente significativas.
Es posible considerar, al igual que en los estudios de otros autores, que estos resultados están íntimamente relacionados con la mayor agresión sistémica4,6,28-31.
Numerosas variables clínicas, de laboratorio y comorbilidades asociadas fueron evaluadas por distintos autores con resultados disímiles6,7,9,11,21,27,28,31.
En el presente estudio se incluyeron, además de edad, sexo, parámetros bioquímicos de inflamación, sepsis y falla multiorgánica, el score pronóstico ASA y dos variables de aspecto técnico, como la cantidad de procedimientos operatorios y si se efectuó el cierre parietal temprano o no. Estas dos variables se comportaron como factores predictivos de protección, ya que ‒cuando los pacientes superan las primeras etapas de la ECD o se logra cerrar el abdomen tempranamente‒ la mortalidad disminuye en forma significativa. Estas dos condiciones no fueron evaluadas en otras series consultadas. No obstante, los resultados son coincidentes con la bibliografía extranjera consultada7,8,11,14,16-26.
A fin de determinar los beneficios de la ECD en la serie, fueron comparadas la mortalidad observada con la esperada, según la puntuación APACHE II. Si bien dicha comparación no alcanzó significación estadística, el menor porcentaje de la mortalidad observada, sobre todo en los grupos entre 20 y 24 puntos y 25 y 29 puntos, estimula a los autores a continuar con esta metodología, ya que un mayor número de casos podría confirmar la hipótesis.
Sobre la base de los resultados expuestos y en respuesta a los objetivos planteados, es posible afirmar que, en la población analizada, la IIG fue la etiología asociada estadísticamente a mayor mortalidad, al igual que el aumento del número de criterios de aplicación y la inclusión de algunos factores de riesgo estudiados. Si bien este estudio presenta la limitación de tratarse de un análisis retrospectivo en un único centro, muestra los resultados de un equipo quirúrgico formado por cirujanos certificados y con experiencia en urgencias, que actuó con criterios compartidos en la selección de pacientes, en una serie consecutiva, en un centro de alta complejidad de la Argentina.
Futuros estudios multicéntricos, con mayor número de casos, permitirán alcanzar conclusiones más firmes sobre el tema.











 texto en
texto en