Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de reumatología
versión impresa ISSN 0327-4411versión On-line ISSN 2362-3675
Rev. argent. reumatolg. vol.32 no.2 Buenos Aires jun. 2021
ARTÍCULO ORIGINAL
Sobrevida, eficacia y seguridad de Golimumab en pacientes con Artritis Reumatoidea y Espondiloartritis: Datos de una cohorte argentina
Survival, efficacy and safety of Golimumab in patients with Rheumatoid Arthritis and Spondyloarthritis: Data from an Argentine cohort
Isnardi Carolina A1, Civit Emma2, García Ciccarelli Agustín2, Sánchez Alcover Jimena2, García Salinas Rodrigo3, Magri Sebastián3, Albiero Eduardo4, Gobbi Carla4, Velozo Edson5, Soriano Enrique R6, Brom Martín6, Zacariaz Johana6, Strusberg Ingrid7, Marcos Baravalle7, Sol Castaños7, Liliana Morales7, Paira Sergio8, Calvo Romina8, Ortiz Alberto8, Rodolfo Pérez Alamino9, Hernán Maldonado Ficco10, Citera Gustavo1
1Instituto de Rehabilitación Psicofísica, Ciudad Autónoma de Buenos Aires, Argentina.
2Hospital El Carmen, Mendoza, Argentina.
3Hospital Italiano de La Plata, Buenos Aires, Argentina.
4Sanatorio Allende, Córdoba, Argentina.
5Universidad y Sanatorio Adventista del Plata, Entre Ríos, Argentina.
6Hospital Italiano de Buenos Aires, Ciudad Autónoma de Buenos Aires, Argentina.
7Instituto Médico Strusberg, Córdoba, Argentina.
8Hospital Provincial Dr. José María Cullen, Santa Fe, Argentina.
9Hospital Dr. Nicolás Avellaneda, Tucumán, Argentina.
10Hospital San Antonio de Padua, Córdoba, Argentina.
Contacto: Dr. Gustavo Citera, Jefe de la Sección de Reumatología, Instituto de Rehabilitación Psicofísica, Echeverría 955, Bs. As. (1429), Argentina, Email: gustavocitera@gmail.com
Resumen
Objetivos: Golimumab ha sido aprobado para el tratamiento de pacientes con artritis reumatoidea (AR), artritis psoriásica (APs) y espondiloartritis axial. Sin embargo, los datos provenientes de nuestra región son escasos. El objetivo de este estudio fue evaluar la eficacia, seguridad y sobrevida acumulada de golimumab en pacientes de la vida real con AR, APs y espondilitis anquilosante (EA) de diferentes centros de Argentina.
Material y métodos: Se llevó a cabo un estudio longitudinal, en el que se incluyeron pacientes consecutivos mayores de 18 años con diagnóstico de AR (criterios ACR/EULAR 2010), APs (criterios CASPAR) y Espax (criterios ASAS 2009), que hayan iniciado tratamiento con golimumab de acuerdo a la indicación médica. Se obtuvieron los datos por revisión de historias clínicas. Se consignaron características sociodemográficas, clínicas, comorbilidades y tratamientos previos. Con respecto al golimumab, se registraron fecha de inicio, vía de administración y tratamientos concomitantes. Se determinó la actividad de la enfermedad mediante DAS28 en el caso de la AR, por DAPSA y MDA para APs y por BASDAI en el caso de Espax. Se consignó la presencia de eventos adversos (EA). En el caso de suspensión del tratamiento, se identificaron la fecha y motivo del mismo. Los pacientes fueron seguidos hasta la suspensión del golimumab, pérdida de seguimiento, muerte, o finalización del estudio (30 de noviembre de 2020).
Resultados: Se incluyeron 182 pacientes, 116 con diagnóstico de AR, 30 con APs y 36 con Espax. La mayoría de ellos (70.9%) eran mujeres con una edad mediana (m) de 55 años (RIC 43.8-64) y una duración de la enfermedad m de 7 años (RIC 4-12.7) al inicio del tratamiento. El 34.6% de los mismos habían recibido al menos una droga modificadora de la enfermedad (DME) biológica (-b) o sintética dirigida (-sd) previamente. El seguimiento total fue de 318.1 pacientes/año. El tratamiento con golimumab mostró mejoría clínica en los tres grupos de pacientes. La incidencia de eventos adversos fue de 6.6 por 100 pacientes/año, siendo las infecciones las más frecuentes. Durante el seguimiento, 50 pacientes (27.5%) suspendieron golimumab, la causa más frecuente fue el fracaso del tratamiento (68%), seguida de la falta de cobertura (16%) y el desarrollo de eventos adversos (10%). La persistencia de golimumab fue del 76% y 68% a los 12 y 24 meses, respectivamente. Se registró una sobrevida de 50.2 meses (IC 95% 44.4-55.9). Los pacientes que habían recibido tratamiento previo con DME-b y/o -sd mostraron una menor sobrevida (HR 2.4, IC 95% 1.3-4.4).
Conclusiones: El tratamiento con golimumab en pacientes de la vida real en Argentina ha demostrado una buena eficacia y seguridad. La sobrevida del fármaco fue de más de 4 años y casi el 80% seguía usando golimumab después de un año. El tratamiento previo con otros DME-b o -sd se asoció con una menor sobrevida al tratamiento.
Palabras clave: Golimumab; Inhibidor de TNFα; Eficacia; Seguridad; Sobrevida
Abstract
Objectives: Golimumab is approved for patients with rheumatoid arthritis (RA), psoriatic arthritis (PsA) and axial spondyloarthritis. However, data from our region are scarce. The aim of this study was to evaluate the efficacy, safety, and cumulative survival of golimumab in real-life patients with RA, PsA and axial spondyloarthritis (axSpa) from different rheumatology centers in Argentina.
Material and methods: We performed a longitudinal study of consecutive adults with RA (ACR/EULAR 2010 criteria), PsA (CASPAR criteria) and axSpa (ASAS 2009 criteria), who have started treatment with golimumab according to medical indication. Data was obtained by review of medical records. Sociodemographic and clinical data, musculoskeletal manifestations, comorbidities and previous treatments were recorded. In reference to golimumab treatment, start date, route of administration and concomitant treatments were identified. Disease activity was assessed using DAS28 for RA patients, DAPSA and MDA for PsA and BASDAI for axSpa. The presence of adverse events was recorded. If golimumab was stopped, date and cause was documented. Patients were followed up until golimumab discontinuation, loss of follow-up, death, or study completion (November 30, 2020).
Results: In total 182 patients were included, 116 with a diagnosis of RA, 30 with PsA and 36 with axSpa. Most of them (70.9%) were female with a median (m) age of 55 years (IQR 43.8-64) and m disease duration of 7 years (IQR 4-12.7) at treatment initiation. Al least one prior biological (-b) and/or targeted synthetic (-ts) disease modifying antirheumatic drug (DMARD) was received by 63 patients (34.6%). Total follow-up was 318.1 patients/year. Golimumab treatment showed clinical improvement in all three groups of patients. The incidence of AE was 6.6 per 100 patients/year, being infections the most frequents ones. During follow-up, 50 patients (27.5%) discontinued golimumab, the most frequent cause was treatment failure (68%), followed by lack of health insurance (16%) and adverse events (10%). Golimumab persistence was 76% and 68% at 12 and 24 months, respectively. Treatment survival was 50.2 months (95% CI 44.4-55.9). Patients who had received prior treatment with b- or ts-DMARDs showed lower survival (HR 2.41, 95% CI 1.3-4.4).
Conclusions: Golimumab treatment in real life patients in Argentina has shown good efficacy and safety. Drug survival was over 4 years and almost 80% were still using golimumab after one year. Prior treatment with other b- or ts-DMARDs was associated with lower treatment survival.
Key words: Golimumab; TNFα inhibitor; Efficacy; Safety; Survival
Introducción
Los agentes inhibidores del factor de necrosis tumoral alfa (TNFα) constituyen actualmente una herramienta fundamental en el tratamiento de pacientes con artritis reumatoidea (AR), espondiloartritis axial (Espax) y artritis psoriásica (APs), ya que sabemos que el TNFα cumple un rol fundamental en la mediación del proceso inflamatorio de estas patologías.1
Existen cinco inhibidores de TNFα aprobados por las agencias regulatorias de medicamentos para el tratamiento de estas artropatías inflamatorias: adalimumab, cetolizumab, etanercept, golimumab e infliximab. Estas drogas han demostrado una muy buena eficacia y seguridad en ensayos randomizados controlados. Sin embargo, los pacientes incluidos en este tipo de estudios son estrictamente seleccionados y vigilados y no reflejan las características generales de la población que habitualmente concurre a nuestro consultorio, así como tampoco se tienen en cuenta los problemas de acceso a la medicación y preferencias de los pacientes. Por este motivo es tan valiosa la información proveniente de registros de la vida real, particularmente locales.2
Además, estudios a largo plazo y con mayor número de pacientes permiten identificar eventos adversos poco frecuentes y evaluar otro punto interesante, la persistencia del tratamiento. La misma hace referencia al periodo durante el cual el paciente recibe el medicamento y puede ser utilizada como un subrogante del éxito del tratamiento a largo plazo en enfermedades crónicas, ya que no solo depende de la eficacia y seguridad de la droga, sino que también es influenciada por la adherencia y la experiencia del paciente. La evaluación de este tipo de desenlaces es fundamental, ya que sabemos que el cumplimiento inadecuado y falta de persistencia resultan en un aumento de la morbilidad y la mortalidad para una amplia variedad de enfermedades, así como también en mayores costos de salud.3
Golimumab es un anticuerpo monoclonal humano dirigido contra el TNFα en sus formas soluble y transmembrana.4 Puede ser utilizado de manera subcutánea o endovenosa y ha demostrado eficacia para su uso en pacientes con AR,5-6 artritis psoriásica (APs),7 espondilitis anquilosante (EA)8 más recientemente para espondiloartritis axial no radiográfica.9
El objetivo de este estudio fue evaluar la eficacia, seguridad y sobrevida acumulada de golimumab en pacientes de la vida real con AR, APs y Espax de diferentes centros de Argentina.
Materiales y Métodos
Se llevó a cabo un estudio longitudinal prospectivo, multicéntrico, observacional, en el que se incluyeron pacientes consecutivos mayores de 18 años con diagnóstico de AR que cumplían criterios ACR/EULAR 201010 y con espondiloartritis, según criterios ASAS 200911 para Espax y CASPAR12 para APs, que hayan iniciado tratamiento con golimumab subcutáneo o endovenoso de acuerdo a la indicación médica en cada centro. Los datos fueron obtenidos por revisión de historias clínicas de pacientes que concurrieron al control reumatológico de diez centros públicos y privados de la Argentina: tres de Córdoba (Sanatorio Allende, Instituto Médico Strusberg, Hospital San Antonio de Padua), dos de Ciudad Autónoma de Buenos Aires (Instituto de Rehabilitación Psicofísica y Hospital Italiano de Buenos Aires), uno de Mendoza (Hospital El Carmen), uno de Buenos Aires (Hospital Italiano de La Plata), uno de Entre Ríos (Universidad y Sanatorio Adventista del Plata), uno de Santa Fe (Hospital Provincial Dr. José María Cullen) y uno de Tucumán (Hospital Dr. Nicolás Avellaneda).
Los pacientes fueron seguidos de manera semestral desde el inicio de la medicación. Basalmente se consignaron características sociodemográficas, clínicas, manifestaciones musculoesqueléticas, comorbilidades y tratamientos previos. Con respecto al golimumab, se registraron fecha de inicio, vía de administración y medicamentos concomitantes. Se determinó la actividad de la enfermedad mediante DAS2813 en el caso de la AR, por DAPSA14-15 y MDA16 para APs y por BASDAI17 en el caso de Espax, al inicio del tratamiento y cada seis meses. Se consignó el desarrollo de eventos adversos y su gravedad, entendiendo como evento adverso severo aquel que requiere hospitalización, tratamiento endovenoso, provoca la discapacidad del paciente, o lleva a su muerte. Los mismos fueron clasificados en: reacción en el sitio de inyección o durante la infusión, según corresponda, alteración gastrointestinal, hematológica, cutánea, infección, neoplasias. En el caso de suspensión del tratamiento, se identificaron la fecha y motivo del mismo. Los pacientes fueron seguidos hasta la suspensión del golimumab, pérdida de seguimiento, muerte, o finalización del estudio (30 de noviembre de 2020).
Para el análisis estadístico, se realizó estadística descriptiva, las variables continuas se expresaron en medianas y rango intercuartilo (RIC) o bien como medias con su correspondiente desvío estandar (± DS), según corresponda y las variables categóricas en frecuencia y porcentaje. La incidencia de eventos adversos se expresó en eventos cada 100 paciente/año de forma global y para cada categoría de evento adverso. Se utilizaron curvas de Kaplan-Meier para determinar la sobrevida de la droga y las comparaciones según datos sociodemográficos o clínicos se realizaron por análisis de log Rank. Los factores asociados a la supervivencia del tratamiento con golimumab, fueron analizados en modelos de regresión proporcional de Cox. Los análisis se llevaron a cabo mediante el programa R.
Resultados
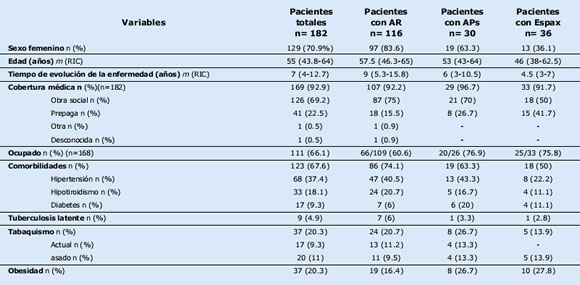
Se incluyeron en total 182 pacientes, de los cuales 116 tenían diagnóstico de AR, 30 de APs y 36 de Espax. La mayoría de ellos (70.9%) eran mujeres con una edad mediana (m) de 55 años (RIC 43.8-64) y una duración de la enfermedad m de 7 años (RIC 4-12.7) al inicio del tratamiento. El 67.6% de los mismos reportaron tener al menos alguna comorbilidad y casi el 65% presentaba sobrepeso u obesidad. Nueve pacientes tenían tuberculosis latente y todos ellos recibieron profilaxis con isoniacida. La mayoría tenía cobertura médica. Otras características basales de la población se informan en la Tabla I. Con respecto a los pacientes con AR, cerca del 90% era seropositivo para factor reumatoideo y/o anti-CCP, 70.2% presentaba enfermedad erosiva y 19.3% nodular. Dos tercios de los pacientes con APs tenían antecedente de compromiso entesítico y 46.7% de dactilitis. El 50% presentaba compromiso mixto, mientras que el 43.3 solo daño periférico y 6.7% axial puro. El 77.1% de los pacientes con Espax tenía HLA-B27 positivo, un tercio tenía antecedentes de uveítis, 50% de entesitis y 16.7% de enfermedad inflamatoria intestinal.
Tabla I. Características basales de la población
Al momento del inicio del golimumab, 34.6% habían recibido al menos una droga modificadora de la enfermedad (DME) biológica (-b) o sintética dirigida (-sd) previamente. El 28.6% tenían antecedente de uso de al menos un inhibidor de TNFα, siendo los más frecuentes Etanercept y Adalimumab. (Tabla II)
Tabla II. Tratamientos previos recibidos por los pacientes

En la mayoría de los casos, el golimumab fue administrado por vía subcutánea (92.9%). La causa de indicación más frecuente fue la falla a DME convencionales (-c) en monoterapia (18.1%) o en combinación (38.5%), seguido por falla a DME-b (24.7%) y -sd (2.7%). En el 80.8% de los casos, el golimumab se asoció a DME-c (AR 93.1%, APs 70%, Espax 50%), siendo el metotrexato el más utilizado (63.2%).
Los pacientes fueron seguidos por una m de tiempo de 14.5 meses (RIC 2-22.8), lo que representa un total de 318.1 pacientes/año. El tratamiento con golimumab mostró mejoría clínica en los tres grupos de pacientes, tanto a los 6 como a los 12 meses. (Figura I)

Figura I. Eficacia de golimumab en los pacientes con artritis reumatoidea, artritis psoriásica y espodiloartritis axial
La incidencia de eventos adversos fue de 5.2 por 100 pacientes/año (IC 95% 3.1 - 8.4), siendo las infecciones las más frecuentes. No se registraron infecciones por Mycobacterium tuberculosis. Se reportaron siete eventos adversos severos (incidencia: 2.2 por 100 pacientes/año). Los mismos ocurrieron en cinco pacientes y fueron: un paciente presentó artritis séptica en codo, otro un tumor benigno ginecológico y otro un cuadro de reactivación de EPOC que requirió hospitalización. Un paciente tuvo un primer episodio de tromboembolismo pulmonar asociado a trombosis venosa profunda e insuficiencia cardíaca y un segundo episodio de neumonía adquirida de la comunidad con ingreso a unidad de cuidados intensivos. Por último, el quinto paciente, de 71 años y con antecedentes cardiovasculares, tuvo un primer evento de cólico biliar que requirió internación para manejo sintomático y un segundo evento caracterizado por accidente cardiovascular isquémico seguido de muerte.
Durante el seguimiento, 50 pacientes (27.5%) suspendieron golimumab, la causa más frecuente fue la falla al tratamiento (68%), seguida de la falta de cobertura (16%) y el desarrollo de eventos adversos (10%). La sobrevida global del fármaco fue de X 50.2 meses (IC 95% 44.4-55.9) (Figura IIA) y no se encontraron diferencias significativas entre los grupos de enfermedades (Figura IIB). Los pacientes que habían recibido tratamiento previo con DME-b y/o -sd mostraron una sobrevida significativamente menor (Figura IIC). Si bien la misma fue numéricamente inferior en pacientes obesos y tabaquistas activos, la diferencia no alcanzó diferencias significativas [obesos: X 37.2 (IC 95% 26.9-47.5) vs no obesos: X 51.4 (IC 95% 45.2-57.6), p= 0.159]; [tabaquistas activos: X 32.1 (IC 95% 15.9-48.3) vs no tabaquistas y ex tabaquistas: X 51.6 (IC 95% 45.7-57.6), p= 0.110]. Tampoco se encontraron diferencias significativas al subanalizar a los pacientes según el sexo, la presencia de comorbilidades, cobertura médica, la vía de administración del golimumab, ni el uso concomitante de DME-c.

Figura II. Sobrevida del tratamiento con golimumab
La persistencia de golimumab fue del 76% y 68% a los 12 y 24 meses, respectivamente. A los 12 meses la misma fue similar entre los tres grupos de pacientes (AR 76%, APs 75%, Espax 76%), pero a los 24 meses los pacientes con Espax presentaron retención del fármaco numéricamente superior (p= NS): AR 67%, APs 65%, Espax 76%. Con respecto a los pacientes con y sin tratamientos previos con DME-b y/o -sd, los primeros tuvieron menor persistencia del golimumab, 67% y 63% vs 81% y 72%, a los 12 y 24 meses, respectivamente (p= 0.044). Teniendo en cuenta que la segunda causa de suspension de Golimumab en esta cohorte fue la falta de cobertura por el sistema de salud, analizamos la persistencia excluyendo a estos pacientes para que los datos puedan ser comparables a otras cohortes y observamos que la sobrevida acumulada del tratamiento con golimumab fue de 53.4 meses (IC 95% 47.6-59.3) y la persistencia a los 12 y 24 meses de 78% y 73%, respectivamente. Todos los pacientes que debieron suspender el golimumab por falta de cobertura por parte del financiador, eran atendidos en centros públicos, tres de ellos no tenían cobertura, tres tenían obra social y 2 prepaga. Siete tenían diagnóstico de AR y uno de EA.
En el análisis multivariado, ajustando por edad, sexo, diagnóstico y duración de la enfermedad, los pacientes que habían recibido al menos un tratamiento con DME-b y/-sd mostraron el doble de riesgo de suspender el tratamiento (HR 2.4, IC 95% 1.3-4.4, p= 0.005) (Tabla III).
Tabla III. Sobrevida del tratamiento con golimumab. Análisis multivariado (variable dependiente: sobrevida del tratamiento con golimumab)

Discusión
Conocer el impacto del uso de las diferentes drogas en pacientes de la vida real, por fuera de los datos reportados por los ensayos controlados, se ha vuelto cada vez más importante. Este estudio es el primero en mostrar información acerca del uso de golimumab en pacientes reales con artropatía inflamatoria en Latinoamérica. Hemos identificado una buena eficacia y seguridad y una sobrevida global mayor a 4 años. Los pacientes con tratamientos previos con agentes biológicos y/o sintéticos dirigidos presentaron dos veces más riesgo de suspender el golimumab.
La tasa de retención de golimumab en las fases de extensión a cinco años de los ensayos controlados en pacientes con AR, APs y Espax con respuesta inadecuada a tratamientos convencionales o analgésicos no esteroideos, según corresponda, es de aproximadamente del 70%.18-20 Sin embargo, como hemos mencionado previamente, estos pacientes se ajustan a estrictos criterios de inclusión y exclusión y en no se estudiaron pacientes con antecedentes de tratamientos previos con otros agentes biológicos o sintéticos dirigidos, variables que pueden explicar esta alta persistencia de golimumab. Resultados similares a los encontrados en nuestra cohorte fueron reportados previamente por otras cohortes de pacientes de la vida real. Por ejemplo, el registro alemán GO-NICE, en el cual se incluyeron más de 1400 pacientes con AR, APs y Espax, de los cuales cerca del 40% tenían experiencia de haber sido tratados con DME-b, evidenció una persistencia de la droga del 45.5% a los dos años. La causa más frecuente de discontinuación fue la falla al tratamiento en el 40% de los casos.21 En el registro italiano GO-AREL, de pacientes con AR, APs y Espax identificaron una tasa de retención levemente superior. La misma fue de 70.2% a los dos años y al igual que lo observado en nuestra cohorte, los pacientes con espondiloartritis axial presentaron una persistencia de golimumab superior, de 78.2%, en comparación con los pacientes con APs y AR, 66.9% y 63.6%, respectivamente.22
En nuestra cohorte, el 16% de los pacientes que debieron suspender el tratamiento con golimumab lo hicieron por falta de cobertura. La problemática de acceso a tratamientos de alto costo ya ha sido descripta previamente en dos cohortes argentinas de pacientes con AR y EsPax, en las cuales se ha demostrado que a diferencia de lo reportado por otros trabajos de vida real de Europa o Estados Unidos, la falta de cobertura por parte del financiador se encuentra entre las primeras causas de suspensión de las DME-b (30.8% y 41%, respectivamente).23-24 Este hecho hace difícil la comparación completa de nuestros datos con otras cohortes, razón por la cual decidimos hacer un análisis secundario, excluyendo esta causa particular de suspensión del tratamiento en nuestro país.
La mayor sobrevida de los inhibidores de TNFα en pacientes con espondiloartritis ya ha sido descripta por otros autores. Varios factores han sido asociados a esta diferencia, como por ejemplo el predominio de sexo masculino, la menor frecuencia de uso de esteroides y la fisiopatología de la enfermedad.25-27 En nuestro registro, la sobrevida de golimumab en pacientes con Espax fue numéricamente mayor, pero las diferencias no alcanzaron significancia estadística. En comparación con la población general estudiada, los pacientes con Espax eran más frecuentemente de sexo masculino (63.9%), más jóvenes (m 46 años, RIC 38-62.5) y tenían menor prevalencia de comorbilidades (50%).
Otro punto a destacar, es la menor retención del golimumab en pacientes con tratamientos previos con DME-b y/o -sd. Datos del registro italiano LORHEN28, en el que se incluyeron 195 pacientes con AR en tratamiento con etanercept, adalimumab o golimumab como drogas de segunda línea luego de presentar respuesta inadecuada a inhibidores de TNFα, la persistencia de las mismas a los 12 y 24 meses fue 46.7%/42.9%/66.5% y 39.8%/31.2%/53.4%, respectivamente. En este caso, la sobrevida de golimumab fue superior a la registrada con los otros inhibidores de TNFα. En nuestra cohorte, la persistencia a 12 y 24 meses en pacientes con experiencia previa a DME-b y/o -sd fue de 67% y 63%, respectivamente.
En relación a la eficacia del tratamiento, hemos detectado cambios sustanciales en los índices compuestos de la enfermedad en los tres grupos de pacientes. A los seis meses observamos un descenso de 2.1 puntos en el DAS28 en los pacientes con AR, 22.1 puntos en el valor de DAPSA en aquellos con diagnóstico de APs y 3.4 puntos en el BASDAI en Espax. Estos resultados son comparables con los reportados por registro de la vida real como el GO-NICE21 o el NOR-DMARD29 y ensayos controlados.18-20
Finalmente, este estudio presenta fortalezas y limitaciones. Con respecto a estas últimas, los datos de este estudio fueron recolectados a partir de revisión de historias clínicas y por lo tanto puede existir un sesgo de datos perdidos. Además, dado que se trata de una cohorte de pacientes con tratamiento con golimumab, no se cuenta con un grupo control para comparar los datos obtenidos. Por último, el seguimiento total de los pacientes fue de m 14.5 meses, la cual es relativamente corta. Sin embargo, cabe destacar, que el registro continúa abierto y esperamos en un futuro poder reportar datos a mayor plazo. Esta cohorte es la primera en evaluar la eficacia, seguridad y sobrevida de golimumab en pacientes con artropatías inflamatorias en Argentina, y hasta nuestro conocimiento, también en Latinoamérica. Esta compuesta por un grupo considerable de pacientes y nos ha permitido conocer información local y de la vida real.
Conclusiones
El tratamiento con golimumab en pacientes de la vida real en Argentina ha demostrado una buena eficacia y seguridad. La sobrevida del fármaco fue de más de 4 años y casi el 80% seguía usando golimumab después de un año. El tratamiento previo con otros DME-b o -sd se asoció con una menor sobrevida al tratamiento.
1. Thompson C, Davies R, Choy E. Anti-cytokine therapy in chronic inflammatory arthritis. Cytokine. 2016;86:92-9. [ Links ]
2. Pincus T, Sokka T. Should contemporary rheumatoid arthritis clinical trials be more like standard patient care and vice versa?. Ann Rheum Dis 2004;63 Suppl 2:ii32-ii39. [ Links ]
3. Cramer JA, Roy A, Burrell A, Fairchild CJ, Fuldeore MJ, Ollendorf DA, et al. Medication compliance and persistence: terminology and definitions. Value Health. 2008;11(1):44-7. [ Links ]
4. Voulgari PV. Golimumab: a new anti-TNF-alpha agent for rheumatoid arthritis, psoriatic arthritis and ankylosing spondylitis. Expert Rev Clin Immunol. 2010;6(5):721-33. [ Links ]
5. Keystone EC, Genovese MC, Klareskog L, Hsia EC, Hall ST, Miranda PC, et al. Golimumab, a human antibody to tumour necrosis factor alpha given by monthly subcutaneous injections, in active rheumatoid arthritis despite methotrexate therapy: the GO-FORWARD Study. Ann Rheum Dis 2009;68(6):789-96. [ Links ]
6. Smolen JS, Kay J, Doyle MK, Matteson EL, Wollenhaupt J, Gaylis N, et al. Golimumab in patients with active rheumatoid arthritis after treatment with tumour necrosis factor alpha inhibitors (GO-AFTER study): a multicentre, randomised, double-blind, placebo-controlled, phase III trial. Lancet 2009;374(9685):210-21. [ Links ]
7. Kavanaugh A, McInnes I, Mease P, Krueger GG, Gladman D, Gomez-Reino J, et al. Golimumab, a new human tumor necrosis factor alpha antibody, administered every four weeks as a subcutaneous injection in psoriatic arthritis: Twenty-four-week efficacy and safety results of a randomized, placebo-controlled study. Arthritis Rheum 2009;60(4):976-86. [ Links ]
8. Inman RD, Davis JC, van der Heijde D, Diekman L, Sieper J, Kim SI, et al. Efficacy and safety of golimumab in patients with ankylosing spondylitis: results of a randomized, double-blind, placebo-controlled, phase III trial. Arthritis Rheum 2008;58(11):3402-12. [ Links ]
9. Sieper J, van der Heijde D, Dougados M, Maksymowych WP, Scott BB, Boice JA, et al. A randomized, double-blind, placebo-controlled, sixteen-week study of subcutaneous golimumab in patients with active nonradiographic axial spondyloarthritis. Arthritis Rheumatol. 2015;67(10):2702-12. [ Links ]
10. Funovits J, Aletaha D, Bykerk V, Combe B, Dougados M, Emery P, et al. The 2010 American College of Rheumatology/European League Against Rheumatism classification criteria for rheumatoid arthritis: methodological report phase I. Ann Rheum Dis 2010;69(9):1589-95. [ Links ]
11. Rudwaleit M, van der Heijde D, Landewé R, Listing J, Akkoc N, Brandt J, et al. The development of Assessment of SpondyloArthritis international Society classification criteria for axial spondyloarthritis (part II): validation and final selection. Ann Rheum Dis. 2009;68(6):777-83. [ Links ]
12. Taylor W, Gladman D, Helliwell P, Marchesoni A, Mease P, Mielants H, et al. Classification criteria for psoriatic arthritis: development of new criteria from a large international study. Arthritis Rheum 2006;54(8):2665-73. [ Links ]
13. Prevoo M, van‘ t Hof M, Kuper H, van Leeuven M, van de Putte L, van Riel P. Modified disease activity scores that include twenty-eight-joint counts. Development and validation in a prospective longitudinal study of patients with rheumatoid arthritis. Arthritis Rheum 1995;38(1):44-8.
14. Eberl G, Studnicka-Benke A, Hitzelhammer H, Gschnait F, Smolen J. Development of a disease activity index for the assessment of reactive arthritis (DAREA). Rheumatology (Oxford) 2000;39(2):148-55. [ Links ]
15. Coronel Ale AL, Schneeberger EE, Cerda OL, Zaffarana C, Fornaro MN, Landi M, et al. Disease Activity in Psoriatic Arthritis-ESR Index Maybe a Valid Tool to Evaluate Disease Activity in Patients with Psoriatic Arthritis When CRP Is Not Available. Arthritis Rheumatol 2017;69(suppl 10):2554. [ Links ]
16. Coates L, Fransen J, Helliwell P. Defining minimal disease activity in psoriatic arthritis: a proposed objective target for treatment. Ann Rheum Dis 2010;69(1):48-53. [ Links ]
17. Garrett S, Jenkinson T, Kennedy LG, Whitelock H, Gaisford P, Calin A. A new approach to defining disease status in ankylosing spondylitis: the Bath Ankylosing Spondylitis Disease Activity Index. J Rheumatol. 1994;21(12):2286-91. [ Links ]
18. Keystone EC, Genovese MC, Hall S, Bae SC, Han C, Gathany TA, et al. Safety and Efficacy of Subcutaneous Golimumab in Patients with Active Rheumatoid Arthritis despite Methotrexate Therapy: Final 5-year Results of the GO-FORWARD Trial. J Rheumatol. 2016;43(2):298-306. [ Links ]
19. Kavanaugh A, McInnes IB, Mease P, Krueger GG, Gladman D, van der Heijde D, et al. Clinical efficacy, radiographic and safety findings through 5 years of subcutaneous golimumab treatment in patients with active psoriatic arthritis: results from a long-term extension of a randomised, placebo-controlled trial (the GO-REVEAL study). Ann Rheum Dis. 2014;73(9):1689-94. [ Links ]
20. Deodhar A, Braun J, Inman RD, van der Heijde D, Zhou Y, Xu S, et al. Golimumab administered subcutaneously every 4 weeks in ankylosing spondylitis: 5-year results of the GO-RAISE study. Ann Rheum Dis. 2015;74(4):757-61. [ Links ]
21. Krüger K, Burmester GR, Wassenberg S, Bohl-Bühler M, Thomas MH. Effectiveness and safety of golimumab in patients with rheumatoid arthritis, psoriatic arthritis and ankylosing spondylitis under real-life clinical conditions: non-interventional GO-NICE study in Germany. BMJ Open. 2018;8(6):e021082. [ Links ]
22. Iannone F, Santo L, Anelli MG, Bucci R, Semeraro A, Quarta L, et al. Golimumab in real-life settings: 2 Years drug survival and predictors of clinical outcomes in rheumatoid arthritis, spondyloarthritis, and psoriatic arthritis. Semin Arthritis Rheum. 2017;47(1):108-14. [ Links ]
23. Rolón Campuzano R, Dal Pra F, Schneeberger EE, Coronel Ale AL, Cerda OL, Correa MA, et al. Patrones de tratamiento con agentes biológicos. Eficacia y sobrevida a largo plazo en pacientes con artritis reumatoidea. Rev Arg Reumatol. 2018;29(4):14-9. [ Links ]
24. Cavalieri M, Schneeberger EE, Dal Pra F, Correa MA, Buschiazzo E, Juárez V, et al. Patrones de tratamiento con agentes biológicos, eficacia y sobrevida a largo plazo en pacientes con espondiloartritis axial. Impacto de los factores sociodemográficos en Latinoamérica. Rev Arg Reumatol. 2018;29(4):22-8. [ Links ]
25. Fafá BP, Louzada-Junior P, Titton DC, Zandonade E, Ranza R, Laurindo I, et al. Drug survival and causes of discontinuation of the first anti-TNF in ankylosing spondylitis compared with rheumatoid arthritis: analysis from BIOBADABRASIL. Clin Rheumatol. 2015;34(5):921-7. [ Links ]
26. Carmona L, Gómez-Reino JJ, BIOBADASER Group. Survival of TNF antagonists in spondylarthritis is better than in rheumatoid arthritis. Data from the Spanish registry BIOBADASER. Arthritis Res Ther. 2006;8(3):R72. [ Links ]
27. Scire CA, Caporali R, Sarzi-Puttini P, Frediani B, Di Franco M, Tincani A, et al. Drug survival of the first course of anti-TNF agents in patients with rheumatoid arthritis and seronegative spondyloarthritis: analysis from the MonitorNet database. Clin Exp Rheumatol. 2013;31(6):857-63. [ Links ]
28. Favalli EG, Sinigaglia L, Becciolini A, Grosso V, Gorla R, Bazzani C, et al. Two-year persistence of golimumab as second-line biologic agent in rheumatoid arthritis as compared to other subcutaneous tumor necrosis factor inhibitors: real-life data from the LORHEN registry. Int J Rheum Dis. 2018;21(2):422-30. [ Links ]
29. Michelsen B, Sexton J, Wierød A, Bakland G, Rødevand E, Krøll F, et al. Four-year follow-up of inflammatory arthropathy patients treated with golimumab: Data from the observational multicentre NOR-DMARD study. Semin Arthritis Rheum. 2020;50(1):12-16. [ Links ]














