Introducción
Actualmente la artritis reumatoidea (AR) es considerada una enfermedad severa dado que, sin un tratamiento adecuado, la mayoría de los pacientes que la padece desarrolla una enfermedad progresiva, con importante daño radiológico, deterioro de su capacidad funcional y laboral, y aumento significativo de la mortalidad. El principal objetivo del tratamiento es lograr la remisión o baja actividad de la enfermedad. Para alcanzarlo, se debe utilizar todo el arsenal terapéutico disponible, para lo cual se ha desarrollado la estrategia de “tratamiento hacia el blanco”, “tratamiento hacia el objetivo” o “treat to target” (T2T)1-2.
Existe un grupo de pacientes en los cuales no es posible controlar la actividad de la enfermedad mediante el uso de drogas modificadoras de la enfermedad sintéticas convencionales (DMARsc) o que, en un porcentaje menor, presentan contraindicación para las mismas. Es en estos casos en los cuales están indicados los agentes biológicos (DMARb) o sintéticos dirigidos (DMARsd)1-3. El intervalo de tiempo que transcurre desde la indicación de alguno de estos últimos hasta que el paciente recibe la primera dosis es muy variable en las distintas áreas geográficas y según el sistema de cobertura médica; esto se relaciona muy probablemente con su alto costo. Bartel et al., del Hospital Británico de la Ciudad Autónoma de Buenos Aires, en el año 2016, informaron que, en dicha institución privada, la demora entre la prescripción y el inicio del tratamiento biológico fue de 39,5 días4. En un estudio más reciente, en el cual participaron cinco centros de Argentina, se observó un retraso promedio para conseguir el agente biológico de 110 días5. Ambos trabajos evidenciaron que los pacientes estuvieron en promedio más de 1 mes padeciendo enfermedad activa con todas las consecuencias que ello implica en el pronóstico de los mismos (no solo a nivel de progresión de daño radiológico sino también del deterioro, tanto de su capacidad funcional y de su calidad de vida).
Objetivos
Dado que en la práctica diaria en el hospital público son múltiples los inconvenientes que presentan los pacientes para acceder a un tratamiento biológico o sintético dirigido, se llevó a cabo este trabajo con los siguientes objetivos:
Materiales y métodos
En un hospital público de la Ciudad Autónoma de Buenos Aires (CABA) se realizó un estudio observacional, analítico y retrospectivo. Se revisaron todas las historias clínicas de los pacientes con diagnóstico de AR (American College of Rheumatology/European League Against Rheumatism, ACR/EULAR 2010)6 que consultaron en la Sección de Reumatología del Hospital General de Agudos Dr. E. Tornú, a quienes se les había indicado un tratamiento biológico o sintético dirigido. Se excluyeron a todos los que accedieron a dichos medicamentos mediante la participación en un trabajo de investigación, o a los que en la primera consulta ya los recibían debido a la indicación en otro centro, y quienes no regresaron a la consulta luego de la indicación del tratamiento.
En una ficha prediseñada se consignaron las siguientes variables en el momento de la indicación del agente biológico o sintético dirigido: datos sociodemográficos (edad, sexo, lugar de residencia), nivel educativo, estado laboral, cobertura de salud y si poseía certificado de discapacidad. Se registró también la presencia de comorbilidades. En cuanto a las características de la AR, se detalló el tiempo de evolución en meses, la presencia de factor reumatoideo (FR) y/o anticuerpos antiproteínas/péptidos citrulinados (ACPA), anticuerpos anti núcleo-citoplasmáticos (ANA), erosiones en algún estudio por imágenes; y se describieron, en caso de estar presentes, las manifestaciones extraarticulares. Para evaluar la capacidad funcional se utilizó el Health Assessment Questionnaire versión Argentina (HAQ-A)7 y para la actividad de la enfermedad se registró el Disease Activity Score 28 (DAS28)8; los pacientes fueron clasificados en los diferentes niveles de actividad según los valores del mismo.
En lo referente al tratamiento, se detalló si el paciente recibía: corticoides y la dosis equivalente de prednisona, DMARsc (de forma aislada o combinada), antiinflamatorios no esteroideos (AINES), otros tratamientos para controlar el dolor como paracetamol y/u opiáceos, y si estos o los AINES estaban combinados con esteroides. Se describió el motivo por el cual se había decidido cambiar o adicionar dicho tratamiento y qué molécula fue la indicada. Tanto la fecha de indicación del tratamiento biológico o sintético dirigido, así como la fecha en que el paciente recibió en forma efectiva la primera dosis del mismo, se dividieron en tres períodos: el primero antes de 2010, el segundo entre 2010 y 2014, y el tercero de 2015 a 2019. Según las fechas detalladas, se calculó el tiempo de demora en días desde que se indicó DMARb o DMARsd. Finalmente, en cada caso, se consignaron los motivos registrados en las historias clínicas por los cuales se retrasó el inicio de dicho tratamiento.
Análisis estadístico
Se describieron las variables cuantitativas con medias, medianas, desvío estándar o rango intercuartílico (RIC), y las variables categóricas con valores absolutos y proporciones. Se comparó el tiempo de demora hasta el inicio del tratamiento entre grupos definidos por características demográficas, socioeconómicas, cobertura social, estado laboral y presencia de certificado de discapacidad con prueba T de Student, ANOVA, prueba de Mann-Whitney o de Kruskall-Wallis, chi-cuadrado o test exacto de Fisher, según correspondiera en cada caso. Todas las pruebas estadísticas se realizaron con un nivel de significación de 0,05. En todos los casos se comprobaron los supuestos en que se basan en las pruebas.
Resguardos éticos
La investigación se desarrolló según los lineamientos que estipula la Ley 3301/09 del Ministerio de Salud del Gobierno de la Ciudad Autónoma de Buenos Aires y los principios de la Declaración de Helsinki. El estudio fue aprobado por un Comité de ética. Los datos personales de los pacientes fueron codificados, sin poder identificarlos a fin de resguardar su confidencialidad.
Resultados
Se incluyeron 102 pacientes que cumplieron los criterios de selección, con una edad promedio al momento de la indicación del tratamiento biológico o sintético dirigido de 52,5 (DE 11,6) años; 93% fue mujer y 58% residente en la Provincia de Buenos Aires. El nivel de educación se registró en 66 pacientes, de los cuales el 28% tenía educación superior. De los 91 pacientes en los cuales se consignó la cobertura de salud, 58% poseía algún tipo de cobertura, siendo la misma el Programa de Atención Médica Integral (PAMI) o el Programa Federal Incluir Salud (ex PROFE) en el 64% de los casos. Treinta y dos de 77 pacientes eran laboralmente activos. En 66 pacientes se detalló que 61 (92%) poseían certificado de discapacidad al momento de indicar el tratamiento biológico o sintético dirigido. El 86% padecía alguna comorbilidad; la más frecuente fue osteoporosis (46%), seguida de hipertensión arterial (34%) y dislipemia (32%), y en el 64% se registró más de una comorbilidad (Tabla 1).
Tabla 1: Características de la población (N=102)

DE: desvío estándar; CABA: Ciudad Autónoma de Buenos Aires; PAMI: Programa de Atención Médica Integral
En el momento de realizar la indicación del tratamiento con DMARb o DMARsd, la mediana de evolución de la AR fue de 66,5 meses (RIC 32-120), el 80% presentaba enfermedad erosiva y se informó seropositividad para FR en el 96%, para ACPA en el 92% y para ANA en el 68%. En 68 pacientes (67%) se constató presencia de manifestaciones extraarticulares, los síntomas sicca fueron los más frecuentes (38%), seguidos por nódulos reumatoideos (29%).
La mediana de DAS28 fue de 5,19 (RIC 4,47-6,05). Según dicho índice, 56% de los pacientes presentaba nivel alto de actividad de la enfermedad y 39% moderado. La mediana de HAQ-A fue de 1,63 (RIC 1-2,1).
Cuando el médico tratante tomó la decisión de iniciar con un agente biológico o sintético dirigido, el 87% de los pacientes recibía esteroides, siendo la dosis promedio de prednisona de 10 mg por día (DE 5,40). El 92% de los pacientes se encontraba en tratamiento con DMARsc y el más frecuente fue el metotrexato (71%), seguido de leflunomida (45%); el 39% recibía tratamiento combinado con diferentes DMARsc. En lo referente a otros tratamientos, el 81% recibía tratamiento con AINES y en el 52% el mismo era concomitantemente con esteroides (Tabla 2).
Tabla 2: Características de la artritis reumatoidea y tratamiento (N=102)
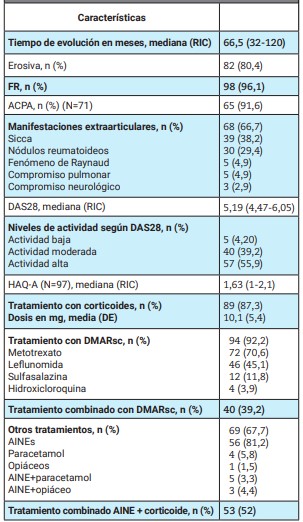
RIC: rango intercuartílico; FR: factor reumatoideo; ACPA: anticuerpos antiproteínas/péptidos cíclicos citrulinados; DAS28: Disease Activity Score 28; HAQ-A: Health Assessment Questionnaire Argentine version; DE: desvío estándar; DMARsc: drogas modificadoras de la artritis reumatoidea sintéticas convencionales; AINES: antiinflamatorios no esteroideos
El mayor porcentaje de indicación de tratamiento biológico o sintético dirigido se observó durante el tercer (2015-2019) y segundo (2010- 2014) período del registro de datos (45% y 38% respectivamente). El agente indicado con mayor frecuencia fue etanercept (32%), seguido de adalimumab (24%). El principal motivo que determinó el cambio en la conducta terapéutica fue la falta de respuesta a DMARDsc (75%).
De los 102 pacientes a quienes se les indicó un tratamiento biológico o sintético dirigido, 71 (70%; IC95: 61-79) lo iniciaron. La mediana de demora desde que el médico especialista decidió un cambio en la medicación y el momento en que el paciente recibió la primera dosis fue de 240 días (RIC 113-504). Los motivos consignados para dicha demora fueron múltiples en el 37% de los casos, y la causa principal fue de índole burocrática (47%). Dentro de la misma se incluyeron, por ejemplo, la necesidad de actualizar resúmenes de historia clínica o de completar formularios para la solicitud del medicamento indicado, entre otros (Tabla 3).
Tabla 3: Características de los tratamientos biológicos o sintéticos dirigidos (N=102)
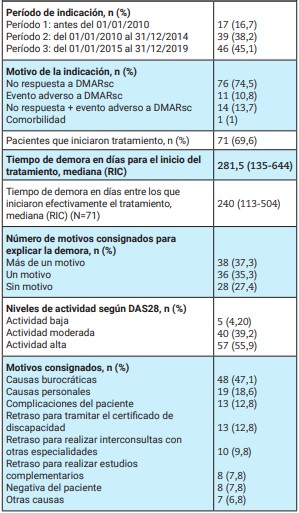
RIC: rango intercuartílico; DMARsc: drogas modificadoras de la artritis reumatoidea sintéticas convencionales; DAS28: Disease Activity Score 28
Al analizar los factores asociados a la demora del inicio del tratamiento biológico o sintético dirigido, se observó que aquellos con bajo nivel de actividad de la enfermedad obtuvieron el tratamiento en menor tiempo que quienes presentaban niveles de actividad moderado o alto (promedio de 113 días vs 242 y 332 respectivamente), y esto resultó estadísticamente significativo (p=0,01). No se encontraron diferencias estadísticamente significativas entre la prescripción y el inicio del tratamiento al comparar las características sociodemográficas, la presencia de comorbilidades ni otras características de la AR. No hubo asociación entre la capacidad funcional, evaluada por HAQ-A, y el tiempo de demora para recibir el DMARb o DMARsd (r=-0,03, p=0,77). Tampoco se hallaron diferencias estadísticamente significativas por recibir tratamiento combinado con DMARsc o esteroide asociado con AINES. No hubo diferencia en el retraso para el inicio según el agente indicado (Tabla 4 y Tabla 5).
Tabla 4: Relación entre el tiempo de demora y las características de la artritis reumatoidea entre quienes efectivamente iniciaron el tratamiento biológico o sintético dirigido (N=71)
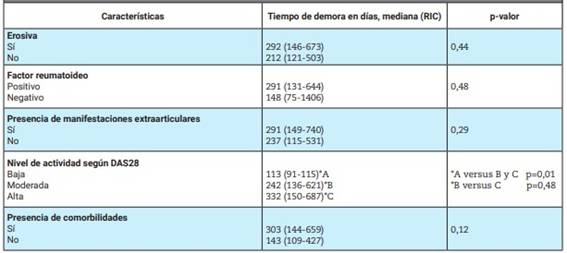
RIC: rango intercuartílico; DAS28: Disease Activity Score 28. A: baja actividad; B: moderada actividad; C: alta actividad
Tabla 5: Relación entre el tiempo de demora y las características sociodemográficas entre quienes efectivamente iniciaron el tratamiento biológico o sintético dirigido (N=71)
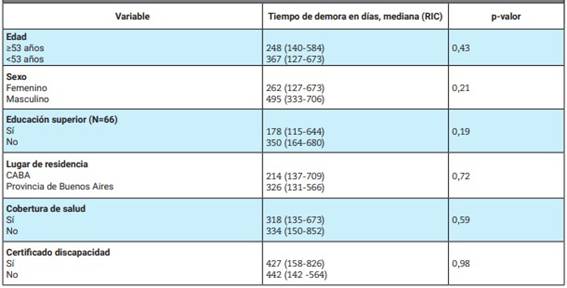
RIC: rango intercuartílico; CABA: Ciudad Autónoma de Buenos Aires
Los factores asociados con las causas burocráticas fueron la educación y el lugar de residencia. Los pacientes con estudio secundario completo o superior refirieron menos dificultades burocráticas que aquellos con menos años de estudio (16,67% vs 60,42%; p=0,002). La residencia en la Provincia de Buenos Aires se asoció con mayor frecuencia a los problemas burocráticos al compararlos con aquellos que vivían en CABA (58,33% vs 30,95%; p=0,006) (Tabla 6).
Discusión
Un requerimiento básico de justicia es que todos tengan las mismas oportunidades para cubrir sus necesidades, y el cuidado de la salud es uno de los derechos elementales para las personas9-10. Los beneficios del tratamiento dirigido al blanco, más conocido como T2T, con una estrategia de seguimiento y control estricto de los pacientes que padecen AR, modificando las conductas terapéuticas con el objetivo de lograr la remisión o baja actividad de la enfermedad, han sido ampliamente demostrados en diversos trabajos clínicos. En todos se ha evidenciado que los pacientes tratados bajo este objetivo alcanzan mejores resultados que aquellos que son seguidos con el control de rutina habitual, no solo en los que se focalizan en el daño clínico, funcional y estructural, sino también en otros aspectos como comorbilidades, productividad laboral y calidad de vida11. Este plan de tratamiento también ha demostrado ser costo-efectivo12. La evidencia existente avala que las guías de tratamiento para la AR recomienden fuertemente dicha estrategia en la cual, para lograr el éxito en los resultados, las modificaciones en el tratamiento deben realizarse cada 1 a 3 meses basados en la evaluación de la actividad de la enfermedad1,11. Sin embargo, el acceso a la medicación en muchos lugares es una importante limitación para cumplir con dicha recomendación13-15.
En el presente trabajo observamos una demora de tiempo mucho mayor para el inicio del tratamiento biológico o sintético dirigido (mediana de 240 días) en comparación a lo informado en los dos trabajos previos realizados en nuestro país. La misma fue más del doble de días de lo reportado en promedio por Collado et al. (110 días)5 y seis veces mayor a la informada por Bartel et al. (mediana de 39,5 días)4. Esta diferencia puede deberse a que en dichos estudios casi todos, o la mayor parte de los pacientes, pertenecían a instituciones privadas y poseían cobertura médica en más del 60% de los casos en el primer trabajo, siendo la misma del 100% en el de Bartel et al.
Lo que determinó con mayor frecuencia la prescripción del tratamiento biológico o sintético dirigido fue la falta de respuesta a DMARsc, observándose que el 95% de los pacientes se encontraba con niveles moderados o altos de la actividad de la enfermedad según DAS28, y el 87% recibía además tratamiento con esteroides, hallándose el mismo combinado con AINES en el 52% de los casos con todos los riesgos que dicha asociación implica.
Es de destacar que la comorbilidad más frecuentemente descripta fue la osteoporosis (46%) la cual, teniendo en cuenta la edad promedio de la población incluida (52,5 años), podría estar asociada al elevado porcentaje de uso esteroides y/o a la actividad persistente de la enfermedad.
Al contrario de lo esperado, la demora en el inicio del tratamiento con DMARb o DMARsd fue menor en el grupo de pacientes que presentaban baja actividad de la AR al compararlos con aquellos con actividad moderada o alta, y fue en este último grupo donde se registró el mayor retraso. Esta asociación podría explicarse en el supuesto de que aquellos pacientes con mayor actividad de la enfermedad también presentaban menor capacidad funcional, determinando mayor dificultad para realizar estudios complementarios, interconsultas y trámites administrativos necesarios para el inicio del tratamiento. Sin embargo, no hallamos asociación entre la capacidad funcional, evaluada por HAQ-A, y el tiempo de demora.
En más de un tercio de las historias incluidas en esta revisión, se encontraron múltiples motivos por los cuales se retrasó el inicio del tratamiento con un DMARb o DMARsd, y los más frecuentes fueron los problemas de índole burocrática. Entre los factores analizados, el mayor nivel de educación y la residencia en CABA fueron los que en forma estadísticamente significativa se asociaron a menor dificultad para la resolución de dichos problemas. Estos datos concuerdan con los resultados del estudio de Collado et al., donde el motivo más frecuente de demora reportado por los pacientes fue de causa administrativa. En este último trabajo, el tiempo de demora fue significativamente mayor en pacientes que residían en la Provincia de Buenos Aires con respecto a quienes lo hacían en CABA. No obstante, no se demostró asociación con el nivel de instrucción.
No observamos qué variables sociodemográficas diferentes al nivel educativo y el lugar de residencia, como ser, comorbilidades, otras características de la AR además del grado de actividad, ni el tipo de DMARb o DMARsd indicado, hayan influenciado en forma estadísticamente significativa sobre el tiempo de demora para el inicio de un tratamiento biológico o sintético dirigido.
Dentro de las debilidades del estudio, se encuentran la pérdida de registro de datos que implica la realización en todo trabajo retrospectivo (dado que no se disponía de todas las variables a consignar en todos los pacientes incluidos), así como no haber podido evaluar correctamente a los pacientes que presentaban pérdida de seguimiento. Tampoco se pudo constatar la influencia de los programas de asistencia a los pacientes en la adquisición de los diferentes tratamientos.
Como fortalezas de este trabajo, se destaca el tamaño muestral, considerando que fue realizado en un solo centro. También haber registrado no solo los motivos que determinaron la indicación del tratamiento biológico o sintético dirigido y la demora para que los pacientes comiencen a recibir dichos fármacos, sino también el detalle de las causas responsables de la misma. Esto último nos permitió analizar los principales factores asociados con dicho retraso y, de este modo, reflejar la gran dificultad que padecen los pacientes que son asistidos en un hospital público para acceder a un tratamiento adecuado para su enfermedad.
Teniendo en cuenta que, para que la estrategia de tratamiento basada en el T2T sea efectiva, los cambios en la conducta terapéutica deben realizarse cada 1 a 3 meses; en nuestro centro detectamos una demora de aproximadamente 8 meses para implementar una modificación adecuada en el tratamiento de los pacientes que padecen AR, y el principal motivo de dicha demora se relacionó con los trámites burocráticos. Dado que estas dificultades se evidenciaron sobre todo en los pacientes con menor nivel educativo y en aquellos residentes en la provincia de Buenos Aires, consideramos la sumatoria de ambos factores como posibles indicadores de mayor vulnerabilidad, constituyendo estas personas la población que precisa más asesoramiento, acompañamiento y asistencia social.
Conclusiones
En el momento de prescribir un tratamiento biológico y/o sintético dirigido, el 95% de los pacientes se encontraba con niveles de actividad moderado y/o alto según DAS28, y el 87% recibía tratamiento con esteroides (asociados a AINES en el 52% de los casos).
La principal causa que motivó un cambio en la conducta terapéutica hacia la prescripción de un DMARb o DMARsd fue la falta de respuesta a DMARDsc.
La mediana en la demora para el inicio de un tratamiento biológico o sintético dirigido en la población de pacientes evaluados que concurrió a un Servicio de Reumatología en un hospital público fue de 240 días. El motivo principal de dicha demora fue de índole burocrática, que se evidenció con mayor frecuencia en aquellos con menor nivel educativo y en los residentes en la Provincia de Buenos Aires.